邻苯二甲醛对还原型谷胱甘肽的光谱分析
——推荐一个仪器分析实验
2021-11-05张鹏张倩钟华丁彩凤
张鹏,张倩,钟华,丁彩凤
青岛科技大学化学与分子工程学院,光电传感与生命分析教育部重点实验室,山东省生化分析重点实验室,山东省生命分析高校重点实验室,山东 青岛 266042
仪器分析是化学学科的重要分支,主要是借助特殊仪器,以物质的理化性质为基础建立起来的分析方法。它具有分析能力强、分析速度快、检测灵敏度高等优点[1,2]。作为高等院校化学及相关专业学生的必修课程,仪器分析实验通常包含了光谱分析、电化学分析和色谱分析等几个领域。其中光谱分析是常用的快速、灵敏、准确的现代仪器分析方法之一,它主要是利用物质的特征光谱研究其结构或测定其成分的方法。光谱分析法主要有紫外-可见吸收光谱、荧光光谱、原子发射光谱、原子吸收光谱、红外光谱等[3,4]。
还原型谷胱甘肽(GSH)是一种含巯基的三肽,由谷氨酸、半胱氨酸及甘氨酸组成,在体内协助维持机体的免疫系统,并具有抗氧化性和解毒功能。因此,对GSH含量的检测可为疾病的诊断和健康评估提供有效的数据。目前GSH的检测方法主要有还原酶法、量热法、分光光度法、色谱法、毛细管电泳法等。与之相比,光谱分析法,尤其是荧光分析法,可在生物体中实现无创原位成像分析,具有良好的生物应用前景。因此,开发可用于GSH检测的光谱分析方法引起了广泛的关注[5]。
近几十年来,有机分子探针的设计与检测性能研究获得了长足的发展,尤其是紫外-可见吸收光谱法(比色法)和荧光光谱法[6],研究者们对其产生了极大的兴趣,遗憾的是在校本科生对该领域的接触机会不多。有机分子探针的研究涉及有机化学、分析化学、无机配位化学以及物理化学等方面的专业基础知识,并且通过多种仪器研究探针分子的检测性能,探索检测机理。因此,如果可以将分子探针的设计和应用研究纳入本科生的教学中,不仅可以使学生掌握分析检测新方法,了解分析仪器的工作原理和使用方法,而且可以促进学生对所学多学科知识的融会贯通,激发学生对前沿科学研究的热情和兴趣。
本实验采用商品化的试剂邻苯二甲醛(OPA)作为探针分子,避免了探针分子的合成与分离,保障了实验教学在有限课时内顺利实施。实验内容包含标准溶液的配制、紫外-可见吸收/荧光光谱测试、检测限的计算、结合比的确定及分析机理的验证(包括核磁共振氢谱和高分辨质谱)等几部分。本实验适用于化学及相关专业高年级本科生的教学,使学生体验科学研究的趣味性与严谨性,培养正确的科学态度,为后续的继续深造和就业打下基础。
1 实验部分
1.1 实验目的
(1) 掌握紫外-可见分光光度计和荧光分光光度计的基本操作。
(2) 掌握分子探针法对分析物的测定方法。
(3) 学习动态弱相互作用的光谱分析方法。
(4) 学习核磁共振波谱仪和质谱仪的使用。
(5) 掌握实验数据处理和实验结果分析能力,培养学生的创新意识。
1.2 实验原理
含巯基的物质和醛类可以发生亲核加成反应形成半缩硫醛,如图1a所示。伯胺类化合物可以和醛脱水反应形成亚胺(图1b)。将此二者有机结合起来,即含有两个醛基的邻苯二甲醛可以和既含有巯基又含有氨基的物质发生反应形成巯基取代的噻唑类化合物(图1c)[7,8],该结构在350 nm紫外光照射下有蓝色荧光。因此,OPA可以和既含有巯基又含有氨基的还原型谷胱甘肽反应生成苯并噻唑类物质(图2),如果将OPA与GSH的溶液混合,二者反应会出现苯并噻唑特有的光谱,在340 nm附近出现明显的紫外吸收峰,420 nm处有亮蓝色荧光出现,说明OPA可以用于GSH的光谱检测。
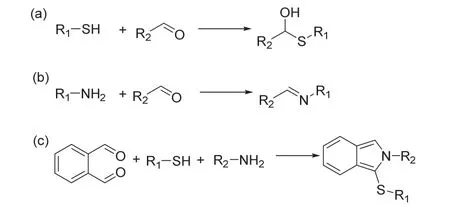
图1 巯基(a)或氨基(b)类化合物与醛类物质的反应和OPA与巯基和氨基类化合物的反应(c)
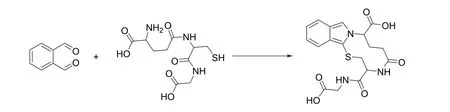
图2 探针OPA与GSH的反应方程式
1.3 仪器与试剂
1.3.1 仪器
EL104电子分析天平(瑞徽电子,中国),FE20实验室用pH计(米科,中国),UH5300紫外-可见分光光度计(Hitachi,日本),F-4600荧光分光光度计(Hitachi,日本),365 nm紫光灯,ICP-MS电耦合等离子体质谱仪(PerkinElmer,美国),500 MHz核磁共振波谱仪(Bruker,瑞士)。
1.3.2 试剂
分析纯邻苯二甲醛(> 99.0%,上海阿拉丁生化科技股份有限公司),还原型谷胱甘肽(≥ 98.0%,上海阿拉丁生化科技股份有限公司),二水合磷酸二氢钠(≥ 99.0%,国药集团化学试剂有限公司),十二水合磷酸氢二钠(≥ 99.0%,国药集团化学试剂有限公司),光谱纯二甲基亚砜(≥ 99.0%,生工生物工程股份有限公司),去离子水(实验室自制)。
1.4 实验内容
1.4.1 溶液配制
准确称量0.0134 g邻苯二甲醛,加入10 mL DMSO溶解,配制成浓度为1 × 10−2mol∙L−1的溶液。准确称取0.0307 g还原型谷胱甘肽,用10 mL去离子水溶解,配制成浓度为1 × 10−2mol∙L−1的溶液。用二水合磷酸二氢钠和十二水合磷酸氢二钠配制浓度1 × 10−2mol∙L−1,pH为7.2的缓冲液。
1.4.2 光谱测试
准确移取25 μL上述邻苯二甲醛溶液,向其中加入2.0 mL磷酸缓冲盐溶液(PBS),再加入一定体积的谷胱甘肽溶液,用PBS缓冲液稀释至5.0 mL。此时溶液中邻苯二甲醛的浓度为5 × 10−4mol∙L−1。将此溶液在25 °C下静置20 min后用1 cm石英池测其紫外-可见吸收光谱和荧光光谱。荧光光谱测试时,设置仪器激发和发射狭缝均为5 nm,激发波长为350 nm。
1.4.3 GSH检测限的测定
向含有5 × 10−4mol∙L−1OPA的PBS缓冲溶液中加入不同浓度的GSH,使得最终溶液中GSH与OPA的比例为0,0.1,0.2,0.3,0.4,0.5,0.6,0.7,0.8,0.9,1.0。溶液静置20 min后测试紫外-可见吸收光谱和荧光光谱,分别以340 nm处吸光度和420 nm处荧光强度对GSH浓度做校准曲线,计算其斜率k。根据LOD = 3.3s/k计算OPA对GSH的检测限[9,10],式中,LOD表示检测限,k为校准曲线的斜率,s为OPA空白样品的标准偏差(测试11次)。
1.4.4 OPA与GSH结合比的测定
OPA与GSH之间以两重动态可逆共价键结合,因此,可采用等摩尔连续变化(Job’s plot)法测定二者结合比[11]。具体实验方法是保持溶液中OPA与GSH的浓度之和为1 × 10−3mol∙L−1,逐渐改变二者比例,配制如表1所示的11组溶液,分别测试其紫外-可见吸收光谱,用420 nm吸光度对X(X=[GSH]/([OPA] + [GSH]))值作图,得到Job’s plot曲线,拟合曲线获得拐点可知二者的结合比。

表1 Job’s Plot (OPA与GSH)浓度配量表
1.4.5 GSH检测机理的验证
(1) 核磁共振氢谱(1H NMR)。分别测试OPA以及OPA与GSH反应生成物的核磁共振氢谱,通过对比分析证实二者的反应机理。
(2) 高分辨质谱(HR-MS)。测试OPA与GSH反应液的高分辨质谱,分析质谱数据,验证反应机理。核磁共振氢谱和高分辨质谱测试样品由学生准备,相关教师负责测试。
2 结果与讨论
2.1 紫外-可见吸收光谱和荧光光谱测试
如图3a所示,OPA在PBS缓冲液中的最大吸收峰在260 nm附近,300 nm处的吸收峰为n–π*跃迁产生的吸收带,溶液呈无色,GSH在所测试范围内没有吸收峰,将二者混合后于340 nm处出现很强的吸收峰,溶液颜色随之变为淡黄色。对应的荧光光谱显示(图3b),OPA与GSH完全没有荧光发射,而二者混合液在420 nm处出现明显的荧光信号,在365 nm紫光灯下显示亮蓝色荧光。这些光谱数据表明OPA可以用于GSH的紫外/荧光双通道检测。

图3 在PBS缓冲溶液中OPA、GSH以及OPA + GSH的紫外-可见吸收光谱(a)和荧光光谱(b)
2.2 检测限测定结果
如图4(a)所示,向含有5 × 10−4mol∙L−1OPA的PBS缓冲溶液中加入不同浓度的GSH,随着GSH浓度的增大,溶液在340 nm处的吸光度不断增加,吸光度与GSH和OPA浓度比呈线性(y= 2.56x− 0.0077,线性相关系数为0.9938),拟合结果如图4(b)所示,依此计算OPA对GSH的检测限是1.6 × 10−7mol∙L−1。

图4 (a) OPA与不同浓度的GSH作用后的紫外-可见吸收光谱;(b) 340 nm吸光度的线性拟合
对应的荧光光谱如图5所示,随着GSH浓度的增大溶液在420 nm处的荧光发射峰不断增强,420 nm荧光强度与GSH和OPA浓度比也呈良好的线性(y= 5706.42x− 100.62,线性相关系数为0.9914),由荧光强度计算OPA对GSH的检测限是8.4 × 10−8mol∙L−1。
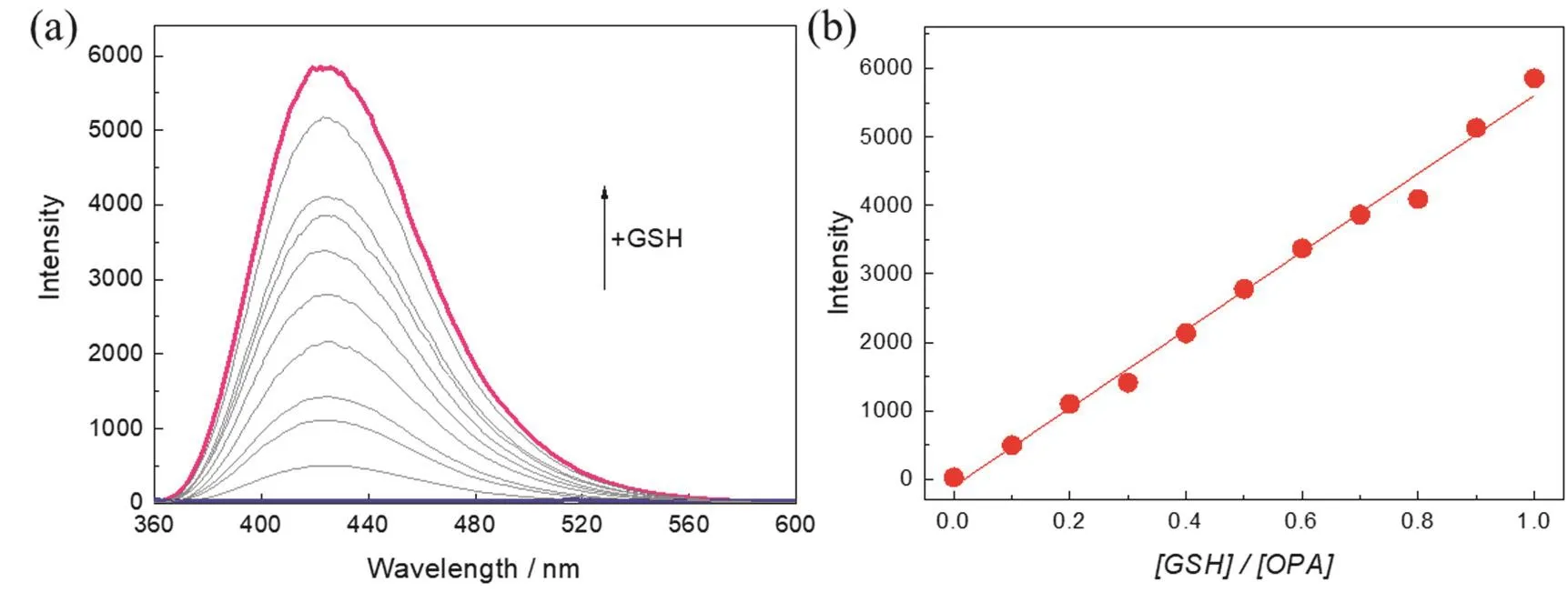
图5 (a) OPA与不同浓度的GSH作用后的荧光光谱;(b) 420 nm荧光强度的线性拟合
2.3 OPA与GSH结合比
采用等摩尔连续变化(Job’s Plot)法探讨OPA与GSH结合比,通过测试配制的11组溶液紫外-可见吸收光谱,以340 nm吸光度对X值作图,得到Job’s plot曲线如图6所示,可见X值为0.5处是两侧曲线拟合线的交点,说明OPA与GSH之间的结合比为1 : 1。
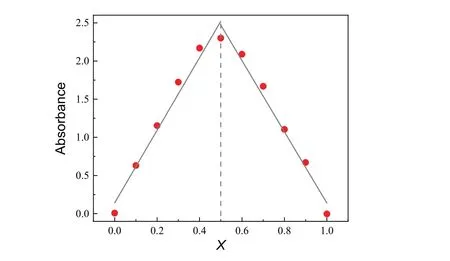
图6 OPA与GSH反应的Job’s plot曲线
2.4 GSH检测机理的验证
2.4.1 核磁共振氢谱
分别测试OPA以及OPA与GSH反应生成物的核磁共振氢谱,通过对比证实二者的反应机理。邻苯二甲醛在水溶液中存在时会有单水合物和二水合物(C6H4(CHO)(CH(OH)2)和C6H4(CH(OH))2O)存在(图7)[12],因此其核磁共振氢谱出现两套峰(图8),10.3处是醛基氢的信号,7.82和7.92处的两组峰为OPA苯环质子信号,6.15、6.36和7.30是OPA二水合物的信号峰;GSH在低场没有信号。将而这混合后可发现10.3、7.82和7.92的信号明显降低,7.3–7.4间的信号增强,说明OPA与GSH作用形成苯并噻唑环。
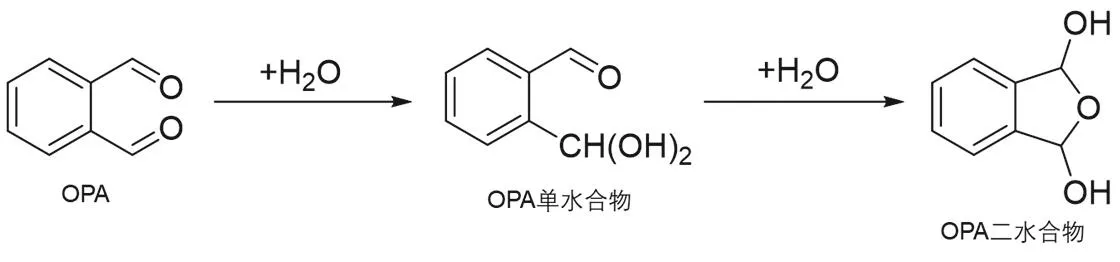
图7 邻苯二甲醛与其单水合物、二水合物的结构式

图8 OPA与GSH反应前后的核磁共振氢谱
2.4.2 高分辨质谱
向含有5 × 10−4mol∙L−1OPA的PBS缓冲液中加入等物质的量的GSH,反应完成后的溶液测试高分辨质谱,采用ESI离子源,负离子模式。由图9可以看出,ESI-MS数据显示OPA与GSH作用后出现404.0923 (m/z)的负离子信号峰,测试结果与预期产物的理论计算值一致(C18H18N3O6S−的理论计算值:404.0922),进一步证实了OPA与GSH的反应机理。
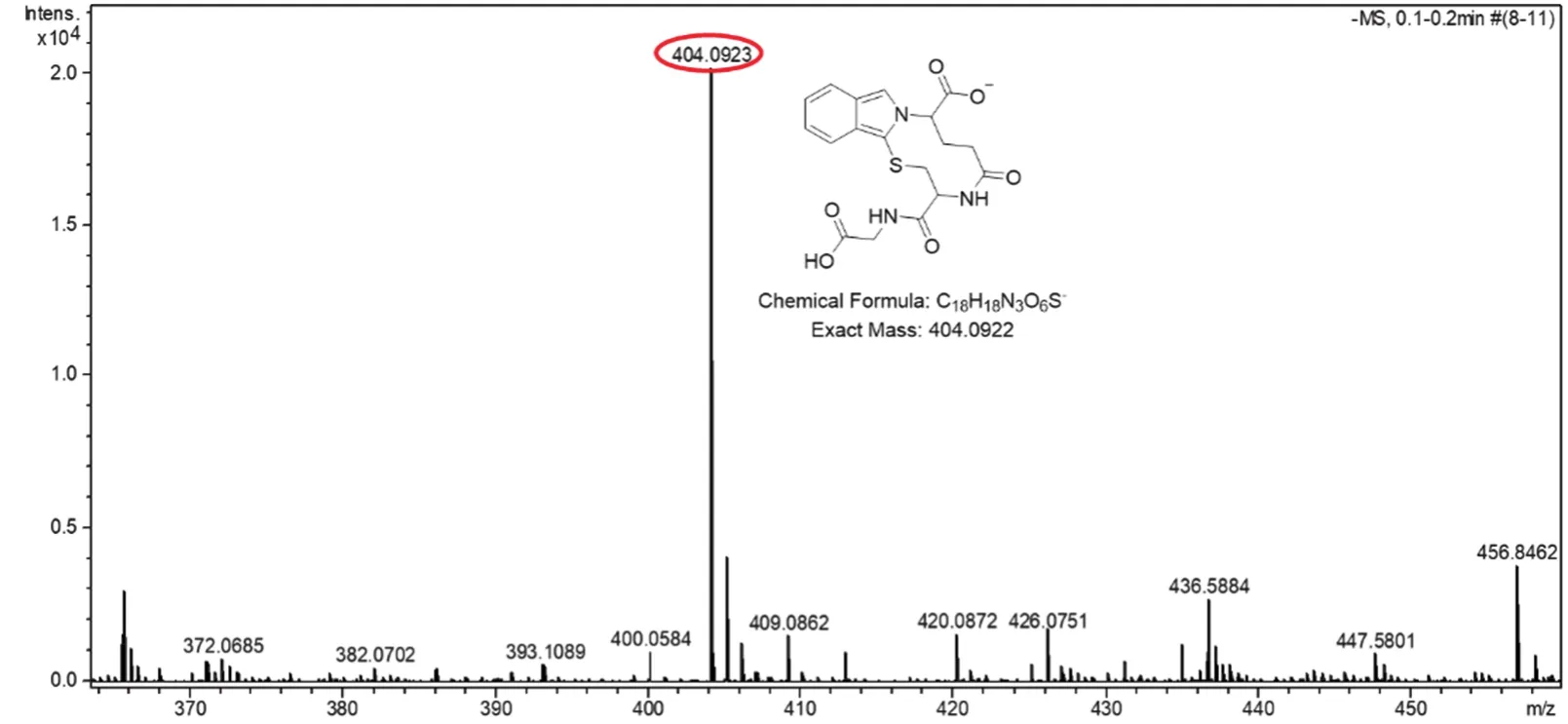
图9 OPA与GSH反应后的高分辨质谱
3 实验的实施与反馈
我们在本学院化学专业本科三年级的学生中已经开展了三轮本实验的教学,教学效果良好,学生反馈积极。具体的实验教学以小组为单位施行,2–3人一组,实验设定4个学时。3次实验教学均顺利完成,学生基本能够在规定时间内完成实验,并能够准确分析实验数据、撰写实验报告。学生普遍反映该实验不仅学习了多种分析仪器的使用以及数据分析方法,并且整个实验过程充满了趣味性,让他们充分体验到了探索性研究的乐趣。
4 拓展思考
(1) OPA的水合作用对GSH的检测有什么影响?
(2) 哪些因素会影响OPA对GSH检测的准确性?
(3) 如果溶液中含有半胱氨酸时会对GSH的检测造成什么样的影响?
5 结语
介绍了一个适合化学及相关专业本科生教学的仪器分析创新实验。本实验用市售试剂OPA作为底物,通过光谱分析法检测GSH,综合了分析化学、有机化学、物理化学等学科的基础知识和实验操作技能,促进学生对不同学科知识的融会贯通,提升了学生的实验操作技能及数据分析处理能力,调动了学生的科研兴趣。本实验与前沿科学研究密切接轨,以实验课堂教学的方式向本科生介绍前沿科研,加速学生对科研的融入,充分激发其科研热情,为学生毕业后的继续深造和就业奠定基础。
