气相色谱-串联质谱法测定花椒中氯菊酯的不确定度评定
2021-11-04袁新跃胡丽霞印方平季昱周阳元沈丹玉
袁新跃,胡丽霞,印方平,季昱,周阳元,沈丹玉
1(杭州市富阳区食品安全检验检测中心,浙江 杭州,311400)2(中国林业科学研究院亚热带林业研究所,浙江 杭州,311400)
花椒(ZanthoxylumbungeanumMaxim.)是芸香科花椒属植物,原产于中国,广泛分布于亚洲、美洲、非洲以及大洋洲的热带和亚热带地区。花椒是传统的香辛料,其果皮被誉为“中国八大调味品之一”。花椒具有药用价值,不仅有温中、行气、逐寒、止痛、杀虫等多种功效,还可医治呕吐、胃痛、腹泻等病症,并可以作为表皮麻醉镇定剂[1]。花椒在我国云南、贵州、四川、重庆等地均有广泛栽植,是云贵川山区农民脱贫致富的重要经济作物[2]。
花椒为多年生灌木,除了有危害根部、叶部和树干等多种病害外,还容易发生铜色跳甲、蓝桔跳甲、红蜘蛛、蚜虫、小吉丁虫、大衰蛾、木撩尺蠖等多种虫害,因此农药的使用不可避免[3]。花椒一年之中打十一、二次农药。催芽、催枝、保花、保果、打蚜虫、治蜘蛛都要打农药,而且打农药经常要重复打2次或3次才能起效果。农药测定是花椒质量安全的重要保证。
测量不确定度是指由于测量误差的存在,对被测量值不能确定的程度[4-5]。测量不确定度直接影响测量结果的判定[6],是检测数据可靠性的重要保证[7]。目前关于菊酯类农药的检测方法很多,对气相色谱法测定氯菊酯和气相色谱-串联质谱法(gas chromatography-tandem mass spectrometry,GC-MS/MS)测定其他种菊酯类农药的不确定度评定也有较多报道[3,8-10],而关于GB 23200.113—2018《食品安全国家标准 植物源性食品中208种农药及其代谢物残留量的测定 气相色谱-质谱联用法》测定氯菊酯的不确定度评定还未见相关报道。本文根据《测量不确定度标示指南》和JJF 1059.1—2012技术规程[11]要求,对GC-MS/MS法测量花椒中氯菊酯结果的不确定度进行评定,分析不确定度来源,确定影响结果的主要因素,提高测定结果的准确度。
1 材料与方法
7000B气相色谱-串联质谱,美国Agilent公司;T10均质机,德国IKA公司;RV10旋转蒸发仪,德国IKA公司;HSC-24氮吹仪,天津市恒奥科技发展有限公司;氯菊酯标准溶液(GSB05-2309-2016,100 μg/mL,不确定度0.11 μg/mL),农业部环境保护科研监测所;环氧七氯标准品(C 14101000,10 mg,99.36%,不确定度0.3%),农业部环境保护科研监测所;正己烷、乙腈、甲苯、乙酸乙酯(色谱纯),美国FISHER公司;氯化钠(优级纯),国药集团化学试剂有限公司;花椒,当地超市。
1.2 实验方法
1.2.1 标准溶液的配制
准确移取1.0 mL氯菊酯标准母液,用正己烷定容得到10 μg/mL氯菊酯标准储备液。储备液用乙酸乙酯稀释成0.01、0.02、0.05、0.1、0.2、0.5 μg/mL系列标准工作液。
内标溶液:准确称取10.0 mg(精确至0.1 mg)环氧七氯标准品,用乙酸乙酯溶解定容为1 mg/mL内标储备液,再进一步用乙酸乙酯稀释为5 mg/L的内标溶液。
1.2.2 样品前处理
根据国标GB 23200.113—2018《食品安全国家标准 植物源性食品中208种农药及其代谢物残留量的测定 气相色谱-质谱联用法》要求,准确称取5.00 g(精确至0.01 g)粉碎好的花椒样品,置于100 mL塑料离心管中,加10 mL超纯水涡旋混匀,静置30 min。再加20 mL乙腈,以15 000 r/min高速均质2 min。加5 g氯化钠剧烈振荡10 s,在4 ℃下以4 200 r/min离心5 min。准确吸取5 mL上清液,40 ℃水浴旋转蒸发近干,待净化。
用5 mL乙腈-甲苯溶液(体积比3∶1)预淋洗活化洗石墨化碳黑-氨基柱,弃去淋洗液。用5 mL乙腈-甲苯溶液溶解旋蒸瓶中待测物,过柱。重复2次,再用5 mL乙腈-甲苯溶液淋洗小柱,收集所有淋洗液,40 ℃水浴旋转蒸发近干,用2.5 mL乙酸乙酯复溶,加50 μL环氧七氯内标溶液涡旋混匀,过0.22 μm滤膜,用于GC-MS/MS测定。以离子对进行定性,内标法定量。
1.2.3 仪器条件
色谱柱:HP-5MS柱(30 m×0.32 mm,0.25 μm);升温程序为初始60 ℃保持1 min,先以40 ℃/min速率升至120 ℃,再以5 ℃/min速率升至240 ℃,最后以12 ℃/min 速率升至300 ℃保持6 min;流速1.2 mL/min;进样口温度280 ℃;接口温度280 ℃;进样量1 μL;进样方式为不分流进样;载气为高纯氦气,纯度≥99.999%;四极杆温度150 ℃;离子源(EI)温度 230 ℃;电离能量70 eV;检测方式,多反应监测模式,氯菊酯的定量离子对183.1>153.0m/z,定性离子对183.1>168.0,碰撞能量分别为15、10 eV;环氧七氯的定量离子对353>262.8m/z,定性离子对353>218.9m/z,碰撞能量分别为15、35 eV。
1.2.4 数学模型的建立
按照标准方法,试样中氯菊酯含量的计算如公式(1)所示:
(1)
式中:X,花椒样品中氯菊酯的含量,mg/kg;Cs,标准工作溶液中氯菊酯质量浓度,μg/mL;A,试样溶液中氯菊酯的色谱峰面积;Ci,试样溶液中环氧七氯的浓度,μg/mL;Asi,标准工作液中环氧七氯的色谱峰面积;As,基质标准工作溶液中氯菊酯的色谱峰面积;Csi,标准工作溶液中环氧七氯的质量浓度,μg/mL;Ai,标准工作溶液中环氧七氯的色谱峰面积;V,试样上机液的最终定容体积,mL;m,花椒的质量,g。
1.2.5 不确定来源的分析
根据测定步骤和数学模型,GC-MS/MS法测定花椒中氯菊酯的不确定度来源包括:氯菊酯标准溶液和内标环氧七氯溶液的配制、标准曲线拟合引入的不确定度(B类评定);花椒样品重复测定引入的不确定度(A类评定);花椒称量过程引入的不确定度(B类评定);提取、净化和定容等前处理过程引入的不确定度(B类评定);分析仪器GC-MS/MS引入的不确定度(B类评定)。
2 结果与分析
2.1 标准储备液配制引入的不确定度
2.1.1 标准物质引入的不确定度

2.1.2 标准溶液配制过程引入的不确定度
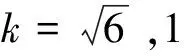
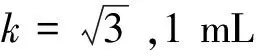
由1 mL单线刻度移液管和10 mL A级容量瓶引入的相对标准不确定度分别如公式(2)~公式(4)所示:
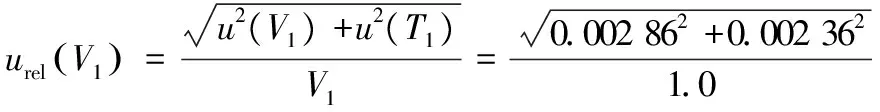
=0.003 71
(2)
0.002 50
(3)
由氯菊酯标准储备液配制所产生的相对不确定度为
(4)
2.1.3 内标物质引入的不确定度
由于在本次花椒测定氯菊酯过程中标准工作液和样品待测液均加入同体积的同一份配制好的环氧七氯内标溶液,环氧七氯的纯度和配制不影响花椒样品中氯菊酯的含量测定,因此内标物质环氧七氯引入的不确定度只由其移取体积所产生。
2.2 标准工作液配制引入的不确定度
分别吸取0.1、0.2、0.5、1、2、5 mL标准储备液于10 mL容量瓶中,用乙酸乙酯定容至刻度,配制成0.01、0.02、0.05、0.1、0.2、0.5 μg/mL这6个不同质量浓度点的标准工作液。再用100 μL移液枪移取50 μL环氧七氯溶液,分别与1 mL不同浓度标准工作液混合于1.5 mL进样瓶中,得到与待测样液相同环氧七氯内标含量的标准工作溶液。此过程产生的不确定度主要由玻璃量器、移液枪和室温变化所引入。玻璃量器和移液枪的最大允许误差按照检定规程[13]规定。前处理室温度设置为20 ℃,实际在±3 ℃范围内波动。标准工作液用乙酸乙酯进行定容,当室温为20 ℃时,其膨胀系数为1.38×10-3/℃。计算相对标准不确定度,具体结果见表1。
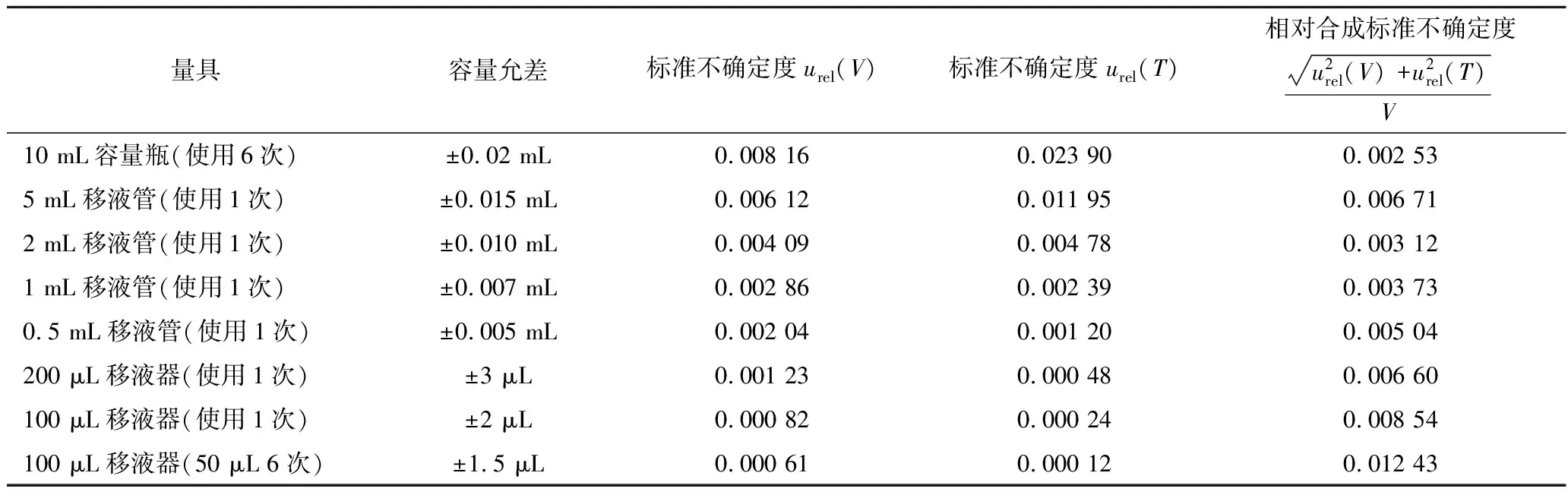
表1 标准溶液配制过程中移液管、移液枪的不确定度Table 1 Uncertainty of pipette and adjustable pipette in preparation of standard solution
由标准工作液配制引入的相对不确定度如公式(5)所示:
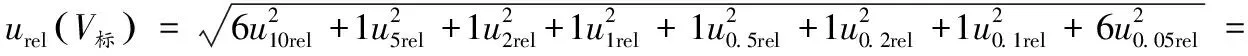
(5)
2.3 校正标准曲线引入的不确定度
配制好的相同环氧七氯含量的6点不同氯菊酯浓度系列标准工作液分别进行3次重复测定。以氯菊酯与环氧七氯的浓度比值作为横坐标x,氯菊酯与环氧七氯的峰面积比值作为纵坐标y,进行线性拟合,得到标准曲线方程y=0.092 112x+0.003 107,R2=0.995 21。标准曲线引入的标准不确定度如公式(6)所示:
(6)
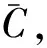
对花椒阴性样品添加氯菊酯,添加水平为0.3 mg/kg,进行6次平行测定,使用前面拟合的标准曲线线性回归方程为定量标准,计算氯菊酯的算术平均值和标准偏差,计算加标花椒重复测定引入的相对不确定度,花椒加标测量结果见表2。

表2 花椒样品添加氯菊酯重复测量结果Table 2 The determination result of permethrin in pepper
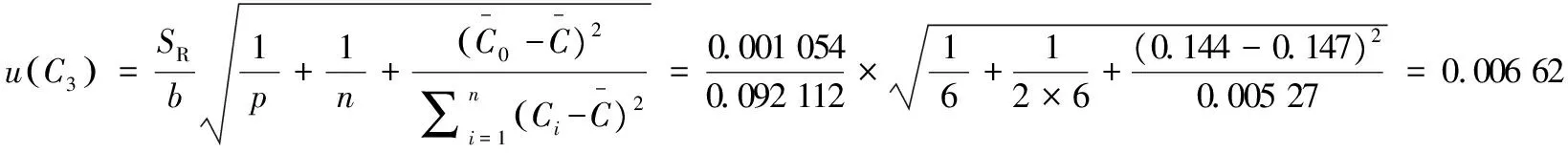
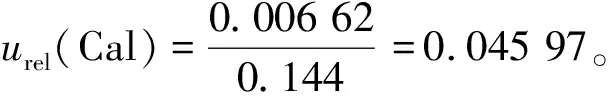
2.4 样品前处理引入的不确定度
2.4.1 样品称量引入的不确定度
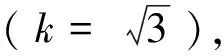
2.4.2 样品提取、净化、定容引入的不确定度
花椒在提取、净化、定容过程引入的不确定度主要是玻璃容量器具和室温变化。前处理室温度设为20 ℃,实际在±3 ℃范围内波动。乙腈和乙酸乙酯在20 ℃时的膨胀系数分别为1.37×10-3/℃和1.38×10-3/℃。本次提取、净化、定容所用到玻璃量具的相对标准不确定度结果见表3。

表3 前处理过程中移液管、移液枪的不确定度Table 3 Uncertainty of pipette and adjustable pipette in pretreatment
花椒提取、净化、定容引入的相对不确定度如公式(7)所示:
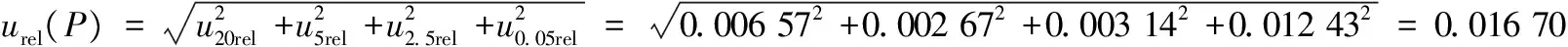
(7)
2.4.3 重复测量不确定度
由表2得花椒添加0.3 mg/kg重复测量6次的平均回收率为95.7%,其标准偏差S(X)计算如公式(8)所示:
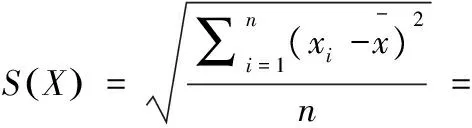
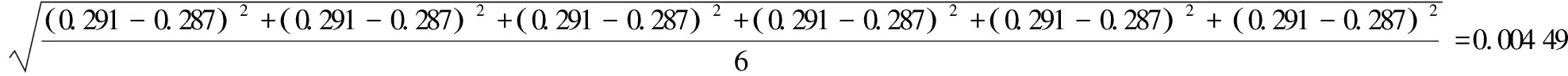
(8)
因此,前处理过程引入的不确定度如公式(9)所示:
(9)
2.5 分析仪器引入的不确定度

2.6 合成不确定度
由上述各相对标准不确定度分量合成花椒中添加氯菊酯相对标准不确定度如公式(10)所示:
urel(Z)
(10)
2.7 扩展不确定度
依据国家计量技术规范JJF 1135—2005《化学分析测量不确定度评定》[14]的要求,正态分布在95.45%置信区间时包含因子k=2。花椒中添加0.3 mg/kg 氯菊酯的测量值为0.287 mg/kg,则花椒中氯菊酯含量测定的相对扩展不确定度为Urel=k×urel(Z)=2×0.063 49=0.127,扩展不确定度为U=Urel×W=0.127×0.287= 0.036 4 mg/kg。
2.8 测量不确定度报告
花椒中添加0.3 mg/kg氯菊酯测量结果表示为:(0.287±0.036 4) mg/kg,k=2。其相对标准不确定度统计见表4。

表4 相对标准不确定度统计结果Table 4 The statistics of the relative standard uncertainty
3 结论
采用GB 23200.113—2018《食品安全国家标准 植物源性食品中208种农药及其代谢物残留量的测定 气相色谱-质谱联用法》中GC-MS/MS法测定花椒中添加0.3 mg/kg氯菊酯的结果平均值为0.287 mg/kg,扩展不确定度为0.036 4 mg/kg (k=2),测量结果表示为(0.287±0.036 4) mg/kg。由表4可知,本方法不确定度来源中标准曲线拟合引入的不确定度为最大影响因素,其次是标准工作液配制过程和分析仪器引入的不确定度。样品前处理对不确定度也有一定贡献,氯菊酯标准储备液配制的影响最小。依据本研究结果,建议在GC-MS/MS检测菊酯类农药过程中选用精度较好的量器,规范移液管和容量瓶的操作,确保标准工作溶液浓度的准确性;选择拟合线性高的工作曲线进行校准;对分析仪器进行日常维护和按时检定;适当增加平行样,规范前处理步骤,进一步提高检测结果的准确度。