食品中副溶血性弧菌检测能力验证结果与分析
2021-11-03陈玥梁颖思周露
陈玥 梁颖思 周露
(广东省食品检验所(广东省酒类检测中心),广东白云 510080)
1 前言
副溶血性弧菌(Vibrioparahaemolyticus)为革兰氏阴性杆菌,是一种嗜盐性细菌。食用含有该菌的食物可导致食物中毒,常见于鱼、虾、蟹、贝类和海藻等海产品及盐渍食品中。副溶血性弧菌一直是食源性疾病的主要致病因子,在亚洲国家和美国等地区尤为严重,在日本和东南亚,近50%的食物中毒事件是由副溶血性弧菌引起的[1];在美国,每年因副溶血性弧菌污染导致约8万人患病、100人死亡[2]。
我国沿海地区水产养殖和捕捞产业发达,动物性水产品食源性污染应引起重视。广东省疾病预防控制中心监测显示,2017—2018年有45起感染事件由副溶血性弧菌引起,感染病例840人,是广东省食源性致病感染的主要病原菌[3]。受人类活动影响,一些嗜盐性弧菌环境适应性增强,甚至出现耐药性[4-5],2006—2019年,广州市市售动物性淡水产品副溶血性弧菌总体检出率达21.84%[6],因此,副溶血性弧菌检验能力尤为重要。
对实验室检验人员进行能力验证是检验机构内部质量控制的重要措施,根据CNAS-CL09:2013《检测和校准实验室能力认可准则在微生物检测领域的应用说明》[7],通过实施能力验证评估检验人员能力和确认其资格,是确保实验室检验质量满足要求的重要手段之一。因此,为提高对食品中副溶血性弧菌的检测能力,增强实验室的竞争力,本实验室参加了由中国检验检疫科学研究院测试评价中心策划的副溶血性弧菌检验能力验证活动。本文总结了这次副溶血性弧菌能力验证的分离与鉴定过程,旨在为副溶血性弧菌的相关检测提供参考。
2 材料
2.1 仪器
Milli-Q Reference超纯水机(德国默克化工技术有限公司);PL6001E电子天平(梅特勒-托利多仪器有限公司);HWS-24电热恒温水浴锅(上海一恒科技仪器有限公司);LRH-250F生化培养箱(上海一恒科学仪器有限公司);SW-CJ-2F超净工作台(苏州安泰空气技术有限公司);AC2-4S1生物安全柜(新加坡ESCO公司);SX-700高压灭菌锅(日本TOMY公司);MALDI-TOF/TOF 4800基质辅助激光吸/电离飞行时间质谱仪(法国梅里埃公司);7500实时荧光PCR仪系统(美国ABI公司)。
2.2 试剂
3%氯化钠碱性蛋白胨水(广东环凯公司);3%氯化钠胰蛋白胨大豆琼脂(广东环凯公司);硫代硫酸盐柠檬酸盐胆盐蔗糖(thiosulfate citrate bile salts sucrose,TCBS)琼脂培养基(广东环凯公司);副溶血性弧菌生化鉴定盒(广东环凯公司);革兰氏染色液(北京陆桥公司);弧菌显色培养基(法国科马嘉公司);CHCA基质(法国梅里埃公司);副溶血性弧菌免核酸提取核酸检测试剂盒(卡尤迪生物)。
2.3 实验样品
样品编号为20-T923、20-S871的2份真空包装白色冻干块状样品(中国检验检疫科学研究院测试评价中心)。
3 实验方法
3.1 检验依据
2名人员根据中国检验检疫科学研究院测试评价中心提供的《食品中副溶血性弧菌(定性)能力验证参试指导书》,对2份样品进行前处理,并按照GB 4789.7-2013《食品安全国家标准 食品微生物学检验 副溶血性弧菌检验》[8]进行后续的副溶血性弧菌分离、纯化、鉴定。同时使用副溶血性弧菌免核酸提取试剂盒(PCR-荧光探针法)进行快速检测,并以VITEK MS快速检测分析分离出的可疑菌落,最终综合以上实验结果进行报告。
3.2 检验步骤
3.2.1 前处理
按照中国检验检疫科学研究院测试评价中心提供的ACAS-PT909《食品中副溶血性弧菌(定性)作检测业指导书》指导的方法,首先分装60 mL和225 mL的3%氯化钠碱性蛋白胨水;样品开启后,立即加入5 mL的3%氯化钠碱性蛋白脉水进行水化;待溶解后,吸出放入无菌瓶中,再反复用余下的3%氯化钠碱性蛋白胨水清洗西林瓶内壁,回收清洗液放入上述无菌瓶中,此溶液即是待测样品原液。操作各环节应保证无菌和充分混匀。本次冻干的能力验证品复原后等于60 mL的待测食品样品。同时将质控菌株ATCC 17802副溶血性弧菌作为阳性对照加入225 mL 3%氯化钠碱性蛋白胨水,并设置空白对照进行实验。
3.2.2 GB 4789.7-2013定性检测法鉴定菌株
增菌培养:使用振荡器震荡使得原液充分混匀,以无菌操作分别取样品原液25 mL,加入3%氯化钠碱性蛋白胨水225 mL,用均质器均质,制备成1∶10的样品匀液,并置于培养箱36℃培养18 h。
分离:将2袋增菌液,分别用接种环沾取1环增菌液,于TCBS平板和弧菌显色培养基平板上划线分离,培养箱36℃培养24 h。
纯培养:在TCBS平板和弧菌显色培养基平板上分别挑取3个可疑菌落,划线接种3%氯化钠胰蛋白脉大豆琼脂平板,于培养箱36℃培养24 h。
鉴定:从上一步的培养基中挑取单菌落进行镜检、氧化酶试验、嗜盐性试验及三糖铁琼脂穿刺,再根据情况使用生化试剂盒进行确定鉴定。
3.2.3 MALDI-TOF MS鉴定菌株
样品增菌、分离、纯培养与国标法同步进行,从纯培养的3%氯化钠胰蛋白脉大豆琼脂平板上挑取新鲜单菌落,厚薄均匀地涂布于VITEK MS靶板上,并立即在靶孔加上HCCA基质液(1μL/孔),以防气溶胶污染。待基质晾干后,转移至质谱仪中,按照说明书进行菌株质谱采集及特征性鉴定,并对数据进行处理分析。
3.2.4 Real-time PCR法鉴定菌株
样品增菌、分离与国标法同步进行,接种可疑菌落至5 mL脑心浸出液肉汤 (brain heart infusion broth,BHI)中,36℃培养24 h,所得菌液即可进行鉴定。依照副溶血性弧菌免核酸提取核酸检测试剂盒的操作说明书对BHI菌液进行鉴定。
PCR反应条件:第一阶段:95℃,5 s,10个循环;55℃,5 s,1个循环。第二阶段:95℃,1 min,1个循环。第三阶段:95℃,5 s,40个循环;60℃,30 s,40个循环。
4 结果与分析
4.1 分离和提纯
样品20-S871和20-T923在TCBS和弧菌显色平板上分离划线培养,并挑取可疑菌株进行分离提纯和生化鉴定(编号为1-6)。菌落形态表现详见表1。

表1 选择性分离培养基上菌落形态
4.2 生化鉴定结果
将分离提纯后的6个菌落进行革兰氏染色镜检,编号为3的菌落为革兰氏阳性菌,呈棒状;其余的均为革兰氏阴性菌,呈棒状。氧化酶试验、三糖铁琼脂穿刺及嗜盐性试验初步鉴定后(见表2),经生化试剂盒鉴定,样品20-S871检出副溶血性弧菌;样品20-T923未检出副溶血性弧菌,生化结果详见表3。
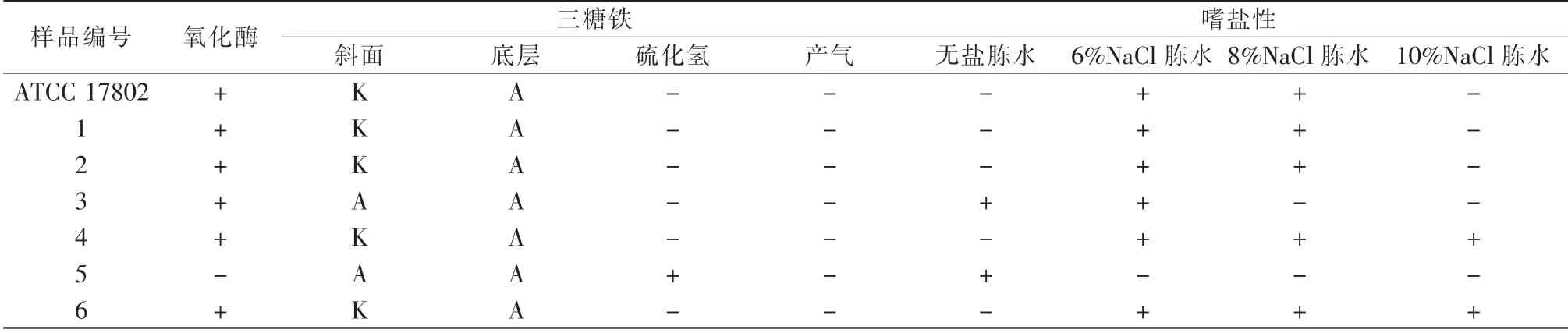
表2 氧化酶试验、三糖铁琼脂穿刺及嗜盐性试验结果

表3 生化实验结果
4.3 Real-time PCR法鉴定结果
在此项鉴定实验中,阳性对照2的FAM通道的CT值为21.280,样品1和样品2的FAM通道的CT值分别为8.961和9.046,均小于28,且有对应的指数增长扩增曲线,即鉴定为副溶血性弧菌阳性。实验图谱见图1。
4.4 MALDI-TOF MS鉴定结果
使用直接涂抹法进行质谱分析,结果显示6株菌株均可鉴定到种水平,且可信度均达99.9%。结果详见表4。

表4 6种菌鉴定结果
5讨论
在本次能力验证,样品编号为20-S871的检出副溶血性弧菌,20-T923的未检出副溶血性弧菌,结果满意,说明本实验室检测人员具备检测副溶血性弧菌的能力。在实验过程中,挑取的初期增菌液较多,导致菌落几乎蔓延至整块TCBS平板,分离出的单菌落较少,若样品中存在多种干扰菌株则容易出现漏检情况。建议通过结合使用TCBS和弧菌显色培养基,筛选出目标菌株。鉴于存在易混淆变异菌株干扰或不典型目标菌株[9-11]的可能,如在TCBS平板上出现显色相近的一类海洋弧菌、创伤弧菌、拟态弧菌等,或在弧菌显色平板上出现非典型淡紫色菌落,应挑取可疑菌落进行生化鉴定,日常检验中需要凭借经验结合实际情况,使用多种方法对菌落进行确证。
使用传统检测方法鉴定副溶血性弧菌需要5 d,通过结合PCR-荧光探针法进行确证,可以直接判断样品中是否存在目标菌株,使检测时限将缩短到2~3 d,对日常检测工作具有积极影响。MALDITOF MS具有高特异性、高灵敏度、高通量、速度快等优点[12-13],近年来应用于对致病菌进行快速识别技术,得到了快速发展。在本次实验中,MALDI-TOF MS的鉴定结果的可信度高、检测效率高。通过多种方法辅助鉴别,保证了本次实验结果的准确性。
近年来副溶血性弧菌的检测方法呈现多样化,如以免疫层析法[14]为代表的免疫学检测法;以多重PCR法[15-16]、环介导等温扩增法[17-18]为代表的分子生物学检测法等。熟悉各检测方法的不同特征和优缺点,结合实际情况实现快速鉴别,可以节省检测时间,提高食品检验工作效率。
