苗药滚山珠HPLC指纹图谱及化学模式识别研究
2021-11-03陈华国龚小见
文 敏,周 欣,赵 超,陈华国,龚小见*
1贵州师范大学 贵州省山地环境信息系统与生态环境保护重点实验室;2贵州师范大学 喀斯特山地生态环境保护与资源利用协同创新中心;3贵州师范大学 贵州省药物质量控制及评价技术工程实验室;4贵州师范大学 天然药物质量控制研究中心,贵阳 550001
滚山珠(PrionobelumqianensisChen),为泽马陆科(Zephroniidae)锯刺马陆属(Prionobelum)黔锯刺马陆的干燥全虫,体呈扁长圆柱形,栖息于山坡较潮湿处、枯枝腐叶或石块下,主要分布于贵州、云南等地区。滚山珠为药用全虫,具有清热、消肿止痛,舒筋活血等功效,主要用于治疗筋脉拘挛、跌打损伤、骨折肿痛等病状,在《中华本草-苗药卷》《贵州苗族医药研究与开发》等书籍中均有记载[1,2]。在贵州苗族地区,用于炎症的治疗非常广泛,对肿瘤的治疗效果极其显著。但是,目前国内外关于滚山珠的相关基础研究非常薄弱,更缺乏质量控制标准体系,严重制约了滚山珠药材的合理开发和广泛利用[3,4]。
指纹图谱是基于对物质群整体作用的认识,借助于波谱或色谱等技术获得的中药化学成分的波谱或色谱图,是实现鉴别产品真实性、评价质量一致性和产品稳定性的可靠手段[5,6,7]。因此,本研究采用HPLC法建立了滚山珠指纹图谱,并进行相似度评价,通过聚类分析[8,9](cluster analysis,CA)、主成分分析[10,11](principal component analysis,PCA)及正交偏最小二乘-判别分析[12,13](orthogonal partial least squares analysis,OPLS-DA)等化学模式识别方法,筛选出引起不同批次滚山珠成分差异的主要标志性成分,旨在为苗药滚山珠的质量控制及进一步研究提供参考[14,15]。
1 仪器与材料
1.1 仪器
DIONEX Ultimate300 高相液相色谱仪(美国Thermo Fisher Scientific公司);KQ-300DE 型数控超声波清洗器(昆明市超声仪器有限公司);明澈TM-D24UV纯水/超纯水系统(法国Millipore公司);XS-105DU 十万分之一和AL204万分之一电子分析天平(梅特勒-托利多仪器上海有限公司)。
1.2 材料
酪氨酸对照品(中国食品药品检定研究院,批号:140609-201513);甲醇、乙腈(购于美国TEDIA公司)均为色谱纯;食用酒精(购于贵州凯鑫工贸有限公司)为食品级;水为超纯水;其余试剂均为分析纯。滚山珠药材自采于贵州省各地区或购于安徽、四川、广西、云南、海南等地,经贵州省生物研究所陈会明副研究员鉴定为泽马陆科动物黔锯刺马陆的全体Prionobelumqianensis的干燥全虫。具体信息见表1。

表1 24批药材来源信息Table 1 Source information of 24 batches of medicinal materials
2 方法与结果
2.1 供试品溶液的制备
取滚山珠药材粉末(过60目筛)1.0 g,精密称定,加70%食用酒精15 mL,超声提取30 min,过滤,滤液浓缩蒸干,用甲醇定容至10 mL,过0.45 μm微孔滤膜,并置于4 ℃冰箱冷藏备用。
2.2 对照品溶液的制备
取酪氨酸对照品适量,精密称定,加水制成浓度为27.1 μg/mL的对照品溶液,并置于4 ℃冰箱冷藏备用。
2.3 色谱条件
色谱柱:Agilent ZORBAX SB-C18柱(250×4.6 mm,5 μm);流动相:甲醇(A)-0.1%乙酸水(B),梯度洗脱(0~15 min,1%→2% A;15~25 min,2%→8% A;25~30 min,8%→14% A;30~35 min,14%→25% A;35~47 min,25%→65% A;47~70 min,65%→85% A);检测波长:254 nm;流速:0.8 mL/min;柱温:25 ℃;进样量:2 μL。
2.4 方法学考察
2.4.1 精密度实验
精密吸取滚山珠供试品溶液,按“2.3”项下色谱条件连续进样测定6次,以4号酪氨酸色谱峰为参照峰(S),计算得到各共有峰的相对保留时间的RSD<0.32%,相对峰面积的RSD<1.16%,表明仪器精密度良好。
2.4.2 稳定性试验
取滚山珠供试品溶液,按“2.3”项下色谱条件,分别在0、4、8、16、24、36 h进样测定,以4号酪氨酸色谱峰为参照峰(S),计算得到各共有峰的相对保留时间的RSD<0.43%,相对峰面积的RSD<1.31%,表明供试品溶液在36 h内稳定性良好。
2.4.3 重复性试验
取同一批滚山珠样品6份,每份1.0 g,精密称定,按“2.1”项下方法制备供试品溶液,按“2.3”项下色谱条件进样测定,以4号酪氨酸色谱峰为参照峰(S),计算得到各共有峰的相对保留时间的RSD<0.52%,相对峰面积的RSD<1.56%,表明该方法重复性良好。
2.5 指纹图谱建立
分别取24批滚山珠各1.0 g,按“2.1”项下方法制备样品溶液,按“2.3”项下色谱条件进样测定,记录各色谱图。采用“中药色谱指纹图谱相似度评价系统(2012版)”对数据进行分析,以S1号样品的色谱图为参照图谱,时间窗宽度为0.1 min中位数法生成对照图谱R,经多点校正后进行色谱峰匹配,建立24批样品的叠加图谱及对照图谱,标定22个共有峰,经与对照品比对,确定4号色谱峰为酪氨酸(见图1~3)。指纹图谱的共有峰保留时间及峰面积见表2。

图1 24批药材的HPLC叠加指纹图谱Fig.1 HPLC superposed fingerprints of 24 batches of medicinal materials

图2 药材HPLC对照指纹图谱Fig.2 HPLC control fingerprints of medicinal materials

图3 酪氨酸对照品溶液的HPLC色谱图Fig.3 HPLC chromatogram of tyrosine reference
2.6 相似度评价
相似度评价采用“中药色谱指纹图谱相似度评价系统(2012版)”对24批滚山珠的HPLC指纹图谱进行相似度评价,结果见表3。24批滚山珠指纹图谱的相似度除花溪S8在0.739以外,其余均在0.844~0.957之间,表明24批样品间差异较小。

2.7 聚类分析
运用SPSS.26软件,采用组间联结法,以平方欧式距离为测度对24批滚山珠样品进行聚类分析(见图4)。24批样品聚为3类:第一类是S1、S3、S4、S5、S15、S16、S19、S20,它们来自2020年于贵州省以外的各省采购的样品;第二类是S8,它是来自2018年采集于贵州省花溪区;第三类是S2、S6~S7、S9~S14、S17~S18、S21~S24,它们除S9、S24以外都是来自2015~2016年间在贵州省内各地采集的。聚类分析结果表明各批次总体差异性较小,其差异性表现出明显的地域差异性,可能与其生长环境、生长年限和气候条件等有关,但具体原因有待进一步研究。

图4 24批药材样品的聚类分析Fig.4 Cluster analysis of 24 batches of medicinal materials
2.8 主成分分析
以共有峰的相对峰面积为变量,利用SPSS26软件对24批样品进行主成分分析,计算相关矩阵的特征值及其方差贡献率[11]。以特征值>1为提取标准,得到了前5个主成分的累积方差贡献率为89.063%,能够较好的代表指纹图谱中的大部分信息,结果见表4。从成分载荷矩阵表可以看出,第一主成分的独立方差贡献率为43.640%,主要反映色谱峰1~5、8、11、12、13、17、18、20、21的信息;第二主成分的独立方差贡献率为20.679%,主要反映色谱峰6、7、9、10、14~16的信息;第三主成分的独立方差贡献率为10.762%,主要反映色谱峰4、6、19的信息;第四主成分的独立方差贡献率为9.235%,主要反映色谱峰22的信息;第五主成分的独立方差贡献率为4.748%,主要反映色谱峰1的信息。

表4 24批药材主成分特征值及方差贡献率Table 4 Characteristic value and variance contribution rate of 24 batches of medicinal materials
利用SIMCA 14.1软件计算主成分得分(见图5)。结果表明24批药材可大致分为三类,S1、S3、S4、S5、S15、S16、S19、S20为第一类;S8为第二类;S2、S6、S7、S9~S14、S17、S18、S21~S24为第三类,其结果与聚类分析结果一致。
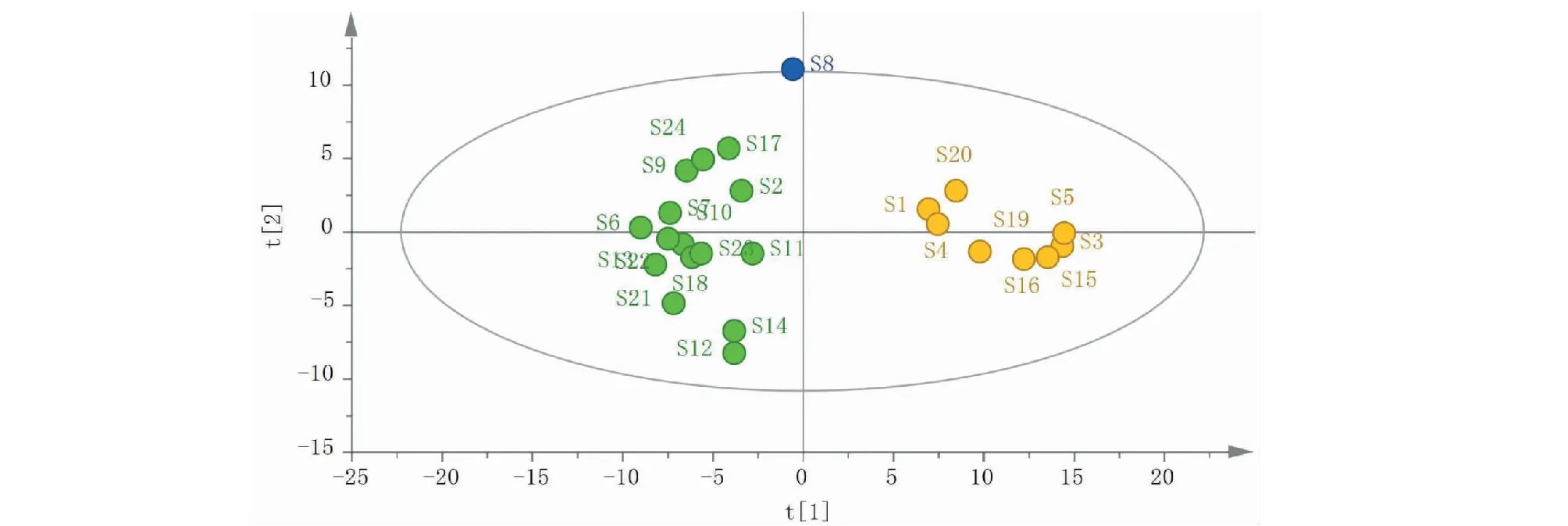
图5 24批药材主成分分析得分Fig.5 Score of principal component analysis of 24 batches of medicinal materials
2.9 正交偏最小二乘判别分析
采用SIMCA 14.1软件对各样品共有峰峰面积进行正交偏最小二乘判别分析,结果见图6。不同批次样品可聚为3类,与聚类分析和主成分分析结果一致。提取模型中的22个变量的VIP值(见图7),变量重要性投影值(VIP)是筛选差异性化合物的重要指标,VIP值越高,对组间差异的影响越大[16]。以VIP>1为阈值,色谱峰从大到小分别为17号峰(VIP=3.155 9)、2号峰(VIP=1.459 1)、1号峰(VIP=1.437 8)、12号峰(VIP=1.032 5)、11号峰(VIP=1.020 7),表明这5个色谱峰是影响滚山珠药材间质量差异的主要标志性成分,在之后的研究中应多关注这几个成分。

图6 24批药材正交偏最小二乘判别分析得分Fig.6 Score of orthogonal partial least squares discriminant analysis for 24 batches of medicinal materials
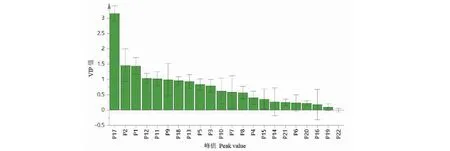
图7 药材的正交偏最小二乘判别分析VIP值Fig.7 VIP value of orthogonal partial least squares discriminant analysis
3 讨论
3.1 色谱条件优化
试验前期考察了甲醇、乙腈洗脱系统对色谱峰分离效果的影响,结果显示甲醇为流动相时分离效果较好,且基线平稳;考察了甲醇-0.1%甲酸水和甲醇-0.1%乙酸水的分离效果,最终选择分离效果较好的甲醇-0.1%乙酸水系统;分析了210~400 nm处全波长扫描的图谱,显示在254 nm下出峰数量多,基线平稳,信号响应值大;通过考察不同流速(0.8、1.0、1.2 mL/min)、柱温(25、30、35、40 ℃)对色谱峰的影响,确定选择流速为0.8 mL/min,柱温25 ℃。
3.2 供试品溶液制备方法优化
试验前期考察了超声和回流2种提取方式,发现其提取效率无明显差别,故选择操作较简单的超声提取;比较了水、甲醇、食用酒精作为提取溶剂,结果显示,食用酒精提取时色谱峰数目多、响应值较大。并比较不同浓度食用酒精(30%、50%、70%、90%)的提取效果,结果表明,70%食用酒精提取时色谱峰响应值较大。综合考虑,选用70%食用酒精超声提取作为供试品溶液的制备方法。
3.3 小结
本研究首次建立了苗药滚山珠的指纹图谱,24批样品指纹图谱的相似度在0.739~0.957,指认了1个成分。通过化学模式识别分析,建立了滚山珠的聚类分析、主成分分析和正交偏最小二乘判别分析的分类模型,明确了样品之间的归类情况。24批样品聚为3类,筛选得到影响滚山珠药材间质量差异的5个主要标志性成分。
综上所述,本研究建立的HPLC指纹图谱方法稳定、可靠、重复性好,可为苗药滚山珠药材的质量控制提供参考。
