光活化过硫酸钾体系下直接蓝15降解动力学及其降解机制
2021-11-03陈聘婷
胡 倩,阳 海,李 鑫,陈聘婷,陈 镇,易 兵
(湖南工程学院 环境催化与废弃物再生化湖南省重点实验室,湖南 湘潭 411104)
双偶氮染料直接蓝15(DB15)主要用于纤维素纤维的染色和印花,为适用范围较为广泛的一类蓝色染料。当前对DB15的研究报道主要集中在脱色率和毒性方面,利用深度氧化技术对其降解过程与机制的研究相对较少[22]。为此,本文选取DB15为目标化合物,利用紫外光(UV)和K2S2O8体系对目标偶氮染料DB15进行降解动力学和转化迁移机制探究。通过考察K2S2O8质量浓度、底物初始浓度和反应温度对其降解动力学的影响得出最佳降解条件。最后,通过对自由基鉴定以及结合降解中间产物和前线电子云密度计算得出DB15在UV/K2S2O8体系下的降解机制。
1 实验部分
1.1 试剂与仪器
直接蓝15(DB15)、过硫酸钾(K2S2O8)、无水硫酸钠(Na2SO4),均为AR级;甲醇(EtOH)、乙酸乙酯(EA)和二氯甲烷(DCM),均为GR级。
净水系统(默克密理博实验室设备有限公司,内置主波长172 nm的灯光以保持总有机碳的总含量 ≤13 μg/L),EMX EPR/band电子顺磁共振仪(德国布鲁克分析仪器公司),HPLC 2030高效液相色谱仪(日本岛津公司),GCMS QP2010气质联用仪(日本岛津公司)。
1.2 实验方法
移取100 mL浓度为100 μmol/L的DB15标准溶液于双层夹空派克玻璃反应器中,汞灯光源与反应器距离15 cm处于平行位置。反应装置如图1所示。向光反应器中加入一定量的K2S2O8,开启磁力搅拌器保持反应液恒速搅拌。反应温度通过循环水装置连接双层夹空派克玻璃反应器来控制反应温度,误差在± 0.5 ℃。设置取样时间间隔用移液枪每次移取出2 mL反应溶液于等体积甲醇的离心管中,甲醇用于淬灭反应停止。反应液用0.22 μm滤膜过滤后收集于细胞瓶用于高效液相色谱仪(HPLC)分析。降解中间产物的鉴定是用EA和DCM分别萃取3次反应液,分别合并有机相,干燥,过滤后脱溶,然后用移液枪分别移取1 mL EA和DCM反复洗脱溶瓶,最后移至细胞瓶内用于气质联用仪(GCMS)分析[23-24]。

1—磁力搅拌器;2—反应容器;3—灯源冷却装置;4—光源。图1 光源及反应装置示意图Fig.1 Light source and reaction device
1.3 分析表征方法
利用高效液相色谱仪对降解率进行定量分析。检测条件:柱温为30 ℃,进样量为 20 μL,流动相 A(甲醇)与B(H2O)体积比为65∶35,波长λ为625 nm,流速为 0.5 mL/min。
利用气质联用仪对降解产物进行定量分析,之后对目标化合物采用面积归一化法进行分析。检测条件:柱温初始温度为60 ℃,稳定2 min,接着以速度10 ℃/min升温至200 ℃,稳定1 min,再以10 ℃/min 升高至275 ℃,稳定10 min;载气He气总流量为1.5 mL/min,不分流,离子源为70 eV的EI源,离子源温度为200 ℃,进样口和连接杆温度为260 ℃,自动进样,进样量为1.0 μL。
利用电子顺磁共振仪鉴定自由基。5,5-二甲基-1-吡咯啉-N-氧化物(DMPO)作为自旋捕获试剂。K2S2O8水溶液在UV光照10 min后取样,置于100 μL样品管中测定。
根据文献[25-26]方法,利用Guassian 09软件,计算前线电子云密度(FEDs)。
2 结果与讨论
2.1 DB15降解可行性研究
双偶氮染料DB15在UV、K2S2O8和UV/K2S2O体系中的降解情况如图2(a)所示。由图可以看出:100 μmol/L 的DB15在UV光照120 min,降解率仅有7.67%;不光照只加入1 g/L K2S2O8条件下降解率为42.23%;而在UV/K2S2O8体系下降解率可达到71.44%。
进一步采用朗格穆尔-欣谢尔伍德的简化方程对DB15在UV/K2S2O8体系下的降解过程进行模拟。
-dc0/dt=kc
式中:c0为DB15初始浓度;c为不同反应时间段DB15的浓度;t为反应时间;k为假一级动力学常数。如图2(b)所示,-ln (c/c0)对时间呈现良好的线性关系,DB15在UV/K2S2O8体系下降解符合假一级动力学模型,其动力学常数k为0.010 7 min-1。

图2 DB15在不同体系中的降解曲线及在UV/K2S2O8体系-ln(c/c0)与时间的关系Fig.2 Degradation of DB15 in different systems (a)and relationship between -ln(c/c0)and time(b)
2.2 K2S2O8质量浓度对DB15降解效果影响
K2S2O8质量浓度(0.25、0.5、1.0、2.0和3.0 g/L)对DB15降解动力学的影响如图3所示。随着K2S2O8质量浓度的增加,降解速率不断加快,原因是K2S2O8质量浓度越大,单位时间产生活性氧物种越多,越有利于DB15的降解。在K2S2O8质量浓度为1.0 g/L时,降解速率较大,随K2S2O8质量浓度增加降解速率也随着上升,但是上升趋势有所平缓。所以选择DB15在该体系下K2S2O8质量浓度为1.0 g/L进行后续实验。
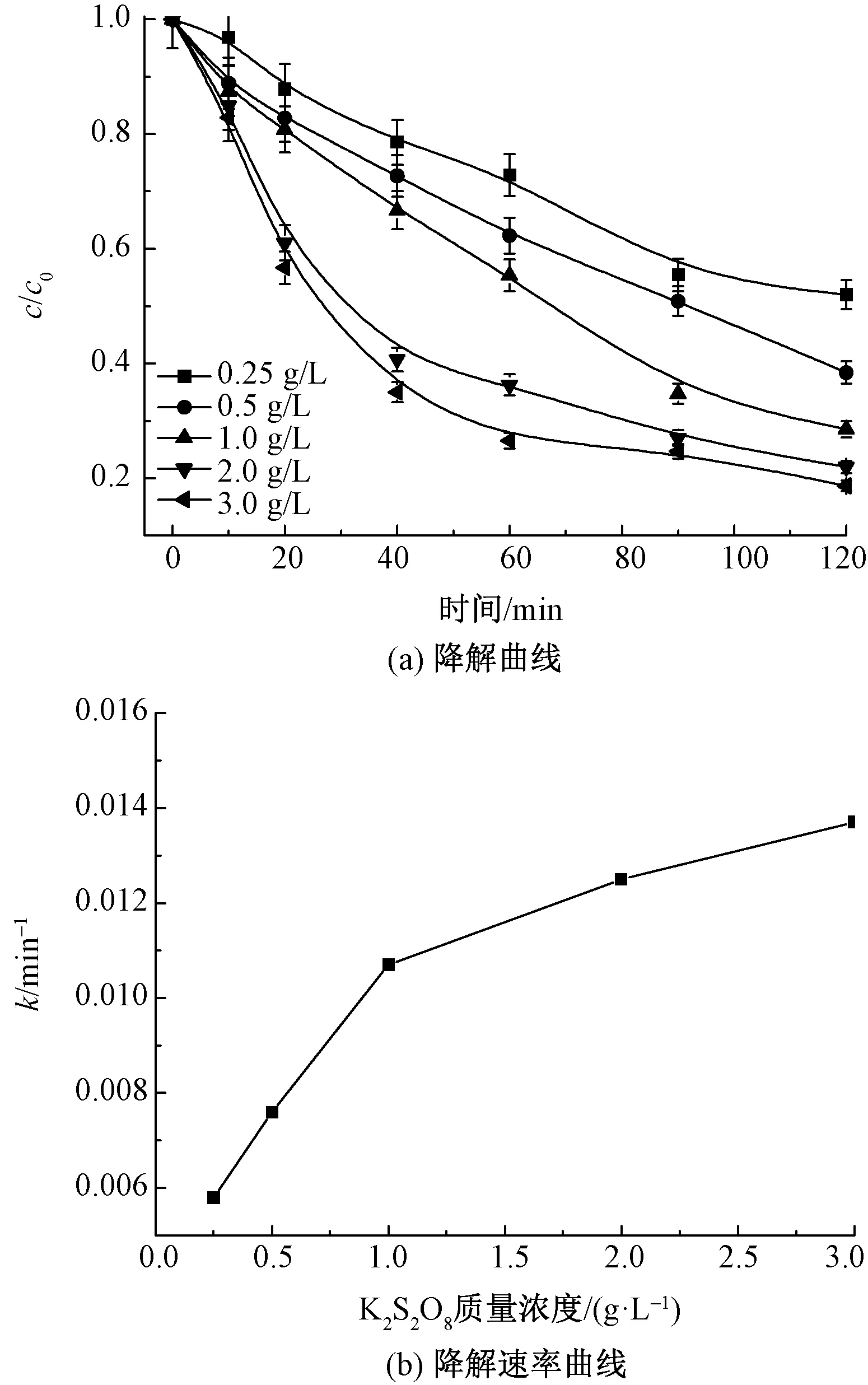
图3 K2S2O8质量浓度对DB15的降解曲线以及对DB15降解速率的影响Fig.3 Degradation curves of DB15 under different K2S2O8dosage (a)and effect of K2S2O8 dosage on degradation kinetics of DB15(b)
2.3 底物浓度对DB15降解效果影响
确定K2S2O8质量浓度为1.0 g/L,温度为25 ℃,探讨底物初始浓度(25、50、100、200和400 μmol/L)对DB15降解动力学的影响,结果如图4所示。由图4(a)可知,随着底物初始浓度的增大,DB15降解速率逐渐降低。由图4(b)可知,降解速率随着底物浓度增大不断减小,原因是由于一定量的K2S2O8在紫外光活化下产生的活性氧物种(ROSs)是一定量的,随着底物浓度的增大会竞争ROSs使得DB15在UV/K2S2O体系下降解速率下降[27]。
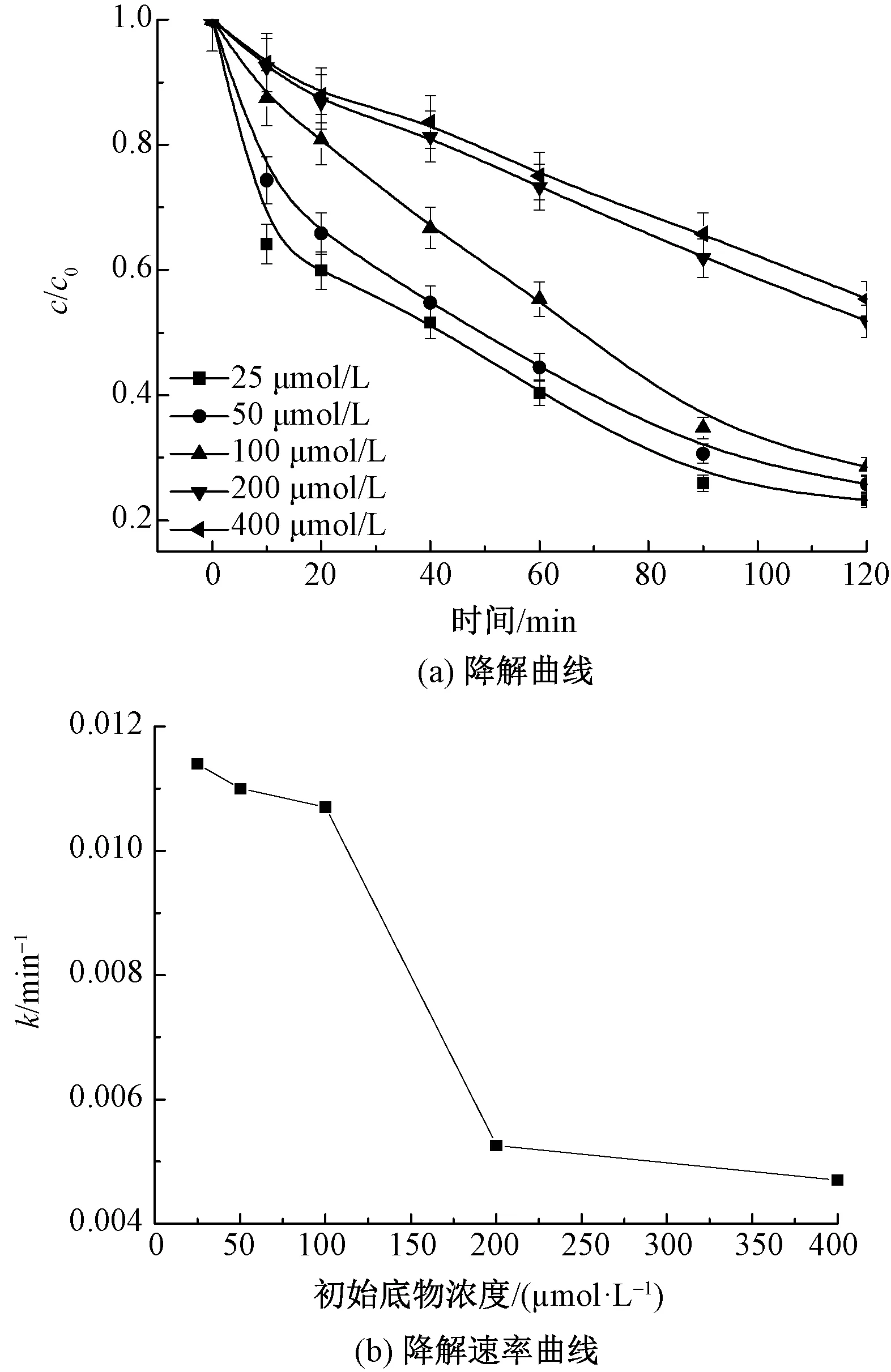
图4 底物初始浓度对DB15的降解曲线以及对DB15降解速率的影响Fig.4 Degradation curves of DB15 under different substrate concentration (a)and effect of substrate concentration on degradation kinetics of DB15(b)
2.4 温度对DB15降解效果的影响


图5 不同反应温度对DB15的降解曲线和底物初始浓度对DB15降解速率的影响Fig.5 Degradation curves of DB15 under different reaction temperature (a)and effect of different reaction temperature on degradation kinetics of DB15(b)
2.5 UV/K2S2O8体系中自由基的鉴定

2.6 DB15在UV/K2S2O8体系中降解机制
降解产物P6的m/z为331,该化合物可能为3,6-二氨基-4-羟基萘-2,7-二磺酸盐。降解产物P7的m/z为126,该化合物可能为苯-1,2,4-三醇。降解产物P8的m/z为112,该化合物可能对应邻二苯酚。降解产物P9的m/z为191,该化合物可能为7-氨基萘-1,3,5-三醇,该化合物的裂解碎片173可能是[M-H2O]。降解产物P10的m/z为223,该化合物可能为7-硝基萘-1,3,5-三醇。降解产物P11的m/z为125,该化合物可能对应着4-氨基苯-1,3-二醇。
利用DB15的前线电子云密度(FDEs)进一步对其活性位点进行预测计算,结果如表2所示。

表2 DB15的前线电子云密度(FDEs)计算结果Tab.2 DB15 frontier electron densities (FEDs)calculation results

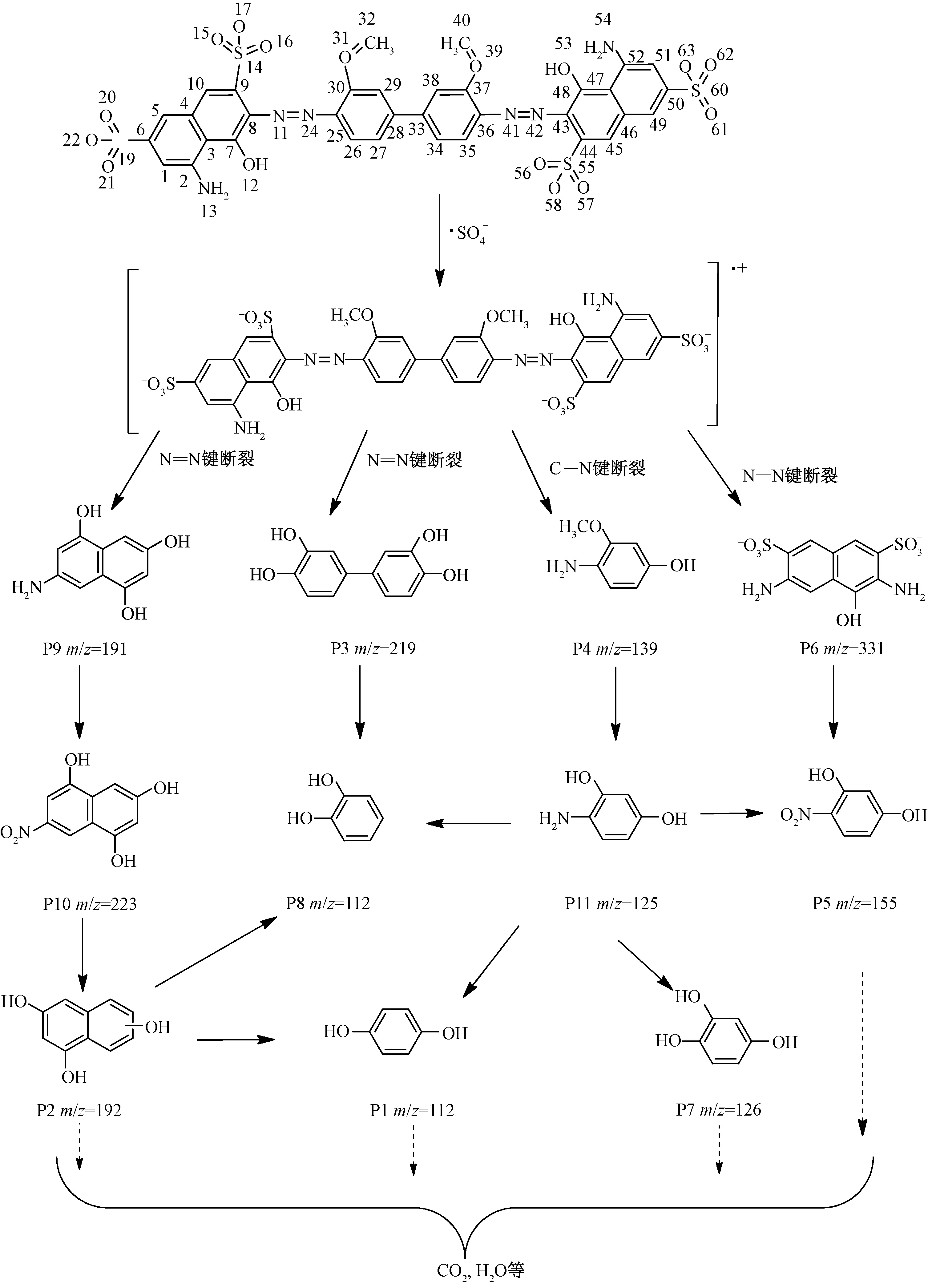
图8 DB15在UV/K2S2O8体系下可能的光催化途径Fig.8 Proposed degradation pathways of DB15 in UV/K2S2O8 system
3 结 论
1)双偶氮染料直接蓝15(DB15)在光解和K2S2O8体系下降解效果都不佳,在UV/K2S2O8体系中,当底物浓度为100 μmol/L,K2S2O8质量浓度为1 g/L 时,降解率可达到71.44%。通过单因素实验发现,底物初始浓度、温度和 K2S2O8质量浓度对UV/K2S2O8体系降解DB15影响显著。

