4种原核表达双链RNA的dsRNA提取方法效果评价
2021-11-02付开赟廖兰兰丁新华郭文超吐尔逊阿合买提
常 瑞,王 俊,付开赟,廖兰兰,丁新华,何 江,郭文超,吐尔逊·阿合买提,任 羽
(1.喀什大学生命与地理科学学院,新疆喀什 844006;2.新疆农业农村厅植物保护站,乌鲁木齐 830049;3.新疆农业科学院植物保护研究所/农业部西北荒漠化绿洲作物有害生物综合治理重点实验室,乌鲁木齐 830091;4.新疆农业科学院微生物应用研究所/新疆特殊环境微生物重点实验室,乌鲁木齐 830091)
0 引 言
【研究意义】马铃薯甲虫(LeptinotarsadecemlineataSay)是马铃薯毁灭性害虫。持续化学防治使马铃薯甲虫对部分拟除虫菊酯、氨基甲酸酯、有机磷、新烟碱类和微生物杀虫剂产生了抗性[1]。使用RNAi技术,喂食马铃薯甲虫涂抹dsRNA的马铃薯叶片,可有效降低、沉默马铃薯甲虫特定基因表达,抑制马铃薯甲虫的正常生长发育,具有高度专一性、安全性强,且植物生长发育不受影响,对挖掘更多生物防治策略具有重要意义[2]。但dsRNA生产成本高、产量无法预测、稳定性低。【前人研究进展】dsRNA在环境中极不稳定,自然条件下3~5 h就会完全降解;San等[3]发现dsRNA在紫外线照射下,4 h就会完全降解。并且其作用机制研究不系统,植物是否会传递、扩增dsRNA以及有害生物对RNAi敏感性差别大等因素[4]。目前,dsRNA主要通过3个方法大量生产:一是合成含有T7启动子的dsRNA特异性引物,运用体外合成试剂盒合成dsRNA[5,6]。二是原核生物发酵生产dsRNA,最早用于干扰秀丽引线虫,喂食秀丽引线虫时可产生强烈干扰。将构建完成的dsRNA表达载体导入RNase III缺陷型大肠杆菌HT115(DE3)感受态中,经异丙基硫代-β-D-半乳糖苷(IPTG)诱导,产生dsRNA[7,8]。三是通过转基因植物表达dsRNA,使植物具有“终生”防御性,害虫啃食植物后,可有效抑制其生长发育甚至直接死亡,无需人为干预[9,10]。【本研究切入点】方法可大量合成dsRNA,快速高效,合成dsRNA可直接使用,但体外合成试剂盒成本较高,实际大规模推广使用不切实际。方法可发酵得到大量dsRNA,且成本较低。但在发酵、诱导过程中,如何保证菌体高活性、持续产生dsRNA,仍需有待研究。针对RNAi的特异性以及原核发酵获得dsRNA良好的应用前景,以pET-2p和L4440为载体发酵产生dsRNA的实验方法为基础。研究筛选并试验4种提取菌液总RNA方法以提高菌液dsRNA的获取率。【拟解决的关键问题】利用720 bp绿色荧光蛋白gfp[11-13]为模板,分别随机改变碱基改变GC含量,并构建5组不同长度组合的dsgfp片段:201 bp长度的30%CG 含量的dsgfp(简称201-30CG,下同)、201-50CG、423-30CG、423-50CG、423-70CG。运用试剂盒体外合成以上5种dsgfp,检测其浓度、纯度作为参照标准。将以上10组表达载体原核发酵后,运用Trizol法、酚氯仿法、RNA-easy提取液、以及75%酒精沉淀法分别提取dsgfp。建立菌液表达dsRNA的最佳提取方法以及最优表达载体提供理论支持。
1 材料与方法
1.1 材 料
1.1.1 载体
pET-2p、L4440质粒实验室保存。
1.1.2 菌株
大肠杆菌HT115(DE3)菌株购自上海唯地生物技术有限公司,培养至二代菌株由该实验室保存。
1.1.3 主要试剂及仪器
试剂:Trans-T1感受态细胞、2xEasyTaqPCR Super Mix(全式金);琼脂糖(西班牙);LB broth(MDBio,Inc);卡那霉素(Kana)、四环素(Tet)、氨苄青霉素(Amp)、IPTG粉末;苯酚∶氯仿混合液(25∶24)等(Solarbio);质粒小抽提试剂盒、琼脂糖凝胶回收试剂盒(OMEGA);HiScribeTMT7High Yield RNA Synthesis Kit(NEB);限制性内切酶EcoRI、NotI、Hinglll、XhoI(Thermo);ClonExpressII One Step Cloning Kit、RNA-easy提取液(Vazyme);Trizol Reagent(ambion);焦炭酸二乙酯(DEPC,biosharp);异丙醇、无水乙醇均为分析纯;Dnase-/Rnase-free离心管、移液器枪头(Biologix)。
仪器:离心机(湘立TGL16M);PCR仪(ICycling 96梯度);摇床(TASITEDY-200B);电热恒温干燥箱(TASITE202-1AB);水浴锅(BATHS);核酸电泳系统(北京六一 DYY-6D);凝胶成像系统(Wealtec Dolphin1D);B-500 BIOPHOTO METER(METASH);-80℃冰箱(Thermo ULTS1368);超净工作台(江苏通净 VD-650);超纯水机(青岛富勒姆 FBZ0502-SUP)。
1.2 方 法
1.2.1dsgfp基因、引物合成
以来自于720 bpgfp的序列为模板,对其基因进行设计优化,随意改变碱基CG含量,交由南京金斯瑞生物科技有限公司完成基因合成。人工合成了5组不同长度组合的dsgfp片段:201 bp长度的30%CG 含量的dsgfp(简称201-30CG,下同)、201-50CG、423-30CG、423-50CG、423-70CG。以T7启动子为起始序列设计、合成引物,用于体外合成dsgfp。以XhoI、HindIII(L4440)和KpnI、NotI(pET-2p)为双酶切位点设计、合成引物,用于构建L4440-gfp和pET-2p-gfp表达载体。表1,图1

图1 不同长度、CG组合的dsgfp片段序列Fig.1 Sequence of dsgfp fragments of different lengths and CG combinations
1.2.2 重组表达载体构建
1.2.2.1 感受态细胞制备
HT115(DE3)二代甘油超低温保存菌种以1∶1 000接种于含四环素(Tet+)液体LB培养基中,37℃ 250 g离心力培养过夜。挑取单克隆37℃ 250 g离心力培养5 h。活化后菌液1∶100在LB液体培养基(Tet+)37℃ 250 g离心力培养2~3 h,至OD为0.4~0.6。将菌液冰上放置10 min,使温度降至0℃,0.1 mol/L CaCl2溶液同时放置冰上预冷。4℃ 4 000 g离心力10 min。沉淀中加入5∶1体积预冷后0.1 mol/L CaCl2溶液悬浮。冰上放置15~30 min,4℃ 4 000 g离心力10 min。沉淀加入25∶1体积0.1 mol/L CaCl2溶液和25∶1体积30%甘油,冰上放置10 min。菌体重悬,分装并-80℃保存。
1.2.2.2 目的基因PCR扩增及回收
以人工合成的目的片段为模板,使用表1引物进行L4440-gfp、pET-2p-gfp目的片段PCR反应:94℃ 3 min;94℃ 30s、61℃ 30s,每个循环降0.5℃、72℃ 30s,10个循环;94℃ 30s、56℃ 30s、72℃ 30s,35个循环;72℃10 min。1.5%琼脂糖凝胶电泳检测,切下目的条带运用试剂盒回收。
1.2.2.3 L4440-gfp与pET-2P-gfp表达载体的构建(1) L4440载体与pET-2p载体线性化
L4440载体双酶切体系为:6 μL DNA、2 μL XhoI、2 μL HindIII、2 μL 10xFastDigest Green Buffer、8 μL dd H2O,总体积为20 μL,37℃ 15 min;80℃ 10 min。pET-2p载体双酶切的体系为:6 μL DNA、2 μLNotI、2 μLKpnI、2 μL 10xFastDigest Green Buffer、8 μL dd H2O,总体积为20 μL,37℃15 min;80℃ 5 min。1%琼脂糖凝胶电泳,回收目的DNA。
(2) L4440-gfp与pET-2p-gfp重组载体构建与表达
使用ClonExpressII One Step Cloning Kit将线性化质粒与目的片段重组,反应体系为:10 μL重组产物加入100 μL Trans-T1感受态,涂布至固体LB培养基(L4440:氨苄青霉素Amp+、pET-2p:卡那霉素KaNa+)37℃倒置过夜。次日挑取单克隆37℃ 250 g离心力培养5 h。运用表1的引物进行菌液PCR验证。验证正确的菌液1∶100接种于LB液体培养基中(L4440:Amp+、pET-2p:KaNa+)37℃ 250 g离心力培养3.5 h,提取质粒进行双酶切验证,剩余菌液送北京华大基因公司测序。
将验证正确的质粒转入HT115(DE3)感受态,涂布至LB固体培养基上(L4440:Amp+、pET-2p:KaNa+)37℃倒置过夜。次日挑取单克隆37℃ 250 g离心力培养5 h。运用表1引物进行菌液PCR验证,保存验证成功的菌液。
1.2.3 dsgfp的诱导表达
将验证正确的菌液1∶1 000接种于LB液体培养基(L4440:Amp+、Tet;pET-2p:KaNa+、Tet+)37℃ 250 g离心力活化过夜。以1∶100接种于LB液体培养基(L4440:Amp+、Tet+;pET-2p:KaNa+、Tet+)37℃ 250 g离心力培养3.5 h,加入IPTG溶液继续振荡培养5 h。取1 mL菌液提取总核酸,1%琼脂糖电泳检测,Image J软件灰度分析电泳条带。将成功诱导dsgfp的菌液加50%甘油(1∶1)-80℃保存。
1.2.4 体外合成dsgfp
1.2.4.1 DNA模板制备
将成功诱导dsgfp的菌液1∶1 000接种于LB液体培养基(L4440:Amp+、Tet+;pET-2p:KaNa+、Tet+)37℃ 250 g离心力培养12~16 h提取质粒。运用含有T7启动子目的引物进行PCR反应,1.5%琼脂糖凝胶电泳检测,切下目的条带运用试剂盒回收。表1
1.2.4.2 体外转录、退火形成dsgfp
反应体系为:NTP Buffer Mix 10μL,Template DNA 8 μL(0.5 μg),T7 RNA polymerase Mix 2 μL,总体积为20 μL。37℃温浴4~6 h。将反应液于70℃水浴10 min,冷却至室温。加入10∶1体积Dnase I和Rnase A稀释液(稀释200倍),37℃ 30 min。取1 μL合成dsgfp溶于10 μL Nuclease-Free water,1.5%琼脂糖凝胶电泳检测,产物-80℃保存。
1.2.5 4种方法分别提取l4440-gfp和pET-2p-gfp表达dsgfp
1.2.5.1 Trizol法
取50 mL诱导菌液,4℃ 7 500 g离心5 min。沉淀加入50∶1体积 Trizol,震荡,室温放置5 min。加入5∶1体积氯仿,震荡15s,室温放置10 min,4℃ 12 000 g离心15 min。上清加入2∶1体积异丙醇,颠倒5~6次,室温静置10 min,4℃ 12 000 g离心力10 min。沉淀加入1∶1体积75%乙醇4℃ 7 500 g离心力5 min。重复洗涤1次。沉淀室温静置5~10 min后加入30 μL DEPC水。溶解的dsRNA加入10∶1体积稀释的Rnase A和Dnase I消化后,37℃ 15 min,-80℃保存。
1.2.5.2 酚氯仿法
取50 mL诱导菌液,4℃ 7 500 g离心力5 min。沉淀加入100∶1 体积STE buffer,涡旋振荡。加入1∶1体积苯酚:氯仿混合液(25∶24),涡旋100s。4℃ 15 000 g离心力15 min,上清加入2∶1体积异丙醇,室温静置10 min,4℃ 12 000 g离心力10 min。沉淀加入1∶1体积 75%乙醇4℃ 7 500 g离心力5 min。重复洗涤1次。沉淀室温静置5~10 min后加入30 μL DEPC水。溶解的dsRNA加入10∶1体积稀释的Rnase A和Dnase I消化后,37℃ 15 min,-80℃保存。
1.2.5.3 RNA-easy提取液
取50 mL诱导的菌液,4℃ 7 500 g离心力5 min,1xPBS清洗沉淀。加入100∶1体积 RNA-easy提取液,室温12 000 g离心力15 min。上清加入1∶1体积异丙醇,室温静置10 min。室温12 000 g离心力10 min。沉淀加入1∶1体积 75%乙醇4℃ 7 500 g离心力5 min。重复洗涤1次。沉淀室温静置5~10 min后加入30 μL DEPC水。溶解的dsRNA加入10∶1体积稀释的Rnase A和Dnase I消化后,37℃ 15 min,-80℃保存。
1.2.5.4 75%酒精沉淀法
取50 mL诱导菌液,4℃ 7 500 g离心力5 min,沉淀加入25∶1体积 75%乙醇,室温静置5 min。加入4∶1体积150 mmol/L NaCl溶液,室温静置60 min,4℃ 12 000 g离心力10 min。上清加入10∶1体积稀释的Rnase A和Dnase I消化后,37℃ 15 min,-80℃保存。
1.2.6 dsgfp浓度、纯度测定
1.2.6.1 体外合成dsgfp浓度、纯度
取2 μL dsgfp样品于B-500 BIOPHOTO METER检测,用Nuclease-Free water分别稀释至浓度为1 000、500、250、125、62.5和31.25 ng/μL并检测A260/A280、A260/A230。稀释dsgfp 1.5%琼脂糖凝胶电泳检测120 V 25 min。
1.2.6.2 菌液提取dsgfp浓度、纯度
取2 μL dsgfp样本于B-500 BIOPHOTO METER检测,用Nuclease-Free water分别稀释至浓度为1 000、500、250、125、62.5和31.25 ng/μL并检测A260/A280、A260/A230。稀释dsgfp 1.5%琼脂糖凝胶电泳检测120 V 25 min。
1.2.7 损失率检测及dsgfp产量
将体外合成的5组dsgfp分别稀释至1 000 ng/μL,将30 μL稀释液混合至50 mL未经IPTG诱导菌液中,运用以上4种方法进行提取,B-500 BIOPHOTO METER检测浓度、A260/A280和A260/A280。运用最佳提取方法分别提取1 mL菌液dsgfp测定浓度,根据提取方法损失率,计算pET-2P、L4440表达的dsgfp产量。
1.3 数据处理
运用Image J软件分析载体表达dsgfp灰度值。Microsoft office Excel 2010、SPSS 25.0软件对体外合成dsgfp以及菌液提取dsgfpA260/A280、A260/A230值进行多重方差分析和新复极差法进行显著性分析。2样本间均数比较采用配对T检验。
2 结果与分析
2.1 IPTG诱导基于PET-2P、L4440产生dsgfp
pET-2p和L4440经IPTG诱导表达产生dsRNA,经RNase A消化后1.5%琼脂糖凝胶电泳检测,pET-2p-gfp和L4440-gfp表达载体。图2
2.2 pET-2P、L4440产生dsgfp电泳条带
研究表明,基于pET-2P载体表达的5组不同长度、不同CG含量的dsgfp灰度值均高于基于L4440载体表达的5组不同长度、不同CG含量的dsgfp灰度值,具有显著差异(P<0.05)。其中pET-2p表达201-30CG以及423-30CG灰度值明显高于L4440表达201-30CG和423-30CG灰度值。图3
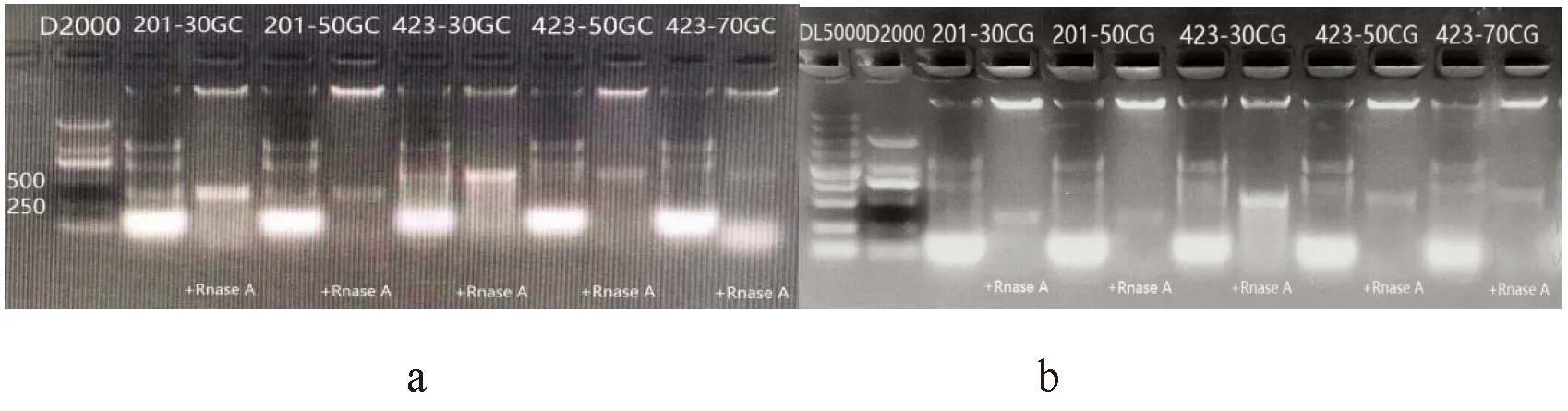
注:a:基于pET-2p表达dsgfp;b:基于L4440表达dsgfp。D2000:分子质量标记(天根),其大小分别是2 000、1 000、750、500、250、100;DL5000:分子质量标记(TaKaRa),其大小分别是5 000、3 000、2 000、1 000、750、500、250、100Note:a:express dsgfp based on pET-2p,b:express dsgfp based on L4440.D2000:molecular mass marker(Tiangen)of 2,000,1,000,750,500,250,100;DL5000:molecular mass marker(TaKaRa)of 5,000,3,000,2,000,1,000,750,500,250,100图2 基于pET-2p和L4440表达dsgfp 1.5%琼脂糖凝胶电泳检测Fig.2 Agarose gel electrophoresis detection based dsgfp 1.5% pET-2p and L4440 expression
2.3 体外合成dsgfp浓度、纯度
研究表明,分别梯度稀释6组浓度,每组dsgfp A260/A280均在1.9~2.2,合成的5组dsgfp纯度较高。稀释至31.25 ng/μL的5组dsgfp稀释液,A260/A230值均在3.2~5.0,浓度过低,达到仪器检测最小阈值,出现偏差。其余5组dsgfp稀释液均在2.2~3.0。5组体外合成dsgfp可以作为标准品,进行后续实验。图4,图5

注:D2000:分子质量标记(天根),其大小分别是2 000、1 000、750、500、250、100Note:D2000:molecular mass marker(Tiangen)of 2,000,1,000,750,500,250,100图4 体外合成dsgfp 1.5%琼脂糖凝胶电泳检测Fig.4 Detection dsgfp 1.5% agarose gel electrophoresis
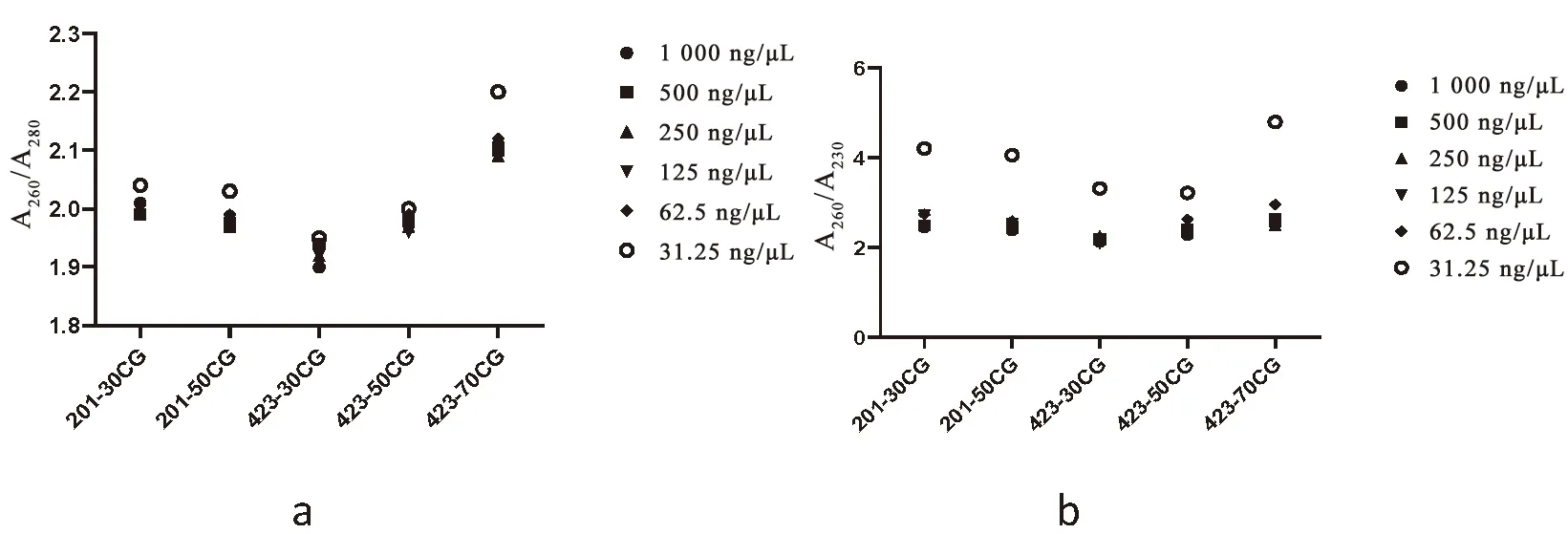
注:a:5组dsgfp稀释至不同浓度检测A260/A280;b:5组dsgfp稀释至不同浓度检测A260/A230Note:a:five groups dsgfp diluted to different concentrations A260/A280 detection;b:five groups dsgfp diluted to different concentrations A260/A230 detection图5 体外合成5组dsgfp浓度、纯度Fig.5 Analysis of dsgfp concentration and purity of five groups synthesized in vitro
2.4 4种方法提取菌液dsRNA
2.4.1 提取基于pET-2p载体表达dsgfp
研究表明,根据提取dsgfp核酸检测值,对A260/A280和A260/A230利用SPSS分别构建多重比较模型,模型截距(F=19 202.406,P=0.000)(F=922.24,P=0.000),提取方法因素(F=28.408,P=0.000)(F=21.833,P=0.000)分别达极显著水平,浓度因素分别达到显著水平(F=2.868,P=0.041)和不显著水平(F=0.297,P=0.909)。新复极差法显著性检验显示不同浓度之间差异不显著。提取纯度最高的Trizol法和酚氯仿法(CK为对照),且这两者差异不显著,其次是75%酒精沉淀法,提取纯度最低的为RNA-easy提取液。图6,图7
2.4.2 提取基于L4440载体表达dsgfp
研究表明,根据提取dsgfp核酸检测值,对A260/A280和A260/A230利用SPSS分别构建多重比较模型,模型截距(F=15 242.017,P=0.000)(F=734.211,P=0.000),提取方法因素(F=30.300,P=0.000)(F=24.085,P=0.000)分别达极显著水平,浓度因素分别达到显著水平(F=3.453,P=0.021)和不显著水平(F=0.344,P=0.880)。新复极差法显著性检验显示不同浓度之间差异不显著。提取纯度最高的Trizol法和酚氯仿法(CK为对照),且这两者差异不显著,其次是75%酒精沉淀法,提取纯度最低的为RNA-easy提取液。图6,图7

注:数据后附不同字母者表示在0.05水平上差异显著(邓肯氏新复极差法);CK:体外合成;Tri:Trizol法;Phe:酚氯仿法;Alc:75%酒精沉淀法;RIR:RNA-easy提取液;a:提取pET-2p和L4440表达dsgfp,分别稀释至不同浓度检测A260/A280;b:提取pET-2p和L4440表达dsgfp,分别稀释至不同浓度检测A260/A230Note:Those with different letters after the data indicate significant differences at the 0.05 level(Duncan's new multiple range method);CK:in vitro synthesis;Tri:Trizol method;Phe:phenol chloroform method;Alc:75% alcohol precipitation method;RIR:RNA-easy extract;a:Extract pET-2p and L4440 to express dsgfp and dilute to different concentrations to detect A260/A280;b:Extract pET-2p and L4440 to express dsgfp and dilute to different concentrations to detect A260/A230图6 4种方法提取pET-2p和L4440载体表达dsgfp纯度Fig.6 Purity analysis of pET-2p and L4440 vector expression extracted by four methods

注:D2000:分子质量标记(天根),其大小分别是2 000、1 000、750、500、250、100;a:酚氯仿法提取基于pET2p表达dsgfp(经Dnase I和Rnase A消化,稀释至500 ng/μL);b:酚氯仿法提取基于L4440表达dsgfp(经Dnase I和Rnase A消化,稀释至500 ng/μL);c:Trizol法提取基于pET2p表达dsgfp(经Dnase I和Rnase A消化,稀释至500 ng/μL);d:Trizol法提取基于L4440表达dsgfp(经Dnase I和Rnase A消化,稀释至500 ng/μL)Note:D2000:Molecular mass marker(Tiangen),its size is 2,000,1,000,750,500,250,100;a:Phenol-chloroform extraction method based on pET2p expression dsgfp(digested with Dnase I and Rnase A,diluted to 500 ng/μL);b:Phenol-chloroform extraction method based on L4440 to express dsgfp(digested with Dnase I and Rnase A,diluted to 500 ng/μL);c:Trizol method extracts dsgfp based on pET2p(digested with Dnase I and Rnase A,diluted to 500 ng/μL);d:Trizol method extracts dsgfp based on L4440(digested with Dnase I and Rnase A,diluted to 500 ng/μL)图7 酚氯仿法和Trizol法提取50 mL菌液表达dsgfp 1.5%琼脂糖凝胶电泳Fig.7 Phenol chloroform method and Trizol method to extract 50 mL bacterial solution to express dsgfp 1.5% agarose gel electrophoresis
2.5 4种提取方法损失率
研究表明,4种方法提取后的体外合成dsgfp与提取前的体外合成dsgfp浓度纯度存在明显差异,经SPSS软件分析,差异有统计学意义(P<0.05)。其中酚氯仿法和Trizol法提取的dsgfp浓度、纯度最高,与体外合成的差异最小,计算提取损失率分别为21.44%、23.83%,75%酒精沉淀法和RNA-easy提取液提取的dsgfp浓度、纯度最低,与体外合成差异最大,计算提取损失率分别为32.3%、37.62%。表2
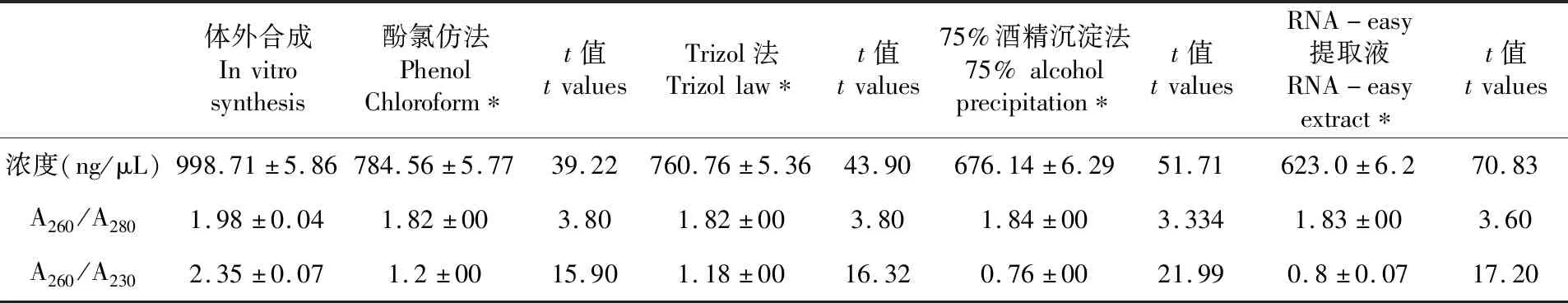
表2 4种方法提取内标混合纯dsgfp浓度、纯度Table 2 Comparison and analysis of the concentration and purity of the internal standard mixed pure dsgfp extracted by four methods
2.6 基于pET-2P、L4440产生dsgfp产量
研究表明,基于pET-2P载体表达5组不同长度、不同CG含量的dsgfp浓度均高于基于L4440载体表达5组不同长度、不同CG含量的dsgfp浓度,具有显著差异(P<0.05)。基于pET-2P和L4440表达载体1 mL诱导菌液可发酵产生8.7~24.39 μg、7.48~22.47 μg dsgfp。图8
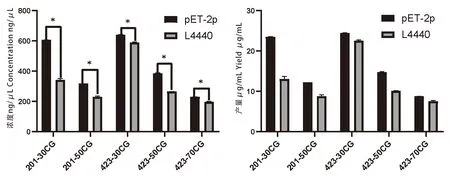
注:*表示在0.05水平上差异显著(配对T检验);a:酚氯仿法提取基于pET-2p和L4440表达dsgfp浓度;b:基于pET-2p和L4440表达dsgfp产量Note:* means significant difference at the 0.05 level(paired T test);a:Phenol chloroform extraction method based on pET-2p and L4440 express dsgfp concentration;b:Based on pET-2p and L4440express dsgfp yield图8 酚氯仿法提取1 mL菌液dsgfp浓度及产量Fig.8 Analysis of the concentration and yield of dsgfp extracted from 1 mL bacterial solution by phenol-chloroform method
3 讨 论
邹晓蕾、Eber以及Tyagi等[14-17]均报道了提取细菌总RNA的方法,主要包括Trizol法,酚氯仿法以及部分市售RNA快速提取试剂盒。其中Trizol法在细菌总RNA提取中使用较为普遍,利用异硫氰酸胍等物质迅速裂解细胞,同时抑制核酸酶的活性,保持RNA的完整性,氯仿使RNA溶于水相,从而与蛋白等物质相分离,为提取细菌总RNA的首选方法[18]。苯酚-氯仿抽提也是提取细菌总RNA常用方法之一,利用酚反复抽提使蛋白质变性,SDS(十二浣基磺酸钠)使细胞裂解,加入氯仿分层,获得含总RNA的水相[19]。市售总RNA提取试剂盒成本较高、使用次数有限,不适用于大量提取检测,故未选用进行实验。研究表明,以体外合成dsgfp为对照CK,通过使用Trizol法和酚氯仿法可高效提取细菌完整总RNA,经Rnase A与Dnase I消化后,可得到较为纯净的dsgfp,损失率最低。RNA-easy提取液和75%酒精沉淀法提取效率明显低于前者,不适用于快速提取细菌总RNA以及dsgfp。与前人的研究结果基本一致。运用酚氯仿法,分别取1 mL诱导菌液提取pET-2p和L4440表达的dsgfp,检测核酸浓度,发现2个载体表达的423-30CG明显高于其他4组,说明pET-2p和L4440均具有较强的表达能力。通过浓度分析,根据提取损失率计算1 mL菌液dsgfp产量,发现基于pET-2p产生的5组dsgfp产量均高于L4440产生的5组dsgfp产量,最高可达24.39 μg/mL,pET-2p可作为dsgfp的相对最优表达载体,用于后续研究。
提取、纯化原核表达dsRNA对于真核生物来说,难度更大,尚无成熟方法借鉴[20],研究采用4种常用提取细菌总RNA的方法,试图通过提取完整纯净的总RNA,经Rnase A、Dnase I消化得到纯净的dsRNA。Trizol法和酚氯仿提取细菌总RNA,经Rnase A、Dnase I消化后,稀释核酸检测A260/A280、A260/A230,均值分别为1.77、1.83和1.74、2.1,与体外合成dsRNA值差异最小。但1.5%琼脂糖凝胶电泳检测后,稀释至不同浓度的dsgfp条带均出现不同程度弥散,无法得到清晰电泳图,可能存在以下原因:原核诱导表达的dsgfp脆弱,使用有机溶剂以及提取过程中反复高速离心损伤dsgfp;核酸检测稀释时间过长,dsgfp在自然环境下发生降解;电泳液含有核酸酶。
4 结 论
通过酚氯仿法提取2种载体表达dsgfp,检测发现随着目的片段CG含量增加,2种载体表达的dsgfp浓度及其产量均逐渐降低。pET-2p载体表达能力高于L4440载体,pET-2p可作为dsgfp的相对最优表达载体。为后续dsgfp在不同环境降解程度研究以及降解产物分析提供了技术支持。
