不同教材中有关生物化学知识表述的差异性分析
2021-11-02吴宸旭
吴宸旭
(安徽省六安市第一中学 安徽六安 237000)
教材是学生学习最重要的依据,可是相同的知识点在不同的教材中却有着不同的描述,有时候会让学生一头雾水、无所适从。现行的人教版《生物学》与《化学》教材中有关生物化学知识的论述存在诸多差异,给教师备课带来许多困惑。两学科在生物化学原理上表述不一或侧重点不同的现象,也给学生的学习带来困扰。相同知识在两版教材中描述的差异主要存在以下几点。
1 糖的检验:斐林试剂与新制的Cu(OH)2悬浊液
1.1 《生物学》
斐林试剂的配制质量浓度为:0.1 g/mL NaOH与质量浓度为0.01 g/mL CuSO4等量混匀后取少量备用。
斐林试剂的使用:取少量试剂与待测液混匀,50~65℃水浴加热2min。作用对象为还原糖。
对斐林试剂的作用原理,教材中未加说明。
1.2 《化学》
新制的Cu(OH)2的配制:2 mL质量分数为10%的NaOH溶液与4~6滴质量分数为2%的CuSO4溶液混匀,振荡。
新制的Cu(OH)2的使用:在上述试管中加入少量待测液混匀,直接在酒精灯上加热至沸腾。作用对象为醛类。
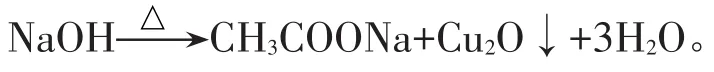
1.3 综合讨论
斐林试剂的本质为酒石酸络铜离子,而高中阶段以氢氧化铜作为其等效成分。之所以生物学与化学教材的表述不同,或许是因为对于低级醛(如化学教材中提到的乙醛)必须加强热才能使得弱氧化剂氢氧化铜转化为氧化亚铜砖红色沉淀,高级多羟基醛(如葡萄糖)对反应条件的要求较温和,而对氢氧化钠量的要求较高(事实上,传统意义上的斐林试剂正如化学教材所述,生物教材中的配法无从考证)。
除了斐林试剂外,在《生物化学原理》中介绍了更为先进且灵活的检测办法,如Molisch反应(运用α-萘酚/乙醇),Seliwanoff反应(运用盐酸/间二苯酚),Benedict反应(运用氢氧化钠,无水碳酸钠,柠檬酸钠),成脎反应,等等。
2 氨基酸的介绍:分子结构与成肽反应
2.1 《生物学》
氨基酸的结构通式如图1所示。
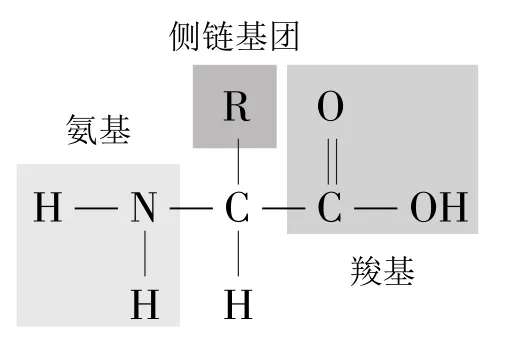
图1 氨基酸的结构通式示意图
成肽反应:脱水缩合。
命名:俗名。
2.2 《化学》
氨基酸的通式为R—CH(NH2)—COOH,指出中心碳原子为手性碳原子,并指出自然界中构成蛋白质的氨基酸大多都是α-氨基酸(均为L-型氨基酸),属于取代羧酸。
物理性质:无色晶体,熔点较高,难溶于乙醇或乙醚,一般能溶于水,都能溶解在强酸或强碱溶液中。
成肽反应:酰基取代氢原子(胺基取代羧羟基)的取代反应。
命名:系统命名法。
2.3 综合讨论
生物化学研究的范畴是物质的生理意义,对于其理化性质没有详述;有机化学研究的层面是分子、原子及其在反应中的变化,故在物质分子描述上更为准确。值得注意的是,部分氨基酸属于亚氨基酸,不能用通式表示,如脯氨酸。
3 蛋白质性质的研究及其变性
3.1 《生物学》
蛋白质的功能:运输,催化,调节,免疫,组成结构等。
蛋白质的多样性:氨基酸数目、种类及排列顺序多样,肽链盘曲折叠的方式不同,使蛋白质分子种类繁多。
检验蛋白质:双缩脲试剂(适用条件为含两个及以上肽键,课本中未加描述)。
蛋白质变性:蛋白质在某些理化因素下特定的空间构象被破坏。从而导致其理化性质的改变与生物活性丧失的现象。
3.2 《化学》
多级结构的概念:详见教材。
水解,盐析,变性:蛋白质在酸或碱或酶的条件下水解成小分子肽,最终形成各种氨基酸的过程称为水解;蛋白质在浓的盐溶液中溶解度降低而析出的现象称为盐析;变性的概念同上。
变性因子:物理因子有加热、加压、搅拌、振荡、紫外线、超声波等;化学因子有强酸、强碱、重金属盐、三氯乙酸、乙醇、丙酮等。
3.3 综合讨论
对于蛋白质的检验,两套教材都未能做到普适且灵活。最为灵活的检验办法是茚三酮反应,还有诸如醋酸铅法、考马斯亮蓝法、福林-酚试剂法、米伦反应、坂口反应、乙醛酸反应等,都比双缩脲法与黄蛋白反应可靠、灵活且普适。
特别地,某些肽水解时,组成它的部分氨基酸会发生化学变化,故蛋白质彻底水解的终产物并不一定是氨基酸。
4 混合物的分离与研究:柱色谱法与纸层析法的异同
4.1 《生物学》
纸层析法的步骤:详见教材。

实验现象:定性滤纸上分离出4条色素带,分别是胡萝卜素、叶黄素、叶绿素a、叶绿素b。
4.2 《化学》
色谱法的步骤:详见教材。
实验构成:玻璃棉(或脱脂棉),沙,碳酸钙(吸附剂),溶剂(石油醚),分液漏斗,锥形瓶,色谱柱等。
实验现象:分为3条色素带,分别是叶绿素、叶黄素、胡萝卜素。
实验活动:用粉笔与菠菜叶做相关课外实验。
4.3 综合讨论
在装置的简洁性与结论的精确性上,生物学教材提供的纸层析方案更优,而对于色谱法的分类(纸上色谱法、薄层色谱法、气相色谱法、液相色谱法、柱色谱法),化学教材则更为准确。对于两种叶绿素的异同,两本教材都没有详述。在颜色上,叶绿素b为黄绿色,叶绿素a为蓝绿色;化学构成上,叶绿素a为C55H72O5N4Mg,叶绿素b为C55H70O6N4Mg,由分子结构可推断出叶绿素b更易溶于极性溶剂;吸收光谱上,二者都主要吸收红光和蓝紫光,但红区和蓝紫区最大吸收峰不同;二者的存在也有区别,叶绿素a存在于所有绿色植物种,叶绿素b只存在于高等植物和绿藻、管藻、眼虫藻等,二者的比值可用于区分阴生植物和阳生植物。
5 原子及原子团标记
5.1 《生物学》
同位素标记法:使用物理性质特殊的同位素来标记化学反应中原子的去向,就是同位素标记法。这种方法可用于示踪物质的运行和变化规律。如果使用的同位素具有放射性,如14C、32P、35S、3H等,需要检测样本的放射性位点。如果使用的同位素不具有放射性,如15N、18O等,可以通过相对分子质量的不同进行比较。教材中运用同位素标记法的实验有:监测分泌蛋白合成与运输的途径,鲁宾与卡门证明光合作用中氧气来自水的光解,卡尔文对碳元素的追踪,赫尔希与蔡斯标记T2噬菌体侵染大肠杆菌实验证明DNA是遗传物质,米希尔森和斯塔尔标记DNA证明其复制方式为半保留复制。
荧光标记法:用荧光染剂标记特定分子来研究某些物质的性质的方法称为荧光标记法。教材中涉及该方法的实验有:小鼠细胞与人的细胞融合实验证明细胞膜的流动性,标记基因证明其在染色体上线性排列。
5.2 《化学》
同位素标记法的运用:在反应CH3COOH+CH3CH218OH→CH3CO18OC2H5+H2O中,用18O标记乙醇中的氧原子,证明了在酯化反应中,羧酸脱去羧基上的羟基,而醇脱去醇羟基上的氢原子,生成酯和水。
荧光标记法的运用:未见使用。
5.3 综合讨论
同位素标记法是运用现代科学技术示踪物质的最常用方法之一,荧光标记法在研究大分子物质的宏观性质时也十分常用。两本教材之所以运用范围不同,是因为学科本身研究范畴有差异。
6 对糖类的专题讨论
6.1 《生物学》
葡萄糖与果糖:统一用C6H12O6表示,未体现其分子结构与反应机理,提到了斐林试剂对其的显色作用。
核糖与脱氧核糖:在ATP一节的框图中提到了核糖的五元环结构,分子式与性质未见讨论;脱氧核糖仅给出Kekulé式,分子式与性质未见讨论。
多糖:插图中提到淀粉、纤维素等的碳骨架不同。几丁质(壳多糖)仅提到其分布,而未提到其单体(N-乙酰葡糖胺)及元素组成。
总述:将糖类的通式表示为(CH2O)n,未提到提出此通式的时代背景(碳水化合物认知)与特例(如双糖、多糖、含氮糖、脱氧核糖等)。
6.2 《化学》
葡萄糖与果糖:将其表示为结构简式形式,如葡萄糖表示为CH2OH—CHOH—CHOH—CHOH—CHOH—CHO。
核糖与脱氧核糖:无专门讨论,安排于核酸一节。
多糖:课后拓展内容中提到了甲壳质的单体为乙酰氨基葡萄糖,并给出了其与葡萄糖结构式的对比.对于淀粉等,提到了葡萄糖的聚合反应(即脱水缩合)。
总述:将糖类的通式表示为Cm(H2O)n,特例更少,也提出了它运用的条件与背景。
6.3 综合讨论
在糖类的结构与性质方面,化学教材的陈叙显然更为科学合理;生理功能和酵解代谢方面,生物学教材则更为详尽。这符合各学科研究范围特点。
7 核酸
7.1 《生物学》
核酸的种类、分布、检验:核酸分为核糖核酸(RNA)与脱氧核糖核酸(DNA),其中脱氧核糖核酸是大多数生物的遗传物质。细胞中,DNA主要分布于细胞核(原核生物为拟核与质粒),RNA主要分布于细胞质,可利用二者对甲基绿和吡罗红的亲和性不同进行染色。
DNA的分子结构:以核苷酸为单体,核苷酸由磷酸基团、五碳糖、含氮碱基组成;以磷酸和五碳糖由磷酸二酯键交替的链接为骨架;以碱基之间的氢键作为维系双螺旋结构的纽带。
DNA分子重组技术(基因工程)的基本操作程序,人类基因库等:详见教材。
DNA的生理过程:复制,遗传变异,表达等。
7.2 《化学》
核酸的种类:DNA,RNA。
核酸的分子结构:同上,详细介绍了腺嘌呤、鸟嘌呤、胞嘧啶、胸腺嘧啶、尿嘧啶、核糖、脱氧核糖、焦磷酸等的组成。
7.3 综合讨论
鉴于核酸的研究对于遗传学和基因工程的重大意义,生物学教材使用了宏伟的篇幅,不吝笔墨地介绍了有关核酸的丰富知识;作为生命科学的重要物质,化学教材则在结构与性质上给予了讨论。有关核酸的介绍尽其善矣。
8 小结
总体上,教材并未出现原则性科学知识错误和矛盾冲突,编者实现了教材应有的严谨性。细节上,两学科在生物化学原理上表述不一或侧重不同的现象,已简要列举如上。考虑到普通高中学生的总体接受能力,教材中出现了一些或与实际不符或过于浅显的解释方法,如糖酵解、三羧酸循环、卡尔文循环的简略处理与大π键(离域π键)的概要介绍,这虽然有一定的意义,但或许有损科学性。上述涉及高等知识的问题或可通过课后拓展阅读等模块来介绍。
