Al-Cu 复合金属粉的电爆炸制备及其反应活性
2021-11-01吕英迪姚冰洁郑晓东
吕英迪,姚冰洁,郭 涛,唐 望,姜 俊,郑晓东
(西安近代化学研究所,陕西 西安 710065)
1 引言
铝粉材料因为其高燃烧热、低成本、无毒等优点在固体火箭推进剂以及新型炸药中有着重要应用[1]。现有的研究表明,减小铝粉颗粒尺寸可以提高铝粉的反应活性与燃烧效率[2-3]。
金属丝电爆炸法(electro explosion wire,EEW)于20 世纪70 年代末由俄罗斯托木斯高压研究院的核物理专家开发[4],其制备原理是将金属丝在充满惰性气体的反应室中施加直流高压对金属丝时进行欧姆加热,由于能量注入率高,沉积能量迅速使金属丝熔化、汽化、电离并产生等离子体,金属蒸气和等离子体膨胀到气体中,高温金属蒸气与气体分子碰撞损失能量,从而在气体中均匀冷凝形成亚微米粉体甚至纳米粉体[4-5]。采用该种方法制备的铝粉与普通铝粉相比具有颗粒尺寸小,表面活性点多,点火温度低,燃烧反应完全率高的特点[5]。在推进剂中以电爆炸铝粉代替普通铝粉,可以提高推进剂的燃烧效率,增加推进剂的燃烧稳定性,提高燃速,降低压强指数,增大推进剂的温度敏感度[7-8]。
Cu,Ni,Ti,Zr 等过渡金属材料粉末,由于其良好的分散性以及催化性能,广泛应用于固体推进剂中,可以有效调节复合推进剂的分解温度和燃烧压力指数并增加其表观放热量和燃速[9-11]。现有的研究表明,可以通过在纳米铝粉的表面和晶格间隙引入少量的Cu、Ni、Ti、Zr 等过渡金属原子,利用金属间的互化稳定作用,以及位阻作用,在常温下抑制铝粉的氧化作用,提高材料中有效组分的含量,在保证燃烧效率的前提下,实现材料整体燃烧热值的提高[12-13]。同时,这些过渡金属材料对高氯酸铵(AP),聚叠氮缩水甘油醚(GAP)等推进剂组分的燃烧分解具有良好的催化效果,可以提高推进剂的燃烧效率,降低弹道信号,提高推进剂的使用效果[14-16]。
本研究利用金属丝电爆炸技术,采用一步法成功制备了Al-Cu 复合金属粉,研究了电爆炸电压、金属丝电爆炸长度等制备工艺条件对材料制备过程的影响,对材料结构、形貌、性能进行了系统表征,采用金属-水蒸汽反应装置完成了Al-Cu 复合金属粉反应活性评价。
2 实验部分
2.1 原料与仪器
原料:Al 丝,纯度大于99.95%,北京中金研科技,0.45 mm;Cu 丝,纯度大于99.95%,北京中金研科技,0.1 mm。
仪器:电爆炸装置(自行研制)见图1;BS 224 S 型分析天平(0.0001 g),北京赛多利斯仪器系统有限公司;复合金属丝缠绕装置,上海隆奔数控绕线设备有限公司。

图1 金属丝电爆炸制备装置图Fig.1 The equipment of electric explosion wire(EEW)
2.2 Al-Cu 复合金属粉制备
将0.45 mm Al 丝与0.1 mm Cu 丝按长度比1∶1的方式缠绕成复合金属丝。将复合金属丝安装于充满氩气的金属丝电爆炸装置内,压强为0.2 MPa,风速为2600 r·min-1。在放电电压为26~30 kV,电容器容量4.0 μF,放电频率1 Hz,电爆炸长度为80 mm 和100 mm的条件下完成复合材料制备。
用作对比样品的铝粉采用电爆炸法制备,在放电为28 kV,电爆炸长度8 cm,其他制备条件与Al-Cu 复合金属粉制备条件一致。
2.3 材料结构与性能表征
X 射线粉末衍射(XRD),日本理学公司D/MAX-2400 型装置,以Cu Kα为射线源,石墨单色器,管压40 kV,管流100 mA,扫描速率1.5 °/min,采用JADE6.0 PDF 卡片比照衍射峰确定晶相。
透射电镜电子能谱成像分析(TEM-MAPPING),FEI Quanta 400 ESEM-FEG,工作电压20 kV,采用自带的EDS-MAPPIG 附件完成MAPPING 图谱测量。
X 光电子能谱(XPS),美国PE 公司PHI-5400,以Al Kα为射线源,真空度-0.096 Pa,束斑大小700 μm×300 μm,扫描模式为CAE,采用Thermal advantage 软件完成结果分析。
差热扫描量热-热重分析仪(DSC-TG),德国Netzsch 公司204HP,升温速率为20 ℃·min-1,分别在空气气氛以及氩气气氛下完成测试。采用空气气氛研究样品的的氧化放热过程,采用氩气气氛研究样品的相变过程。
2.4 材料性能评价
Al-Cu 复合金属粉的活性评价在自行研制的金属-水蒸气反应评价装置(如图2 所示)上进行,该装置主要由微量进样泵、汽化室、反应室、气相色谱经气路连接构成,在测试过程中利用六通阀实现连续,准确的数据采集。将0.18 g Al-Cu 复合金属或铝粉样品粉置于反应评价装置中的石英管中进行评价。评价过程:采用氩气为载气;流速约为40 ml·min-1。以5 ℃·min-1的升温速率将反应温度升至600 ℃,当反应温度达到60 ℃时通入0.007 mL·min-1的水蒸气进行氧化反应,氧化还原过程中的氢气含量用气相色谱(GC)热导检测器(TCD)在线检测。由于反应中产生H2的物质量,与消耗单质铝的物质量存在固定的定量关系:3Al→2H2,所以可以通过记录产生氢气的物质量推算消耗的单质铝的物质量,所以引入氧化度(kDO)即氧化反应进行程度这一参数来评价材料的反应活性。其数学推导如下:

图2 金属-水蒸气反应评价装置示意图Fig.2 The schematic diagram of matal-vapor reactivity assessment facility

式中,mtAl为t时刻参加反应铝的质量,g;m0为全部铝的质量,g;ntAl为t时刻参加反应铝的物质量,mol;n为全部铝的物质量,mol。
ntH2,为至t时刻累计产生氢气的物质量(mol),可以通过积分计算t时刻前每个采集点的产氢量得到;ntotal为样品理论上可产生的氢气物质量(mol),可以通过样品中理论铝含量计算得到。
3 结果与讨论
3.1 Al-Cu 复合金属粉电爆炸制备
选取0.1 mm 的Cu 丝以及0.45 mm 的Al 丝为主要原料,采用双丝复合缠绕的方式得到了电爆炸用的原料复合金属丝,以此为原料在自制的电爆炸装置上完成了Al-Cu 复合金属粉的制备。采用示波器记录电爆炸过程中的回路感应电流,以波形图为依据分析电爆炸过程的进程。
图3 为电爆炸长度10 cm 的条件下,不同输入电压的电爆炸波形曲线。观察图3 的波形图发现,放电开始时,金属丝电流迅速增大,金属丝温度也随着焦耳加热的进行而升高。到达A 点时,复合丝开始向气态丝转变,电阻急剧增大,电流迅速下降。在B 点时,电流又开始增大,到C 点时,发生金属丝的快速膨胀爆炸,金属丝表面气体击穿并形成等离子体,电流从高电阻的金属蒸汽丝切换到高电导的等离子体表现为电流二次上升,随后电流迅速下降,并出现幅值衰减的正弦振荡波形(D),即电弧放电[17]。由图2 可知,随着输入电压的增加,沉积在金属丝表面的电流能量逐渐增加,波形图表现为C 点的相对强度逐渐增加,以及幅值衰减的正弦振荡波形的振幅增大,电弧震荡明显;26~28 kV 波形图表现为电爆炸不充分,等离子体过程的能量脉冲较低,无末端的电弧震荡;29~30 kV 随着等离子体过程能量脉冲逐步提升,电爆炸越来越充分,末端电弧震荡也更加明显,但是随着输入电压的提高,空气开关被异常击穿的概率大幅提升,导致电爆炸装置的异常放电频率增大,影响电爆炸设备的使用寿命与使用安全[17]。

图3 电爆长度10 cm 条件下不同输入电压电爆炸过程波形图Fig.3 EEW waveform graphs of 10 cm wire at different voltages
研究了28 kV 电压下,电爆炸金属丝长度为10 cm和8 cm 的电爆炸波形,结果如图4 所示。由图4 可知,缩短金属丝电爆炸长度后,电爆炸过程中等离子体击穿状态强度明显加强,电爆炸效果明显改善。分析原因是由于缩短电爆炸长度,可以减少单次参与电爆炸过程金属丝用量,在输入能量不变的前提下,减少金属丝的长度可以提升单位质量金属丝上的电爆炸能量,使电爆炸过程更加充分,导致电爆炸过程中气态产物浓度大幅提升,这些气态产物在环境温度下快速冷却形成均匀的颗粒。而当电爆炸能量不足时,电爆炸产物不仅有气态产物,也存在大量的液态产物,在冷凝过程中气态产物形成的颗粒较小而液态产物形成的颗粒较大,导致材料的粒度分布不均匀[17]。
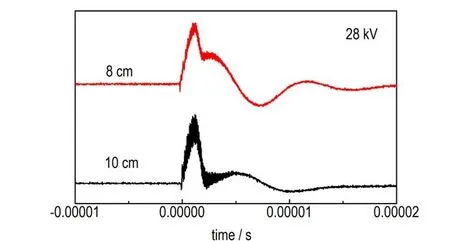
图4 不同电爆炸长度条件下电爆炸波形图Fig.4 EEW waveform graphs of wires with different length
图5 为输入电压28 kV 下电爆炸长度分别为8 cm与10 cm 条件下制备的Al-Cu 复合金属粉的SEM 图。由图5 可知,电爆炸长度为8 cm 时,Al-Cu 复合金属粉的粒度均匀,无大颗粒,粒度为150~300 nm;电爆炸长度为10 cm 时,在Al-Cu 复合金属粉中可以观察到明显的微米级颗粒,以及大量平均粒度为150 nm 左右的颗粒,粒度分布跨度较大,所形成的微米级颗粒就是由于电爆炸过程中,电爆炸能量不足,电爆炸产物中既存在金属液滴也存在金属蒸汽,金属液滴最终形成了微米级颗粒,电爆炸产生的金属蒸汽则形成了纳米颗粒。

图5 不同电爆炸长度制备的Al-Cu 复合金属粉的SEM 图Fig.5 SEM images of Al-Cu composite metal powder with different wire length
样品SEM 粒径测试结果与根据电爆炸过程波形图分析的样品粒度结果一致,因此,综合考虑金属丝电爆炸过程的稳定性和电爆炸产物粒度均匀性,最终采用28 kV 输入电压、电爆炸长度8 cm 的电爆炸工艺条件制备Al-Cu 复合金属粉用于其性能测试与表征。
3.2 Al-Cu 复合金属粉结构表征
图6 为Al-Cu 复合金属粉样品的XRD 图谱,通过与JADE6.0 软件中的PDF-2004 标准图谱比照,所制备的Al-Cu 复合金属粉主要由CuAl2,Al 两种物质组成。其中20.6°,29.2°,38.5°,41.9°,42.5°,47.3°,57.1°,66.2°为CuAl2的特征衍射峰,39.0°,44.6°,65.9°,74.6°为单质铝的衍射峰,分析原因是由于电爆炸过程的特殊性,高能脉冲电流瞬间作用于金属丝使其汽化产生大量的金属蒸汽,经快速凝结互化形成具有合金态CuAl2,由于电爆炸过程形成的铝蒸汽是过量的,同时金属蒸汽的冷凝在微秒时间尺度快速完成,部分铝粉蒸汽直接快速冷凝成亚微米颗粒[14-15]。

图6 Al-Cu 复合金属粉的XRD 图谱Fig.6 The XRD graph of Al-Cu composite metal powder
图7 为Al-Cu 复合金属粉样品的XPS Al2p测试结果。由图7 可知,样品的Al2p曲线经分峰处理后可以归纳为样品中Al 元素的3 种存在形式,73.6eV 处对应的为Al-O 键特征结合能[18-19],表明材料表面经钝化处理后形成了氧化层,而在样品的XRD 测试结果中并未发现氧化铝的特征衍射峰,表明材料表面形成的氧化铝钝化层为非晶态结构;71.8 eV 处对应的是单质铝特征结合能,表明在Al-Cu 复合金属粉表面仍有部分单质铝存在;71 eV 处对应的是Al-Cu 合金态特单质铝的特征结合能,由于形成了Al-Cu 合金,铝的结合能向低电子能方向移动[18-20]。以上结果表明,采用电爆炸法制备的Al-Cu 复合金属粉主要由CuAl2和Al 组成,与XRD 测试结果一致,经微钝化处理后表面仍有大量的单质铝存在,微钝化形成的氧化层为无定型结构,材料表面仍可以检测出单质结构的铝元素。

图7 Al-Cu 复合金属粉的XPS Al2p测试结果Fig.7 The XPS graphs of Al-Cu composite metal powder illustrating Al2p
图8 为Al-Cu 复合金属粉的TEM-MAPPING 测试结果。由图8 可知,铝元素与铜元素在颗粒的表面均匀分布,观察元素分布可以发现,在铜元素分布较多的区域氧元素含量明显降低,可以认为铜铝合金态物质的生成有效地抑制了单质铝的持续氧化,使得材料表面的活性铝含量提升,进而有可能进一步提升材料的反应活性。

图8 Al-Cu 复合金属粉的TEM-MAPPING 分析Fig.8 The TEM-MAPPING images of Al-Cu composite metal powder
3.3 Al-Cu 复合金属粉反应活性表征
电爆炸法制备的Al-Cu 复合金属粉和铝粉在空气气氛下DSC 及DSC-TG 测试结果如图9 所示。由图9a可知,Al-Cu 复合金属粉与铝粉的氧化过程类似,主要分两步,Al-Cu 复合金属粉的初始放热峰温为550 ℃,该放热过程为单质铝与空气发生氧化反应而导致氧化放热过程,与铝粉的初始放热峰温(600 ℃)相比降低了50 ℃,反应活性明显增强,Al-Cu 复合金属粉的初始氧化过程放热过程集中,温度跨度由520~650 ℃变为500~600 ℃,反应历程由7.5 min 缩短到5 min,表明反应速率提升了33%。Al-Cu 复合金属粉的第二放热峰温为830 ℃,与铝粉相比滞后30 ℃,与铝粉不同在Al-Cu 复合金属粉DSC 曲线上并未出现660 ℃的单质铝熔化吸热现象。由图9b 可知,Al-Cu 复合金属粉的TG 曲线在500~600 ℃的放热区间对应着一个明显的急剧的质量增加过程,表明在该温度区间内的氧化反应速率较快,与DSC 曲线结果一致,该温度区间内样品的质量增加率为24.3%。样品在750~900 ℃的放热区间对应一个缓慢的质量增加过程,表明在该温度区间内氧化反应速率较慢,这与DSC 曲线结果一致。

图9 Al-Cu 复合金属粉与铝粉在空气下的DSC 及DSC-TG 曲线Fig.9 A The DSC and DSC-TG curves of Al and Al-Cu composite metal powder in air
为了进一步分析Al-Cu 复合金属粉特殊的反应活性原因,在氩气气氛下对Al-Cu 复合金属粉进行了DSC-TG 测试,结果见图10。由图10 可见,Al-Cu 复合金属粉在550 ℃存在一个明显的吸热熔化过程,这是因为材料放热过程为氧化放热,所以在无氧的条件(氩气气氛)下无放热现象发生,只存在一个吸热峰,故其DSC 曲线表现与空气气氛下的DSC 曲线不同。

图10 Al-Cu 复合金属粉氩气下的DSC-TG 曲线Fig.10 The DSC-TG curves of Al-Cu composite metal powder in argon
Al-Cu 复合金属粉在氩气气氛的分解过程无明显的质量变化,同时在660 ℃并未再观察到铝的熔化峰,以上现象证明Al-Cu 复合金属粉中的单质铝与CuAl2由于特殊的制备方法及结合方式发生了协同熔化现象,即在同一温度区间完成熔化过程。而这一熔化峰温的位置,与Al-Cu 复合金属粉氧化峰温的位置一致,表明Al-Cu 复合金属粉的初始氧化过程与熔化过程是同时发生的,并且将原有的铝-氧气固相反应变为铝-氧气-液相反应提高了反应速率,宏观表现为放热速率大幅提升[5]。
图11 为Al-Cu 复合金属粉空气气氛下DSC 测试后残渣的XRD 图谱,通过与JADE6.0 软件中的PDF-2004 标准图谱比照,31.2°,36.8°,44.8°,55.6°,59.4°,65.3°为CuAl2O4特征衍射峰,25.5°,35.1°,37.8°,43.3°,52.6°,57.3°,61.3°,66.4°,68.2°为Al2O3特征衍射峰,35.4°与38.5°为CuO 特征衍射峰。实验结果表明,燃烧产物主要以CuAl2O4与Al2O3分别为CuAl2与Al 对应的燃烧产物,测试结果证明在燃烧反应过程中CuAl2结构稳定,并未发生合金结构解体的现象,氧化反应以CuAl2为主体进行。
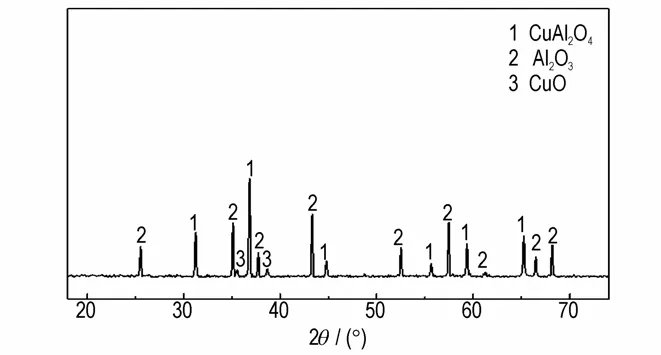
图11 Al-Cu 复合金属粉空气气氛下燃烧产物的XRD 图谱Fig.11 The XRD graph of Al-Cu composite metal powder combustion products
图12 为Al-Cu 复合金属粉与铝粉的水蒸气反应活性评价曲线,实验条件见2.4。由图12 可知,Al-Cu复合金属粉在反应的初始阶段(0~10 min),产生了大量的H2,反应完全度为0.36,而同样条件下铝粉的反应完全度为0.036,在反应初始阶段Al-Cu 复合金属粉的反应完全度为铝粉的10 倍。分析主要原因是由于单质铝与水蒸气的反应是典型的气-固相反应,在反应的初始阶段,Al 颗粒表面化学结构对于反应活性有重要影响。Al-Cu 复合金属粉样品的TEM-MAPPING 结果表明,由于Al-Cu 的合金化作用使得表面铝元素的氧化被大幅抑制,导致表面存在大量铝原子,这些表面铝原子处于价键不饱和状态,所以具有特别高的反应活性,同时其微钝化形成的氧化层为无定型结构,与水蒸气接触后瞬间发生化学反应,放出大量的氢气。电爆炸制备的铝粉,虽然其表面的钝化层也为无定型结构,但表面活性的单质铝与Al-Cu 复合金属粉相比较少,铝水反应的界面较小,影响了放氢过程。
随着反应温度的提高,单质铝与水蒸气反应的进程不断推进,反应速率也不断提高,在这一过程中,水蒸气在单质铝内部的传质速率是影响反应速度的决定因素。由图12 可见,反应进行20 min 后反应速率明显下降,趋于停止,一方面是由于随着反应的进行,参加反应单质铝的含量逐渐减小,另一方面反应过程中生成的氧化铝会不断增加反应过程的传质阻力,使反应达到传质平衡,而不能顺利继续进行。

图12 水蒸气反应活性评价曲线Fig.12 The assessment results of vapor reactivity
在评价过程结束时,Al-Cu 复合金属粉和Al 粉的氧化度分别为0.88 和0.73。结果表明,Al-Cu 复合金属粉反应完全度要高于铝粉。可见,Al-Cu 复合金属粉与铝粉相比既有反应活性的优势,也具有反应效率的优势。
图13 为铝粉与Al-Cu 复合金属粉水蒸气评价反应后产物的XRD 测试图谱,与JADE6.0 软件中的PDF-2004 标准图谱比照发现,对于Al-Cu 复合金属粉,反应后材料主要由CuAl2O4与Al2O3组成,有少量未完全反应的单质铝,单质铝的衍射峰较弱,表明反应后Al-Cu 复合金属粉大部分已完全反应,生成相应的氧化态物质,而且并未发现CuAl2相态存在,表明材料中合金态的CuAl2完全反应;对于铝粉,反应后材料中仍然含有大量的单质铝,反应过程中不断形成的氧化铝,极大的阻碍了铝水反应的进行,水蒸气无法通过表面致密的氧铝化层与内部的单质铝发生反应。对于Al-Cu 复合金属粉,一方面由于CuAl2的形成抑制了铝粉表面的氧化,在反应初期材料表面存在大量的单质铝可以参加反应,提高气固相反应的效率;另一方面,在反应初始阶段大量的铝与水蒸气反应与单质铝相比可以放出更多的热量,进一步促进了铝水反应的传质效率。

图13 铝粉与Al-Cu 复合金属粉水蒸气评价反应后产物的XRD 图谱Fig.13 The XRD graphs of vapor reaction products for Alpowder and Al-Cu composite powder
4 结论
采用金属丝电爆炸法制备了Al-Cu 复合金属粉,并对材料的结构、形貌与性能进行了系统表征。得到结论如下:
(1)Al-Cu 复合金属粉为球形,主要由CuAl2与Al组成,粒度分布为150~300 nm。电爆炸过程的特殊性是形成铜铝合金状态的主要原因。
(2)采用DSC 法评价了材料的氧化反应活性,Al-Cu 复合金属粉初始氧化峰温为550 ℃,与铝粉相比降低了50 ℃,放热过程集中,放热反应速率提升了33%。
(3)水蒸气反应评价结果表明,在反应初始阶段Al-Cu 复合金属粉的反应活性与铝粉相比大幅提升。Al-Cu 复合金属粉反应完全度为0.88,铝粉反应完全度为0.73,与铝粉相比Al-Cu 复合金属粉反应完全度大幅提升。
(4)Al-Cu 复合金属粉中的铝铜合金结构是大幅提升材料氧化反应活性、水蒸气反应活性及反应完全度的重要因素。
