安罗替尼在晚期非小细胞肺癌疗效和安全性荟萃分析
2021-10-30高莉蓉刘泽毅黄建安
高莉蓉 刘泽毅 黄建安
苏州大学附属第一医院呼吸与危重症医学科215006
肺癌是全球癌症相关死亡的主要原因[1],非小细胞肺癌(non-small cell lung cancer,NSCLC)约占肺癌的85%,许多患者在确诊时就已发展为局部晚期或出现转移[2]。由于缺乏有效的治疗策略,发生转移的NSCLC 患者五年生存率仅为5%[3]。美国国立综合癌症网络 (National Comprehensive Cancer Network,NCCN)指南推荐化疗、靶向治疗和免疫治疗作为晚期NSCLC 的标准治疗方案,然而对于进展的NSCLC 患者没有统一的三线治疗标准,这促使医生寻求新的有效的治疗方案。
安罗替尼是一种新型口服多靶点酪氨酸激酶抑制剂(tyrosine kinase inhitor,TKI),其靶点包括血管内皮生长因子受体 (vascular endothelial growth receptor,VEGF)1~3 (VEGFR1、VEGFR2、VEGFR3)、干细胞因子受体 (c-Kit)、血小板衍生生长因子受体(platelet-derived growth factor receptor,PDGFR)、成纤维细胞生长因子受体1~3 (fibroblast growth factor receptor,FGFR)(FGFR1、FGFR2、FGFR3)[4-5]。2018年5月8日,中国国家药品监督管理局 (CFDA)基于ALTER0303试验结果[6]批准通过了安罗替尼用于进展的晚期NSCLC的三线治疗[7]。本研究在于系统评价安罗替尼治疗晚期NSCLC的疗效和安全性。
1 资料与方法
1.1 数据检索策略 通过检索Pub Med,EMbase,Web of Science,Cochrane Library,Clinical Trials gov databases,中国知网、万方、维普数据库来获取文献。中文检索词为“安罗替尼”、“肺癌”,英文检索词为“anlotinib”,“lung neoplasms”,“lung cancer”,“lung carcinoma”等肺癌相关自由词,检索时限至2020年9月,没有语言限制。此外本研究还手动检索了所选文献中的参考文献。
1.2 纳入和排除标准 纳入标准:(1)研究对象:明确诊断的ⅢB/Ⅳ期NSCLC患者;(2)干预:实验组给予安罗替尼或安罗替尼联合其他药物治疗;(3)对照组:安慰剂、最佳支持治疗、化疗、其他;(4)结局指标:至少含有无进展生存期(progression free survival,PFS)、总生存期(overall survival,OS)、客观缓解率 (objective response rate,ORR)、不良反应中的一项;(5)研究类型:国内外公开发表的随机对照试验。排除标准:(1)回顾性研究、综述、病例汇报等;(2)结局指标不明确;(3)重复发表的研究。
1.3 数据提取 由两名研究者独立进PFS行资料提取,并进行交叉核对,如果存在分歧则重新讨论或咨询第三方直至达到共识。资料提取的内容包括:作者、分型、治疗方案、样本量、ORR、PFS、PFSHR(95%CI)、OS、OSHR(95%CI)、不良事件;若文献没有直接告知HR,则利用Tierney等[8]文献所述方法,从生存曲线中提取HR(95%CI)。
1.4 文献质量评价 根据Cochrane偏倚风险评估工具进行文献质量评价,包括7个方面:是否根据随机序列生成、是否存在分配隐藏、对患者或实验人员是否实施盲法、对结局评估者是否实施盲法、数据结果是否完整、是否存在选择性报告、其他偏倚[9]。ReVman 5.3被用来制作纳入文献的偏倚风险图。
1.5 统计学分析 应用Re Vman 5.3和STATA 12.0软件进行统计学分析。对于二分类变量ORR和治疗相关不良反应采用相对危险度 (relative ratio,RR)及95%CI作为效应量;对于生存资料PFS、OS 则采用风险比 (hazard ratio,HR)及95%CI表示效应量。对纳入研究的异质性进行Q 值检验和I2检验,当P≥0.1、I2≤50%时,说明各研究间有较好的同质性,采用固定效应模型,反之则说明各研究之间存在异质性,采用随机效应模型。当文献数量≥10篇时使用Egger法进行发表偏倚的检验,剪补法进行敏感性分析。P<0.05为差异有统计学意义。
2 结果
2.1 文献检索结果和纳入文献的基本信息 使用上述文献检索策略共检索到文献150篇,其中13篇存在数据重复,74篇文献涉及机制和小细胞肺癌与本研究不相关。在阅读全文后排除51篇文献,具体过程总结见图1。共纳入12篇随机对照试验文献[6,10-20],包含1 101 例NSCLC 患者,其中第1~5篇文献含PFS、OS,11篇文献含ORR,4篇文献含不良事件统计。纳入文献的基本信息具体见表1。
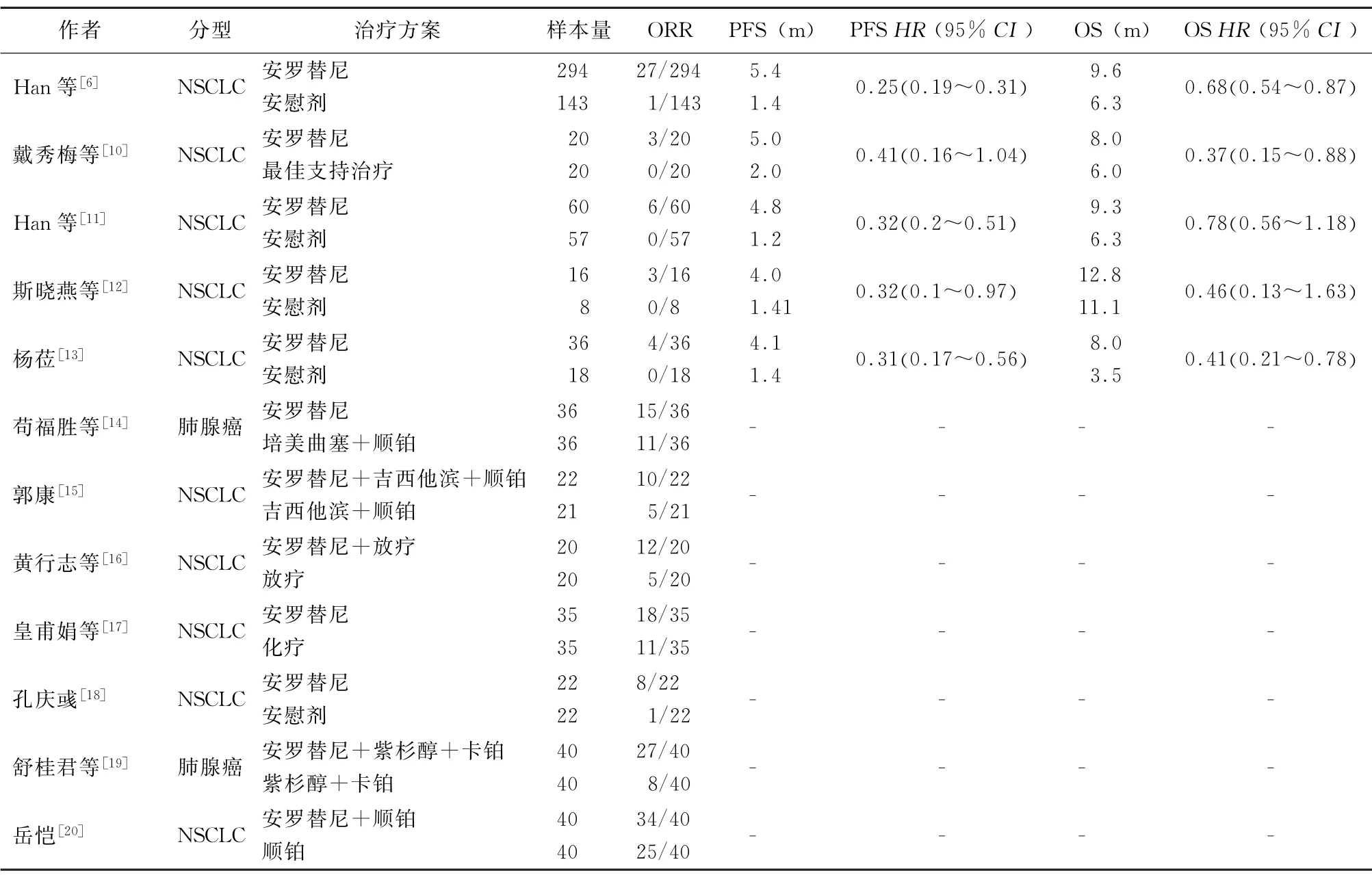
表1 Meta分析纳入文献基本信息

图1 文献检索及筛选流程
2.2 纳入文献的质量评价 纳入12篇文献的质量评价见图2。

图2 纳入文献的偏倚风险
2.3 疗效结果
2.3.1 无进展生存期 (PFS) 5篇文献[6,10-13]讨论了PFS,异质性P=0.77,I2=0%,故使用固定效应模型。结果显示,安罗替尼组能显著延长NSCLC患者的PFS,差异有统计学意义 (Z=11.90,P<0.01),见图3。

图3 安罗替尼组和对照组无进展生存期的森林图
2.3.2 OS 5篇文献[6,10-13]讨论了OS,异质性P=0.31,I2=17%,故使用固定效应模型。结果显示,安罗替尼组能显著延长NSCLC 患者的OS,差异有统计学意义 (Z=4.62,P<0.01),见图4。

图4 安罗替尼组和对照组总生存期的森林图
2.3.3 ORR 11篇文献[6,10-19]讨论了ORR,异质性P=0.17,I2=29%,故使用固定效应模型。结果显示,安罗替尼组能提高NSCLC 患者的ORR,且差异有统计学意义 (Z=6.53,P<0.01),见图5。

图5 安罗替尼组和对照组客观缓解率的森林图
2.4 安全性结果 4篇文献[6,10-12]具体报道了安罗替尼治疗晚期NSCLC的不良事件。结果显示,在3~4级不良反应方面,除高血压(Z=3.53,P<0.01)和手足综合征 (Z=2.07,P=0.04)之外,其他差异均无统计学意义,包括:转氨酶升高、腹泻、恶心呕吐、咯血、高甘油三酯血症、促甲状腺激素升高。Q值和I2检验异质性均较小,故采用固定效应模型。见图6~13。

图6 安罗替尼组和对照组高血压发生率的森林图

图7 安罗替尼组和对照组手足综合征发生率的森林图

图8 安罗替尼组和对照组转氨酶升高发生率的森林图

图9 安罗替尼组和对照组腹泻发生率的森林图

图10 安罗替尼组和对照组恶心呕吐发生率的森林图

图11 安罗替尼组和对照组咯血发生率的森林图

图12 安罗替尼组和对照组高甘油三酯血症发生率的森林图

图13 安罗替尼组和对照组促甲状腺激素升高发生率的森林图
2.5 发表偏倚和敏感性分析 Egger检验对纳入研究为11的ORR 进行发表偏倚的检验,结果显示存在发表偏倚 (P=0.014;图14,图15),但使用剪补法进行敏感性分析后,结果并未发生翻转(见图16)。

图14 客观缓解率的漏斗图

图15 Egger法检验客观缓解率的发表偏倚

图16 剪补法进行敏感性分析
3 讨论
本系统评价使用统计学方法比较安罗替尼组与对照组的PFS、OS、ORR 和不良事件,其结果表明安罗替尼对于晚期NSCLC 患者有良好的疗效和安全性。
PFS、OS采用HR表示效应量,ORR 和治疗相关不良事件 (treatment related adverse events,TRAE)则采用RR作为效应量,区间估算采用95%可信区间。对于PFS、OS,HR<1说明安罗替尼组疗效优于对照组,HR>1则相反。显然与对照组相比,安罗替尼能显著延长患者的PFS和OS,差异有统计学意义 (PFS:HR=0.28,95%CI:0.23~0.34;P<0.01;OS:HR=0.64,95%CI:0.53~0.78;P<0.01)。对于ORR,RR>1说明安罗替尼组疗效优于对照组,RR<1 则相反。结果显示RR=2.74,95%CI:2.02~3.71;P<0.01,说明安罗替尼能提高NSCLC 患者的ORR,差异有统计学意义。以上结果说明,安罗替尼与对照组相比,具有良好疗效。
2018年5月8日,中国国家药品监督管理局基于ALTER0303试验结果[6]批准通过了安罗替尼用于进展的晚期NSCLC 的三线治疗[7]。因此,本研究应将研究重点放在基于安罗替尼联合其他药物的疗效和安全性分析上。目前免疫疗法具有更好的疗效、更长的反应持续时间和可控的毒性反应,已成为晚期NSCLC的主要治疗选择之一[21]。Liu等[22]研究报道了安罗替尼可以抑制程序性死亡受体1 (programmed cell death protein-1,PD-L1)在血管内皮细胞上的表达,从而打破免疫耐受屏障,促进CD8+T 细胞浸润,改善CD8/FoxP3 的平衡。这项研究为临床应用安罗替尼联合免疫治疗提供新的理论和实践依据。
对于不良反应,RR<1说明安罗替尼的不良反应发生率较对照组低,RR>1则相反。Sun等[5]报道,安罗替尼最常见的3~4级不良反应是高血压(10%)、高甘油三酯血症(10%)、手足综合征(5%)和脂肪酶升高(5%)。在本研究中,除高血压(RR=23.06,95%CI:4.37~121.65;P=0.000 2)和手足综合征 (RR=5.99,95%CI:1.10~32.70;P=0.04)之外,其他3~4级不良反应方面差异均无统计学意义。安罗替尼产生高血压与手足综合征的具体发生机制目前尚不明确,但可能与抑制VEGF 通路有关。其潜在的发生机制为:阻断了VEGF 信号通路,血管内皮细胞发生凋亡,微血管网络变稀疏,抑制NO 合成,抑制血管扩张,内皮素1 增加,使血管收缩,产生高血压[23];同时活性氧 (reactive oxygen species,ROS)数量增多,内皮细胞受损,组织细胞和皮肤重建减少[24],引起手足综合征。这些不良事件都能通过患者教育、预防性措施、早期主动干预和安罗替尼剂量调整得到有效控制[25]。但需要指出的是,在使用安罗替尼过程中需要关注一些少见的不良事件,Zhang等[26]报道了2 例伴有纵隔转移的鳞癌患者在接受安罗替尼治疗中出现了气管食管瘘。Li等[27]报道1例安罗替尼引起支气管胸膜瘘的不良事件。Jiang等[28]报道了1例Ⅳ期鳞癌患者使用安罗替尼后出现主动脉夹层的不良事件,以上不良事件可能与患者的个体化差异有关,因此在使用安罗替尼治疗过程中要注意严密监测。
然而本研究存在以下局限性。(1)纳入的部分研究为单中心、小样本量的研究。(2)以PFS、OS为疗效指标的研究,对照组均为安慰剂或最大支持治疗,其结果只能说明安罗替尼疗效优于安慰剂;本研究无法得知其与其他治疗策略相比时的疗效。(3)对于ORR 这一指标结果,Egger检验显示存在发表偏倚,但使用剪补法进行敏感性分析后,结果并未发生翻转,说明数据结果稳定,后续仍需要更多研究来验证这一结果。(4)本研究未对患者进行分层的亚组分析,如肿瘤的病理类型、是否存在转移等,这些因素可能会对患者预后产生影响。(5)目前安罗替尼只在中国上市,纳入的人群均为中国人,因此本研究无法了解到安罗替尼对于其他人群的疗效和安全性。(6)安罗替尼上市时间短,目前较多试验仍处于研究中,数据结果难以获得。因此,未来需要进行更多样本量较大的研究来验证这些结果,尤其是安罗替尼与其他治疗策略相比较,或安罗替尼联合其他药物的疗效与安全性分析。
综上,本研究证实安罗替尼可以延长NSCLC患者的PFS、OS,提高客观缓解率ORR,安罗替尼对晚期NSCLC具有良好的疗效。安罗替尼可能会引起某些3-4级不良事件,尤其是高血压和手足综合征,但此类不良事件可以通过细致的管理得到有效控制。
利益冲突所有作者均声明不存在利益冲突
