基于深度学习的重建算法在CCTA高分辨率成像中的应用
2021-10-28王怡然詹鹤凤吴文杰侯佳蒙马雪妍张永高
王怡然,詹鹤凤,吴文杰,侯佳蒙,马雪妍,张永高
郑州大学第一附属医院 放射科,河南 郑州 450052
引言
多层螺旋CT技术的发展提高了心脏和冠状动脉的非侵入性成像能力,支持冠状动脉CT血管成像(Coronary CT Angiography,CCTA)在识别冠状动脉狭窄方面的广泛应用,但其性能受图像质量的影响。近年来,CCTA带来的辐射暴露问题不容忽视,迭代重建算法获得的CCTA与标准滤波反投影相比可以提高图像质量和诊断准确性。但目前冠状动脉钙化所导致的晕状伪影、射束硬化伪影等仍然限制CCTA评估阻塞性冠状动脉疾病(Coronary Artery Disease,CAD)的能力[1]。较低的图像噪声[2]可以允许使用更清晰的卷积核,这有助于在存在广泛冠状动脉钙化的情况下改善图像质量。但高权重迭代重建算法[3]会改变图像的噪声幅度和纹理特征,斑片状、不自然的图像纹理在多项研究中被证实。
目前,人工智能(Artificial Intelligence,AI)已经在心血管系统有初步应用,例如东芝的Advanced Intelligent Clear-IQ Engine (AiCE)[4]以及东软的AI辅助优化算法[5]。最近,作为机器学习和AI的一个子集,深度学习(Deep Learning,DL)显示出改善CT图像重建的潜力,因为它可以处理更多的模型和参数,远多于基于统计的迭代重建方法。GE公司研发的深度学习图像重建(Deep Learning Image Reconstruction,DLIR)[6](TrueFidelity,GE Healthcare)已经在体模[7]和临床研究[8-9]中被一些研究人员初步验证,并且图像纹理与高剂量条件下获得的滤波反投影相似。
本研究目的是与自适应统计迭代算法相比,探讨DLIR对高分辨率CT血管成像图像质量和诊断准确性的影响,并以有创冠脉造影作为验证。
1 材料与方法
1.1 研究对象
本研究经医院伦理委员会批准(2021-KY-0043-002),所有患者均签署知情同意书。前瞻性纳入在2021年2月至5月在Revolution CT接受扫描的56例疑似CAD患者,男31例,女25例,平均年龄(59.7±12.3)岁。入选患者平均BMI为(24.1±3.21)kg/m2,扫描平均心率为(72±10.6)次/min,排除造影剂过敏、慢性肾病(血肌酐>1.5 mg/dL或肾小球滤过率<45 mL/min/1.73 m2)、BMI>40 kg/m2、有冠状动脉支架置入史以及冠状动脉旁路移植术史的患者。
1.2 采集与图像重建
所有检查均在256层 Revolution CT扫描仪上进行,扫描参数如下:所有扫描均以高分辨率模式进行,平面内空间分辨率为0.23 mm×0.23 mm,准直256 mm×0.625 mm,矩阵大小为512×512像素,层厚和层间距为0.625 mm。Z轴空间分辨率0.23 mm,机架旋转时间280 ms,扫描范围140 mm或160 mm,显示视野为25 mm。为了最大限度地减少辐射暴露,根据心率,分别为每个患者选择回顾性心电门控或前瞻性心电门控。管电压120 kVp,采用自动管电流调制技术。扫描前舌下含服硝酸甘油0.5 mg,用双筒高压注射器经肘前静脉注射对比剂35~60 mL(碘海醇,350 mgI/mL,扬子江药业),流速3.5~6 mL/s,并追加生理盐水50 mL。用50%权重自适应迭代重建技术(Adaptive Statistical Iterative Reconstruction,ASIR)-V以及中、高级别DLIR(分别为DLIR-M和DLIR-H)重建CCTA图像,所有重建都应用了高清晰度卷积核。
1.3 图像评价
随后的测量在离线工作站(Advantage Workstation 4.7)上进行。将感兴趣区(Region of Interest,ROI)放置在左主干(Left Main Artery,LMA)、左前降支(Left Anterior Descending Artery,LAD)近段、左回旋支(Left Circumflex Artery,LCX)近段、右冠状动脉(Right Coronary Artery,RCA)近段和主动脉根部(Aorta Root,AR)的同一平面上测量CT值及其标准差(SD)代表噪声。根据SCCT18分段法[10]进行冠状动脉分段。同时将ROI放置在邻近血管周围组织中,用来计算血管的对比度噪声比。管腔直径小于1.5 mm的冠状动脉节段被排除在分析之外。为了计算信噪比(Signal to Noise Ratio,SNR)和对比噪声比(Contrast to Noise Ratio,CNR)[11],见式(1)~ (2):

图像质量定性评估由两位有经验的放射科医生对三支主要冠状动脉及整体图像质量目测进行,评分不一致则商讨达成共识。根据图像噪声、伪影大小、管腔的清晰度和对图像的总体印象用Likert评分法[12-13]进行评分(1=差,2=一般,3=中等,4=良好,5=优秀),得分在2~5分的图像视为满足诊断要求。
1.4 狭窄程度评估
两位有三年以上经验的放射科医生使用SCCT18分段法[10]在CT影像上共同评估是否存在管腔狭窄。显著的冠状动脉狭窄定义为狭窄程度大于50%,读者对重建技术未知。有创冠状动脉造影(Invasive Coronary Angiography,ICA)作为狭窄检测的参考标准,至少获得冠状动脉的两个正交视图以进行狭窄程度判定。
1.5 辐射剂量
容积CT剂量指数(Volumetric CT Dose Index,CTDIvol)、剂量长度乘积(Dose Length Product,DLP)在剂量报告中记录。用有效辐射剂量乘以心脏转换系数(k=0.026 mSv/mGy·cm)估算有效辐射剂量(Effective Radiation Dose,ED)。
1.6 统计学分析
使用专业统计软件SPSS 22.0进行统计分析。采用Kolmogorov-Smirnov检验对数据进行正态分布检验。连续变量用(±s)表示,分类变量用百分比和计数表示。采用Wilcoxon符号秩和检验比较三种不同重建算法的图像质量,通过Bonferroni校正调整后的成对比较以进行多次比较。P<0.05被认为有显著差异。McNemar检验比较每患者的敏感度、特异度和准确度,ICA作为参考标准比较三种重建技术在诊断准确性上的差异。
2 结果
2.1 图像质量
表1总结了主要冠状动脉和AR的图像质量的客观测量数据(噪声、SNR和CNR)。与ASiR-V 50%相比,DLIR-H的噪声明显减少,SNR和CNR明显增加(P值均<0.05)。在AR,DLIR-H(20.5 HU)和DLIR-M(23.7 HU)的噪声值明显低于ASiR-V 50%(51.1 HU)(P值均<0.001)。DLIR-H在每个测量位置有类似的趋势(P值均<0.05),DLIR-M也有类似的结果,但只有在AR、LMA、RCA的差异有统计学意义。DLIR-H的SNR和CNR明显高于ASiR-V 50%(P值均<0.05),而DLIR-M有相同的趋势,但在LAD和LCX,DLIR-M和ASiR-V 50%之间的差异不显著(P值均>0.05)。DLIR-H和DLIR-M在噪声、SNR、CNR方面没有发现显著差异(P值均>0.05)。表2显示了主观图像质量的详细定性分析。与ASIR-V相比,LAD、LCX、RCA在DLIR-H和DLIR-M的图像质量评分均有统计学意义的改善(P值均<0.001)。
表1 三组重建算法的图像噪声值、SNR及对比噪声比(±s)

表1 三组重建算法的图像噪声值、SNR及对比噪声比(±s)
项目 ASiR-V 50%组 DLIR-M组 DLIR-H组 P值P值ASiR-V 50% vs.DLIR-M ASiR-V 50% vs.DLIR-H DLIR-M vs.DLIR-H AR CT值/HU 440.9±70.1 441.1±70.3 441.3±70.4 0.977 — — —AR 噪声值 /HU 51.1±7.8 23.7±3.5 20.5±3.7 <0.001 <0.001 <0.001 0.071 AR SNR 8.7±1.5 18.9±3.7 22.8±9.9 <0.001 <0.001 <0.001 0.080 RCA 噪声值/HU 54.8±30.1 40.2±15.5 37.9±14.9 <0.001 0.002 <0.001 0.506 RCA SNR 8.1±3.2 11.4±5.3 12.1±5.7 <0.001 0.004 <0.001 0.586 RCA CNR 6.5±2.8 9.3±4.5 9.8±4.9 <0.001 0.006 0.001 0.611 LMA 噪声值/HU 49.1±14.6 36.9±14.2 34.7±14.0 <0.001 <0.001 <0.001 0.415 LMASNR 8.9±3.0 12.6±5.4 14.1±6.9 <0.001 <0.001 <0.001 0.402 LMA CNR 7.2±2.7 10.3±4.7 11.6±6.3 <0.001 <0.001 <0.001 0.423 LAD 噪声值/HU 57.7±18.0 48.7±17.7 46.9±17.0 0.014 0.085 0.017 0.594 LAD SNR 6.9±2.7 8.9±4.7 9.2±4.9 0.014 0.064 0.019 0.695 LAD CNR 5.5±2.3 7.1±3.9 7.4±4.0 0.016 0.066 0.023 0.726 LCX 噪声值/HU 58.0±15.6 50.8±16.3 48.5±15.7 0.006 0.068 0.006 0.458 LCX SNR 6.9±3.3 8.0±2.9 8.3±3.2 0.03 0.039 0.016 0.672 LCX CNR 5.5±3.2 6.3±2.5 6.6±2.8 0.029 0.125 0.036 0.666
表2 三组图像主观图像质量评分的对比(±s)

表2 三组图像主观图像质量评分的对比(±s)
项目 ASiR-V 50%组 DLIR-M组 DLIR-H组 P 值 P 值ASiR-V 50% vs.DLIR-M ASiR-V 50% vs.DLIR-H DLIR-M vs.DLIR-H RCA 3.1±0.6 4.0±0.6 4.2±0.5 <0.001 <0.001 <0.001 0.001 LAD 3.0±0.6 3.9±0.6 4.0±0.6 <0.001 <0.001 <0.001 <0.001 LCX 3.0±0.5 3.9±0.5 4.1±0.5 <0.001 <0.001 <0.001 <0.001基于病人分析 3.1±0.5 4.5±0.6 4.7±0.5 <0.001 <0.001 <0.001 <0.001
2.2 诊断准确性
两位读者评估了总共32例患者理论上480个冠状动脉节段,而107个节段由于解剖变异或起始处直径<1.5 mm(根据美国心脏协会的15段模型的参考标准定义)而排除。合并QCA的ICA发现17例(47%)患者的33处狭窄。其中单支病变10例,2支病变5例,3支病变2例。
用ASiR-V 50%重建的CCTA在17例经ICA确认的CAD阳性患者中正确检出15例,在15例阴性患者中正确排除7例,其敏感性、特异性和准确性分别为88%、60%和75%。用DLIR-M重建的CCTA正确识别了17名阳性患者中的15例,并正确排除了15名阴性患者中的9名,其敏感性、特异性和准确性分别为88%、60%和75%。用DLIR-H重建的CCTA正确检出了17例阳性患者中的16例,并正确排除了15例阴性患者中的10例。结果显示其敏感性、特异性和准确性分别为94%、66%和81%。不同重建的敏感性、特异性和诊断准确性均无明显差异(P>0.05)。
2.3 辐射剂量
CTDIvol的中位数是6.4 mGy(四分位数5.3~7.6 mGy),DLP中位数是103 mGy·cm(四分位数85~122 mGy·cm),ED中位数是2.7 mSv(四分位数2.2~3.1 mSv)。
3 讨论
本研究选择的患者冠脉钙化积分(Agatston积分)范围0~2326,涵盖了不同心血管疾病风险分层[14]。对于疑似冠心病的患者,采用高分辨率扫描模式和高清晰度卷积核进行重建。一般情况下,高分辨率扫描适合含钙化病变较多或支架置入术后患者,这可以减少与晕状效应相关的伪影。然而,对于体重较大的患者,其图像质量甚至下降到影响诊断的水平[15]。因此,本研究尝试通过一种新的重建算法来改善图像质量从而提升诊断信心。已知迭代重建算法,如模型迭代重建可以减少斑块周围的晕状伪影,并表现为所测量钙化斑块体积的减少。DLIR是否能减少晕状伪影的影响有待进一步研究。
关于客观图像质量,我们发现在大动脉和小冠状动脉中,DLIR产生的图像噪声更低,SNR和CNR比ASiR更高。DLIR的主观总体图像质量明显优于ASiR。特别是与ASiR-V 50%相比,DLIR-H可以在高清晰度卷积核下显著降低图像噪声。如图1所示,它还能提高非钙化斑块的识别率,但还没有经过大样本的验证。对于钙化斑块较严重的冠状动脉节段,DLIR只能改善钙化以外的血管壁的划分,因为高密度钙化的溢出效应[16]明显遮蔽了冠状动脉管腔,导致高估冠状动脉管腔的狭窄程度,尤其是对管腔直径原本较小的远段冠状动脉。一些研究利用改良后的减影冠状动脉计算机断层扫描血管成像[17]技术或去晕状伪影算法[5]来解决这一问题,但其成功率受到设备、扫描方案和后处理软件的限制。
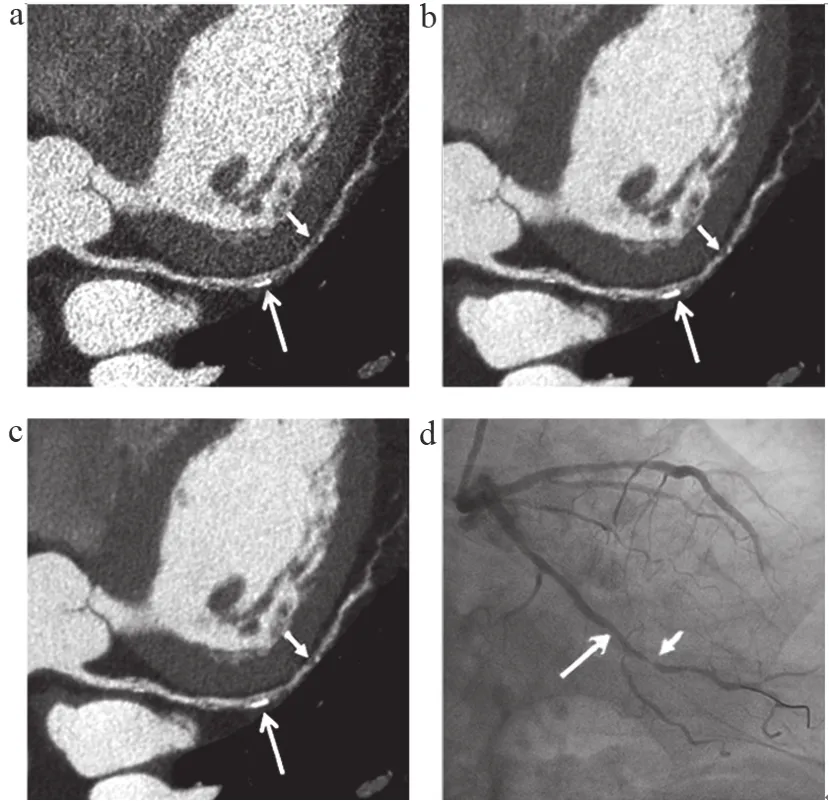
图1 患者男,70岁,分别用ASIR-V 50%(a)、DLIR-M(b)、DLIR-H(c)重建的曲面重组图和ICA图像(d)
我们的研究有以下局限性:① 这是一项单中心研究,纳入的人数相对较少,需要更大规模的多中心研究来进一步确定DLIR的诊断性能;② 对图像质量的定性评价可能会受到主观性和固有偏见的影响;③ 对于严重钙化的冠状动脉节段,目前仍没有很好的方法来减少钙化对管腔的遮蔽效应。
综上所述,DLIR提升了高分辨率扫描下冠状动脉CTA检查的图像质量,同时不影响CAD诊断的准确性,这有助于扩大CCTA的应用范围,从而减少不必要的后续检查,如ICA或放射性核素心肌灌注成像,从而节省经济成本并减少辐射暴露的风险。
