手术对合并髋部脆性骨折的血液透析住院患者生存的影响分析*
2021-10-25杨洁康建国李欣张利平王晓飞左力
杨洁 康建国 李欣 张利平 王晓飞 左力
(1.北京积水潭医院肾内科,北京 100035;2.首都医科大学教学医院国家电网北京电力医院骨科,北京 100073;3.北京大学人民医院肾内科,北京 100044)
随着老龄化社会的到来,髋部脆性骨折的发生率正在迅速增加。目前研究已经证实老年髋部骨折与高死亡率相关。我国慢性肾脏病(chronic kidney diseases,CKD)的发病率为11.8%,终末期肾病(endstage renal disease,ESRD)乃至透析患者人数日益增多,CKD 患者发生脆性骨折的风险极高[1-3],ESRD 患者因肾小球滤过率(glomerular filtration rate,GFR)降低,出现钙磷代谢异常,维生素D浓度降低,成纤维细胞生长因子23 和甲状旁腺素(parathyroid hormone,PTH)水平升高,这些均导致骨代谢异常,骨强度降低[4]。与普通人群相比,ESRD 患者的髋部骨折风险从4.1 倍增加到17.4 倍,因基础疾病重、并发症多,CKD 患者髋部骨折后的1 年死亡率为50%~64%。因此,不仅髋部骨折是临床医师需要面对的主要问题,合并髋部脆性骨折的血液透析患者的治疗方式选择是临床医师必须面对的更棘手问题[4]。然而,国内外对于合并髋部脆性骨折的血液透析患者,手术治疗与保守治疗相比能否延长骨折后的生存时间,鲜有报道。因此,本研究旨在探寻血液透析患者并发髋部脆性骨折经住院治疗后的生存状况,分析影响其生存时间的危险因素,探讨骨科手术是否能降低其死亡率,提高生存时间,以此来引起临床工作者对于这部分特殊人群治疗上的关注。
1 资料与方法
1.1 一般资料
纳入标准:①年龄≥55岁;②持续血液透析≥3个月;③髋部脆性骨折,包括股骨颈、股骨转子间和股骨近段粉碎骨折。排除标准:①髋部非脆性骨折患者;②开放骨折患者;③多发骨折或存在严重复合伤者;④失随访者;⑤合并恶性肿瘤者。
回顾性研究我院2008 年1 月到2019 年5 月收治的合并髋部脆性骨折的血液透析患者52 例,经纳入与排除标准筛查,42 例患者纳入本研究。根据入院后治疗方案选择的不同,分为手术组18 例和非手术治疗组24例。手术组男性6例,女性12例,年龄55~94 岁,平均(76.8±10.6)岁;非手术组男女各12 例,年龄57~95 岁,平均(74.0±10.9)岁。两组性别和年龄对比,差异无统计学意义(表1)。
表1 两组入院时一般资料比较()
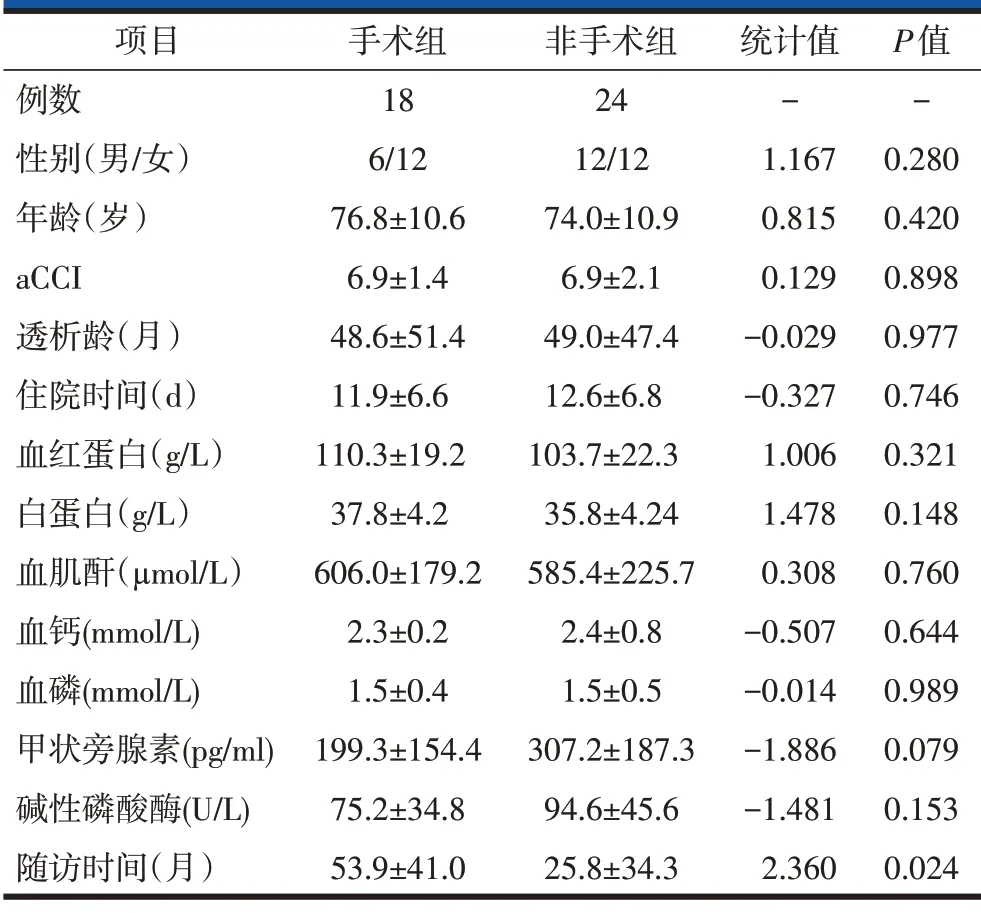
表1 两组入院时一般资料比较()
本研究获得伦理委员会批准,患者均签署知情同意书。
1.2 手术方法
根据髋部骨折的部位决定手术方式:股骨颈骨折8 例,给予人工髋关节置换手术(半髋或全髋关节);股骨转子间骨折10 例,患者给予闭合复位带锁髓内钉内固定手术。
1.3 观察指标
收集性别、年龄、年龄校正Charlson 合并症指数(age-adjusted charlson comorbidity index,aCCI)、入院前透析时间、住院时间、入院时的实验室检查(血红蛋白,白蛋白、血肌酐、血钙、血磷、甲状旁腺素、碱性磷酸酶)。记录患者从入院到死亡的时间,所有患者均随访至2021年5月1日终止。
1.4 统计学方法
采用SPSS 26.0软件进行统计分析。计量资料以均数±标准差表示,组间比较采用独立样本t检验;计数资料以百分比表示,组间比较采用χ2检验。通过Kaplan-Meier 法描述两组生存率,并绘制生存曲线,记录两组中位生存时间(月)和平均生存时间。通过log-rank 检验对比两组生存率的统计学差异。单因素Cox比例模型分析各个观察指标,筛选出有意义的指标进行多因素Cox回归分析,确定影响生存率的危险因素。以P<0.05为差异有统计学意义。
2 结果
手术组患者随访3~152 个月,平均(53.9±41.0)个月;非手术组随访1~160 月,平均(25.8±34.3)个月。两组患者经住院治疗后的Kaplan-Meier 生存曲线见图1。手术组生存率明显高于非手术组,两组的中位生存时间和平均生存时间分别是:手术组79.0个月和(71.6±13.3)个月,非手术组13.0个月和(39.7±12.0)个月。Log-rank检验发现两组生存率差异有统计学意义(P<0.05)。单因素Cox 比例模型分析显示,是否手术、年龄、透析龄是影响生存率的危险因素(表2)。多因素Cox回归分析显示手术治疗可延长患者生存率4.437 倍(95%CI:1.782~11.050),但同时也受到患者年龄大小和透析龄长短的影响,年龄越高、透析龄越长,患者的生存率越低(表3)。

图1 两组患者治疗后的Kaplan-Meier生存曲线

表2 单因素Cox比例模型分析相关指标对生存率的影响

表3 多因素Cox回归分析生存率的危险因素
3 讨论
对于合并髋部脆性骨折的血液透析人群预后研究相对较少,据文献报道,终末期肾病髋部骨折患者死亡率高[5,6]。美国7636例血液透析患者在髋部骨折后一年的死亡率约为50%[7]。合并髋部脆性骨折的血液透析患者预后较差,手术后较非透析髋部骨折患者死亡率更高,并发症更多[8-13]。此类患者手术对于预后的影响,鲜有报道。
本研究关注合并髋部脆性骨折的血液透析患者的生存情况,发现手术后患者的生存时间较非手术组明显延长,手术组生存率明显高于非手术组,而对手术患者预后功能恢复情况并未关注。因为此类人群较普通人群死亡率明显增高,若找到能改善生存状况的方法或者影响因素显得更有意义,如何延长生存时间、降低死亡率是目前此类人群急需破解的难题。
本文回顾性研究了我院合并髋部脆性骨折的血液透析患者,对他们治疗后的生存情况分析发现,手术组的生存率和生存时间明显高于非手术组,手术治疗可明显提高此类患者的生存率,延长生存时间。
患者入院时的一般状况是决定患者是否能够手术治疗的决定因素。患者入院后是否采取手术治疗受到多因素影响,合并髋部脆性骨折的血液透析患者手术和麻醉评估的时间较普通人群明显延长,手术和麻醉医师对这部分特殊人群的手术态度相对保守、谨慎,导致术前住院时间长。文献指出,术前住院时间往往是影响患者预后生存率的重要危险因素,建议尽快评估,尽早手术,可降低患者术后并发症和死亡率,但此类人群评估时间过久易产生并发症或合并症加重而不能手术,因此能手术的患者占比相对非透析人群要小[8]。
本研究两组患者入院时相关指标比较差异均无统计学差异(P<0.05),因此极大降低了本研究的抽样误差,结果可信度较高。
有研究对老年人髋部骨折进行荟萃分析,确定总体死亡率的危险因素为年龄较大、男性、养老院或设施住所、术前行走能力差、日常活动差、精神状态差、合并症等[9]。除上述因素外,血液透析患者髋部骨折后的死亡危险因素相对更多,ESRD和血液透析本身就是增加髋部骨折术后并发症和死亡率的危险因素[10-16]。
多因素Cox 回归分析结果显示是否采取手术治疗、年龄、患者入院前持续透析龄是影响患者住院治疗后生存率的危险因素,这与文献报道一致[8,10,15,16]。其中是否手术治疗的HR 为4.437,可以解读为保守治疗组死亡的风险是手术组的4.437倍,手术组预后生存情况更好。年龄的HR 为1.067、入院前透析龄HR为1.015,即在治疗方案相同时,年龄越大,透析龄越长,患者的预后生存情况越差。文献报道Charlson合并症指数对髋部骨折预后死亡率有影响[17],本研究代表总体健康状态的aCCI 的P值>0.05(表2),未发现统计学差异,可能与研究入组患者aCCI均很高,样本量少有关。aCCI包括16种疾病,且与年龄相结合,反映了患者总体健康状况。本研究中两组aCCI值均很高,提示合并髋部脆性骨折的血液透析患者合并症多、年龄大、短期和长期死亡率高,这对于手术是个极大的挑战,需要骨科、麻醉科、肾病内科及其他科室多学科协同处理,围手术期要给予患者特殊护理关照[4]。
由于本组数据骨密度数值缺失,遂未分析。文献报道,桡骨远端[18,19]、髋部[20,21]、椎体[22,23]等部位骨密度和透析患者死亡率存在相关性。
本研究还存在诸多局限性,首先是回顾性研究,且病例数较少,因为ESRD特别是血液透析患者合并骨折后,如何处理是临床上相对棘手的问题,骨科手术医师处理起来相对保守,手术意愿相对较低,能够收入院治疗的患者相对较少,本研究跨度十余年,最终入组42例。虽然病例数较少,除骨密度外,其余观察指标完整,随访期间绝大多数患者发生了终点事件,因此研究结果可信度仍较高。今后随着老龄化社会的到来,此类人群会越来越多,本研究将继续扩大样本量,关注骨密度对于血液透析人群的骨折及生存的影响,通过进一步研究来验证结果的可靠性。另外血液透析患者采用的透析方式是否会对结果产生影响,还有骨折的部位、骨折的严重程度、手术组患者手术方式及手术创伤的大小、患者入院后产生的并发症等因素均未考虑,需要在今后研究中进一步完善。
虽然本研究存在诸多局限性,但因为国内外对合并髋部脆性骨折的血液透析患者生存状况的研究鲜有报道,因此本研究可能会引起国内学者对这部分特殊人群治疗的关注,随着研究的不断深入,可增强我国临床医师,特别是骨科和麻醉医师,对这部分人群积极开展手术治疗的信心。
