美国FDA MAUDE数据库呼吸机不良事件监测分析
2021-10-23王新茹胡永新王丽夏兵马雪皎刘伟
王新茹 胡永新 王丽 夏兵 马雪皎 刘伟*
1 河南省药品评价中心 (河南 郑州 450005)
2 郑州大学药学院 (河南 郑州 450005)
内容提要: 目的:分析呼吸机不良事件相关数据,探讨影响呼吸机安全性的相关因素,为临床合理及安全使用呼吸机提供建议。方法:通过对美国MAUDE数据库中1287份呼吸机不良事件情况进行统计分析,初步探讨呼吸机的风险因素。结果:呼吸机不良事件器械故障主要为触摸屏故障、报警系统故障、设备部件故障和通电故障等;患者伤害主要为血氧饱和度下降和损伤。结论:呼吸机生产企业应当加强呼吸机易损零部件质量控制,主动对自身产品进行可疑不良事件的监测;使用单位应加强对呼吸机使用人员的培训和护理改善,并加强对呼吸机的维护;监管部门应强化监测工作力度,加强风险管控。
呼吸机是医疗机构常用的急救设备之一,用于抢救危重患者的生命。其能改变、控制或代替人的正常生理呼吸,改善呼吸功能,增加肺通气量,减轻呼吸功消耗,节约心脏储备能力。主要原理是呼吸机在吸气相时会产生正压,患者会将气体压入到肺内,当压力上升到一定水平时,呼吸机会停止供气,呼气阀打开,胸廓和肺产生被动性的萎陷,产生呼气[1]。按连接方式可以分为有创呼吸机及无创呼吸机两大类。
自新冠疫情以来,呼吸机作为急救设备得到了广泛使用,呼吸机不良事件应得到高度重视。根据国家药品监督管理部门发布的《国家医疗器械不良事件监测年度报告》,呼吸机不良事件报告数从2016年1980例到2020年118730例,呈逐年增加的趋势[2]。但相较于美国,我国医疗器械不良事件监测工作起步较晚,在基础数据的维护、报告质量的控制等方面仍有一定差距,而美国的MAUDE数据库内容比较丰富,在国际医疗器械不良事件报告系统中属于数据完整性、有效性、可追溯性均较高的数据库[3]。本文通过对美国FDA MAUDE数据库中的呼吸机不良事件报告进行统计分析,为临床合理安全使用呼吸机提供参考。
1.数据收集
检索FDA MAUDE(Manufacturer and User Facility Device Experience)数据库,以“Ventilator”作为Brand Name的检索条件,由于检索到不良事件报告中“RESPIRONICS CALIFORNIA,INC”公司生产的呼吸机的报告数占比最多,因此选取RESPIRONICS CALIFORNIA,INC公司生产的呼吸机不良事件报告为本文研究对象,在Manufacturer信息框中输入“RESPIRONICS CALIFORNIA,INC”,共获取2020年第三季度RESPIRONICS CALIFORNIA,INC公司生产的呼吸机不良事件报告1287份。将导出的CSV文件用Excel进行汇总,作为数据源进行分析。
2.数据分析
2.1 不良事件报告来源
1287份报告中,1279份来源于生产单位,占比达99.38%;仅8份来源于使用单位,占0.62%。呼吸机不良事件报告主要由生产企业报告,这表明美国医疗器械生产企业的不良事件监测意识较强。
2.2 不良事件类型
呼吸机不良事件类型可分为:①导致患者伤害31例,占2.41%;②器械故障1256例,占97.59%。数据显示,呼吸机不良事件主要为器械故障,患者伤害类型所占比例较小。
2.3 不良事件表现与原因分析
器械故障主要表现为触摸屏故障、报警系统故障、设备部件故障和通电故障等;患者伤害主要为血氧饱和度下降和损伤。具体表现形式及原因分析见表1。
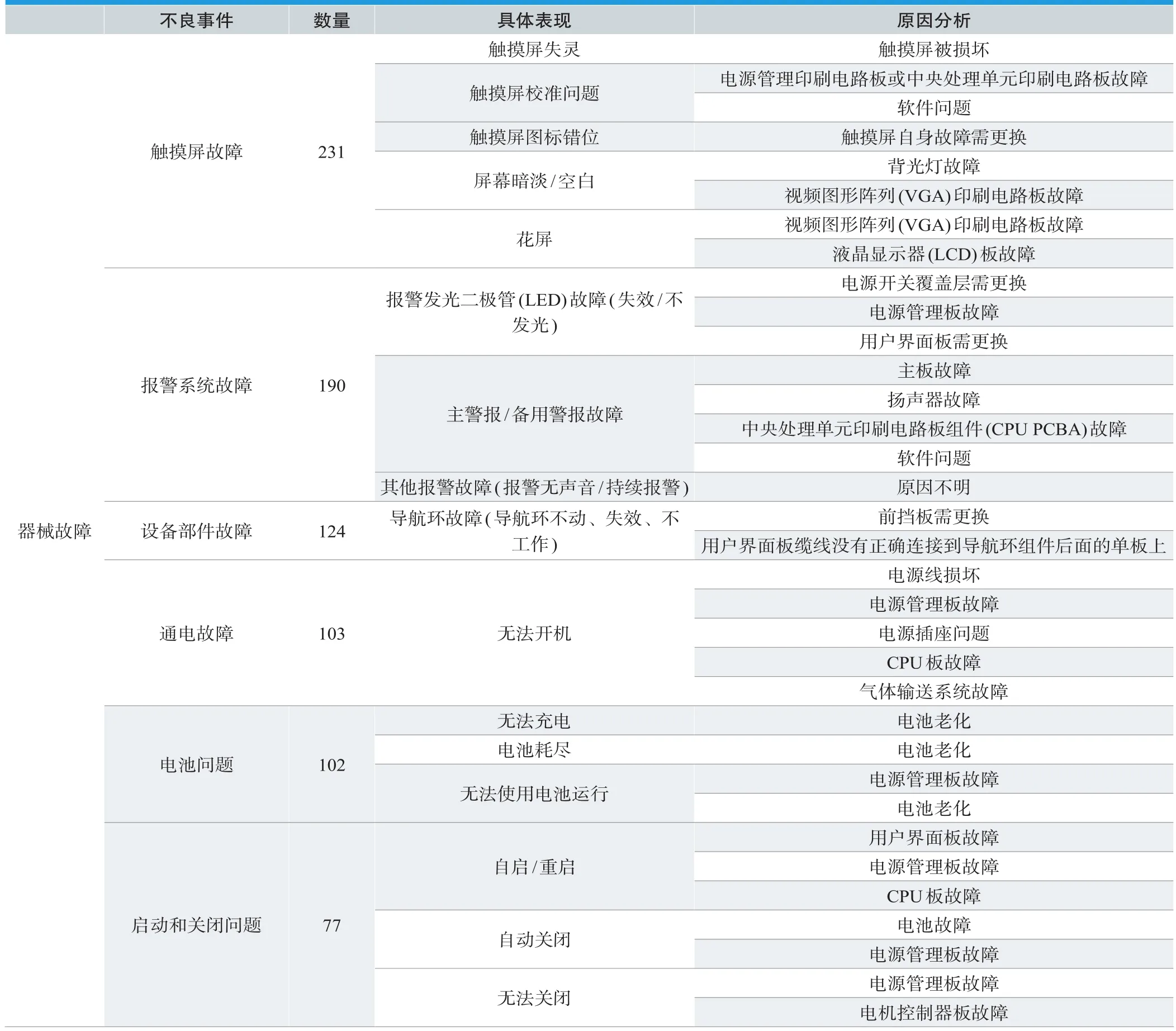
表1. FDA数据库呼吸机不良事件汇总及原因分析
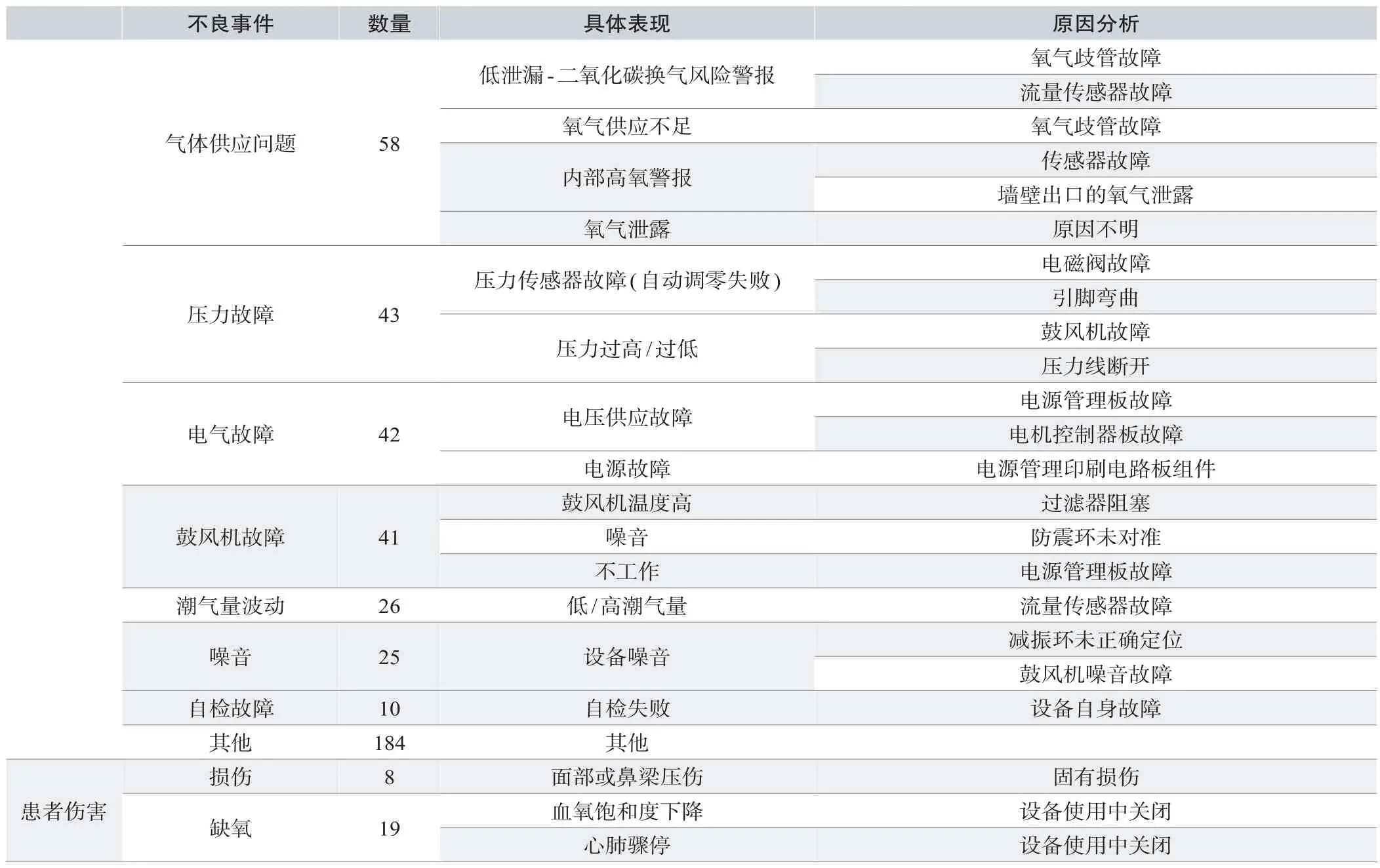
不良事件 数量 具体表现 原因分析低泄漏-二氧化碳换气风险警报 氧气歧管故障流量传感器故障氧气供应不足 氧气歧管故障内部高氧警报 传感器故障墙壁出口的氧气泄露氧气泄露 原因不明气体供应问题 58压力传感器故障(自动调零失败) 电磁阀故障引脚弯曲压力过高/过低 鼓风机故障压力线断开电气故障 42 电压供应故障 电源管理板故障电机控制器板故障电源故障 电源管理印刷电路板组件压力故障 43鼓风机温度高 过滤器阻塞噪音 防震环未对准不工作 电源管理板故障潮气量波动 26 低/高潮气量 流量传感器故障噪音 25 设备噪音 减振环未正确定位鼓风机噪音故障自检故障 10 自检失败 设备自身故障其他 184 其他鼓风机故障 41损伤 8 面部或鼻梁压伤 固有损伤缺氧 19 血氧饱和度下降 设备使用中关闭心肺骤停 设备使用中关闭患者伤害
4例死亡报告中,患者死亡原因均为使用呼吸机期间患者缺氧无法呼吸而致死。分析患者缺氧原因,1例原因不明,其余3例疑似为呼吸机器械故障,如患者在使用过程中呼吸机关闭,使用人员参数设置错误未产生警报以及屏幕变黑无法重启等。
3.讨论
3.1 报告来源
美国呼吸机不良事件报告主要来源于生产单位,占比99.38%。2020年,我国共收到536055例不良事件报告,其中报告来源大部分属于使用单位,上报455782份,占报告总数的85.03%[2]。提示我国生产企业不良事件报告意识薄弱,产品质量安全和不良事件监测主体责任意识有待进一步加强。
3.2 呼吸机不良事件表现
美国MAUDE数据库中,呼吸机不良事件以器械故障为主,器械故障主要表现为触摸屏故障、报警系统故障、设备部件故障和通电故障等;患者伤害主要为血氧饱和度下降和损伤。发生原因主要为电源管理印刷电路板故障、中央处理单元印刷电路板故障、电池老化、传感器故障、参数设置不当、设备未定期维护、未定期更换电池、未定期更换传感器,患者没有谨遵嘱咐等。
通过检索汇总我国呼吸机召回情况(2015年~2020年),国内呼吸机生产企业召回原因主要是由于设备本身硬件或软件故障,如触摸屏故障、指示灯故障、设备组件故障、软件设置故障等。查询呼吸机监督抽检不合格公告及通告,发现近年来国内呼吸机主要不合格项或主要问题主要集中于设备外部标记和设备本身的故障。因此,呼吸机生产企业要提高风险意识,加强呼吸机质量控制,保证产品质量,从而保障患者的用械安全。
3.3 对策与建议
3.3.1 对生产企业的建议。呼吸机一旦发生机械故障,如屏幕突然变黑关机,时间不允许工作人员对呼吸机进行故障排除,因此生产企业应当加强呼吸机质量控制,特别是易损零部件如传感器、电路板和氧电池等,应保证易损部件质量,降低设备零部件故障发生率,主动对自身产品进行可疑不良事件的监测,提高风险意识,努力改进产品性能和研发新产品;同时,要加强对企业人员的培训,通过更加全面、严谨、详细的说明书告知医务人员和使用者呼吸机的操作要点和注意事项,从而保障呼吸机的安全使用,减少不良事件的发生[4]。
3.3.2 对使用单位的建议。美国FDA MAUDE数据库中患者伤害大多属于通气过程本身的固有伤害,如血氧饱和度下降、心肺骤停以及面部或鼻梁压伤等,呼吸机机械通气患者有发生多种相关并发症的风险,包括呼吸机相关性肺炎(VAP)、急性呼吸窘迫综合症(ARDS)、气压伤、肺水肿和肺不张等,以及通气过程本身相关的并发症,如低氧血症、心脏骤停、面部或喉部损伤等,这些所有可能的并发症可以统称为呼吸机相关性事件(VAE)[5]。VAE通常由感染、液体超负荷以及患者自身疾病引起。通过一些护理干预措施能够降低VAE风险,如口腔护理、每日协同自主觉醒试验(SAT)和自主呼吸试验(SBT)、限制或缩短插管时间等[5-7]。4例死亡报告显示,患者缺氧主要原因为使用不当。另有文献报道的4例死亡案例也均为呼吸机使用不当造成的,如使用前缺乏验证,无法检查通气效果以及在发生事故时延迟求助于备用通气系统[8]。因此,使用单位应加强对呼吸机使用者的培训与设备维护。确保临床医务人员能够标准化并熟练使用呼吸机,快速响应常见警报或故障,并及时进行处理,从而预防不良事件的发生。
3.3.3 对监管部门的建议。建议监管部门强化上市后监管力度,特别是强化医疗器械不良事件监测工作力度,加强风险管控,完善呼吸机不良事件填报和收集工作;同时关注国内外呼吸机风险,及时发布预警信息,并督促相关企业采取修改说明书、完善警示标识、自主召回等相应的控制措施降低产品风险,以减少呼吸机使用中的安全风险问题发生[9-11]。
