甲烷/氮气辉光放电产物的红外吸收光谱研究
2021-10-23钱佳丽黄晓东刘珂邓伦华
钱佳丽,黄晓东,刘珂,邓伦华
(华东师范大学精密光谱科学与技术国家重点实验室,上海 200062)
0 引言
甲烷(CH4)是很多类地星体的主要气体成分。在地球上,CH4是天然气中的主要化合物,是一种很有前途的替代燃料和化学品原料[1]。CH4的来源多种多样,包括小型天然气田、页岩气、煤层气、农业沼气和深海甲烷水合物。大部分天然气储量位于偏远地区,运输成本高昂。此外,分散的天然气储量没有较高商业价值,工业上通常把低商业价值CH4转化为增值产品,但在转化过程中会生成有毒物质[2]。
氰化氢(HCN)是烷烃转化过程中极易产生的一种剧毒化学物质,人们一直关注HCN 的生成和测量[3-17]。HCN 容易由碳氢化合物和含氮物质产生,特别是在含碳、氢、氮元素的放电等离子中,可以产生较高浓度的HCN 分子。Driessen 等[4]对四(二甲氨基)钛有机物在N2-H2-Ar 混合气体中放电得到HCN。Pirali 和Vervloet[5]发现气相多环芳香烃在微波和射频放电时的主要产物之一为HCN。Fujii 等[6]研究了N2和C2H2的微波放电,用质谱技术检测到了HCnN(n=1~7)物质。Smith 等[7]利用NH3研究NHx+H=NHx-1+H2反应,发现加入C1碳氢化合物就能生成HCN。此外,CN 基团和一些碳氢化合物在一定条件下反应也可生成HCN[8]。HCN 生成机制与含氮物质息息相关,Alzueta 等[9]早在1997 年就进行了碳氢化合物和NO 反应机制的研究,发现大部分NO 都转换为HCN,这一结论在Meunier 等[10]做丙烷燃烧反应实验时得到验证。
CH4是简单的烷烃分子,在含氮氛围下极易产生HCN。Jauberteau 等[11]、Guan 等[12]在N2的放电余晖中研究CH4的反应,得到主要产物为C2N2、CN 以及HCN。Hempel 等[13]在CH4和甲醇中加入H2-Ar-N2微波等离子体,发现产生了C2H2、HCN 等九种稳定的物质。Pringle 等[14]研究了大气压下的CH4等离子反应,得到HCN 和NH3是最主要的终端产物。Tanarro 等[15]则在低气压下对CH4-N2-H2混合气进行直流放电,发现只产生少量的HCN。Gorodetskii 等[16]发现在放电管的阴极附近形成了碳氢薄膜(a-C:H),并认为是HCN 的主要来源。Horvath 等[17]对CH4-N2(2:98)进行了电晕放电,发现最主要的产物是C2H2,却只有少量的HCN 存在。Torokova 等[18]研究了大气压下CH4-N2混合气体的辉光放电,发现C2H2、HCN 和CH3CN 是最主要的产物。检测HCN 气体生成和转化途径的方法主要有质谱、傅里叶变换发射光谱、激光诱导荧光光谱以及激光吸收光谱技术等[3,4,6,13,14,16,17]。其中,激光吸收光谱法(LAS)具有高灵敏度、高选择性、高分辨率、非侵入性测量和快速响应等特点。
在含有氮元素分子时,CH4生成HCN 机制是非常复杂的,与母体分子、气压和放电方式等都息息相关。在CH4和N2混合气体放电等离子中,产生HCN 的参数以及途径仍旧不很明确。本文研究CH4和N2辉光放电等离子中的主要产物,采用中红外激光吸收光谱技术,结合波长调制技术测量产物中HCN和C2H2的吸收光谱。通过改变母体分子中CH4和N2分子的浓度比例来调控主要产物的生成方向;研究主要产物生成浓度与母体分子组分浓度的依赖关系;分析主要产物HCN 的生成途径。
1 实验方案与装置
实验装置如图1 所示。放电管是90 cm 长、带有水冷套管的圆筒直柱型玻璃管,两端各用紫铜电极和氟化钙窗片密封。辉光放电采用20 kHz 交流高压电激发,在管中形成较均匀的等离子体。放电管内充入流动气体,气体流量用机械泵配合质量流量控制器(北京七星华创,D07-19B)控制,并用热偶真空计(家君真空,ZDJ-3 型)测量放电管中的气压。采用光源的工作波长在3.06 μm(Nanoplus GmbH)。函数发生器(RIGOL DG811)产生的三角波与锁相放大器(Stanford Research Systems SR830)产生的正弦波叠加后,通过激光控制器(Stanford Research LDC 501)对激光进行波长扫描和调制。激光的波长利用C2H2吸收光谱的波长进行校正。激光通过吸收池后,用光电探测器(Vigo PVI-4TE-3.4)接收,所测信号送到锁相放大器进行解调(时间常数为30 μs)。光谱利用数字示波器(Tekronix MSO 2024B)采集。
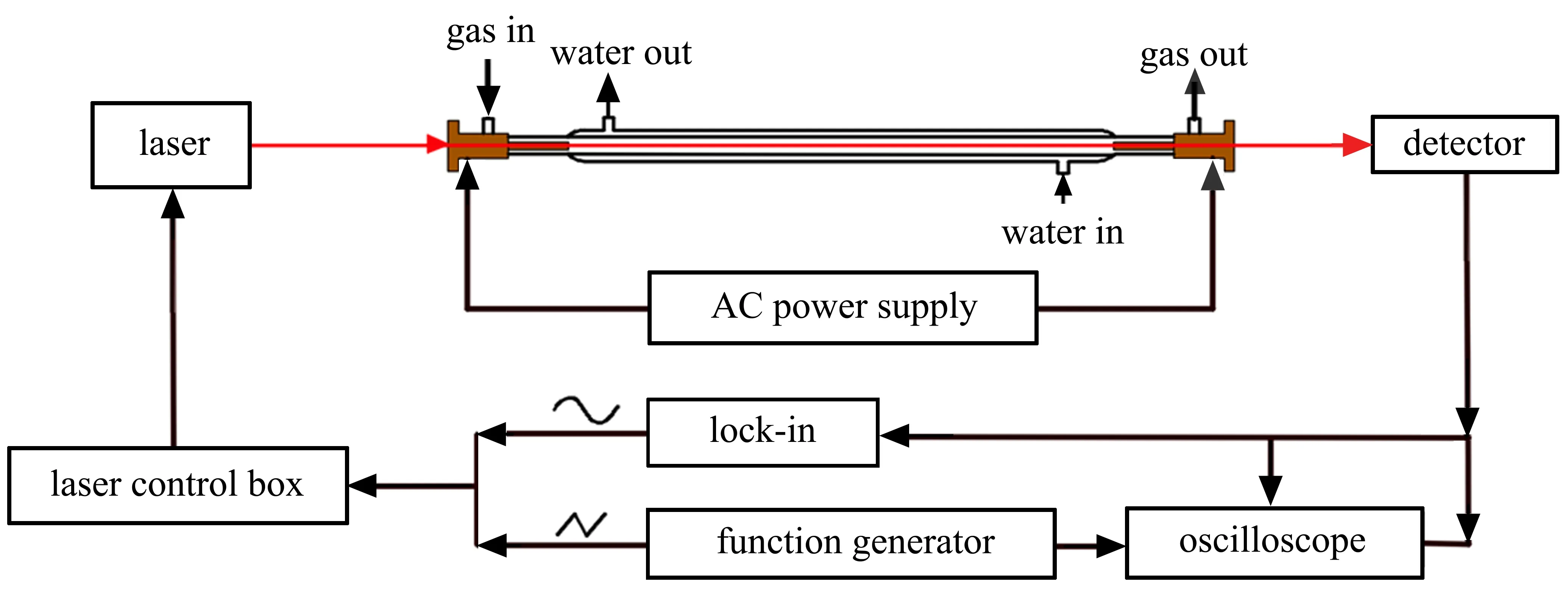
图1 CH4-N2 辉光放电实验装置示意图Fig.1 Schematic diagram of CH4-N2 glow discharge experimental setup
2 实验结果与讨论
2.1 纯CH4 放电吸收光谱
图2 所示为CH4放电等离子体的波长调制吸收光谱。实验中,放电管中的本底气压为3 Pa,充入纯CH4的气压为10 Pa,在该气压下可以产生稳定的辉光放电。为了校准测量光谱的频率,实验时在放电管前面的光路上放了一个低气压C2H2气体池,图2 中标注了来源于C2H2分子的吸收光谱。除了C2H2气体的吸收光谱,还测量到很强的HCN 分子的吸收光谱,图中C2H2和HCN 分子的吸收光谱标识参考了HITRAN 数据库[19]。Raulin 等[20]研究CH4-N2反应时,发现主要产物之一为HCN。Torokova 等[21]研究N2/CH4混合气辉光放电时也发现HCN 是主要产物之一。这些研究中,CH4都混合了含氮元素分子。图2 是纯CH4放电得到的光谱,认为HCN 是空气中痕量N2渗透到CH4放电等离子体中反应的产物。虽然实验中只充入纯CH4气体到放电管,但极其微量的大气也可能进入到放电管中,大气中的N2是HCN分子中N 元素的来源,该实验说明CH4等离子体极易生成HCN 分子。
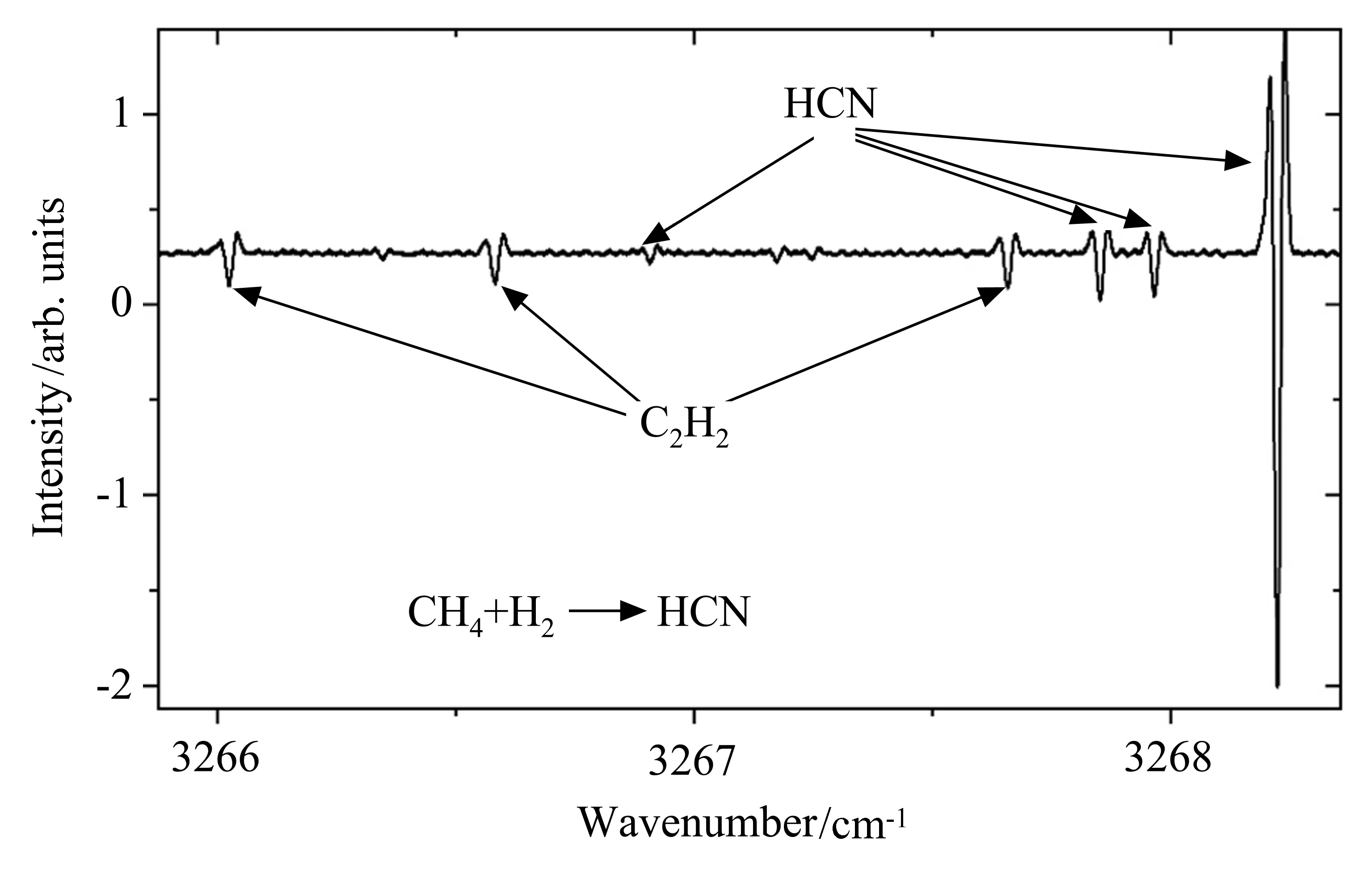
图2 纯CH4(10 Pa)辉光放电等离子体波长调制吸收光谱(WMS)Fig.2 The observed WMS absorption spectrum of pure CH4 plasma(10 Pa)
Gorodetskii 等[16]在CH4直流放电时,发现阴极区域的碳沉积速率远强于阳极区域,但向阴极引入与CH4等量的N2后,发现碳沉积速率急剧降低,从而认为在阴极处C-H 消耗一个N 生成了HCN。Torokova等[18]利用气相色谱-质谱技术(GS-MS) 联用,并结合X 射线光电子能谱技术,研究了CH4/N2辉光放电产物。他们得出HCN 的主要来源途径是CH3+N→HCN+H2;以及通过H2CN 中间产物的两步反应:CH3+N→H2CN+H,H2CN+N→HCN+NH。这一结论得到Horvath 等利用傅里叶变换红外光谱(FTIR)和发射光谱(OES)实验测量结果的验证[22]。由于两步反应会产生NH 自由基,并且NH 自由基A2Σ+-Χ2Π电子态跃迁在当前激光波段有很强的跃迁[23]。但是,在实验中没有看到NH 分子的吸收光谱。因此,当前实验条件下,即CH4浓度远大于N2浓度时,HCN 的主要产生途径为CH3+N→HCN+H2。
由于CH4放电等离子本身也可能产生C2H2分子[18,22,24],去掉放电管之前的C2H2标准气体池,并逐渐增加放电管中的CH4气压到30 Pa,进行辉光放电所测光谱如图3(a)所示。除了HCN 分子的吸收光谱外,还监测到C2H2分子的吸收光谱,这些C2H2分子均来自CH4的放电等离子体。图3(b)记录了HCN和C2H2光谱强度随放电管中CH4流量的变化。从图中可以看出,HCN 的浓度随CH4浓度增加而增加,但当CH4浓度持续增加时,HCN 的浓度会缓慢减小。因为当CH4浓度比较低时,增加CH4能够提供足够的气体与泄露进放电管的N2反应生成HCN,从而使HCN 光谱强度随CH4气体浓度增加而增加。但是,随着CH4气体的持续增加,挤压了泄露进放电管的N2,同时快速流动的CH4使得CH4与N2的反应时间缩短,因此放电等离子中气体参与反应的时间也至关重要[18]。
在图3(b)中,C2H2的浓度随CH4浓度的增加而持续增加。Horvath 等[22]基于C2的光谱和积碳现象,得出CH4产生C2H2有两种可能途径:1)CH+CH→C2H2;2)CH2+C→H+C2H,CH2+C2H→CH+C2H2。Torokova 等[18]分析了CH4分解所需的电子能量,认为C2H2的产生主要源于CH2+CH2→C2H2+2H 的方式。本实验中,CH4辉光放电产生了大量积碳,并且同样的CH4放电装置可以产生CH 自由基[25],所以C2H2的产生可能更符合Horvath 等分析的途径。
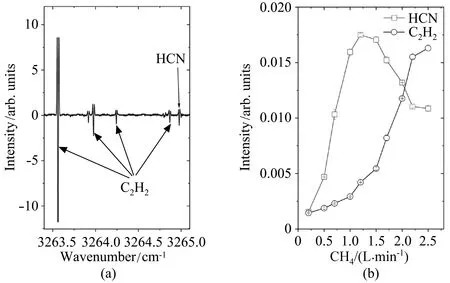
图3 (a)放电管中动态CH4 气压为30 Pa 时放电等离子体的吸收光谱;(b)HCN(@3264.981596 cm-1) [19] 和C2H2 (@3265.255045 cm-1) [19] 的光谱强度随CH4 流量的变化Fig.3 The absorption spectrum of the discharge plasma was obtained when the CH4 pressure in the discharge tube is 30 Pa;(b)The change of spectral intensity of HCN(@3264.981596 cm-1) [19] and C2H2 (@3265.255045 cm-1) [19] with methane flow rate
鉴于CH4/N2放电等离子生成C2H2和HCN 的浓度强烈依赖于CH4和N2分子的浓度,进一步优化放电管的真空,排除泄露到放电管中大气中的N2对实验结果的干扰。然后,通过精确操控CH4和N2在放电管中的浓度比来调控C2H2和HCN 的生成方向。
2.2 CH4/N2 辉光放电产物与CH4 和N2 浓度比的关系
Chen 等[26]研究了CH4/N2微波等离子体,发现当n(CH4)/n(N2) <0.995 时,HCN 为优势产物;而n(CH4)/n(N2) >0.995 时,则C2H2为优势产物。在设计实验时,以n(CH4) :n(N2)=1 :1 为基准,分CH4过量和N2过量两种条件,研究C2H2和HCN 光谱强度随n(CH4):n(N2)比率的变化。
图4 显示的是保持CH4浓度不变(2.0 L/min),当n(CH4):n(N2)<1:1 时,HCN 和C2H2光谱强度随N2浓度增加的变化。在图4(a)中,HCN 的光谱强度随着N2浓度增加而增大;在图4(b)中,C2H2的光谱强度随着N2浓度的增加而减小。在CH4流量更小(0.5 L/min)或者更大(3.0 L/min)时进行类似实验,HCN和C2H2浓度变化跟n(CH4) :n(N2)比率也有类似图4 的趋势。这些结果表明,当n(CH4) :n(N2) <1 :1时,增加CH4/N2混合气体中的N2浓度,反应过程会趋向氮化反应。当混合气体中N2的浓度比例较大时,在等离子体的上、中游中活性的N 微粒浓度增加,下游中的CN 微粒相应增加,因而提高了生成HCN的选择性[26]。此外,Hamann 等[27]认为石墨电极完全可以替代含碳气体作为反应的前物,而这个过程也称为活性等离子体氮碳共渗透技术(ASPNC)。由于吸收池管道里早已积累了固体碳杂质,HCN 光谱强度增加的另一个可能原因是放电管中的积碳也参与了反应,所以在反应物N2较多的情况下,反应趋势是朝着HCN 的方向进行的。
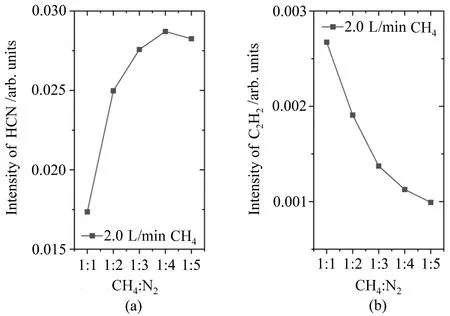
图4 保持CH4 浓度不变时,不同CH4/N2 配比下(a)HCN(@3264.981596 cm-1) [19] 和(b)C2H2 (@3265.255045 cm-1) [19] 的光谱强度Fig.4 When keeping the CH4 concentration stable,the spectral intensity of(a)HCN(@3264.981596 cm-1) [19] and(b)C2H2 (@3265.255045 cm-1) [19] under different ratio of CH4/N2
图5 显示的是保持N2浓度不变(2.0 L/min),当n(CH4) :n(N2) >1 :1 时,HCN 和C2H2光谱强度随CH4浓度增加的变化。在图5(a)中,HCN 的光谱强度随着CH4的浓度增加而减小;而在图5(b)中,C2H2的光谱强度则是随CH4浓度的增加而增加。在N2流量更小(0.5 L/min)或者更大(3.0 L/min)时进行类似实验,HCN 和C2H2浓度变化与n(N2) :n(CH4)比率也有类似图5 的趋势。在放电等离子体中,电子的传能作用产生了活性微粒,进而影响了产物的选择性[26]。打破CH4的C-H 键所需能量比打开N2的N≡N 键所需能量小得多,当混合气体中CH4浓度增加时,更多能量用于裂解CH4产生CH3、CH2和CH以及H 等自由基,从而最终导致C2H2浓度随混合气体中CH4浓度增加而增加。相应地,虽然混合气体中N2浓度不变,但随着N2分配到的裂解能量在减小。此前的研究表明,CH4/N2混合气体等离子体产生CN 自由基有一个最佳的母体浓度混合比[12,26];当CH4浓度超过最佳浓度比例后,随着CH4浓度的增加,会导致产生的CN 浓度减少[12],这样最终导致HCN 浓度随CH4浓度而减少。
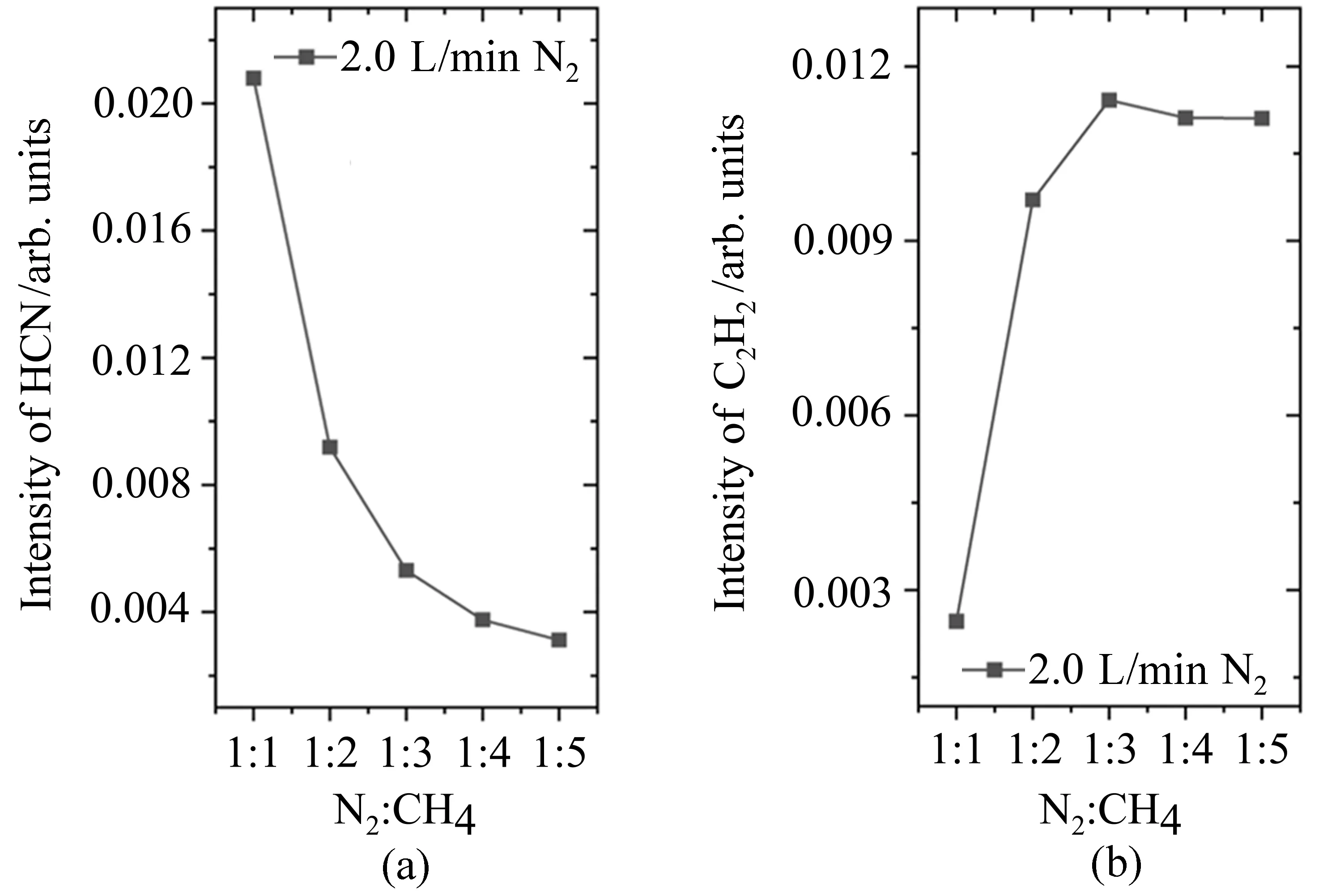
图5 保持N2 浓度不变时,不同CH4/N2 配比下(a)HCN(@3264.981596 cm-1)和(b)C2H2 (@3265.255045 cm-1) [19] 的光谱强度Fig.5 When keeping the N2 concentration stable,the spectral intensity of(a)HCN(@3264.981596 cm-1)and(b)C2H2 (@3265.255045 cm-1) [19] under different ratio of N2/CH4
由于CH4/N2混合气体放电等离子产生大量C2H2,此处也对C2H2/N2混合气体进行了辉光放电。实验发现C2H2/N2放电也能产生HCN。Rimmer 等[28]总结HCN 形成的必要条件是:1)N2的N≡N 三键需要被打开;2)在争夺自由N 的竞争中,C 要战胜O,因此需要满足C/O≥1,而C 的提供者不仅可以是CH4,也可以是CO2或者C2H2[6]。因此,在含CH4的放电等离子中,不仅能生成HCN,而且能生成C2H2,而后者能够进一步生成HCN。
3 结论
利用红外吸收光谱技术测量了CH4/N2放电等离子体的主要产物HCN 和C2H2。实验发现HCN 和C2H2的产生强烈依赖于CH4和N2在放电管中的浓度比率。当N2浓度远大于CH4浓度时,HCN 是优势产物;当CH4浓度远大于N2浓度时,C2H2是优势产物。因此,CH4在含氮元素等离子中会产生有害的HCN 分子,但HCN 的浓度与等离子中C/N 比率密切相关。通过调控CH4转化环境中N 元素的浓度,有可能抑制转化过程中产生HCN 的浓度。
