加温加氧超声雾化对急性加重期慢性阻塞性肺疾病的疗效观察
2021-10-13陈彩明经庆玲宋小睛戴小英唐悦婵
陈彩明, 经庆玲, 郑 立, 宋小睛, 戴小英, 唐悦婵
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是一种常见的,可以预防和治疗的疾病,以持续呼吸症状和气流受限为特征。当COPD患者的呼吸症状在某一时期急剧恶化需要增加治疗方案则称为急性加重期慢性阻塞性肺疾病(acute exacerbation chronic obstructive pulmonary disease,AECOPD)[1-2]。雾化吸入是一种以呼吸道和肺为靶器官的直接给药方法,具有起效快、局部药物浓度高、用药量少、应用方便和全身不良反应少等优点,是AECOPD的重要治疗手段之一。不同的雾化吸入装置会直接影响治疗效果,目前临床应用最广泛的射流雾化器,其因文丘里效应导致雾化液温度降低,使不良反应增加。既往的超声雾化器在工作时会使容器内药液升温,影响蛋白质或肽类化合物的稳定性,从而使其在临床应用中受限。通过对超声雾化器进行改良,实现雾化液温度的精确控制,为超声雾化在AECOPD治疗中的应用提供了条件。本研究旨在探讨加温加氧超声雾化吸入疗法在AECOPD的应用效果,现报道如下。
1 对象与方法
1.1研究对象 选取2018年4月至2019年8月我院收治的AECOPD患者60例,采用随机数字表法将其分为对照组和观察组,每组30例。观察组中男24例,女6例,年龄(67.23±8.25)岁;对照组中男23例,女7例,年龄(66.37±8.26)岁。两组年龄、性别比较差异无统计学意义(P>0.05),具有可比性。纳入标准:符合COPD的诊断标准[3],且病情处于急性加重期。排除标准:(1)合并不稳定型心绞痛、新近发生的心肌梗死(发生时间<15 d)、急性肺心病、控制不良的心律失常、重度瓣膜狭窄症、活动性心肌炎等心脏疾病;(2)合并肺部肿瘤;(3)合并控制不良的高血压;(4)新近发生的肺栓塞、重度肺动脉高压(发生时间<15 d);(5)合并肝、肾等其他器官功能衰竭;(6)合并高度认知障碍。本研究获医院伦理委员会批准,全部患者知情同意参与本研究。
1.2主要仪器与药物 观察组使用有加温功能的VGR-001超声雾化器(东莞永胜医疗制品有限公司生产),对照组使用无加温功能的医用雾化器(杭州京泠医疗器械有限公司生产)。两组均使用中心供氧,疗程7 d。两组雾化吸入药物均包括:(1)吸入用布地奈德混悬液(普米克令舒,阿斯利康公司,规格2 ml∶1 mg),1 mg/次,3次/d;(2)硫酸特布他林雾化液(博利康尼,阿斯利康公司,规格2 ml∶5 mg),5 mg/次,3次/d;(3)吸入用异丙托溴铵溶液(爱全乐,勃林格殷格翰,规格2 ml∶500 μg),500 μg/次,3次/d。
1.3治疗方法 两组均给予抗感染、祛痰、平喘、氧疗等内科常规治疗。(1)观察组:先在加温加氧超声雾化器水槽内加常温的水(水位不超过最大水位线),放入已盛6 ml药液的药杯,旋好盖子,连接加热连管、咬嘴,接好温度探头,打开电源,确认气源驱动模式(氧气模式),调整氧流量维持指脉氧在90%以上,温度(32±5)℃,时间15~20 min,个性化调整雾量大小。(2)对照组:将装入6 ml药液的医用雾化器插入中心供氧氧气接头上,调节氧气流量为6~8 L/min。咬嘴放入患者口中,让患者以深呼吸将雾粒吸入肺部。两组疗程均为1周。
1.4观察指标 在治疗前及疗程结束时检测以下指标:(1)COPD评估测试(COPD Assessment Test,CAT)评分[4]。问卷内容包括咳嗽程度、胸闷程度、咯痰程度、睡眠情况、精力情况、日常生活受限程度、活动量增加后困难程度以及户外活动信心程度8个方面,每个方面根据严重程度分为0~5分,总分0~40分,得分越高表示患者病情越严重。(2)动脉血气分析。采用血气分析仪(沃芬,型号GEM3000)检测患者血气指标,包括动脉血氧分压(PaO2)和动脉血二氧化碳分压(PaCO2)。(3)肺功能检测。采用德国CareFusion肺功能仪(型号MasterScreen)检测患者第1秒用力呼气容积占预计值百分比(FEV1%pred)。
2 结果
2.1两组治疗前后CAT评分比较 治疗前,两组CAT评分比较差异无统计学意义(P>0.05)。治疗后,两组CAT评分均较治疗前显著降低(P<0.05),且观察组CAT评分低于对照组,差异有统计学意义(P<0.05)。见表1。
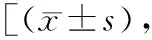
表1 两组治疗前后CAT评分比较分]
2.2两组治疗前后动脉血气分析指标比较 治疗前,两组PaO2、PaCO2比较差异无统计学意义(P>0.05)。治疗后,两组PaO2显著升高、PaCO2显著下降(P<0.05),且观察组PaO2水平高于对照组,PaCO2水平低于对照组,差异有统计学意义(P<0.05)。见表2。

表2 两组治疗前后动脉血气分析指标比较
2.3两组治疗前后肺功能水平比较 治疗前,两组FEV1%pred水平比较差异无统计学意义(P>0.05)。治疗后,两组FEV1%pred水平均显著提高(P<0.05),且观察组FEV1%pred水平高于对照组,差异有统计学意义(P<0.05)。见表3。

表3 两组治疗前后肺功能水平比较
3 讨论
3.1COPD以持续呼吸症状和气流受限为特征,具有患病率高、致残率高、病死率高的特点,严重威胁人类的健康。有研究表明,气道黏液高分泌导致COPD死亡的风险是非气道黏液高分泌的3.5倍[5]。相对于常规的静脉或口服用药,雾化吸入治疗可直接将药物作用于肺部病变部位,促进患者的康复[6]。雾化吸入装置是一种将药物转变为气溶胶形态,并经口腔(或鼻腔)吸入的药物输送装置[7]。目前临床常用的雾化器有射流雾化器、超声雾化器和振动筛孔雾化器3种[8-10]。有研究表明,COPD患者在吸入寒冷空气时容易发生气道痉挛,加重气道阻塞[11]。安全、有效地改善AECOPD患者呼吸症状,促进气道分泌物排出,改善通气是呼吸科医师关注的热点问题。本研究给予AECOPD患者常规雾化吸入及加温加氧雾化吸入治疗,对比不同雾化吸入疗法对患者CAT评分、血气分析及肺功能的影响,探讨加温加氧雾化吸入治疗在改善AECOPD患者呼吸症状及通气功能方面的疗效。
3.2常规氧气雾化吸入采用的是射流雾化器,根据文丘里效应原理,利用压缩气体高速运动通过狭小开口后突然减压,在局部产生负压,将气流出口旁另一小管因负压产生的虹吸作用吸入容器内的液体排出,当遭遇高压气流时被冲撞裂解成小气溶胶颗粒,特别是在高压气流前方遇到挡板时,液体更会被冲撞粉碎,形成药雾颗粒。在高压气流下,雾化液的温度也会降低,而寒冷气体刺激会引起呼吸道过度紧张收缩,甚至引起气促和呼吸困难等不良反应,影响药物的利用与吸收[12]。本研究采用的加温雾化原理是通过超声波驱动板驱动雾化换能片,使药杯中药物产生雾化,并将雾化液加热到预定温度(32~35 ℃),使吸入的雾化气雾温度接近人体的正常生理温度,结果显示观察组患者在CAT评分、血气分析和肺功能方面均较对照组改善更显著。有研究显示,通过加温雾化吸入药物可以提升患者雾化吸入的舒适度和治疗依从性,有利于患者改善临床症状[13-16]。
3.3雾化颗粒直径与药物沉积位置相关[17],其中粒径5~10 μm的雾粒主要沉积于口咽部,3 μm≤粒径<5 μm的雾粒主要沉积于肺部,粒径<3 μm的雾粒50%~60%沉积于肺泡,有效雾化颗粒直径应为0.5~10 μm。加温加氧超声雾化湿化排痰效果显著[18]。常见的超声雾化器原理是通过使用药液剧烈振动,破坏其表面张力和惯性,形成细小气溶胶颗粒并释出,但其工作时可使容器内药液升温,影响蛋白质或肽类化合物的稳定性[19]。本研究采用有恒温功能的超声雾化器,避免了常见的超声雾化器工作时因温度升高对药物的影响,且其释出的雾化粒子中心直径为1~5 μm,雾粒主要沉积于肺部,治疗效果良好。
综上所述,加温加氧超声雾化吸入可提高患者治疗的舒适性、安全性,疗效显著,值得临床推广应用。但本研究结论仍需扩大样本量进一步观察验证。
