超声和剪切波弹性成像对经颈静脉肝内门体静脉分流术后支架功能障碍的价值
2021-10-13金伟奎黄艳丽诸葛宇征孔文韬
金伟奎,黄艳丽,韩 浩,杨 建,诸葛宇征,孔文韬,吴 敏
0 前 言
门静脉高压是肝硬化患者常见并发症,也是肝硬化失代偿期的重要临床表现。经颈静脉肝内门体分流术(transjugular intrahepatic portosystemic shunt,TIPS) 通过在肝静脉与门静脉之间建立分流道,以微创的方式,从结构上显著降低门静脉阻力,是降低肝硬化患者门静脉压力的关键措施之一[1]。而支架通畅是保持其疗效的关键,但TIPS术后支架功能障碍发生率为18%~78%[2]。早期发现和监测支架功能障碍是提高TIPS临床疗效和患者生活质量的重要影响因素。门静脉造影及门静脉压力梯度的测量是诊断支架功能障碍的金标准,但因其有创、费用高、操作复杂等因素,限制其成为一项常规随诊的应用。因此寻找一种无创、操作简单、可重复性好的方法来诊断和监测支架功能障碍是非常必要的。
近年发展起来的剪切波弹性成像(shear-wave elastography,SWE)技术是一种在二维超声基础上新兴的弹性技术,是通过测定感兴趣区组织的剪切波传播速度(shear wave velocity,SWV),获取量化的SWV值,来反应组织硬度,SWV值越低,表示该组织弹性模量越小,即组织质地越软,反之越硬[3]。SWE技术可通过测量肝、脾等器官的硬度用于预测临床显著的门静脉高压、食管静脉曲张的存在或预测远期预后[4-5]。目前临床上,评价TIPS支架功能的常用方法是常规超声,但存在一些不足且无统一的诊断标准。本文分析经门静脉造影和门静脉压力梯度测定诊断的TIPS支架功能障碍者26例,旨在评价超声和剪切波弹性成像技术在评估支架功能障碍中的应用价值。
1 资料与方法
1.1 研究对象回顾性分析2015年10月至2017年8月因肝硬化门脉高压在南京鼓楼医院接受TIPS术治疗患者,术后行超声及SWE技术规律随访,经DSA证实支架功能障碍者26例。入组标准:①病毒性肝炎肝硬化门静脉高压行TIPS术的患者;②TIPS术后3~5 d、1个月、6个月及以后每隔6个月行超声和剪切波弹性成像技术规律随访;③经门静脉造影和门静脉压力梯度测定诊断支架功能障碍者。排除标准:①TIPS术后1个月内发生支架功能障碍者;②脾切除或脾栓塞术后;③严重右心衰;④年龄≥80岁。
1.2 仪器与方法
1.2.1 常规超声检查使用 Philips iU22及Acuson S2000超声诊断仪,凸阵探头。检查前患者禁食8 h以上,取仰卧位及左、右侧卧位检查,必要时辅以其他体位扫查。分别测量门静脉主干及最高流速、脾静脉主干内径及最高流速和支架内最高流速。门静脉测量点定于主干距左右分支2~3 cm 处,脾静脉测量点定于主干近脾门1~2 cm处;根据血管内径及其走行调整合适的取样容积,使声束与血流束夹角≤60°。
1.2.2 剪切波弹性检查使用西门子Acuson S2000超声诊断仪,频率为1~4 MHz凸阵探头。患者检查前准备同常规超声。以二维超声斜切面清晰显示肝、脾后,分别行SWE检查。选择肝右前叶下段为检测点,检查时嘱患者屏住呼吸,探头与扫查部位垂直并固定,取样位置距体表4~5 cm,同时避开肝内管道结构,测量肝的SWV,测量5次取其中位数;选择脾中部包膜下正对脾门的区域为检测点,检查时嘱患者屏住呼吸,取样位置距体表3~4 cm,避开脾血管,测量脾的SWV,测量5次并取其中位数。超声诊断支架功能障碍包括支架狭窄和闭塞,诊断标准:①支架狭窄,支架内血流信号充盈缺损,狭窄处血流速度≥300 cm/s;②支架闭塞,支架内无血流及多普勒信号[6]。
1.3 观察指标观察支架通畅与功能障碍时,支架内流速、门静脉主干内径及流速、脾静脉主干内径和流速、肝及脾SWV值,以及门静脉流速的变化差值(△PV)、脾静脉流速的变化差值(△SV)及脾SWV的变化差值(△SWV)。

2 结 果
2.1 临床资料经DSA证实支架功能障碍患者26例,包括支架内狭窄19例,支架内闭塞7例。其中男9例,女17例,年龄31~77岁,平均年龄54.9岁。此26例患者支架功能通畅时,仅6例有少量腹水(液体最大深度<3 cm),余患者无门静脉高压临床表现。支架功能障碍时,患者临床表现为呕血15例,黑便2例,腹水17例,其中顽固性腹水6例。此26例患者支架再通后,仅7例患者有少量腹水,余患者无门静脉高压临床表现。
2.2 超声结果超声诊断有支架功能障碍26例,支架内狭窄19例,支架内流速(364.80±41.17)cm/s,与通畅时流速(196.63±20.46)cm/s相比,支架内流速明显升高(t=4.549,P<0.001);支架闭塞7例,支架内无血流信号。支架再通后,支架内流速(184.33±16.44)cm/s,与狭窄时相比,流速显著降低(t=19.119,P<0.001)。
支架通畅时与功能障碍时比较,支架功能障碍时门静脉、脾静脉血流速度均显著下降,脾SWV值显著升高(P<0.001),而门静脉、脾静脉内径及肝SWV值变化差异无统计学意义(P>0.05),见表1,图1。支架功能障碍时与支架再通时比较,支架再通术后,门静脉、脾静脉流速均显著升高,脾SWV值显著下降(P<0.001),门静脉内径、脾静脉内径、肝SWV值的变化差异无统计学意义(P>0.05),见表1。
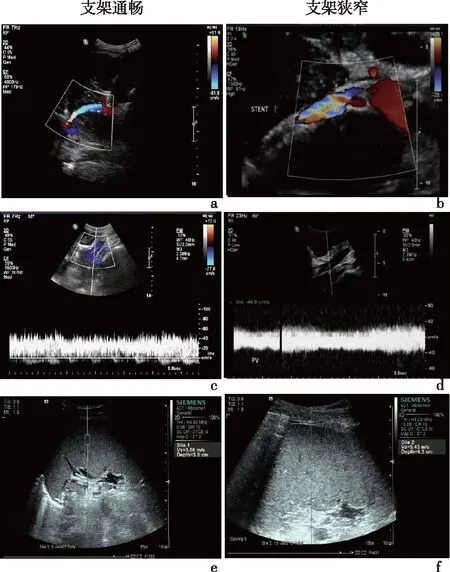
a:支架内血流通畅;b:支架中段内血流充盈缺损;c:门静脉流速59.9cm/s;d:门静脉流速44.6cm/s;e:脾SWV3.08m/s;f:脾SWV3.45m/s图1 支架通畅与狭窄时支架和门静脉彩色多普勒及脾弹性图
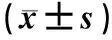
表1 支架通畅、功能障碍及再通时门、脾静脉内径及流速和肝、脾弹性值的对比分析
支架通畅时与功能障碍时进一步相比,△PV、△SV、△SWV的ROC曲线下面积分别为0.969、0.967、0.892,差异无统计学意义(P=0.115,0.924,0.136)。见表2,图2。
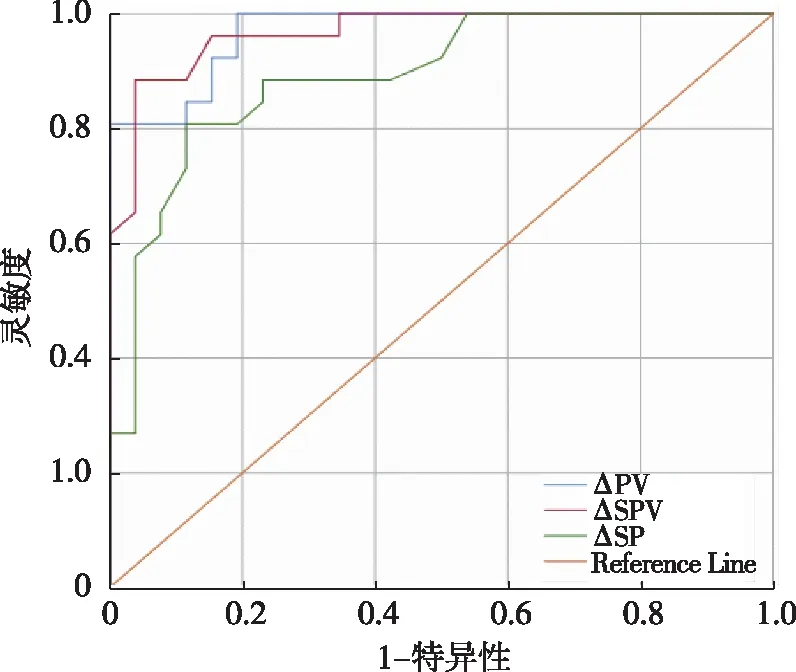
图2 门静脉、脾静脉流速及脾SWV的变化差值ROC曲线
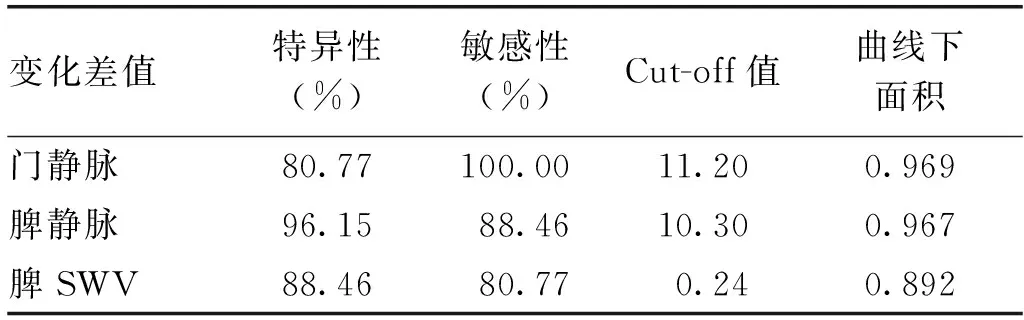
表2 支架通畅与障碍时门、脾静脉及脾SWV的变化值ROC曲线各参数
3 讨 论
TIPS是一种微创的介入治疗术,可有效降低门静脉压力。但TIPS术后并发症较多,尤其中远期支架易发生狭窄或闭塞,严重者会再次引起食管静脉曲张破裂出血、顽固性腹水等门静脉高压的症状。因此早期发现支架功能障碍,及时处理是维持其疗效和避免症状复发的关键。
超声作为一种无创、经济、可重复的检查手段,用于检测 TIPS支架、评价TIPS疗效有重要价值,已成为术后随访的重要手段[7]。本研究中,TIPS支架功能障碍门静脉流速较通畅时明显下降,与文献报道相符[8]。此外本课题组研究进一步发现支架再通后与支架障碍时比较,门静脉流速、脾静脉流速较障碍时明显升高。常规超声检查评价支架功能障碍方面仍然存在一定局限性:①肝硬化患者肝体积缩小,声衰减较明显、支架位置较深或受胃肠道气体影响均可导致门静脉、支架全程显示欠清晰,血流显像差,导致所测流速较实际情况有所偏差;②门静脉、脾静脉、支架内的血流速度受患者呼吸运动及腹腔积液影响较大;③由于超声成像特点,对于低速血流显像不佳,会造成血管或支架闭塞误诊的可能性;④常规超声只能半定量的提供门静脉系统血流动力学参数的变化,不能评估与门静脉压力密切相关的脾的生物力学性质的变化。
本研究发现,TIPS功能障碍与通畅时肝SWV值与门静脉压无相关性。这与Jansen等[9]报道不符。我们认为造成这种差异是由入组患者的病因不同所导致。①本研究入组患者是肝炎肝硬化患者,其肝硬化病理特征是肝结构的变形和再生结节的形成。肝硬化后的表现是肝的萎缩和质地变硬,大量再生结节被较厚的纤维隔隔开[10-11]。②有研究发现,患者放置TIPS后,肝SWV值会显著降低[12-13]。在之前的三项研究中,共计124例患者,其中半数以上是酒精性肝硬化[9,12-13]。而酒精性肝硬化的典型病理特征是小结节型肝硬化和隔膜增厚。③病理和临床表现之间的相关性表明,组织学上小结节的大小和增厚的隔膜与门静脉高压密切相关。此外,肝SWV值与继发性肝硬化的肝内血管高阻力相关;但它并不能说明肝硬化失代偿期患者的复杂的血流动力学变化[14]。因此本课题组认为肝SWV值不能用于肝炎肝硬化患者TIPS术后的随访与监测。
此前研究报道中,Han等[15-16]认为脾硬度与门静脉压力有较好的相关性。本课题组发现是与之相符的:支架功能障碍时门静脉压力上升,脾SWV值较通畅时明显升高。我们分析其原因TIPS术后支架功能障碍时门静脉压力再次升高,导致脾静脉回流受阻,脾淤血程度加重,导致脾硬度增加。脾SWV值变化与门静脉、脾静脉流速变化对于诊断TIPS支架功能障碍,具有同等效能。有助于降低对常规超声的依赖性,提高诊断信心。本研究发现超声和SWE技术诊断TIPS术后支架功能障碍有较好的准确性,有助于降低DSA的检查次数。但门静脉造影和门静脉压力梯度不能被超声完全取代,因为它即是诊断支架功能障碍的金标准,也是治疗的手段。本课题组研究也存在相应的不足之处:①支架功能障碍的样本量较少,门静脉、脾静脉流速变化幅度及脾SWV值的诊断效能,还需更进一步大样本的研究。②本研究是单中心回顾性研究,研究结果还需前瞻性研究证实。③入组患者均为肝炎肝硬化,此结果并不能适用于所有肝硬化患者。
综上所述,门静脉流速、脾静脉流速及脾SWV值可用于肝硬化门脉高压症患者TIPS术后支架功能障碍诊断,三者具有同等的诊断效能。门静脉流速的变化差值、脾静脉流速的变化差值及脾SWV值的变化差值对支架功能障碍,有一定的辅助诊断价值。
