贝伐单抗对原发性肝癌患者KPS评分及血清AFP和CEA水平的影响
2021-10-12黄凌敏
黄凌敏
(赣西肿瘤医院外一科,江西 萍乡 337000)
原发性肝癌为临床的常见疾病,该病起病较隐匿,早期缺乏典型症状,易被患者忽略,随着病情进展,多数患者出现黄疸、腹水、恶病质,但此时已进展至中晚期,错失最佳手术治疗时机,导致患者预后较差[1]。目前,对失去手术指征的患者多予以综合治疗,但临床发现肝癌细胞对于放疗或全身化疗敏感性欠佳,整体治疗效果不佳。导管动脉化学栓塞(TACE)可直接将药物送至肿瘤血管内,迅速提高病灶部位药物浓度,抑制肿瘤细胞增殖,加快肿瘤血管消退,从而抑制病情进展,改善患者的生存质量。目前,TACE 已成为无法行手术治疗的原发性肝癌患者的首选方案。但有研究发现,部分患者经TACE治疗后会再次出现肿瘤血管复发[2]。贝伐单抗是一种靶向治疗药物,可竞争性结合人血管内皮生长因子(VEGF),抑制肿瘤血管生成,加快异常血管恢复正常,阻止肿瘤组织转移[3]。基于此,本研究旨在分析贝伐单抗治疗原发性肝癌的临床效果,现报道如下。
1 资料与方法
1.1 临床资料 选取2017年5月至2019年5月于本院就诊的原发性肝癌患者60例,按照随机数字表法分为两组,各30例。对照组男18例,女12例;年龄48~72岁,平均年龄(61.38±4.57)岁;体重指数18~24 kg/m2,平均体重指数(22.04±1.15)kg/m2;病灶大小5.5~11.5 cm,平均病灶大小(8.53±1.24)cm;TNM分期:Ⅲ期21例,Ⅳ期9例;Child-Pugh分级:A级20例,B级10例。观察组男17例,女13例;年龄49~72岁,平均年龄(61.45±4.59)岁;体重指数18~25 kg/m2,平均体重指数(22.08±1.17)kg/m2;病灶大小4.5~11.5 cm,平均病灶大小(8.51±1.22)cm;TNM分期:Ⅲ期22例,Ⅳ期8例;Child-Pugh分级:A级21例,B级9例。
1.2 纳入及排除标准 纳入标准:符合《原发性肝癌诊疗规范(2017 年版)》[4]中相关诊断;经肝穿刺活检、病理组织学检查确诊;TNM 分期Ⅲ~Ⅳ期;精神状态正常;患者及家属均对本研究知情同意,并签署知情同意书;本研究经医院伦理委员会批准。排除标准:弥漫性肝癌或继发性肝癌;伴随其他部位恶性肿瘤;存在TACE 禁忌证;对本研究药物过敏。
1.3 方法 对照组行TACE治疗,以改良Seldinger技术经皮股动脉穿刺插管,在DS引导下进行腹腔干动脉、肠系膜上动脉血管造影,以明确患者肿瘤位置、大小、数目等信息,之后将导管插入肿瘤供血血管,向其内注入奥沙利铂90~140 mg、5-氟尿嘧啶1.0 g、8.0%碘化油10~30 mg及明胶海绵碎块混合乳化物。观察组在对照组基础上加用贝伐单抗[Roche Pharma(Schweiz)Ltd.,国药准字S20170035)治疗,在TACE注入化疗药物前,经导管注入4.0~6.0 mg/kg贝伐单抗,其他操作同对照组。两组均治疗6周。
1.4 观察指标 ①客观缓解率,评价标准:完全缓解,肿瘤病灶消失;部分缓解,肿瘤病灶缩小>50%;病情稳定,肿瘤病灶缩小≤50%;进展,肿瘤病灶增大或出现新的病灶。客观缓解率=完全缓解率+部分缓解率+病情稳定率。②KPS 评分,采用KPS评价体力状况,总分100分,评分越高表明体力越好,化疗耐受力越强。③AFP和CEA水平,治疗前和治疗6 周后,抽取两组患者空腹静脉血3 mL,以全自动化学发光免疫分析仪测定AFP、CEA水平。④不良反应发生率,包括乏力、骨髓抑制、头痛、血细胞减少。
1.5 统计学方法 采用SPSS 22.0统计软件进行数据分析,计量资料以“x±s”表示,比较采用t检验,计数资料用[n(%)]表示,比较采用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组客观缓解率比较 观察组客观缓解率高于对照组,差异有统计学意义(P<0.05),见表1。

表1 两组客观缓解率比较[n(%)]
2.2 两组KPS评分及血清AFP、CEA水平比较 治疗后,观察组KPS评分高于对照组;观察组AFP、CEA水平均低于对照组,差异有统计学意义(P<0.05),见表2。
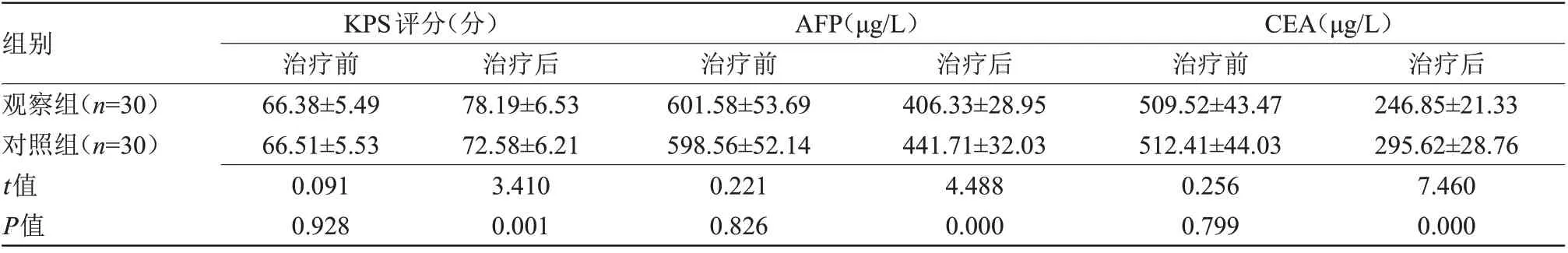
表2 两组KPS评分及血清AFP、CEA水平比较(x±s)
2.3 两组不良反应发生率比较 对照组出现乏力3例,头痛2 例,骨髓抑制1 例,不良反应发生率为20.00%(6/30);观察组出现乏力4 例,骨髓抑制1 例,血细胞减少2 例,不良反应发生率为23.33%(7/30)。两组不良反应发生率比较差异无统计学意义(χ2=0.098,P=0.754)。
3 讨论
原发性肝癌发病机制较复杂,临床认为肝硬化、病毒性肝炎等基础疾病长期反复发作是引起癌性病变的重要因素,且肝癌侵袭力强,早期即可突破肝血窦于肝内进行转移,而早期无明显症状,加之部分微小肿瘤灶显像不明显,导致患者无法满足手术切除指征[5]。TACE是临床治疗无法进行手术的原发性肝癌患者常用手段,通过于肿瘤组织供血动脉内注入碘化油,可对肿瘤四周供血进行阻断,促使肿瘤细胞发生缺血、缺氧性坏死[6]。同时,其可直接将化疗药物注入肿瘤组织处,利于药物沉积于肿瘤血管内,提高局部药物浓度,延长药物作用时间,以快速灭杀肿瘤细胞,且局部给药可减轻对正常组织损伤,减少药物不良反应[7]。但肝脏解剖结构复杂,血供丰富,部分患者经TACE治疗后,体内VEGF仍呈持续高表达,导致肿瘤血管再生,预后效果不佳。
AFP、CEA 是常见血清肿瘤标志物,其中AFP 属于糖蛋白,当机体肝细胞出现癌变时,会刺激AFP基因表达,促使部分肝细胞恢复AFP分泌能力,血清中AFP水平升高;CEA是一种自胎儿肠组织及结肠癌中提取的肿瘤相关抗原,在正常情况下CEA会通过胃肠道代谢,血液中水平较低,当机体出现异常时会进入血和淋巴循环,促使血液中CEA 水平异常升高[8-9]。本研究结果表明,观察组客观缓解率高于对照组,KPS 评分高于对照组,AFP、CEA 低于对照组(P<0.05),两组不良反应发生率比较差异无统计学意义,表明贝伐单抗治疗原发性肝癌效果显著,可提高临床客观缓解率,加快血清肿瘤标志水平恢复正常,且未增加不良反应发生风险。贝伐单抗是重组人源化抗IgG1 单克隆抗体,属于抗血管生成药物,经导管注入肿瘤血管后,可特异性结合VEGF,抑制其活性,从而阻断肿瘤心血管生成,并可干扰内皮细胞有丝分裂,促使肿瘤血管退化,以切断肿瘤组织氧气和血液供给,阻止其生长分化[10]。贝伐单抗还可截除未成熟或渗漏脉管,并具有重塑剩余脉管的作用,可加快剩余脉管结构正常化,减少脉管渗漏,促使基底膜功能恢复正常,使周细胞覆盖范围大幅增加。而脉管形态改变后,可减小间质压力,使药物可更好深入肿瘤细胞内,以提高化疗药物敏感性,改善疾病预后效果。
综上所述,贝伐单抗可增强原发性肝癌治疗效果,提高KPS 评分,促进血清肿瘤标志物水平降低,改善患者生存质量,且安全性高,值得临床推广运用。
