铁基改性椰壳生物炭对砷的吸附效果及机制研究
2021-10-12张苏明张建强周凯陈志良
张苏明 ,张建强, ,周凯,陈志良, *
1. 河南科技学院园艺园林学院,河南 新乡 453000;2. 生态环境部华南环境科学研究所,广东 广州 510000;3. 广东省农田重金属污染土壤治理与修复工程技术研究中心,广东 广州 510000
砷(As)是一种剧毒且致癌的类金属,能通过食物链富集,对生态环境、食品安全以及人类健康都构成了严重威胁(Zhang et al.,2017)。中国土壤背景值为 11.2 mg·kg−1,远高于全球的土壤背景值(5—10 mg·kg−1)(Boyle et al.,1973;Chen,2005);同时,由于化肥和农药的施用,矿山开采以及金属冶炼含砷固体废物和废水的排放等人为活动导致大量砷进入环境,如有色金属冶炼每年排放近10×104t,进一步加剧了土壤和水体砷污染(Hu et al.,2017)。由于砷的剧毒性,国内外学者都十分关注砷污染土壤和水体治理修复技术的研究。环境中砷主要以砷酸根和亚砷酸根离子的形式存在(杨居荣,1986),对于砷含氧阴离子的去除,相比于传统的沉淀、膜分离以及离子交换等,吸附处理技术具有效率高、成本低和易操作的特点(平森文等,2019)。
生物炭原料来源广泛,价格低廉,且疏松多孔,比表面积大,表面官能团丰富,具有良好的吸附特性,在重金属污染修复领域具有积极的应用前景,因而受到广泛关注(杨放等,2015)。椰壳是中国热带典型的农业废弃物,每年产出10亿颗以上(罗海艳等,2019)。目前,椰壳的利用方式主要包括生产生物质肥料及椰衣纤维床垫等,较为粗放,附加值不高。针对椰壳高值化利用,一些学者制备椰壳生物炭用于污水重金属吸附处理,取得了较好的效果(邱家枝,2016)。然而,环境中砷主要以含氧阴离子形式存在,生物炭对砷污染的修复效果并不明显(楚颖超,2015)。楚颖超等(2015)研究了不同裂解温度制备的椰衣生物炭对 Cd(Ⅱ)、As(Ⅲ)、Cr(Ⅲ)和Cr(Ⅵ)的吸附性能,结果表明不同温度下制备的椰衣生物炭对 As(Ⅲ)的最大饱和吸附量为 1.073 mg·g−1。因此,有必要对椰壳生物炭的微观结构以及表面性能进行改性,以提高其修复能力(Rajapaksha et al.,2016)。
生物炭改性处理旨在扩大生物炭使用范围,提升其应用效果,是目前生物炭研究的热点方向之一。生物炭的吸附机理主要是特异性吸附和非特异性吸附,包括静电吸引、离子交换、沉淀作用和络合作用等化学反应。近年来,一些金属如铁、锰的氧化物被广泛应用于生物炭吸附材料改性,均取得了较好的处理效果(陈坦等,2019;赵天赐等,2019)。朱司航等(2019)的研究表明,用针铁矿改性的秸秆生物炭对 As(Ⅲ)的最大吸附量为 65.20 mg·g−1,吸附机制包括静电吸引和特异性吸附(配位、络合、离子交换等)。改性材料在生物炭表面对污染物的吸附起到重要作用。常见的铁基材料包括磁性氧化铁、纳米零价铁和铁硫化合物,其中铁硫化合物改性生物炭在重金属的去除方面应用较多(Guo et al.,2017;Rattanachueskul et al.,2017;Hyun et al.,2019)。然而,这些改性生物炭的制备方法相对复杂且成本较高,对砷的吸附效果相对有限。本研究拟采用硫酸铁与硫酸共热解制备改性椰壳生物炭,通过静态吸附实验,探究改性椰壳生物炭砷吸附过程的影响因素,分析其对砷的吸附机理,为改性椰壳生物炭的规模化使用提供理论依据。
1 材料与方法
1.1 实验材料
本实验所用椰壳购自广州市增城区镇龙镇农贸市场,稍微去毛后用自来水冲洗,去离子水润洗后85 ℃烘干备用。本实验中所用H2SO4、HNO3、NaOH、Fe2(SO4)3和Na2HAsO4均为分析纯,购自阿拉丁试剂(上海)有限公司,实验用水均为超纯水。
1.1.1 生物炭的制备
将干椰壳敲碎至大约1 cm×1 cm的方块放于石英舟中,并置于管式炉,通入 N2(流量:200 mL·min−1)吹扫 5 min,随后以 10 ℃·min−1的升温速率升温至600 ℃后保温2 h,继续通入N2,自然冷却至室温后取出,称质量,研磨过100目筛,制得椰壳生物炭(CSB),密封干燥保存备用。
1.1.2 改性生物炭的制备
称5 g椰壳生物炭放入石英舟中,加入硫酸铁(Fe-C质量分数之比分别为5%、10%、15%)和10 mL浓硫酸,搅拌均匀后静置过夜;然后置于管式炉中以10 ℃·min−1升温至 300 ℃后保温 2 h,继续通入 N2,自然冷却至室温后取出,去离子水冲洗去除未负载的Fe,清洗至滤液pH接近中性,抽滤后105 ℃烘干,再次研磨过100目筛,转入干燥器中备用,分别标记为SFCSB-5、SFCSB-10和SFCSB-15。另取5 g椰壳生物炭,加入5 mL硫酸,其他过程同上,制得硫酸改性椰壳生物炭(SCSB)。
1.2 生物炭材料表征
使用扫描电镜-能谱分析仪(SEM-EDS,TESCAN VEGA3 SB)观察生物炭的外观形貌及表面元素组成;傅里叶红外光谱分析仪(FT-IR Nixolet iS50)对与KBr混合后的样品进行测试,分析生物炭表面官能团,获得生物炭表面官能团种类;X射线粉末衍射仪(RigakuD Ultima Ⅳ型)测定生物炭晶相结构;X射线光电子能谱(XPS;ESCALAB 250Xi)分析生物炭表面元素组成及化学状态;BET仪测定比表面积。采用表面电位滴定法测定生物炭Zeta电位。生物炭pH根据《木质活性炭试验方法-pH值的测定》(GB/T 12496.7—1999)测定。
1.3 吸附实验
1.3.1 pH对吸附性能的影响
称取0.1 g生物炭样品于25 mL离心管中,分别加入20 mL质量浓度为60 mg·L−1(以砷计),初始pH值分别为2、4、5、7、9的砷酸氢二钠溶液(Na2HAsO4)溶液,置于恒温振荡箱中,在恒温25 ℃及 220 r·min−1条件下振荡 24 h。然后,4000 r·min−1条件下离心 10 min,取上清液过 0.45 μm 滤膜,原子荧光分光光度计(AFS-52,北京普析通用仪器有限公司)测定溶液As浓度。每个pH设3组平行,同时设1组空白对照(即不加生物炭),结果取平均值。
生物炭砷吸附量计算公式如下:
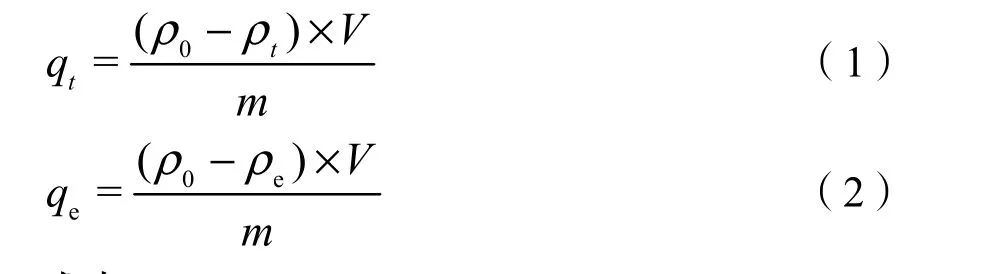
式中:
qt和 qe——t时刻吸附量和平衡吸附量(mg·g−1);
ρ0、ρt和ρe——溶液的初始质量浓度、t时刻质量浓度和平衡时的质量浓度(mg·L−1);
V——溶液体积(L);
m——生物炭质量(g)。
1.3.2 吸附动力学试验
分别称取0.1 g CSB、SCSB、SFCSB-5、SFCSB-10、SFCSB-15置于 25 mL离心管中,加入浓度为 60 mg·L−1的砷酸氢二钠溶液20 mL。将离心管放入恒温振荡箱中,在 25 ℃、220 r·min−1条件下振荡 5、15、30 min,1、2、4、8、16、24 h,每个时间段做3个平行样。振荡后取出,4000 r·min−1条件下离心10 min,上清液过0.45 μm滤膜,稀释后用原子荧光分光光度计测定As的浓度。
利用式(1)计算不同时刻生物炭砷吸附量,通过准一级动力学模型(式3)、准二级动力学模型(式4)以及Elovich模型(式5)进行动力学拟合,研究生物炭及改性生物炭材料对砷的吸附动力学。准一级动力学模型及动力学方程及准二级动力学模型如下所示:

式中:
qe——生物炭的平衡吸附量(mg·g−1);
qt——t时刻生物炭的吸附量(mg·g−1);
k1——准一级动力学方程的吸附速率常数(min−1);
k2——准二级动力学方程的吸附速率常数[g·(mg·min)−1]。
Elovich模型是广泛应用于描述水溶液污染物的吸附过程,该模型的假设是吸附剂表面具有高度的不均匀性。方程式如下:

式中:
α——初始 Elovich 吸附速率[mg·(mg·min)−1];
β——与化学吸收活化能和表面覆盖率有关的Elovich 解吸常数(g·mg−1)。
1.3.3 吸附等温线试验
称取0.1 g生物炭样品于25 mL离心管中,分别加入 20、40、60、120、240、280 mg·L−1的砷酸氢二钠溶液20 mL,在25 ℃的恒温条件下,以220 r·min−1的速度振荡 24 h 后取出,4000 r·min−1的条件下离心10 min,上清液过0.45 μm滤膜,原子荧光分光光度计测定As浓度,每个初始浓度设3个平行样,结果取平均值,并采用 Langmiur模型和Freundlich模型进行拟合。
Langmiur模型反应了单分子层吸附剂单位吸附量与溶液中离子浓度的关系,方程式如下:

式中:
Ce——吸附平衡时的吸附质量浓度(mg·L−1);
qe和Q0——静态平衡吸附量和静态理论饱和吸附量(mg·g−1);
KL——吸附常数(L·mg−1)。
Freundlich模型是基于多相吸附表面或表面支撑的活性位点具有不同的表面能这一猜想建立的经验表达式,被广泛应用于多层吸附并假设吸附热在吸附过程中是不均匀分布的。其非线性表达式为:

式中:
Ce——吸附平衡时的吸附质量浓度(mg·L−1);
qe——静态平衡吸附量(mg·g−1);
KF——吸附系数;n为方程参数。
1.3.4 数据处理
每种试验处理设置3个重复,最终结果以平均值表示。运用Microsoft Excel 2019、OriginPro 8.5、Jade 6软件对数据进行图表分析与处理。
2 结果与讨论
2.1 生物炭和改性生物炭表征
SEM-EDS表征结果如表1及图1所示,CSB(图1A)经过高温碳化后呈碎片状,颗粒大小不均匀,表面形状不规则且凹凸不平,比表面积为247.382 m2·g−1;经硫酸改性后(图 1B),比表面积增加至297.483 m2·g−1,没有出现破碎及孔洞塌陷;而经硫酸及硫酸铁共同改性后,SFCSB-10(图1C)比表面积增大到 387.224 m2·g−1,比 CSB 提高了56.53%,且表面粗糙,未呈现出穿透状,在一定程度上影响了生物炭的理化性质。有研究表明,强酸洗涤可以改变生物炭的多孔结构和表面性质(Peng et al.,2017;Zhou et al.,2017)。同时,因为低温制备的生物炭内部还残留着本身生物质样品材料的碳骨架结构,但是酸会腐蚀生物炭表面的细小颗粒,加热条件下硫酸与炭反应有大量的气体析出,使得生物炭的比表面积显著增加。比表面积的增大既有利于物理吸附,孔隙结构也有利于重金属离子进入生物炭内层,并与内层的吸附点位和活性基团结合,从而提高生物炭对重金属离子的化学吸附能力。
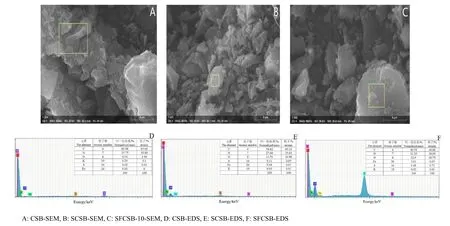
图1 生物炭的SEM-EDS图Fig. 1 SEM-EDS image of biochar
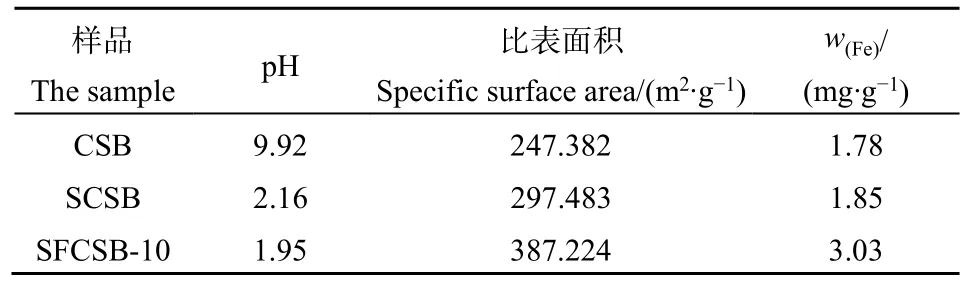
表1 生物炭的基本性质Table 1 Basic properties of biochar
椰壳生物炭pH高达9.92,可能由于热解过程中酸性官能团不断分解,碱性矿物析出,导致椰壳生物炭呈较强碱性(Park et al.,2019)。经硫酸及硫酸铁改性后,椰壳生物炭pH分别降低至2.16和1.95,可能是改性后酸性基团增加所致。通过 EDS半定量分析(图1)可见,CSB的主要成分是C及N元素,O元素含量相对较低,而改性后的SCSB及SFCSB-10氧元素含量增大,改性生物炭的C/O逐渐降低,O比例增大,表明经改性后生物炭表面形成了大量的含氧官能团(马洁晨等,2019)。此外,SFCSB表面Fe及S元素含量增加,表明经硫酸及硫酸铁改性后椰壳生物炭表面负载了含铁、硫的基团。
为进一步探究改性生物炭物相组成,对生物炭进行了 XRD衍射分析。结果表明,椰壳生物炭主要矿物结构为SiO2,改性后椰壳生物炭未观察到铁的结晶物质产生(图2)。在改性生物炭的低温制备过程中,硫酸与碳反应生成二氧化碳和二氧化硫,而铁矿物晶体结构一般在高温下生成。

图2 生物炭的X射线衍射图Fig. 2 X-ray diffraction pattern of biochar
酸碱或氧化剂对生物炭进行化学改性可以引入所需的表面官能团(Sajjadi et al.,2019)。图3为生物炭改性前后的FTIR光谱图,由图可知,改性前后生物炭的红外特征峰位置基本不变,而峰的强度稍有不同。改性前 CSB在 3435.41 cm−1处出现了一个宽峰,表示此处为–OH基团。2922.15 cm−1的谱带是甲基和亚甲基CH键的延伸。在1578.06 cm−1处出现峰值,表现为C=O的反对称拉伸(Yuan et al.,2011)。1081.27 cm−1处的峰值可以归因于C–N键和硫酸根(SO42−)反对称伸缩振动。改性后的生物炭在2854.43 cm−1和1722.90 cm−1处新增了亚甲基(–CH3)和羧基(–COO)的伸缩振动(Keiluweit et al.,2010)。这可能是因为,酸改性生物炭的过程中,强酸中和了碱性基团,同时氧化了其中部分不稳定的官能团;另外,酸也可能与表面官能团结合,形成π键或以氢键方式结合,从而使得生物炭表面酸碱官能团发生变化。H2AsO4−可与质子化反应的–OH、–COOH等官能团发生静电作用,而生物炭表面含有大量C=O键,因此可与H2AsO4−、HAsO42−以氢键的方式结合;改性后的生物炭表面酚羟基、羧基等酸性官能团含量增多,相比于未改性椰壳生物炭,改性后的生物炭通过与这些附加的官能团的阳离子交换和表面络合增加对 As的吸附亲和力(Rajapaksha et al.,2016)。
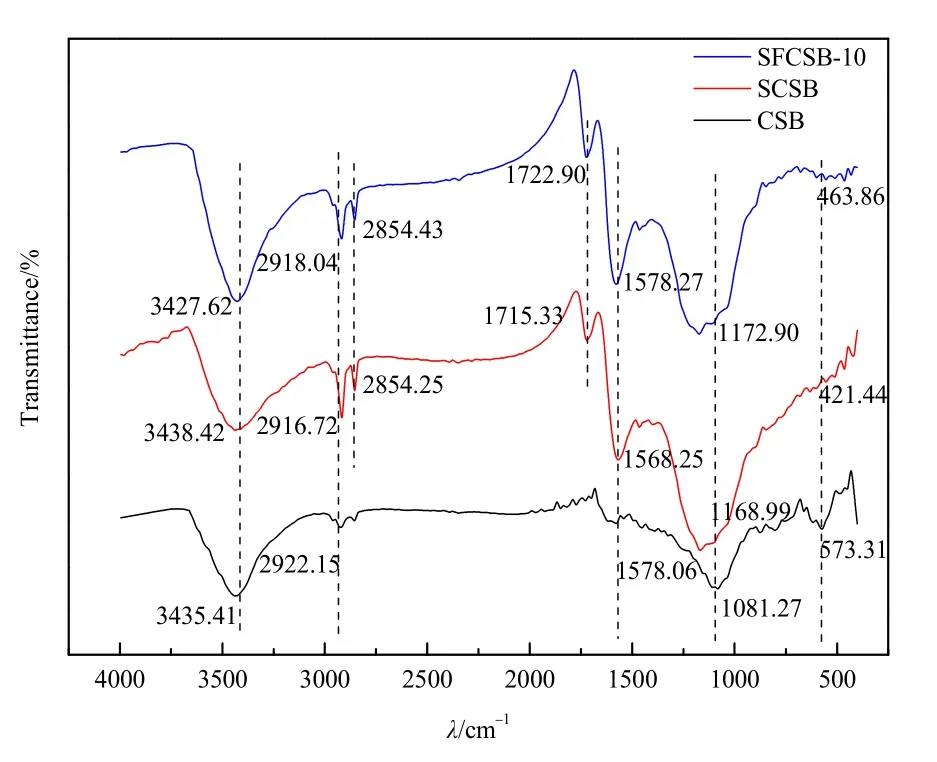
图3 生物炭的FTIR光谱Fig. 3 FTIR spectra of biochar
图4为生物炭改性前后的XPS(C1s、O1s、Fe2p和S2p)分析图谱。由图可知,改性前CSB在结合能284.75 eV处出现了C–C峰,532.45 eV处出现了C=O键,而经硫酸改性后的SCSB在168.80 V处出现了S2p峰,硫酸及硫酸铁共同改性的SFCSB在712 eV处出现了Fe2p峰,表明SFCSB表面成功负载铁、硫基团。
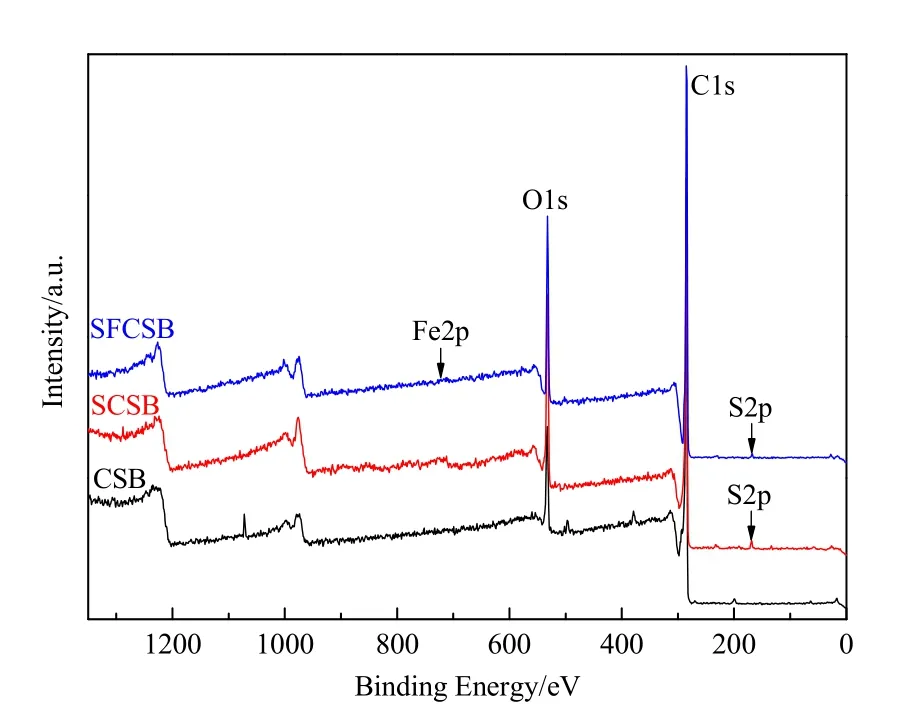
图4 生物炭的XPS(C1s、O1s、Fe2p和S2p)分析图谱Fig. 4 XPS (C1s, O1s, Fe2P and S2P) analysis patterns of biochar
2.2 pH对生物炭吸附砷的影响
当As溶液初始浓度为60 mg·L−1,生物炭投加量为 5 g·L−1,吸附时间为 24 h时,溶液 pH 值对As(Ⅴ)吸附量的影响如图5所示。由图可知,在溶液pH为2时,CSB、SCSB、SFCSB-5、SFCSB-10和SFCSB-15对As的吸附量较低,仅有0.04—2.15 mg·g−1。随着 pH 的增大,5 种生物炭对 As(Ⅴ)的吸附量先增大后减小,在pH=5时吸附量最大,分别为0.08、1.42、9.16、10.93、14.65 mg·g−1,铁基改性生物炭对砷的去除率达到 90%以上。5种生物炭的吸附能力表现为SFCSB-15>SFCSB-10>SFCSB-5>SCSB>CSB。由生物炭在溶液pH为3.0—9.0时的Zeta电位图(图6)可知,硫酸及硫酸铁改性提高了椰壳生物炭的Zeta电位,Zeta电位随着溶液pH的增加而逐渐降低,生物炭表面负电荷也随之增大(Chang et al.,2020)。当溶液pH小于4时,SCSB带正电荷,其他生物炭表面带负电,然而5种生物炭对As的吸附量均较低,表明生物炭的吸附性能受到明显抑制。因为在酸性条件下,As(Ⅴ)主要是以 H2AsO4−的离子形态存在,生物炭上负载的铁表面带正电荷,虽然对H2AsO4−离子有较好的吸引力,但是吸附能力有限,吸附过程主要由内层络合作用主导(Yang et al.,2018)。当pH大于7时,生物炭表面负电荷增大,与含砷阴离子之间的静电斥力增加,吸附能力降低。当pH高于电荷零点时的pH时,含氧官能团的去质子化导致生物炭表面负电荷增加,静电吸附作用减弱(Tan et al.,2020),但pH值范围4.0—5.0内SFCSB-10对As的吸附并没有受到抑制,吸附量反而上升,表明静电吸引不是 SFCSB-10对As(Ⅴ)的主要吸附机制。
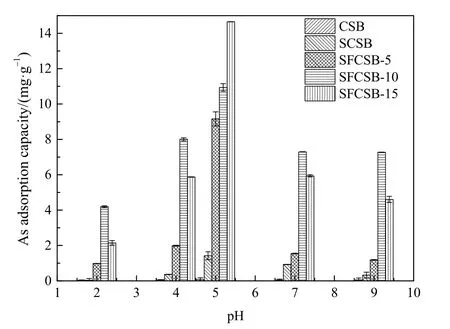
图5 pH对生物炭吸附As(Ⅴ)的影响Fig. 5 Effect of pH on the adsorption of As(Ⅴ) by biochar
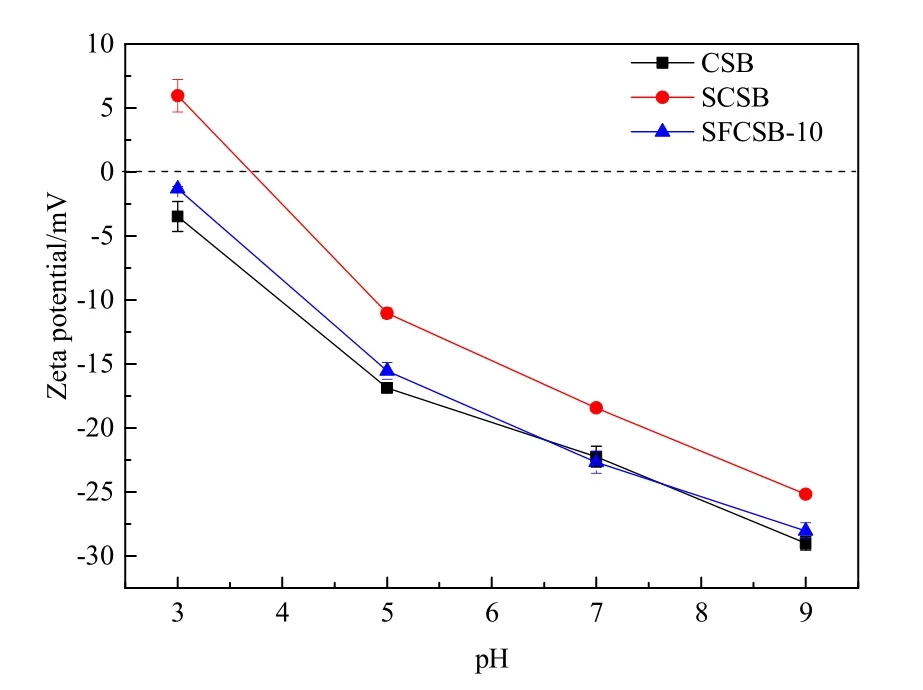
图6 不同溶液pH下生物炭Zeta电位的变化Fig. 6 Changes of Biochar’s Zeta Potential under Different Solution pH
2.3 生物炭的砷吸附动力学
图7为生物炭对As(Ⅴ)的吸附动力学曲线。从图7可知,CSB和SCSB、SFCSB-5、SFCSB-10、SFCSB-15对 As(Ⅴ)的吸附过程可分为快速吸附和吸附平衡两个阶段。前120 min是快速吸附阶段,生物炭对 As(Ⅴ)的吸附量随着时间的增加迅速增大,在240—480 min左右达到吸附平衡。因为在吸附初期,生物炭表面孔径通道和官能团充足,溶液中的 As(Ⅴ)能够迅速占据生物炭的孔隙和吸附点位,同时溶液中的As(Ⅴ)含量相对较高,有利于吸附反应的进行。当吸附过程达到平衡阶段,随着时间的增加,生物炭的吸附位点逐渐被占据,吸附能力趋近饱和,达到吸附平衡后吸附量不再增加。

图7 生物炭对As(Ⅴ)的吸附动力学曲线Fig. 7 Adsorption kinetic curve of As(Ⅴ) on biochar
生物炭及改性生物炭对As(Ⅴ)的吸附是个复杂的固液间反应过程,采用准一级动力学方程、准二级动力学方程以及 Elovich方程进行拟合处理,拟合结果见表2。由表2可知,Elovich动力学方程的相关系数最高,能较好地描述5种生物炭在液相中的扩散过程,也揭示了其他动力学方程所忽视的数据的不规则性。说明在生物炭吸附砷的过程中,活化能变化较大,因此可以判断生物炭对砷的吸附形式属于非均相扩散的吸附-脱吸过程。
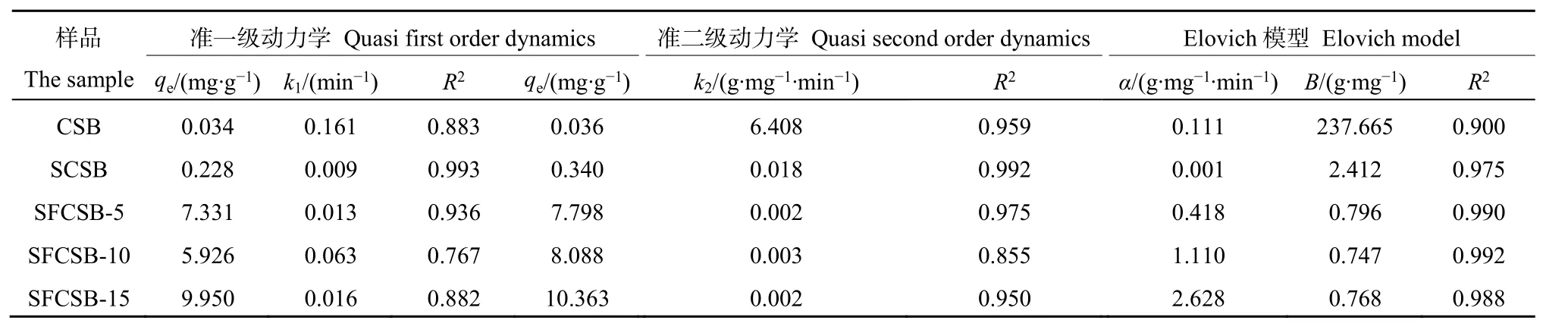
表2 动力学吸附As(Ⅴ)拟合参数Table 2 Kinetic adsorption of As(Ⅴ) fitting parameters
2.4 生物炭对砷的吸附容量
通过 Langmiur及 Freundlich等温吸附模型对改性前后生物炭的 As(Ⅴ)吸附实验数据进行拟合(图8),研究改性前后生物炭对As(Ⅴ)的吸附容量及其吸附机制,分析结果见表3。
由图8及表3可知,5种生物炭对As(Ⅴ)的吸附量随初始浓度的增加而迅速增大,最后基本达到平衡。Langmiur模型与该吸附等温曲线拟合程度优于Freundlich模型(R2>0.954),能更好地描述生物炭对As(Ⅴ)的吸附过程,表明5种生物炭对As(Ⅴ)的吸附均为单分子层吸附,且表面吸附位点的分布区域均匀(Bulut et al.,2008;阳昕,2016;Jung et al.,2015)。结合表3可知,Langmiur模型拟合出CSB 对 As(Ⅴ)的饱和吸附量为 0.06 mg·g−1,SCSB对 As(Ⅴ)的饱和吸附量为 5.21 mg·g−1,铁基改性生物炭 SFCSB-5、SFCSB-10、SFCSB-15对 As(Ⅴ)的饱和吸附量分别为 9.16、10.26、14.29 mg·g−1,经硫酸和硫酸铁改性处理,生物炭对As(Ⅴ)的吸附能力增强。

表3 改性前后生物炭对As(Ⅴ)吸附等温线模型的拟合参数Table 3 Fitting parameters of As(Ⅴ)-adsorption isotherm model of biochar before and after modification
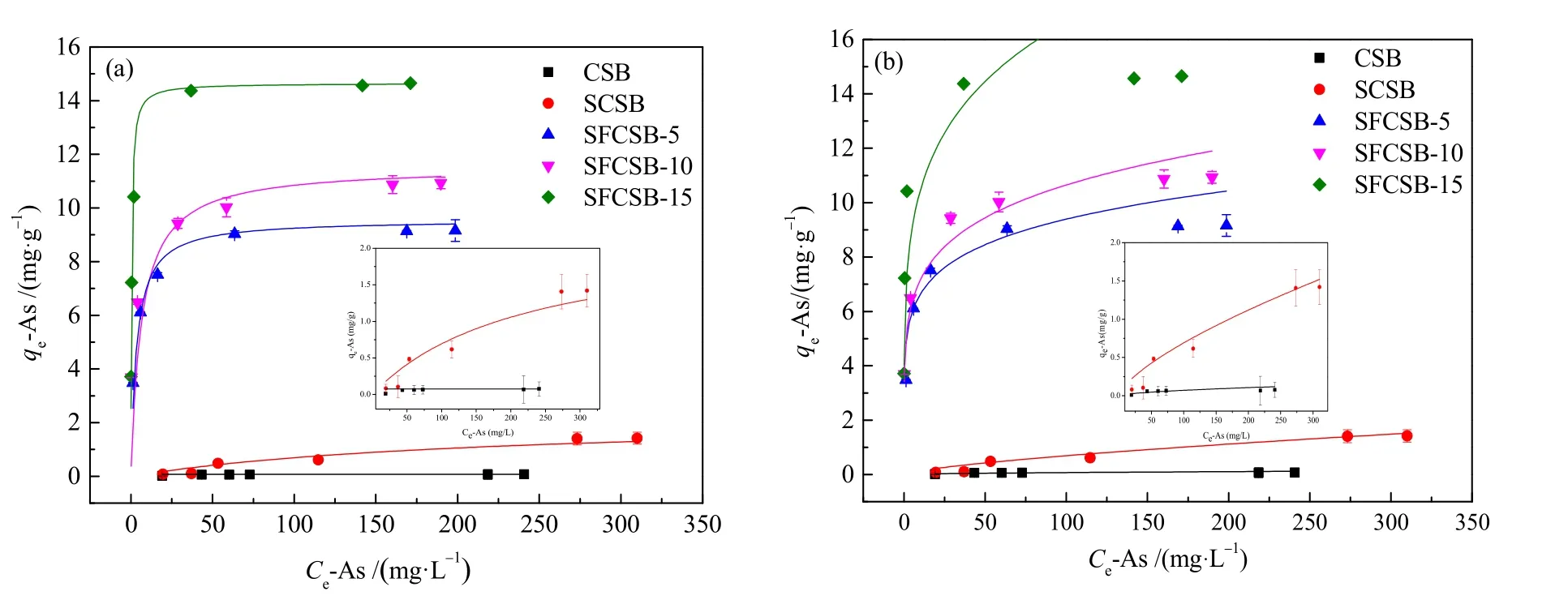
图8 生物炭对As(Ⅴ)的等温吸附曲线Fig. 8 Adsorption isotherm of As(Ⅴ) on biochar
2.5 改性椰壳生物炭的吸附机制
为了进一步探究铁基改性生物炭对As(Ⅴ)的吸附机理,对SFCSB-10吸附As(Ⅴ)后的FTIR(图9)进行分析。由图3结合图9可得,吸附后3398.68 cm−1处–OH宽峰带强度有一定的减弱,也可以观察到O–H–As的氢键结合。另外,2854.43 cm−1处的C–H消失,1573.04cm−1处C=O的变化表明吸附质在生物炭表面羟基发生络合反应,芳香族化合物发生亲电取代反应(Wu et al.,2018)。
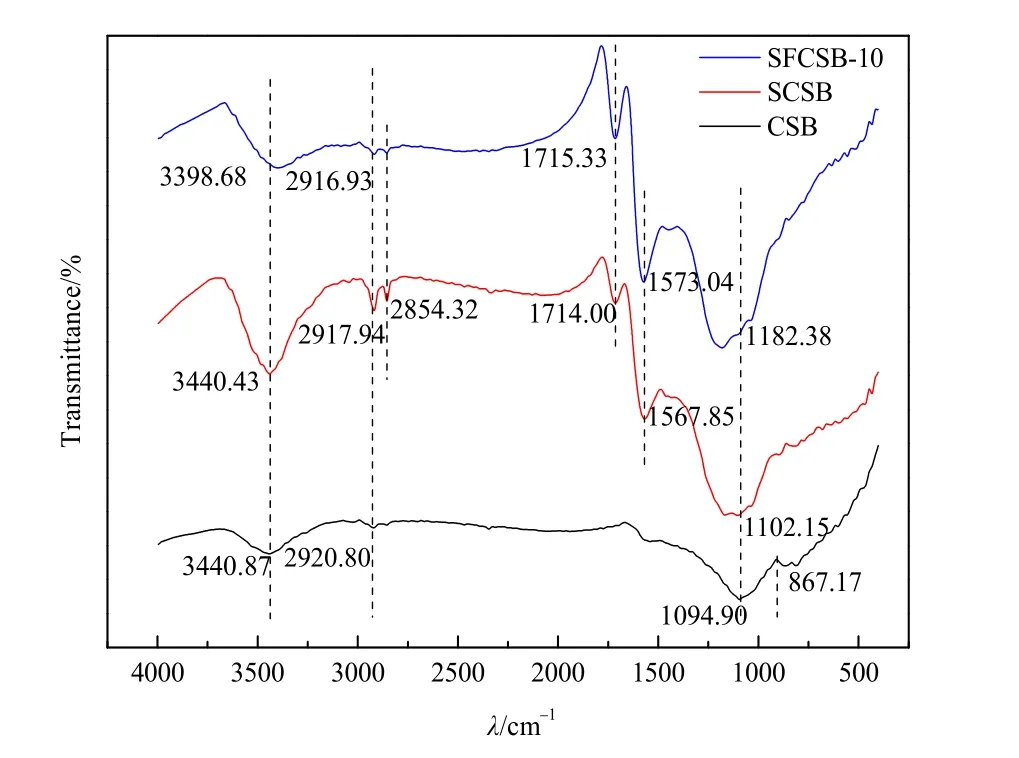
图9 SFCSB-10吸附As(Ⅴ)后的FTIR光谱Fig. 9 FTIR spectra of SFCSB-10 after adsorption of As(Ⅴ)
图10a为SFCSB-10吸附As(Ⅴ)后的XPS高分辨谱。As(Ⅴ)可以通过静电吸附和共沉淀吸附在SFCSB表面(Yang et al.,2020)。由于SFCSB吸附As(Ⅴ)后 As2p 能级(f)的电子发射,分别在 1327.28 eV和1363.04 eV结合能处出现了As2p3和As2p1的峰值,在表面区域的XPS探针测定出1.76% As原子百分比。由图10c可知,生物炭表面的Fe在712.66 eV处生成了 Fe2O3,725.85 eV处生成了FeOOH,因此吸附过程可能发生了氢键结合,这与FTIR的结果相一致。Anderson et al.(1976)研究表明,阴离子通过与表面羟基官能团相互交换可以吸附在氢氧化物上。化学式大致表示如下:

图10 SFCSB-10吸附As(Ⅴ)后的XPS(C1s、Fe2p、S2p、O1s、As2p)射线图谱Fig. 10 XPS (C1s, Fe2p, S2p, O1s, AS2p) spectrum of SFCSB-10 after adsorption of As(Ⅴ)
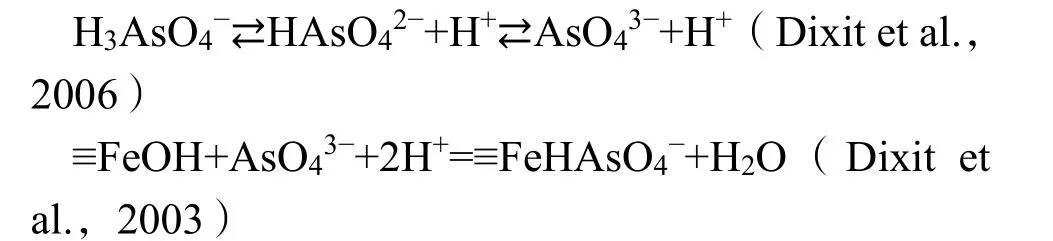
吸附As(Ⅴ)后C1s峰(b)与O1s峰(e)在结合能531.63 eV处出现了Fe–OH和C=O,533.27 eV出现了CO32−和–COOH(Zhang et al.,2020),生物炭表面的含氧官能团与金属-氧键能够与 As(Ⅴ)发生配位反应。而S2p(d)能级的168.91 eV处SO42−说明硫酸改性的作用主要是增大了生物炭的比表面积。
结合上述分析及2.2节Zeta电位分析,SFCSB-10对As(Ⅴ)的吸附机制可以归因为静电吸引、氢键结合、配位体反应及表面羟基官能团络合。
3 结论
(1)本研究以椰壳为原料,采用硫酸及硫酸铁共同改性制备的生物炭增加了生物炭的比表面积和含氧官能团数量,提高了对As(Ⅴ)的吸附效果。
(2)Elovich动力学和Langmiur等温吸附方程能够很好地描述生物炭对 As(Ⅴ)的吸附过程,在Fe–C质量分数之比为 15%条件下制备的生物炭材料对 As(Ⅴ)的吸附量最大,最大吸附量可达 14.65 mg·g−1。溶液pH在 4—5时,改性生物炭对As(Ⅴ)的吸附效果最好。
(3)SEM-EDS、FTIR、XPS等分析表明,铁基改性椰壳生物炭对As(Ⅴ)既有物理吸附也有化学吸附,吸附机制为生物炭表面正电荷与阴离子之间的静电吸引(非特异性吸附),O–H–As氢键结合、砷氧阴离子与铁氧化物的配位体效应和表面羟基官能团络合(特异性吸附)。
