海藻酸盐基胃黏膜保护胶作为黏膜下注射剂的可行性研究及其安全性
2021-10-11何牧野孙聪慧王苗苗曲明悦王春仁王涵
【作 者】何牧野,孙聪慧,王苗苗,曲明悦,王春仁,王涵
1 中国食品药品检定研究院,北京市,102629
2 烟台大学,烟台市,264000
0 引言
内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)是由最早的针对早期胃癌的内镜下黏膜切除术(endoscopic submucosal resection,EMR)演变而来。ESD术与EMR术相较于普通的外科手术有创伤小,具有患者术后生存质量高,花费小的优点[1]。ESD术与EMR术相比[2]实现了对较大较深的肿瘤的摘除,使得肿瘤剥离更加彻底,术后复发率大幅降低,然而随着技术的不断改进,黏膜下剥离术操作的难度越来越大,术后穿孔现象也越来越多。
在ESD术中,良好的黏膜下注射液可避免手术操作穿孔、手术操作困难等问题。生理盐水安全性高、价格低廉,是常用的黏膜下注射液,但形成隆起效果差、扩散快需多次注射,这些缺点使得生理盐水不能成为最佳的黏膜下注射液。本研究所用海藻酸盐基胃黏膜保护胶是一种新型复合材料,主要用于ESD术后的溃疡修复,内含有海藻酸盐[2]、多聚赖氨酸[3]等成分,起到止血、促进溃疡愈合的作用,是非常创新的医疗器械产品。笔者前期的研究结果也证明该胃黏膜保护胶在胃黏膜修复方面有较好的效果。胃黏膜保护胶是一种弹性水凝胶,具备成为黏膜下注射剂的必要条件,本研究主要探究胃黏膜保护胶作为黏膜下注射剂的可行性以及其安全性。
1 材料及方法
1.1 材料与试剂
实验材料:胃黏膜保护胶(浙江杭州英健生物科技有限公司,中国);新鲜猪肚(奥博屠宰场,河北),保存于4 ℃冰箱中,实验结束到屠宰时间不超过12 h;L929细胞株(来源:中国食品药品检定研究院细胞资源中心)。
实验动物:SD雄性大鼠32只,平均质量(250±20)g,术前禁食不禁水24 h。8~9周龄雄性金黄地鼠5只(中国食品药品检定研究院实验动物资源中心),适应性喂养5 d;雄性小鼠30只,平均质量(20±2)g。所有动物来源于中国食品药品检定研究院实验动物资源中心,实验动物生产许可证号:SCXK(京) 2014-0013;实验动物使用许可证号:SYXK(京) 2017-0013。独立通气笼(IVC)条件下饲养,环境温度20~25 ℃,湿度40%~70%。
试剂:亚甲基蓝(国药集团化学试剂有限公司,中国);水合氯醛(国药集团化学试剂有限公司,中国);0.9%氯化钠溶液(石家庄四药股份有限公司,中国);MEM培养基(Corning,美国);胎牛血清(天杭生物科技有限公司,浙江);0.25%胰酶(Hyclone,美国);精制玉米油(江苏康普生物医药科技有限公司,中国);二甲基亚砜(Sigma-Aldrich,美国);高密度聚乙烯(日本Hatano研究所,日本)。
1.2 设备与耗材
使用的设备与耗材:1 mL注射器;计时器;流变仪(安东帕,奥地利);白色泡沫板;游标卡尺(苏测计量仪器有限公司,中国);手术器械包;测量隆起装置。
1.3 方法
1.3.1 可行性研究
离体实验:10个新鲜猪肚(离体未超过12 h),将其上1/3段切割成小块并固定于泡沫板上。实验设置对照组和实验组(n=6),其中对照组为0.9%氯化钠溶液(生理盐水)组,实验组为用生理盐水稀释成10%、30%、50%、80%四个浓度梯度的胃黏膜保护胶稀释液组。对照组与实验组均加入一定量的亚甲基蓝粉末配制成含有0.5%的亚甲基蓝的生理盐水或不同浓度保护胶组。用1 mL注射器斜45o在每组猪肚上黏膜下注射对应的试剂。使用专门的测量工具测量黏膜下隆起的高度,记录对照组及样品组溶液黏膜下注射后1 min、10 min、30 min、60 min的黏膜下隆起高度[10]。
体内实验:将32只SD大鼠随机分为4组(n=8),禁食24 h后用10%的水合氯醛(称取一定量的水合氯醛溶于生理盐水配成1 mg/mL的水合氯醛溶液)腹腔注射麻醉,固定于无菌手术台上,打开腹腔,取出胃并沿胃大弯处割开,清理胃内容物,暴露胃黏膜。实验设置对照组和实验组(n=8),对照组为生理盐水组,实验组为用生理盐水稀释成30%、50%、80%三个浓度梯度的胃黏膜保护胶稀释液组。在每组大鼠的胃黏膜下用1 mL注射器斜45o注射对应的试剂。用游标卡尺测量胃壁原始厚度,再测量隆起高度,并用测量的隆起厚度减去黏膜厚度为黏膜隆起的实际厚度,记录黏膜下注射1 min、10 min、20 min、30 min的黏膜隆起厚度[11]。
不同浓度胃黏膜保护胶与生理盐水黏度测试:将稀释成10%、30%、50%、80%的胃黏膜保护胶与生理盐水,在25oC下,采用流变仪在剪切速率1 s-1下进行蠕动扫描,测试其剪切黏度值。
1.3.2 安全性评价
细胞毒性试验:实验分为四组,样品组(胃黏膜保护胶按3 cm2/mL加入含血清的MEM培养基中37oC,120 r/min摇床中浸提24 h)、阴性对照组(高密度聚乙烯)、阳性对照组(含有10%DMSO的含血清培养基)及空白对照组(含血清MEM培养基)溶液,将处于对数生长期的L929细胞按照国标16886.5使用MTT法测试样品细胞毒性[5-6]。
急性毒性试验:实验分为四组,样品盐水组(胃黏膜保护胶按3 cm2/mL加入生理盐水中37oC,120 r/min摇床浸提72 h)、样品植物油组(胃黏膜保护胶按3 cm2/mL加入精制玉米油中37oC,120 r/min摇床浸提72 h)、对照油组(植物油)和对照水组(生理盐水),按国标16886.11进行后续急性毒性实验[7]。
口腔黏膜刺激试验:实验分为四组,样品水组(胃黏膜保护胶按3 cm2/mL加入生理盐水中37oC,120 r/min摇床浸提72 h)、样品油组(胃黏膜保护胶按3 cm2/mL加入植物油中37oC,120 r/min摇床浸提72 h)、对照油组(植物油)和对照水组(生理盐水),按GB 16886.10进行后续口腔黏膜刺激实验[8-9]。
1.4 统计学分析
所有数据均采用SPSS 21.0统计软件包进行统计分析。安全性评价实验中采用了独立样本t检验,有效性实验中采用单因素方差分析,组间比较采用LSD检验,检验水准为α=0.05。
2 结果
2.1 可行性研究
离体胃黏膜隆起高度的变化:不同浓度的样品与生理盐水在猪胃黏膜下注射隆起效果见表1和图1,稀释成不同浓度的黏膜保护胶组隆起高度均显著高于生理盐水组(P<0.05);不同浓度的胃黏膜保护胶组中80%隆起高度均显著高于30%和10%(P<0.05);30%和50%在10 min、30 min、60 min时间隆起高度显著高于10%(P<0.05);50%和30%隆起高度无统计学差异。10%组与生理盐水组下降趋势很大,30%组、50%组和80%组下降趋势较小,50%组与30%组下降趋势无统计学差异,80%组隆起下降速度最慢。

表1 各时间点不同浓度溶液注射形成的隆起高度(mm)Tab.1 Elevation of different solution injection at each time point (mm)

图1 不同溶液所致猪胃黏膜下注射隆起形态随时间推移的变化Fig.1 Changes over time in the morphology of submucosal injection ridges of pigs caused by different solutions
体内胃黏膜隆起高度的变化:不同浓度的样品与生理盐水组在大鼠黏膜下注射隆起效果见表2,稀释成不同浓度的胃黏膜保护胶组在大鼠胃黏膜上注射时隆起厚度均显著高于生理盐水组(P<0.05),不同浓度黏膜保护胶组中80%组和50%组注射隆起厚度均显著厚于30%组。30%组与生理盐水组下降趋势很大,50%组与80%组下降较慢,80%组下降速度慢。
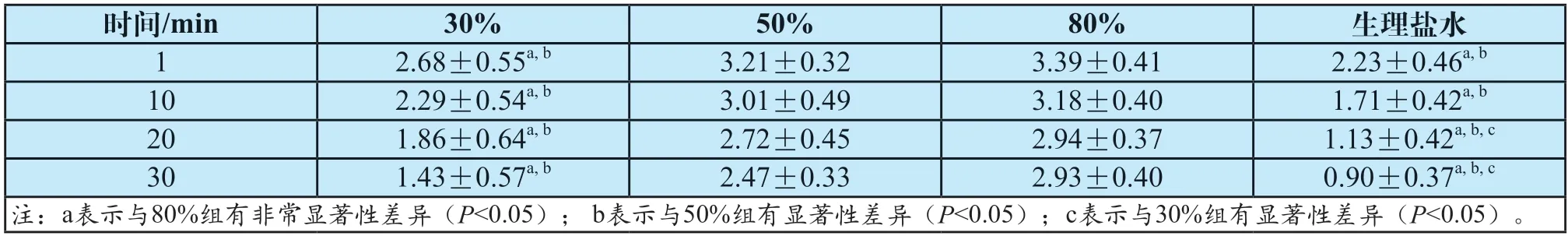
表2 各时间点不同溶液注射形成隆起厚度(mm)Tab.2 Uplift thickness formed by injection of different solutions at each time point(mm)
不同浓度胃黏膜保护胶和生理盐水黏度值:使用黏度计测试10%、30%、50%、80%以及生理盐水的黏度值(见图2),其中不同浓度胃黏膜保护胶黏度值与生理盐水均形成显著性差异(P<0.05),黏膜保护胶的浓度越高,黏度越大,注射难度越大。

图2 不同浓度黏膜下保护胶和生理盐水黏度值Fig.2 The viscosity values of different concentrations of submucosal protective glue and normal saline
2.2 安全性评价
细胞毒性试验:不同浓度的样品浸提液与空白、阳性、阴性对照24 h后的细胞存活率(见表3)。各浓度组样品细胞存活率均大于70%,样品无潜在细胞毒性。

表3 不同浓度样品浸提液下细胞存活率Tab.3 Cell viability of samples at different concentrations
急性毒性试验:灌胃后的样品水组、样品油组、对照水组、对照油组小鼠4 h、24 h、48 h、72 h小鼠未发现呼吸、肌肉运动、痉挛、反射、心血管、立毛、胃肠不适、皮肤红肿的异常现象,也未出现死亡现象。24 h、48 h、72 h后质量变化,质量呈逐渐增长趋势,如图3所示。

图3 小鼠灌胃后三天质量增长Fig.3 Mass gain of mice three days after gavage
口腔黏膜刺激试验:金黄地鼠口腔颊囊内放置各组棉球24 h后,对照生理盐水组、对照植物油组、样品生理盐水组,样品植物油组肉眼均未有糜烂、溃疡、充血及肿胀,其中样品组与对照组不同浸提液组织病理学观察(见图4)上皮完整、无白细胞浸润、未有血管充血,水肿等现象,记分为0分。

图4 口腔黏膜刺激组织病理图(5×10)Fig.4 Histopathology of oral mucosa stimulation (5×10)
3 讨论
20世纪90年代以来,内镜黏膜下剥离术的发展使得早期胃癌存活率大大提高,但其术后形成的较大较深的溃疡面容易发生出血和穿孔等并发症[12-13]。海藻酸盐基胃黏膜保护胶能促进止血和溃疡愈合并预防穿孔的发生,但保护胶除了需要关注其有效性外,其安全性也非常重要,本研究探究了胃黏膜保护胶的安全性,在细胞相容性实验中样品组细胞存活率均大于70%,样品拥有良好的细胞相容性。在急毒和口腔黏膜刺激实验中,样品植物油浸提组与样品生理盐水浸提组均未出现明显的急性毒性反应以及对口腔黏膜的刺激反应,有良好的生物相容性。
黏膜下注射剂的应用是ESD术操作过程中重要的一步,目前临床常用的黏膜下注射剂有生理盐水和透明质酸[15],但生理盐水扩散较快增加了术中穿孔的风险[14],而透明质酸研究表明长期在创口使用能促进癌细胞增殖[16]。除此以外还有一些新型黏膜下注射剂如异戊烷[17]、热敏二原水凝胶TBSH[18]、EleviewTM[19]、瑞巴派特溶液[20]等。目前的新型黏膜下注射剂应用途径较为单一,难以在降低黏膜下注射难度的基础上促进溃疡愈合,本研究探究了胃黏膜保护胶的黏膜下注射可行性,结果显示80%的胃黏膜保护胶能形成较高较持久的隆起,具有成为黏膜下注射剂的可行性。
