牛角瓜茎的化学成分及其细胞毒活性研究
2021-10-09戴好富黄圣卓冉红玲盖翠娟蔡彩虹梅文莉
于 淼,戴好富,黄圣卓,冉红玲,盖翠娟,蔡彩虹,梅文莉,王 昊
中国热带农业科学院热带生物技术研究所 海南省黎药资源天然产物研究与利用重点实验室;海南热带农业资源研究院,海口 571101
牛角瓜(Calotropisgigantea(L.)Dry.ex Ait.f.)又名断肠草、五狗卧花心,为萝藦科(Asclepiadaceae)牛角瓜属(Calotropis)植物,主要分布在中国南部、印度、越南、斯里兰卡和缅甸等地,在我国云南、海南、广东和四川等地均有分布,生长于低海拔向阳山坡、旷野地及海边[1]。牛角瓜具有祛痰平喘功效、抗菌、抗氧化、消炎和解毒等作用[2]。牛角瓜花具有镇痛作用[3];茎干具有保肝作用[4];叶具有抗腹泻作用[5];乳汁具有促进伤口愈合及抗菌的功效[6,7]。现代研究表明牛角瓜中含有多种化学成分,包括强心苷类、甾体类、三萜类及黄酮类等成分[8-11]。由于其显著的抗肿瘤活性,诸多学者已对牛角瓜化学成分进行分离纯化和结构鉴定。为了更好的研究牛角瓜化学物质基础,进一步完善该植物的生物活性内容,本课题对牛角瓜茎的化学成分及其细胞毒活性进行研究,采用硅胶、Sephadex LH-20等多种色谱分离技术对牛角瓜茎乙醇提取物的乙酸乙酯部位进行分离,并采用四甲基唑蓝(MTT)法测定化合物对4种肿瘤细胞的体外细胞毒活性。
1 材料与方法
1.1 仪器与试剂
Bruker AV-500型超导核磁共振波谱仪,TMS为内标(德国Bruker公司);Autospec 300质谱仪(英国VG公司);高效液相色谱仪(Agilent 1260)(美国安捷伦科技有限公司);旋转蒸发仪(Heidolph Laborota);核磁管TA1008-200(河流科技有限公司);ZHJH-C1109C超净工作(上海智诚分析仪器制造有限公司);HHB11360-S CO2培养箱(上海跃进医疗器械厂);Sephadex LH-20(德国Merck公司);C18反相硅胶(日本Fuji公司);柱层析硅胶G(200~300、60~80目)(青岛海洋化工厂);薄层层析硅胶H(青岛海洋化工厂);甲醇、乙腈为色谱纯(天津市科密欧有限公司);水为超纯水;10%硫酸乙醇显色剂。
1.2 材料
牛角瓜于2019年8月采自海南省海口市,并经中国热带农业科学院热带生物技术研究所黄圣卓博士鉴定为萝藦科(Asclepiadaceae)牛角瓜属(Calotropis)植物牛角瓜(Calotropisgigantea),凭证标本(WANG202001),保存于中国热带农业科学院热带生物技术研究所。
1.3 实验方法
1.3.1 提取与分离
牛角瓜茎(5.2 kg),干燥粉碎后用95%乙醇浸泡提取3次,提取液减压浓缩得到乙醇提取物(219.7 g)。将提取物分散于水中成悬浊液,依次用石油醚、乙酸乙酯和正丁醇萃取,得到石油醚萃取物、乙酸乙酯萃取物(14.1 g)和正丁醇萃取物。乙酸乙酯萃取物经正相硅胶柱色谱,以石油醚-乙酸乙酯(15∶1→0∶1)、丙酮梯度洗脱,得到14个流份(Fr.1~Fr.14)。Fr.10经反相硅胶柱色谱(甲醇-水3∶7→1∶0)得到13个流份(Fr.10.1~Fr.10.13),其中流份Fr.10.8(633.6 mg)经减压硅胶柱色谱和Sephadex LH-20凝胶柱色谱(甲醇)分离得到化合物1(2.0 mg)、2(5.9 mg)、4(22.0 mg)、5(402.7 mg);流份Fr.10.6(14.5 mg)经Sephadex LH-20凝胶柱色谱(甲醇)分离得到化合物3(5.1 mg)。流份Fr.2(964.4 mg)经反相硅胶柱色谱(甲醇-水3∶7→1∶0)得到6个流份(Fr.2.1~Fr.2.6),其中流份Fr.2.1(87.7 mg)经减压硅胶柱色谱分离得到化合物9(4.1 mg)和10(5.0 mg);流份Fr.2.2(9.0 mg)通过结晶得到化合物8(5.4 mg),流份Fr.2.3(27 mg)经Sephadex LH-20凝胶柱色谱(甲醇)分离得到化合物6(15.0 mg),Fr.2.4(11.3 mg)经Sephadex LH-20凝胶柱色谱(甲醇)分离得到化合物7(5.4 mg)。
1.3.2 活性测试
采用MTT法测试化合物1~10对慢性髓原白血病细胞K562、人胃癌细胞SGC-7901、人肺癌细胞A549和人宫颈癌细胞HeLa的体外细胞毒活性。化合物分别用DMSO溶解后配成20 mmol/L储备液,临用前稀释到适合的浓度。将4种人体肿瘤细胞制成单细胞悬浮液,接种于96孔板上,并设空白组、对照组以及实验组,每组设3个平行孔,实验组为0.078、0.156、0.312、0.625、1.25、2.5、5、10、20、40 μmol/L的含药样品溶液,在96孔板中直接加入各个样品溶液10 μL,连续培养72 h后。再加入15 μL配制好的MTT溶液(5 mg/mL),在CO2恒温培养箱中恒温培养,孵育后使用酶标仪测量其在波长为490 nm下的吸光度(A),并计算生长抑制率及IC50值。盐酸阿霉素为阳性对照。
2 实验结果
2.1 结构鉴定
化合物1白色粉末;C26H32O11;ESI-MS:m/z521.1 [M+H]+;1H NMR(500 MHz,CD3OD)δH:7.15(1H,d,J= 8.4 Hz,H-5),7.03(1H,d,J= 1.8 Hz,H-2),6.95(1H,d,J= 1.8 Hz,H-2′),6.93(1H,dd,J= 8.4,1.8 Hz,H-6),6.82(1H,dd,J= 8.1,1.8 Hz,H-6′),6.77(1H,d,J= 8.1 Hz,H-5′),4.88(1H,m,H-1′′),4.77(1H,d,J= 4.1 Hz,H-7′),4.71(1H,d,J= 4.1 Hz,H-7),4.25(2H,m,H-9a,9′a),3.90(1H,m,H-6′′a),3.87(3H,s,3-OCH3),3.86(3H,s,3′-OCH3),3.88(2H,m,H-9b,9′b),3.69(1H,m,H-6′′b),3.49(1H,m,H-2′′),3.45(1H,m,H-3′′),3.40(1H,m,H-4′′),3.39(1H,m,H-5′′),3.15(2H,m,H-8,8′);13C NMR(125 MHz,CD3OD)δC:137.5(C-1),111.6(C-2),151.0(C-3),147.5(C-4),118.0(C-5),119.8(C-6),87.5(C-7),55.3(C-8),72.7(C-9),133.8(C-1′),111.0(C-2′),147.3(C-3′),149.1(C-4′),116.1(C-5′),120.0(C-6′),87.9(C-7′),55.8(C-8′),72.7(C-9′),102.8(C-1′′),74.8(C-2′′),77.8(C-3′′),71.3(C-4′′),78.2(C-5′′),62.5(C-6′′),56.7(3-OCH3),56.4(3′-OCH3)。以上数据与文献报道对照基本一致[12],故鉴定化合物1为(-)-松脂醇-4′-O-β-D-葡萄糖苷。
化合物2棕色粉末;C34H38O14;ESI-MS:m/z671.6 [M+H]+;1H NMR(500 MHz,CD3OD)δH:7.58(1H,dd,J= 8.2,1.8 Hz,H-6′′′),7.54(1H,br s,H-2′′′),6.99(1H,d,J= 8.3 Hz,H-5),6.98(1H,s,H-2′),6.97(1H,br s,H-2),6.88(1H,d,J= 8.3 Hz,H-5′),6.82(1H,dd,J= 8.3,1.8 Hz,H-6′),6.78(1H,d,J= 8.2 Hz,H-5′′′),6.45(1H,br d,J= 8.3 Hz,H-6),4.87(1H,d,J= 7.3 Hz,H-1′′),4.69(2H,m,H-7,7′),4.66(1H,dd,J= 11.7,2.2 Hz,H-6′′a),4.48(1H,dd,J= 11.7,8.2 Hz,H-6′′b),4.26(1H,dd,J= 9.0,7.9 Hz,H-9a),4.15(1H,dd,J= 9.0,7.9 Hz,H-9′a),3.89(3H,s,3-OCH3),3.84(1H,m,H-9b),3.82(3H,s,3′-OCH3),3.82(3H,s,3′′′-OCH3),3.82(1H,m,H-9′b),3.78(1H,m,H-5′′),3.54(2H,m,H-2′′,3′′),3.43(1H,dd,J= 9.2,8.9 Hz,H-4′′),3.10(1H,m,H-8′),3.00(1H,m,H-8);13C NMR(125 MHz,CD3OD)δC:137.3(C-1),111.7(C-2),150.7(C-3),147.1(C-4),117.7(C-5),119.3(C-6),87.0(C-7),55.4(C-8),72.8(C-9),133.7(C-1′),111.1(C-2′),149.1(C-3′),144.3(C-4′),116.0(C-5′),120.2(C-6′),87.6(C-7′),55.3(C-8′),72.5(C-9′),102.4(C-1′′),74.8(C-2′′),77.8(C-3′′),72.2(C-4′′),75.6(C-5′′),65.0(C-6′′),122.5(C-1′′′),113.9(C-2′′′),148.8(C-3′′′),153.1(C-4′′′),116.1(C-5′′′),125.3(C-6′′′),167.8(C-7′′′),56.7(3-OCH3),56.5(3′-OCH3),56.5(3′′′-OCH3)。以上数据与文献报道对照基本一致[13],故鉴定化合物2为(+)-pinoresinol-4-O-[6′′-O-vanilloyl]-β-D-glucopyranoside。
化合物3黄色油状;C31H36O11;ESI-MS:m/z607.2 [M+Na]+;1H NMR(500 MHz,CD3OD)δH:6.97(2H,br s,H-2,6),6.97(2H,br s,H-2′,6′),6.96(1H,br s,H-2′′),6.77(1H,dd,J= 8.1,1.6 Hz,H-6′′),6.72(1H,d,J= 8.1 Hz,H-5′′),6.55(1H,d,J= 15.8 Hz,H-7′),6.24(1H,dt,J= 15.8,6.0 Hz,H-8′),5.58(1H,d,J= 6.0 Hz,H-7),4.90(1H,d,J= 5.1 Hz,H-7′′),4.25(1H,dd,J= 8.9,5.1 Hz,H-8′′),4.20(2H,d,J= 6.0 Hz,H-9′),3.92(1H,m,H-9′′a),3.91(3H,s,5-OCH3),3.88(2H,d,J= 5.2 Hz,H-9),3.82(3H,s,5′-OCH3),3.81(3H,s,3-OCH3),3.79(3H,s,3′-OCH3),3.59(1H,m,H-9′′b),3.48(H,m,H-8);13C NMR(125 MHz,CD3OD)δC:139.4(C-1),103.9(C-2,6),154.6(C-3,5),136.3(C-4),88.9(C-7),55.5(C-8),64.9(C-9),132.8(C-1′),116.5(C-2′),130.0(C-3′),149.1(C-4′),145.5(C-5′),112.1(C-6′),131.9(C-7′),127.7(C-8′),63.8(C-9′),133.8(C-1′′),111.3(C-2′′),148.6(C-3′′),146.8(C-4′′),115.6(C-5′′),120.7(C-6′′),74.0(C-7′′),87.3(C-8′′),61.6(C-9′′),56.3(3-OCH3),56.3(3′-OCH3),56.6(5-OCH3),56.8(5′-OCH3)。以上数据与文献报道对照基本一致[14],故鉴定化合物3为(-)-jatrointelignan B。
化合物4棕色粉末;C42H50O16;ESI-MS:m/z833.2 [M+Na]+;1H NMR(500 MHz,CD3OD)δH:6.94(2H,br s,H-2′′,H-2′′′),6.74(2H,br d,J= 8.1 Hz,H-6′′,H-6′′′),6.69(2H,d,J= 8.1 Hz,H-5′′,H-5′′′),6.65(4H,s,H-2,H-6,H-2′,H-6′),4.91(2H,br s,H-7′′,H-7′′′),4.71(2H,d,J= 2.5 Hz,H-7,H-7′),4.23(2H,m,H-9b,9′b),3.91(2H,m,H-8′′,H-8′′′),3.87(2H,m,H-9′′a,9′′′a),3.86(2H,m,H-9a,9′a),3.83(12H,s,3′′-OCH3,3′′′-OCH3,5′′-OCH3,5′′′′-OCH3),3.82(12H,s,3-OCH3,3′-OCH3,5-OCH3,5′-OCH3),3.55(2H,m,H-9′′b,9′′′b),3.08(4H,m,H-8,H-8′);13C NMR(125 MHz,CD3OD)δC:138.8(C-1,C-1′),104.2(C-2,C-6,C-2′,C-6′),154.5(C-3,C-5,C-3′,C-5′),136.1(C-4,C-4′),87.2(C-7,C-7′),55.6(C-8,C-8′),73.0(C-9,C-9′),133.8(C-1′′,C-1′′′),111.3(C-2′′,C-2′′′),148.6(C-3′′,C-3′′′),146.8(C-4′′,C-4′′′),115.6(C-5′′,C-5′′′),120.7(C-6′′,C-6′′′),74.0(C-7′′,C-7′′′),87.2(C-8′′,C-8′′′),61.7(C-9′′,C-9′′′),56.7(3-OCH3,3′-OCH3,5-OCH3,5′-OCH3),56.3(3′′-OCH3,3′′′-OCH3,5′′-OCH3,5′′′-OCH3)。以上数据与文献报道对照基本一致[15],故鉴定化合物4为(+)-(7R,7′R,7′′S,7′′′S,8S,8′S,8′′S,8′′′S)-4′′,4′′′-dihydroxy-3,3′,3′′,3′′′,5,5′-hexamethoxy-7,9′;7′,9-diepoxy-4,8′′;4′,8′′′-bisoxy-8,8′-dineolignan-7′′,7′′′,9′′,9′′′-tetraol。
化合物5白色粉末;C29H44O9;ESI-MS:m/z559.2 [M+Na]+;1H NMR(500 MHz,DMSO-d6)δH:5.90(1H,s,H-22),4.97(1H,d,J= 18.3 Hz,H-21a),4.88(1H,d,J= 18.3 Hz,H-21b),4.53(1H,d,J= 7.9 Hz,H-1′),3.51(1H,m,H-3),3.79(1H,m,H-3′),3.64(1H,m,H-19a),3.53(1H,m,H-5′),3.49(1H,m,H-19b),3.06(1H,m,H-2′),2.96(1H,m,H-4′),2.70(1H,dd,J= 9.0,5.3 Hz,H-17),2.19(1H,d,J= 12.8 Hz,H-1a),1.99(1H,m,H-16a),1.98(1H,m,H-7a),1.94(1H,m,H-15a),1.76(1H,m,H-7b),1.68(1H,m,H-2a),1.62(1H,m,H-4a),1.62(1H,m,H-8),1.56(1H,m,H-15b),1.54(1H,m,H-11a),1.45(1H,m,H-11b),1.40(1H,m,H-2b),1.36(1H,m,H-12a),1.28(1H,m,H-4b),1.24(1H,m,H-12b),1.20(1H,m,H-6a),1.09(3H,d,J= 6.1 Hz,H-6′),1.09(1H,m,H-6b),1.08(1H,m,H-5),0.94(1H,m,H-16b),0.86(1H,td,J= 12.0,3.3 Hz,H-9),0.80(3H,s,H-18),0.63(1H,t,J= 12.8 Hz,H-1b);13C NMR(125 MHz,DMSO-d6)δC:31.3(C-l),29.5(C-2),76.5(C-3),34.6(C-4),44.0(C-5),28.0(C-6),26.4(C-7),41.2(C-8),49.6(C-9),38.8(C-10),22.4(C-11),39.5(C-12),49.5(C-13),83.9(C-14),32.1(C-15),27.3(C-16),50.2(C-17),15.8(C-18),57.8(C-19),176.5(C-20),73.2(C-21),116.2(C-22),173.9(C-23),98.1(C-1′),70.7(C-2′),71.4(C-3′),72.7(C-4′),68.6(C-5′),18.0(C-6′)。以上数据与文献报道对照基本一致[16],故鉴定化合物5为弗如糖苷。
化合物6白色粉末;C13H18O3;ESI-MS:m/z245.1 [M+Na]+;1H NMR(500 MHz,CD3OD)δH:7.00(1H,d,J= 15.8 Hz,H-7),6.43(1H,d,J= 15.8 Hz,H-8),5.95(1H,d,J= 8.0 Hz,H-4),2.59(1H,d,J= 17.2 Hz,H-2a),2.30(3H,s,H-10),2.25(1H,d,J= 17.2 Hz,H-2b),1.89(3H,s,H-11),1.06(3H,s,H-12),1.02(3H,s,H-13);13C NMR(125 MHz,CD3OD)δC:42.6(C-1),50.5(C-2),200.4(C-3),128.0(C-4),164.7(C-5),80.0(C-6),148.4(C-7),131.7(C-8),200.7(C-9),27.6(C-10),23.5(C-11),24.7(C-12),19.2(C-13)。以上数据与文献报道对照基本一致[17],故鉴定化合物6为(+)-dehydrovomifoliol。
化合物7白色粉末;C9H7NO2;ESI-MS:m/z162.1 [M+H]+;1H NMR(500 MHz,CD3OD)δH:8.07(1H,br d,J= 7.5 Hz,H-5),7.95(1H,s,H-2),7.43(1H,br d,J= 7.5 Hz,H-8),7.20(1H,br t,J= 7.5 Hz,H-6),7.17(1H,br t,J= 7.5 Hz,H-7);13C NMR(125 MHz,CD3OD)δC:133.4(C-2),108.8(C-3),127.6(C-4),122.0(C-5),123.6(C-6),122.3(C-7),112.9(C-8),138.2(C-9),169.3(C-10)。以上数据与文献报道对照基本一致[18],故鉴定化合物7为3-吲哚甲酸。
化合物8白色粉末;C9H10O4;ESI-MS:m/z183.1 [M+H]+;1H NMR(500 MHz,CD3OD)δH:7.25(1H,d,J= 7.2 Hz,H-6),7.13(1H,d,J= 7.8 Hz,H-4),7.06(1H,dd,J= 7.8,7.2 Hz,H-5),3.81(3H,s,3-OCH3),3.80(3H,s,2-OCH3);13C NMR(125 MHz,CD3OD)δC:127.4(C-1),149.9(C-2),154.7(C-3),117.2(C-4),123.2(C-6),125.2(C-5),169.7(C-7),61.9(2-OCH3),56.5(3-OCH3)。根据以上数据及二维核磁数据,故鉴定化合物8为2,3-二甲氧基苯甲酸。
化合物9白色粉末;C7H6O3;ESI-MS:m/z139.1 [M+H]+;1H NMR(500 MHz,CD3OD)δH:7.89(2H,d,J= 8.8 Hz,H-2,H-6),6.84(2H,d,J= 8.8 Hz,H-3,H-5);13C NMR(125 MHz,CD3OD)δC:122.7(C-1),133.0(C-2,C-6),116.0(C-3,C-5),163.3(C-4),170.1(C-7)。以上数据与文献报道对照基本一致[19],故鉴定化合物9为对羟基苯甲酸。
化合物10白色粉末;C8H8O4;ESI-MS:m/z169.1 [M+H]+;1H NMR(500 MHz,CD3OD)δH:7.57(2H,m,H-2,H-5),6.86(1H,d,J= 8.7 Hz,H-6),3.91(3H,s,3-OCH3);13C NMR(125 MHz,CD3OD)δC:123.1(C-1),113.8(C-2),152.7(C-3),148.7(C-4),115.8(C-5),125.3(C-6),170.1(1-COOH),56.4(3-OCH3)。以上数据与文献报道对照基本一致[20],故鉴定化合物10为香草酸。
2.2 活性测试结果
化合物1~10的细胞毒活性测试结果(见表1)显示化合物4和5对4种肿瘤细胞具有不同程度的细胞毒活性,其他化合物无明显细胞毒活性。其中,化合物4对人宫颈癌细胞HeLa具有的抑制活性较强,IC50为12.37 μM;化合物5对慢性髓原白血病细胞K562的抑制活性最强,IC50为0.29 μM。
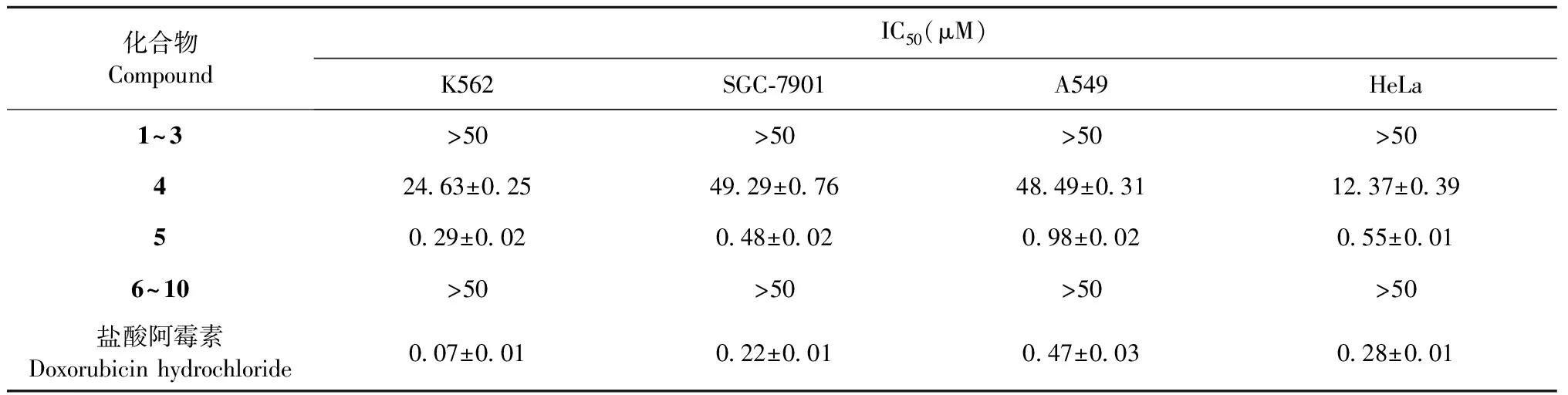
表1 化合物1~10的体外细胞毒活性测试结果Table 1 Results of compounds 1-10 cytotoxic activity in vitro
3 结论
从牛角瓜茎中分离得到10个化合物,化合物1、3、4和6~8为首次从该植物中分离得到,其中化合物1~4为木脂素类化合物,8~10为酚酸类化合物。测试化合物1~10对4种肿瘤的细胞毒活性,结果表明化合物4和5对4种肿瘤细胞具有不同程度的细胞毒活性,IC50值范围分别为12.37~49.29和0.29~0.98 μM,其他化合物没有显示出明显活性。根据文献报道化合物4对人卵巢癌细胞SK-OV-3具有微弱的细胞毒活性,化合物5弗如糖苷是牛角瓜中主要的强心苷成分,超过提取物含量的2.8%,且对多种肿瘤细胞具有较强的细胞毒活性。最近的研究表明,弗如糖苷可通过诱导线粒体介导黑色素瘤细胞凋亡[21],可能有助于预防黑色素瘤,这表明该化合物可能具有很多潜在活性尚未开发,具有进一步研究的价值。
