药物经济学评价中“免费仍不经济”类结果的原因分析
2021-09-28管欣王璐颖李洪超
管欣 王璐颖 李洪超

中图分类号 R956 文献标志码 A 文章编号 1001-0408(2021)18-2242-06
DOI 10.6039/j.issn.1001-0408.2021.18.11
摘 要 目的:为今后开展相关药物经济学评价提供参考和借鉴。方法:通过4个药物经济学评价典型案例展示可能出现“免费仍不经济”的特殊情况,定义“净价值”的概念来协助进行理论分析,并归纳导致这种情况的可能原因。结果与结论:目标药物之外的背景治疗成本过高、患者存活期间生命质量过低、增量成本-效果比的意愿支付阈值过低、延长生存期间风险事件的成本过高或者健康损失过高以及对照方案价格过低等都有可能影响经济性评价的结果,甚至出现“免费仍不经济”的药物经济学评价困境。药物经济学评价讨论的是干预方案的經济性而非药物的经济性问题,对于存在多种原因所导致的不经济的结果,需要客观看待;从理论上来说,药物经济学评价中应当将所有“相关”和“不相关”的成本都纳入计算范畴;药物经济学主要解决的是若干治疗方案之间“性价比”问题,而医疗卫生领域常常还需要面对伦理和公平性等问题,故研究者可能需要跳出药物经济学分析的框架,从更高、更广的角度进行深入讨论。
关键词 药物经济学;免费仍不经济;背景治疗;成本;原因分析
Cause Analysis of “Not Cost-effective at a Zero Price” Results in Pharmacoeconomic Evaluation
GUAN Xin1,2,WANG Luying1,2,LI Hongchao1,2(1. School of International Pharmaceutical Business, China Pharmaceutical University, Nanjing 211198, China; 2. Pharmacoeconomic Evaluation Research Center, China Pharmaceutical University, Nanjing 211198, China)
ABSTRACT OBJECTIVE: To provide reference for the future pharmacoeconomic evaluation. METHODS: Four typical cases of pharmacoeconomic evaluation showed the special situation that “not cost-effective at a zero price”, defined the concept of “net value” to assist in theoretical analysis, and summarized the possible causes of this situation. RESULTS & CONCLUSIONS: The background treatment cost other than the target drug was too high, the patients quality of life during survival was too low, the threshold of willingness to pay of incremental cost-effectiveness ratio was too low, the cost of risk events during extended survival was too high or the health loss was too high, and the price of the control scheme was too low, which might affect the results of economic evaluation, and even led to the dilemma of pharmacoeconomic evaluation of “not cost-effective at a zero price”. Pharmacoeconomic evaluation discusses the economy of intervention programs rather than the economy of drugs. The uneconomic results caused by various reasons need to be treated objectively; theoretically, all “relevant” and “irrelevant” costs should be included in the calculation category in pharmacoeconomic evaluation; pharmacoeconomics mainly solves the problem of “cost performance” comparison among several treatment schemes, and the medical and health field often needs to face problems such as ethics and fairness. Therefore, researchers may need to jump out of the framework of pharmacoeconomics analysis and conduct in-depth discussion from a higher and broader perspective.
KEYWORDS Pharmacoeconomics; Not cost-effective at a zero price; Background therapy; Cost; Cause analysis
自2016年人力资源和社会保障部发布《2016年国家基本医疗保险、工伤保险和生育保险药品目录调整工作方案》以来,药物经济学评价证据作为价格测算的一项重要科学依据,开始被逐步应用于我国医保药品目录调整过程中[1-2]。因此,药物经济学评价方法的合理性以及在应用过程中客观合理地理解药物经济学评价证据十分重要。然而,在一些比较特殊的情况下,采用传统的药物经济学评价方法可能得到一些不合乎情理的结果。例如,一些具有明确临床疗效的新药,在一个似乎合理的价格下开展的药物经济学评价得到的却是“不经济”的结果;甚至在某些更为极端的情况下,这些具有明确临床价值的药物即使价格降为0,其药物经济学评价结果仍然显示该药不具有经济性[3]。本文将首先通过4个药物经济学评价的研究案例展示临床疗效明确且价格似乎合理但经济学评价结果为不经济的情况,分析讨论 “免费仍不经济”类结果产生的原因和主要情况,以期为今后开展相关药物经济学评价提供参考和借鉴。
1 案例分析
1.1 “联合治疗 vs.单药治疗”的困境
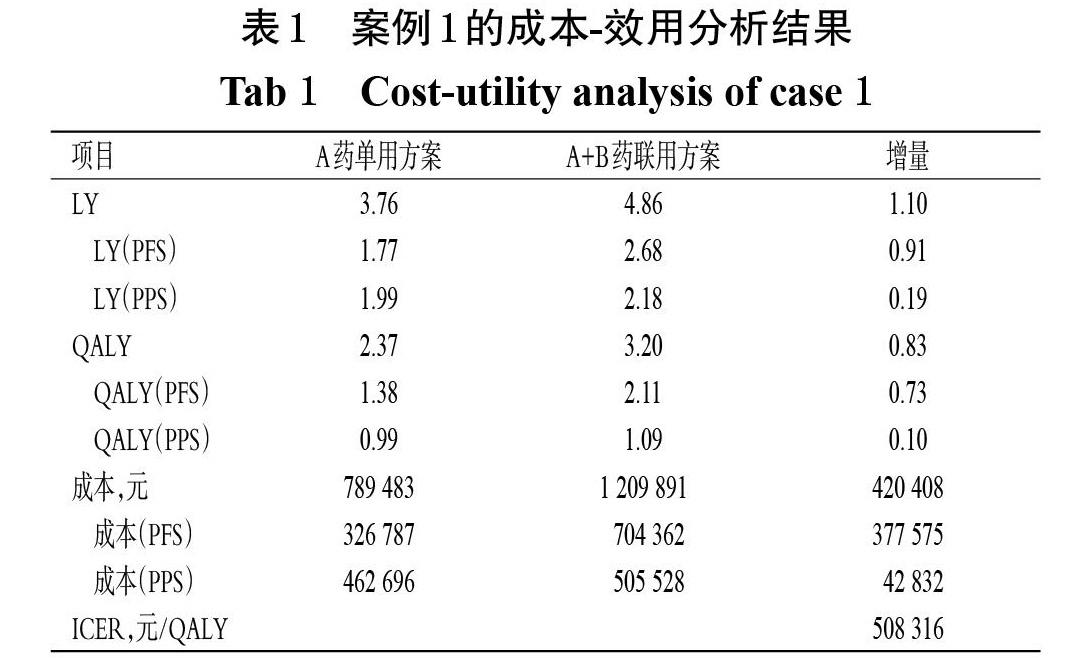
案例1:在某晚期恶性肿瘤的一线治疗中,A药物为临床治疗指南推荐的标准治疗药物,B药物为治疗该肿瘤的新药。临床试验结果表明,在A药物治疗基础上联用B药物,可显著延长患者的无进展生存期(PFS,18.7个月vs. 12.4个月)和总生存期(OS,56.5个月vs. 40.5个月)。即相比于A药单用方案,A+B药联用方案平均可以延长PFS 6.3个月和OS 16.0个月,延长进展后生存期(PPS)9.7个月,临床疗效明确且显著。以该临床试验数据为基础,构建包括PFS、PPS和死亡的三状态Markov模型,从医疗卫生系统角度出发,比较A+B药联用方案与A药单用方案治疗该恶性肿瘤的经济性。效用值数据从已发表文献中获取,成本数据来自中国真实世界数据,以此进行成本-效用分析,结果见表1。由表1可见,相比于A药单用方案,A+B药联用方案可以明显提高患者的生命年(LY)和质量调整生命年(QALY),但同时平均成本也大幅增加,最终增量成本-效果比(ICER)为508 316元/QALY。由于1个ICER的阈值本来就很难确定,本研究采用《中国药物经济学评价指南2020》[4]中推荐的1~3倍人均国内生产总值(GDP)的上限作为阈值标准进行讨论,则本案例中的ICER值远高于2020年我国3倍人均GDP(217 341元)。可以得出,采用A+B药联用方案治疗该恶性肿瘤在我国不具有经济性。
尽管无法判断在上述分析中B药物的价格相对于其给患者带来的健康获益是否合理,但是若令ICER值等于2020年我国3倍人均GDP,进而倒推B药物每盒价格必须要低于-63元,才能保证A+B药联用方案具有经济性。也就是说,即使B药物价格降为0元/盒,ICER值为220 983元,仍高于上述阈值,A+B药联用方案相对于A药单用方案仍然不具有经济性。进一步对A+B药联用和A药单用方案的治疗成本进行分析,结果见表2。A+B药联用方案在PFS阶段的背景治疗成本(PFS阶段治疗期间除了B药物之外的所有成本)为466 721元,较A药单用方案增加了139 934元,该阶段的增量QALY为0.73,ICER值为191 631元/QALY,略低于上述阈值。由于在两种方案下,患者进展后都会换用相同的二线治疗方案,A+B药联用方案在PPS阶段的治疗成本(包括PPS阶段的治疗费用和临终关怀费用)为505 528元,较A药单用方案增加了42 832元,该阶段的增量QALY为0.10,ICER值为442 321元/QALY,远高于上述阈值。按照每个QALY的意愿支付值为217 341元计算,PPS期的净效益为-21 098元(217 341×0.10-42 832=-21 098元),也就是说,与A药单用方案相比,A+B药联用方案可延长患者PPS 9.7个月这一健康结果本身就是“不值得”的,净效益为负。
进一步对成本和健康收益进行分析。在PPS阶段,患者的健康效用值为0.50,同时其二线治疗平均每月需支付约19 350元(考虑到临终关怀成本,因此两组间略有差异,但对结果影响不大,此处差异忽略不计),在此基础上以2020年我国3倍人均GDP为阈值可以推算,患者在PPS阶段每生存1个月的价值为-10 294元(217 341×0.50×1/12-19 350=-10 294),即患者在PPS阶段存活是“负价值”事件。同理,以0.50的健康效用值和2020年我国3倍人均GDP为阈值倒推,患者在PPS阶段的治疗成本需小于9 056元/月才具有“生存价值”。在PFS阶段,患者的健康效用值为0.786,若不考虑B药物的成本,患者每月约花费14 945元,其在PFS阶段每生存1个月的价值为-709元,即患者在PFS阶段存活也是“负价值”事件。同理可推算,在效用值和阈值不变的条件下,患者在PFS阶段的治疗成本需低于14 236元/月才具有“生存价值”。基于上述分析,该晚期恶性肿瘤患者不考虑B药物成本,仅在A药物治疗的基础上延续存活状态,便已经是一个“不经济”的方案,因此无论B药物如何降价,A+B药联用方案都不具有经济性。
由此可见,本案例中导致有效药物“免费仍不经济”的主要原因有以下几个:①药物治疗方案的背景治疗成本高(如PFS阶段联合使用的药物成本和PPS阶段的二线治疗成本);②患者存活期间健康效用值太低(如PPS阶段的效用值)等。
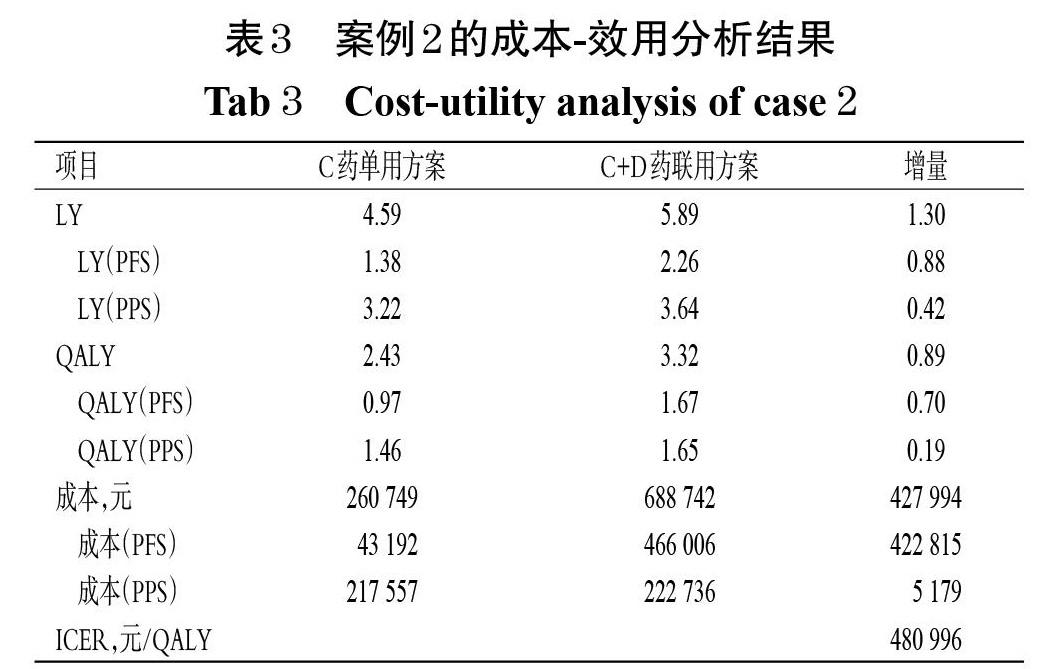
案例2:针对另一种恶性肿瘤,已知C药物是治疗该病的一线药物之一。临床研究数据表明,在C药物治疗的基础上,联用D药物进行一线治疗可以显著延长患者的PFS(20.0个月 vs. 12.1个月)和OS(48个月时尚未观测到中位OS vs. 38.1个月)。与案例1类似,以我国真实世界数据计算成本,结合该临床研究中的生存数据和效用值,构建包括PFS、PPS和死亡的三状态Markov模型,从医疗卫生系统角度出发,比较C+D药联用方案与C药单用方案治疗该恶性肿瘤的经济性。成本-效用分析结果见表3。由表3可见,相比于C药单用方案,采用C+D药联用方案可使患者多获得0.89个QALY,但同时需要多支付427 994元,ICER值為480 996元/QALY,远高于2020年我国3倍人均GDP这一阈值,故C+D药联用方案在我国不具有经济性。
同理,令ICER值等于2020年我国3倍人均GDP,倒推D药物的价格。计算结果显示,当D药物价格低于6 055元/盒时,C+D药联用方案方具有经济性。与案例1不同,D藥物可以通过降价来使C+D药联用方案具有经济性。进一步对两种方案的成本进行分析,结果见表4。在PFS阶段,C+D药联用方案的背景治疗成本为70 810元,较C药单用方案增加了27 618元。在PFS阶段,C+D药联用方案较C药单用方案的增量QALY为0.70,若D药免费,则该阶段的ICER值为39 486元/QALY,远低于上述阈值。在PPS阶段,C+D药联用方案的治疗成本(治疗费用+临终关怀成本)为222 736元,较C药单用方案增加了5 179元;在PPS阶段,C+D药联用方案较C药单用方案的增量QALY为0.19,该阶段的ICER值为27 258元/QALY,远低于上述阈值。假设D药物价格为0元/盒,C+D药联用方案的总成本为293 546元,相比于C药单用方案增加了32 797元,增量产出为0.89 QALY,ICER值为36 859元/QALY,远低于上述阈值。在本案例中,背景治疗成本的存在会对D药物的经济性判断造成影响,但是并没有出现“免费仍不经济”的极端现象。
在案例2中,患者在PFS和PPS阶段的效用值分别为0.740和0.710。参考案例1,使用2020年我国3倍人均GDP阈值进行推算,若不考虑D药物的成本,患者在PFS阶段存活的价值为13 403元/月,在PPS阶段存活的价值为12 859元/月,即患者存活是具有“正价值”的事件。
在案例1和案例2中,联合用药方案相比于单一用药方案所增加的LY和QALY较为接近,但D药物可以通过降价以确保联合用药方案的经济性,而B药物即使免费仍然不具有经济性。结合上述分析,笔者认为两个案例最主要的区别在于,在只考虑背景治疗成本时,患者存活是否具有“正价值”:在案例1中,患者无论在PFS阶段还是PPS阶段均不具有“存活价值”;而在案例2中,患者在PFS和PPS阶段均具有“存活价值”。可见,在只考虑背景治疗成本的条件下,患者的“存活价值”=阈值×QALY-背景治疗成本。在恶性肿瘤治疗中,可将患者的“存活价值”进一步分为PFS阶段“存活价值”和PPS阶段“存活价值”。结合案例1和案例2可以发现,若仅考虑背景治疗成本,当患者在PFS和PPS阶段的“存活价值”均小于0时,则肯定会出现“免费仍不经济”的极端现象;当PFS和PPS阶段的“存活价值”一个大于0而另一个小于0时,则有可能会出现“免费仍不经济”的极端现象;当PFS和PPS阶段的“存活价值”均不小于0但接近于0时,则需要联合使用的新药价格很低才可能使整个联用方案具有经济性。
1.2 “肾透析成本”引发的争论
案例3:英国国家卫生与临床优化研究所(NICE)决策支持小组(DSU)曾报道过有关西那卡塞治疗终末期肾病(ESRD)致继发性甲状旁腺机能亢进(SHPT)的经济性评价结果[5]。肾透析是目前ESRD患者最为主要的治疗方案,但其价格非常昂贵。在英国,每位ESRD患者的年均透析成本为15 643英镑。根据NICE的评价结果,患者1年能获得的最大QALY为0.675 3,仅透析这项背景治疗措施的ICER已经达到了23 165英磅/QALY。若1个QALY的意愿支付阈值为20 000英磅,除非治疗药物能大幅提高患者的生命质量或降低患者的其他相关背景治疗费用,否则以透析为基础的治疗方案联用任何治疗药物均不具有经济性。由此NICE得出结论,由于透析所带来的高昂的背景治疗费用,即使西那卡塞降价为0,该治疗方案仍然不具有经济性。
案例4:与案例3类似,根据是否需要采取透析治疗,肾性贫血患者可被分为透析亚组和非透析亚组。本案例为针对透析亚组患者的研究,其从医疗卫生系统角度出发,通过文献和我国真实世界数据收集相关参数,构建包括透析、肾移植、心血管事件和死亡的多状态Markov模型,比较肾性贫血治疗药物E与原有治疗药物F的经济性。结果,E药方案在延长患者生命、提高患者生命质量的同时,也增加了患者的医疗成本支出,最终ICER值为223 197元/QALY,高于2020年我国3倍人均GDP的阈值,E药方案相对于F药方案不具有经济性,结果见表5。但在该案例中,若不考虑患者透析治疗这一背景治疗成本,则ICER值可降至164 992元/QALY,低于上述阈值,则E药方案相对于F药方案更具经济性。
无论是案例3还是案例4,透析治疗这一背景治疗措施均对经济学评价结果产生了决定性的影响。作为延长患者生命的必要治疗手段,而非针对SHPT或是肾性贫血的治疗方案,在药物经济学评价中,是否需要将透析治疗的背景成本纳入到分析中去,曾一度引起很多学者的争论。Grima等[6]在2012年发表的一篇研究中表示,相关药物经济学评价指南推荐在成本计算中纳入“干预措施相关成本”,但是对于什么是“相关成本”的定义较为模糊,以往很多研究中并没有将透析相关成本纳入研究,而该成本会对结果产生巨大影响。如果在分析中纳入透析治疗的背景成本,则将带来一个公平性问题:对于非透析患者经济的、可以纳入报销的医疗干预项目在透析患者中是不经济的,可能导致相关项目不被纳入报销范围。因此该研究者认为:①药物经济学评价指南中暗含透析治疗的背景成本是“不相关成本”,不应纳入计算;②透析相关的高成本为证明此类疗法的经济性设置了不合理且无法逾越的障碍,尤其是在已经决定了透析是否应被纳入报销的前提下,可以不再考虑透析成本;③现有临床和报销实践包括了接受透析的慢性肾病亚组患者,因此根据当前的药物经济学评价指南,不纳入透析成本在方法学上是合理的,也符合目前的临床和报销实践。van Baal等[7]在2013年发文回应了上述学者的观点,他认为建议不纳入“不相关成本”的推理会导致十分荒唐的结果,与经济学评价的潜在目标之间也会形成激烈的冲突。尽管很多指南都建议不纳入“不相关成本”,但是不论从医疗系统角度还是从全社会角度出发,纳入“不相关成本”都是与决策目标相一致的。如果为了得到一个经济的结果而不纳入真实发生的背景治疗成本的做法是非常危险的,会损害经济学评价证据的可靠性和价值。如果这样做是对的,则被忽略的一些健康产出可能也是对的。因此,研究者需要做的是去完善指南,并应当明确指出药物经济学评价中需要包含的所有成本,不论该项成本是相关的还是不相关的,是直接的还是间接的,这样才能与经济学评价的理论背景和目标一致。针对“透析成本”的争论,DSU的专家同样认为,所有成本都应被纳入ICER的计算框架,因为这些成本都在国家卫生机构的决策范围之内。
2 3种不同情境的解读
由上述4个药物经济学评价的案例可以发现,一个药物治疗某疾病是否具有经济性,除了与该药物自身成本有关外,还与很多因素有关。在有些情境下,这些因素会导致该药物即使免费也不具有经济性。
为了更加清晰地分析本文讨论的问题,本文定义一个新的概念——净价值(net value,NV),即在药物经济学评价中,将某个药物的价格设定为0时,包含该药物的干预方案与对照方案相比的净效益,可以由增量健康产出(ΔQALY)的价值与增量成本(ΔCbackground)的差值计算得到。假设1个QALY的阈值为λ,则有:
NV=λ×ΔQALY-ΔCbackground
例如,某药物的价格为0,该药物干预方案相对于对照方案的增量效果为1个QALY,增量成本为30 000元,而QALY的阈值为100 000元,那么NV就等于70 000万元。NV反映了患者愿意为该药物支付的最大成本,相当于经济学中保留价格(reserve price)的概念,所以净效益(net benifit,NB)=NV-Cnewdrug。NV越大,该药物所在干预方案具有经济性(NB>0)的时候,该药物可以有更高的售价;反之,药物的售价越低。当NV小于0时,就会出现“免费仍不经济”的极端情况。
2.1 情境一:新药仅可使患者在背景治疗下的生存时间延长
假设某疾病患者在存活期间均需要维持性地接受某背景治疗(如ESRD患者的透析),在此治疗基础上接受某新药治疗可以延长其生存时间。若该新药的成本为Cdrug,患者生存质量维持不变且健康效用值为u,使用该药物后延长的存活时间为ΔLY,同时每年的背景治疗成本为CBSC。令QALY的阈值为λ,则该新药治疗方案具有经济性的条件为:
ICER=[ΔC
ΔQALY] =[CBSC×ΔLY+Cdrug
u×ΔLY] <λ,即Cdrug<(λ×u-CBSC)×ΔLY
将(λ×u-CBSC)×ΔLY定义为该疾病背景治疗下的NV,当NV<0(即λ×u
2.2 情境二:新药联合治疗可使患者在疾病早期状态和/或晚期状态下生存时间延长
假設某疾病在早期疾病状态(如肿瘤的PFS阶段)需要使用M药物进行维持治疗,进展到疾病晚期状态(如肿瘤的PPS阶段)则需要换用N药物维持治疗。如果在早期疾病阶段联用新药O进行强化维持治疗,可以延长患者在早期和/或晚期疾病状态的存活时间。在M+O药联用方案与M药单用方案比较的经济学评价中,假设新药O的总成本为Cdrug,药物M和N的年治疗成本分别为CM和CN;M药单用方案可以让患者在早期状态存活LB年,M+O联用方案可以让患者在早期状态生存时间延长ΔLE年,同时使晚期状态下的生存时间延长ΔLA年;新药O的联用假设不改变患者生存质量,早期状态和晚期状态的效用值分别为uE和uA。令QALY的阈值为λ,则M+O药联用方案具有经济性的条件为:
ICER=[ΔC
ΔQALY] =[Cdrug+CM×ΔLE+CN×ΔLA
uE×ΔLE+uA×ΔLA] <λ,即Cdrug<(λ×uE-CM)×ΔLE+(λ×uA-CN)×ΔLA
其中,(λ×uE-CM)×ΔLE可以定义为早期疾病状态的净价值(NVE),(λ×uA-CN)×ΔLA可以定义为晚期疾病状态的净价值(NVA),两部分加到一起构成了整个治疗方案的NV。此时,导致NV很小甚至为负值的原因可能有5个:①患者早期状态生存质量低,健康效用值很小;②患者早期状态治疗成本很高;③患者晚期状态生存质量低,健康效用值很小;④患者晚期状态治疗成本很高;⑤ICER的阈值过低。该情境可理解为情境一的特殊情况。
2.3 情境三:患者存活时间延长导致其发生高成本疾病事件
假设某创新药物延长了患者的存活时间,而在这一段延长的存活时间中,患者发生了对照组没有发生的疾病事件。假设某个新药P与老药Q都是用于治疗某疾病的有效药物,新药P相对于老药Q可以让患者存活时间延长ΔL年,若患者在延长生存期间将发生R事件(为简化计算公式,本文暂不考虑R事件的发生概率)。假设新药P和老药Q的治疗成本都是固定的,分别为Cdrug和CQ;R事件发生时将产生医疗成本CR;患者延长生存期间健康效用值为u,发生R事件将导致健康损失ΔQALYR(u×ΔL>ΔQALYR)。令QALY的阈值为λ,则新药P治疗方案具有经济性的条件为:
ICER=[ΔC
ΔQALY] =[Cdrug+CR-CQ
u×ΔL-ΔQALYR] <λ,即Cdrug<λ×(u×ΔL-ΔQALYR)+CQ-CR
其中,λ×(u×ΔL-ΔQALYR)+CQ-CR可以定义为新药P治疗的净价值(NVP)。此时,导致净价值很小甚至为负值的原因可能有6个:①患者生存质量低,健康效用值很小;②新药P相对于老药Q能延长的生存时间很短;③老药Q的成本很低;④R事件发生时的治疗成本很高;⑤R事件发生时导致患者的健康损失很大;⑥QALY阈值过低。相比于前两种情境,在本情境中,原因④导致的“免费仍不经济”的情况较为特殊,一般而言在延长的生命周期内,患者发生高成本的事件R具有一定的概率,即出现“免费仍不经济”这一现象也存在一定的概率。
3 讨论
药物经济学中所说的经济性是干预方案的经济性,而非单一药物的经济性。综合上述具体案例和相关情境假设可以发现,某干预方案的经济性不仅仅受到主要治疗药物价格的影响,同时也受到背景治疗成本、联合用药成本、患者生存质量等多个因素的影响。因此,干预方案的定义不仅需要考虑所含药物是什么,还需要考虑剂量、规格、用法用量、联合用药、伴随检查、后线治疗等所有相关内容。
根据本研究中对于NV的定义,过高的背景治疗成本可能导致药物“免费仍不经济”的评价困境,因此也出现了将“不相关”治疗成本剔除分析的讨论。但从经济学评价本身的理论背景与研究目标来看,不能在ICER计算框架内剔除任何用药成本、疾病进展后用药成本、背景治疗成本等与目标干预措施或目标疾病“相关”或“不相关”成本,这其中的任何一部分成本都是医保决策部门需要决策的“相关”部分。
在组成成本无法“被剔除”的情况下,决策者仍然需要去考虑如何解决“免费仍不经济”的极端问题。根据前述分析,一个药品是否具有正的NB除了药品本身的价格外,还受到NV大小的影响,因此面对“免费仍不经济”或药品价格极低(超出合理范围)情况下方案才经济的现象,决策者除了需要考虑药品本身是否具有临床价值(如疗效、安全性等)外,还需要进一步考虑上述现象是否是由背景治疗成本过高、患者生存质量偏低等原因所导致。
(1)若该药品不具有经济性是由于背景治疗成本过高导致,则决策者需要对背景治疗成本作进一步剖析,以判断背景治疗中是否存在定价过高的治疗措施,特别是在原有药物基础上的强化治疗方案。此外,原有治疗药物本身是否具有经济性也是决策者需要特别注意的问题。很多时候,当决策部门遇到了能够满足目前尚未解决的临床问题需求的首个创新药物时,在医保准入过程中可能会给予较为宽松的待遇(如适当提高ICER阈值等),但这可能会给后续上市药物的经济性评价带来影响。若后续上市新药与原有治疗药物是相互替代关系,则两者进行比较时,也可以在较高价格时保证治疗的经济性;若新药与原有治疗药物为联合使用关系,则可能出现新药“免费仍不经济”的情况。因此,当后续药物上市时,应同时对首个上市药物价格的合理性进行重新考量。
(2)若背景治疗成本在正常范围内,出现极端现象的主要原因在于患者疾病治疗过程中的生命质量(健康效用值)过低,那么在此基础上又可以进一步分为两种情况:若新上市药品延长了患者的存活时间,但因为药品自身原因导致了患者生命质量降低,则需要进一步评估该药品的临床价值,即仅考虑使用该药品对患者存活时间的延长而忽略药品对生命质量的影响,会导致对药品临床价值的高估;若患者生命质量过低主要是因为疾病本身所导致,而新上市药品主要是延长患者的生存时间而未对其生命质量产生较大影响,则建议决策者参考终末期疾病治疗、孤儿药评估等,跳出经济性的范畴,从伦理、公平性等更广的范围进行评估,从而判断是否需要提高QALY的阈值。
综上所述,药物经济学归根结底都是在衡量若干治疗方案健康产出与成本投入之间的“性价比”问题,若超出了这一范畴,药物经济学便无法解决。例如,本文案例1中只要患者存活便是一个“不经济的方案”的伦理问题、案例4中非透析患者经济而透析患者不经济的公平性问题都已不再是简单的经济学问题,可能需要跳出传统经济学分析的框架从伦理和公平性角度进行更加广阔、深入的讨论。
参考文献
[ 1 ] 人力资源社会保障部.人力资源社会保障部关于《2016年国家基本医疗保险、工伤保险和生育保险药品目录调整工作方案(征求意见稿)》公开征求意见的通知[EB/OL].(2016-09-29)[2020-09-22]. http://hrss.ah.gov.cn/pub-
lic/6595721/8442559.html.
[ 2 ] 国家医保局.关于公布《2019年国家医保药品目录调整工作方案》的公告[EB/OL].(2019-04-17)[2020-09-22]. http://www.gov.cn/xinwen/2019-04/19/content_5384349.htm
[ 3 ] Decision Support Unit. Assessing technologies that are not cost-effective at a zero price[R].London:NICE,2014.
[ 4 ] 刘国恩.中国药物经济学评价指南2020:中英双语版[M].
北京:中国市场出版社,2020:46-47.
[ 5 ] GARSIDE R,PITT M,ANDERSON R,et al. The effectiveness and cost-effectiveness of cinacalcet for secondary hyperparathyroidism in end-stage renal disease patients on dialysis:a systematic review and economic evaluation[J]. Health Technol Assess,2007,11(18):1-167.
[ 6 ] GRIMA D T,BERNARD L M,DUNN E S,et al. Cost-effectiveness analysis of therapies for chronic kidney di- sease patients on dialysis:a case for excluding dialysis costs[J]. Pharmacoeconomics,2012,30(11):981-989.
[ 7 ] VAN BAAL P,MELTZER D,BROUWER W. Pharmacoeconomic guidelines should prescribe inclusion of indirect medical costs:a response to Grima et Al[J]. Pharmacoeconomics,2013,31(5):369-373,375-376.
(收稿日期:2021-06-10 修回日期:2021-08-19)
(編辑:孙 冰)
