2种植物体内NO3-含量检测方法的比较*
2021-09-28张立涛张家豪刘祎良徐国豪
刘 飞 张立涛 申 彤 张家豪 刘祎良 徐国豪 徐 娜
(济宁医学院生物科学学院 山东日照 276826)
实验教学是植物生理学教学工作中必不可少的一部分。将实验与教学有机结合,有助于学生充分理解理论知识,提高学习效率,积极运用基础知识,达到学以致用的教学效果[1-2]。随着科学技术的快速发展,用于科研工作的仪器也日益先进且自动化,将学科和科技前沿引入到实验教学中,可提高学生把握科技脉络的能力,不断创新,与时俱进[3]。
氮素是生命体内蛋白质、核酸、磷脂等多种有机体的重要组成成分,参与生命体内物质与能量的代谢过程,被誉为“生命的元素”[4]。氮素是植物体生长发育所必须的大量元素,植物缺氮会造成植株矮小,叶片发黄,最终会影响作物的产量[5]。
土壤中存在NO3-、NO2-、NH4+、含氮有机物等多种形式的氮素,而多数陆生植物,例如,小麦、玉米等都是以吸收NO3-作为主要的氮源,因此,植物吸收利用NO3-的能力对植物的生长发育具有重要的作用[6]。植物体内NO3-的积累量(NO3-含量)是衡量植物对NO3-吸收利用能力的一个关键的指标,因此,需要一种快速有效地测定植物体内NO3-含量的方法。目前,植物体内NO3-含量的测定方法主要有2 种,分别为水杨酸浓硫酸比色法[7]和硫酸肼还原并流动分析仪法。为比较2 种NO3-含量测定方法的优、缺点,笔者以10 mmol/L NO3-处理不同时间的拟南芥幼苗为样品,采用2 种方法对样品内的NO3-含量进行测定,发现流动分析仪法具有省时、省力、安全系数高、测定样品量大、数据稳定性好、易于操作等优势。
1 材料与方法
1.1 实验材料准备 将野生型拟南芥在琥珀酸铵培养基上培养生长7 d,用10 mmol/L KNO3分别处理0 h、0.5 h、1 h、2 h、4 h,每个处理设置3 个生物学重复,取全苗作为实验样品,共15个样品。
1.2 NO3-提取 取所需测定的拟南芥全苗材料(约20 株,不超过0.1 g)于1.5 mL 离心管中,称重,液氮冷冻研磨,加入1 mL ddH2O,100℃煮沸30 min,13 000 r/min 离心10 min,取上清液作为所需测定的样品。
1.3 实验方法
1.3.1 水杨酸-浓硫酸比色法 2017年Zhao 和Wang[7]发表的文章中详细介绍了硝态氮含量测定方法。该方法以氮浓度为横坐标,光密度为纵坐标,绘制标准曲线并计算出回归方程为C(μg/mL)=140.86×OD410-1.1831。利用标准曲线所得的回归方程计算出NO3--N 浓度,再用以下公式计算样品中的NO3--N 含量。NO3--N 含量=C*V/W,式中:C 为回归方程计算的NO3--N 浓度,V 为提取样品液总量,W 为样品鲜重。
1.3.2 硫酸肼还原并流动分析仪法
1)配制溶液。KNO3标准溶液、0.1%硫酸铜储备液、1%硫酸锌储备液。
显色剂:称取2 g 磺胺溶于120 mL ddH2O 中,加入0.1 g NEDD(N-甲萘基盐酸二氨基乙烯)混合均匀,然后加入20 mL 磷酸,定容至200 mL,储存于棕色瓶中。
氢氧化钠溶液:称取10 g 氢氧化钠溶于600 mL ddH2O 中,小心地加入3 mL 磷酸并混合均匀,定容至1 L 并加入1.36 mL 22%的Brij-35 溶液。
硫酸肼溶液:称取0.4 g 硫酸联胺溶于120 mL ddH2O 中,加入2 mL 硫酸铜储备液和2 mL 硫酸锌储备液,定容至200 mL。
2)流动分析仪检测样品NO3-含量。标准曲线测定样品准备。分别吸取4 mL KNO3标准溶液至样品管中,用于使用流动分析仪(AA3)制作标准曲线。
样品测定准备。吸取0.8 mL 样品液至样品管中,然后加入3.2 mL ddH2O,混匀。
流动分析仪上机测定。将上述样品管置于样品架上,将吸管插入相应的试剂中,按照流动法分析仪的操作步骤操作,检测样品中NO3-的含量。
2 实验分析与讨论
2.1 实验操作分析 实验效率是衡量实验方法的一个关键指标,在有多种选择的条件下,应选择耗时少、效率高的实验方法。本实验对2 种NO3-提取的方法——水杨酸浓硫酸比色法和硫酸肼还原并流动分析仪法进行了比较。从实验操作步骤上比较,水杨酸浓硫酸比色法需要配制试剂、测定并绘制标准曲线、样品液与试剂反应、比色等步骤,实验操作繁琐,耗时长;而硫酸肼还原并流动分析仪法只需准备试剂,然后上机检测,整个过程包括标准曲线和样品的测定均实现了全自动化,操作步骤简易,极大提高了实验效率。2.2 样品测定量分析 样品测定量是影响实验效率的一个重要因素。从测定样品的数量上比较,水杨酸浓硫酸比色法需要研究者自己操作,并且为了减小操作误差,一般每个样品会做3 个技术重复,这就使得该法一次能检测的样品数量受限,因此,该法适用于样品量少的情况。硫酸肼还原并流动分析仪法采用机器取样、反应、比色自动化的检测形式,缩短了样品检测的时间,并且实现了样品检测的连续性,使得该法测定样品的数量极大增加,提高了实验效率,因此,该法适用于大批量样品检测的情况。
2.3 安全性分析 实验室安全一直是研究者关注的焦点。由于实验需求,实验过程中可能会使用一些有毒或强酸、强碱等危险试剂,这就要求研究者在实验操作中做好防护,注意自身安全。此外,若实验目的相同,但存在多种实验方法时,在实验结果不受影响的条件下,一般选择安全系数高的实验方法。由于水杨酸浓硫酸比色法需要使用大量的浓硫酸,该方法存在较大的安全隐患,在有条件的情况下,尽可能选择硫酸肼还原并流动分析仪法。
2.4 数据稳定性分析
2.4.1 实验结果 将15 个样品磨碎、煮沸后制备NO3-提取液。然后利用水杨酸法浓硫酸比色法对样品中的NO3-含量进行检测,每个样品设置3 个技术重复。利用分光光度计得到每个样品的OD410值,根据1.3.1 中的公式,可计算出每个样品中的NO3--N浓度C(μg/mL),并得出最终的NO3--N 含量(μg/g),结果如表1 所示。
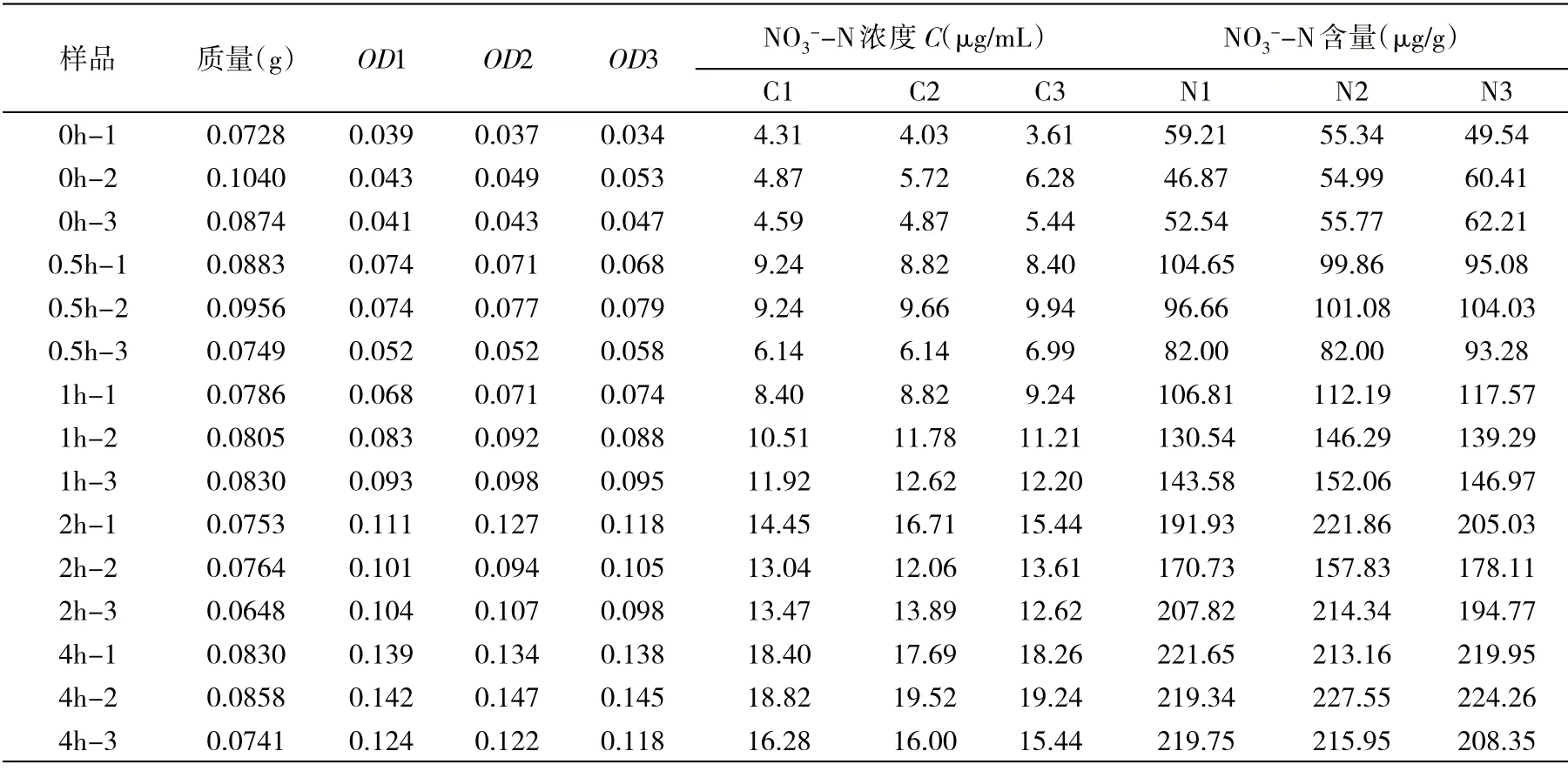
表1 水杨酸法浓硫酸比色法结果
吸取每个样品的NO3-提取液0.8 mL 至3.2 mL ddH2O 中,将提取液稀释5 倍,按照流动分析仪操作步骤操作,每个样品设置重复吸取3次,即为3个技术重复。由于流动分析仪可自动获得标准曲线,其所输出的结果为所测溶液的NO3--N 浓度C(μg/mL),则利用1.3.1 中的公式可计算出样品的NO3--N 含量(μg/g),所得结果如表2 所示。

表2 硫酸肼还原并流动分析仪法结果
2.4.2 数据稳定性分析 计算不同方法测定的每个样品的3 个技术重复的标准偏差(图1、表3),结果显示硫酸肼还原并连续流动分析仪法的标准偏差显著小于水杨酸浓硫酸比色法。流动分析仪法是系统自动化操作,误差率较低,而水杨酸浓硫酸比色法需要人工操作,实验过程中存在待测液吸取误差、试剂吸取误差、反应时间控制误差等一系列不可控的人工操作误差,使其误差率偏大,表明连续流动分析仪法的技术重复性好,数据稳定性高,保障结果更加精准。

图1 2 种NO3-测定方法的数据稳定性分析

表3 2 种NO3-测定方法的数据稳定性分析(单位:μg/g)
3 结语
随着科学技术的快速发展,越来越多的高精尖仪器用于科研工作中,极大提高了实验效率,降低了实验过程中的危险性,并且能保障实验结果的精确性和稳定性。由上述2 种植物体内NO3-含量测定方法的比较可知,相对于传统的水杨酸浓硫酸比色法,硫酸肼还原并流动分析仪法具有省时、高效、安全性高、稳定性好等优势,是目前NO3-含量检测的理想方法。
