“氨基酸组成蛋白质”动态学具的制作与使用
2021-09-28郑彬琼莆田市秀屿区教师进修学校福建莆田351146
郑彬琼 (莆田市秀屿区教师进修学校 福建莆田 351146)
《普通高中生物学课程标准(2017年版2020年修订)》(以下简称“课程标准”)倡导通过归纳与概括、模型与建模等方法阐释分子与细胞等相关概念的内涵,建议设置恰当的探究性学习活动达成科学思维等生物学学科核心素养[1]。“蛋白质是生命活动的主要承担者”是2019年6月第1 版普通高中生物学(人教版)第2 章第4 节的教学内容,在实际教学过程中,由于高一学生缺乏有机化学知识基础,因此,缺乏氨基酸三维空间结构想象力,对氨基酸空间结构的理解只停留在教材中的平面结构模式,甚至不少学生上完本节课后依然认为H2N-CH2-COOH 和HOOC-CH2-NH2是不同的氨基酸,经过访谈得知学生误以为必须与教材中的一样,氨基酸的氨基必须在左侧、羧基在右侧。因此,探索制作可拼接的三维学具,并通过小组合作的方式,完成模拟“氨基酸组成蛋白质”的动态过程,以突破教学难点[2],让学生在“做中学、做中思、做中悟”,从平面转立体、以实践代替讲授、化抽象为形象培养科学思维,从分子水平构建结构与功能相适应的生命观念[3]。
1 探究氨基酸的结构特点
1.1 制作可拼接氨基酸立体模型 材料准备:直径1 cm 的泡泡球、打印纸、彩色卡纸、铁线、双面胶、牙签等。用画图工具或手工绘制组成氨基酸的4 种基团—H(蓝色)、—COOH(红色)、—NH2(绿色)、R 基(黑色),在泡泡球的中间用黑色水笔标记C,代表碳原子。打印并分别剪下4 种化学基团,用双面胶固定牙签代表化学键(图1),其中—COOH、—NH2、—CH2—SH 这3 种化学基团需要剪下与相应基团等比的卡片用双面胶固定,以便制作部分空心夹层形成可拼接的结构(图2)。1.2 教学应用 教学实践中学生常困惑于组成氨基酸的4 个基团是如何连接在同1 个碳原子上?如何理解组成氨基酸的基团中至少有1 个氨基和1 个羧基?学生4 人1 组,阅读教材第29 页的资料,运用—H、—COOH、—NH2和侧链基团组装具有三维空间结构的氨基酸(图3),通过旋转氨基酸三维模型,从不同角度观察其结构,完成氨基酸平面结构到立体结构的概念转变,更直观地理解氨基酸的结构特点。要求学生用蓝笔圈出表1 中每种氨基酸的相同结构,用红笔圈出每种氨基酸的特殊结构并用R 表示,总结并写出氨基酸的结构通式,小组成员间互相评价、修正。

图1 组成氨基酸的基团

图2 可拼接的氨基酸基团

图3 半胱氨酸立体模型
最后合作小组共同分析每种氨基酸中的氨基数和羧基数。分析表1 数据,学生发现有的氨基酸,例如,赖氨酸有2 个氨基和1 个羧基,天冬氨酸有2 个羧基和1 个氨基,通过比较分析,学生总结出每种氨基酸都至少有1 个氨基和1 个羧基。学生在独立思考的基础上,通过合作学习进一步理解氨基酸概念的内涵。
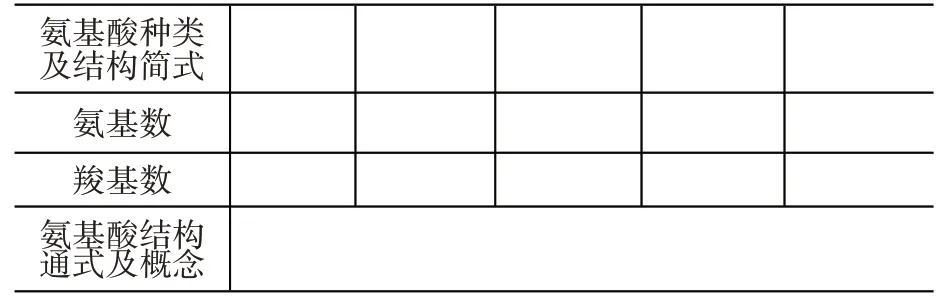
表1 氨基酸结构通式
以氨基酸三维学具模型制作创设探究性的学习情境,让学生亲自实践,运用独立思考与合作学习相结合的学习策略,基于学生的化学学科知识储备和认知规律,设计简单到复杂的学具制作任务,再让学生通过观察比较21 种氨基酸的模型总结出氨基酸的结构特点,建立氨基酸的抽象的空间结构模型概念,突破教学难点。在此学习过程中,培养学生的实践和合作交流能力。
2 探究氨基酸脱水缩合过程
2.1 二肽和多肽立体模型制作
1)选择2 个已制作好的氨基酸模型,拆卸其中一个氨基酸模型中—CO—OH 基团的—OH,再拆卸另一个氨基酸模型中—NH—H 基团的—H。
2)将氨基酸模型—CO—中代表化学键的长方形小纸片插入另一个氨基酸的—NH—基团中的空心夹层,结合形成—CO—NH—,2 个氨基酸模型通过肽键结合在一起形成二肽,同时脱去1 分子的水(图4)。

图4 氨基酸脱水缩合形成二肽示意图
3)按照步骤2 将剩余的氨基酸模型都经过脱水缩合成多肽链。
2.2 教学应用 学生对于氨基酸脱水缩合的过程很感兴趣,但很难理解2 个氨基酸分子在脱水缩合过程中如何脱去—OH 和—H、肽键的形成等问题。因此,根据教材中图2-10 氨基酸脱水缩合示意图,利用之前制作的可拼接的氨基酸模型,模拟氨基酸脱水缩合形成二肽的过程(图4),让学生指出模型中肽键的位置,并重复氨基酸脱水缩合的过程形成三肽、四肽、五肽。学生先计算二肽、三肽、四肽和五肽的形成过程中脱去的水分子数和肽键数,可总结得出氨基酸在脱水缩合形成多肽的过程中脱去的水分子数与肽键数的数量关系。
经过初中阶段的生物学课程学习,学生已知蛋白质在消化系统内最终分解成氨基酸被人体吸收,但对蛋白质的水解过程尚不清楚,因此,让学生将二肽(图4)脱去的—H 和—OH 重新组装到原来的氨基酸残基上,形成2 个氨基酸,模拟蛋白质的水解过程。
通过模型的制作、拆卸、组装及氨基酸脱水缩合形成多肽,学生不但获得直观性体验,更能将这种体验融入到自己的知识体系中,从而对氨基酸分子的空间结构及脱水缩合的过程理解更到位,培养其运用推演、计算的方法解决学习情境中的问题,以及动手操作能力和逆向思维。
3 探究蛋白质结构多样性的原因
3.1 人胰岛素立体模型制作
1)制作2个—COOH、2个—NH2和6个—CH2S—H基团,其中—CH2—SH 中的S—H 之间制作成可拼接的结构。
2)取21 个直径为1 cm 的泡泡球用铁丝连接成1 条链,并在每个泡泡球上贴上所代表氨基酸名称构建人胰岛素A 链框架。另取30 个泡泡球用铁丝连接成1 条链,同样贴上所代表的氨基酸名称构建人胰岛素B 链框架(图5)。

图5 人胰岛素A、B 链和3 种化学基团
3)取出A 链,将4 个—CH2—H 基团的铁丝插到4 个代表半胱氨酸的泡沫球上,将2 个—CH2—H 基团铁丝插到另外1 条多肽链中的2 个半胱氨酸的泡沫球上,最后分别将—COOH 和—N2H 基团的铁丝接入每条多肽链首、尾2 个的泡沫球里,完成组成人胰岛素A 链和B 链2 条多肽链的构建(图6)。

图6 人胰岛素A 链和B 链模型
3.2 教学应用 学生很难理解组成人胰岛素的A、B 2 条多肽链是通过哪些特殊结构结合在一起的?组成蛋白质2 条或多条肽链如何弯曲、折叠形成具有一定空间结构的蛋白质?针对这2 个问题,先让学生观察教材第30 页中的图2-11“某种胰岛素的二硫键示意图”,合作小组取出已制作完成的人胰岛素A 链和B 链,将A 链中A6 和A11的半胱氨酸中—CH2—S—H 各脱去1 个—H 形成二硫键,用同样的方法在A7 和B7、A20 和B19 的位置再形成2 个二硫键,通过这3 个二硫键人胰岛素的A 链和B 链结合在一起(图7);让学生将此模型进一步盘曲、折叠形成更复杂的三维结构(图8),并讨论分析除了形成二硫键以外,肽链可折叠为更复杂的三维结构的原因;最后,让学生分享模型构建过程并运用构建的模型解释为什么蛋白质结构具有多样性。

图7 人胰岛素二硫键示意图
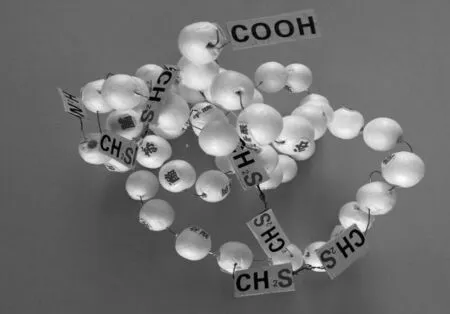
图8 人胰岛素三维结构模型
学生利用铁丝和泡沫实心球自主探究人胰岛素三维空间结构形成过程,使抽象的空间结构形象化。设计活动让学生运用氨基酸脱水缩合的概念合作完成人胰岛素A、B 2 条多肽链间3 个二硫键的形成,训练知识迁移能力,加深对肽键、氢键、二硫键等化学键的理解,跨越学科知识障碍,实现不同学科之间知识的融合,同时培养学生的动手能力和团队协作能力。
4 反思
“氨基酸组成蛋白质”动态学具在教学中的应用通过“氨基酸分子物理模型—氨基酸分子脱水缩合动态模型—胰岛素分子物理模型”的构建,让学生在实践与合作中运用直观模型辅助学习新知识,渗透数学的统计学思想,在此过程中还涉及归纳、概括、解释、推断、预测等能力的培养,训练学生运用系统性的科学思维解决问题,这些基本上属于科学思维中水平一至水平四的范畴。
这些教具的设计和应用是依据课程标准对科学思维4 个素养水平的阐述而展开的,但在课堂教学中,如何通过合理的时间安排和恰当的教学活动,引导学生从基础的归纳、演绎科学思维到建模的创造性高级科学思维,是值得一线教师继续研究的问题。
