地骨皮HPLC特征图谱建立及灰分检测
2021-09-26王丹丹赵林松聂依文吴佩颖
李 婷, 王丹丹, 赵林松, 高 崎, 聂依文, 吴佩颖,3*, 张 彤
(1.上海中医药大学教学实验中心,上海 201203;2.上海中医药大学中药学院,上海 201203;3.芸豆数字科技有限公司,四川 成都 610031;4.上海上药杏灵科技药业股份有限公司,上海 201703)
地骨皮为常用中药,功能凉血除蒸、清肺降火,用于阴虚潮热、骨蒸盗汗、内热消渴、肺热咳嗽、咯血等症[1]。2015年版《中国药典》收载的地骨皮为枸杞LyciumchinenseMill.和宁夏枸杞Lycium.barbarumL.的干燥根皮[1]。春初或秋后采挖根部,洗净,剥取根皮,晒干[1]。中药地骨皮来源于茄科枸杞属植物,本属植物约80种,主要分布在南美洲,少数种类分布于欧、亚大陆温带,《中国植物志》里记载我国产7种3变种[2-3],全国大部分地区均有分布,其中主产于华北和西北地区,并且只有枸杞为广布种。 华北地区是商品地骨皮的主产地,其中以山西省产量最大,主要是野生枸根皮作地骨皮用,主产于该省的平遥、阳曲、晋城等地[4]。根据实际调查和研究,现作药用的地骨皮主要来源于枸杞的根皮,同属的宁夏枸杞和北方枸杞Lyciumchinensevar. Potaninii 根皮仅在个别地区作地骨皮用[5]。
国内外在植物分类生药鉴定、化学成分、药理作用等方面对中药地骨皮已作了一定的工作。地骨皮中含有生物碱类、酰胺类、有机酸类、黄酮类等多种成分[6],其中酚类成分为地骨皮中主要成分,包括地骨皮甲素、地骨皮乙素、咖啡酰丁二胺等[7]。地骨皮甲素和地骨皮乙素属于精胺类生物碱,体外实验表明,地骨皮甲素和乙素可以阻断细胞的炎症活化,避免免疫反应紊乱等[8],另外,还可以拮抗细菌内毒素[9],同时,地骨皮甲素和地骨皮乙素还是降压的主要成分[10]。 地骨皮也是某些中成药的主要组成药味,如地骨降糖胶囊、十味降糖颗粒、养血退热丸等。除药用外,地骨皮还可用于辅助降血糖保健食品中。以地骨皮为主要原料制成的地骨皮露常用于体虚骨蒸、虚热口渴等证的治疗,具有凉营血、解肌热的功能[2]。2015年版《中国药典》中,地骨皮检验项除性状、显微、薄层、水分、总灰分、酸不溶性灰分外,并没有含量测定项。陈倩倩等[11]对47批地骨皮饮片进行质量分析,发现各厂家地骨皮质量差异较大,洁净度差和掺伪问题是不合格的主要原因。为了提高地骨皮药材质量,保障临床用药的安全有效,本实验在前人工作的基础上,对地骨皮类药材进行含量测定、特征指纹图谱、灰分等方面的系统研究,以期为地骨皮药材的质量评价与控制提供参考。
1 材料
1.1 药材 21批地骨皮购自成都诚实通贸易有限公司,均为野生资源,由上海中医药大学张彤教授鉴定为正品,具体信息见表1。

表1 样品信息
1.2 仪器与试剂 Agilent1260系列高效液相色谱仪(四元泵、DAD检测器),配置Chemstation色谱工作站(美国Agilent公司);BS124S型电子天平(万分之一, 北京赛多利斯科学仪器有限公司);XS105DU型电子天平(十万分之一,瑞士梅特勒-托利多公司);JP-100 型数控超声波清洗器(深圳市洁盟清洗设备有限公司); Thermo Sorvall ST16R 高速冷冻离心机(美国Thermo Fisher Scientific公司);HH-S2 四孔智控水浴锅(郑州长城科工贸有限公司);SXL-1008程控箱式电炉(上海精宏实验设备有限公司)。
地骨皮乙素对照品(批号120099-201903,纯度≥98%,安徽西青果生物科技有限公司)。乙腈(色谱纯,美国 Honeywell公司);其他试剂均为分析纯;水为超纯水。
2 地骨皮乙素含量测定
2.1 色谱条件 Dikmatech PlatisilODS色谱柱(4.6 mm×250 mm, 5 μm);流动相0.15%磷酸(A)-甲醇(B),梯度洗脱,程序见表2;体积流量1 mL/min;柱温30 ℃;检测波长280 nm;进样量5 μL。理论塔板数按地骨皮乙素峰计,应不低于10 000。

表2 梯度洗脱程序
2.2 对照品溶液制备 取地骨皮乙素适量,精密称定,20%甲醇和0.15%磷酸的混合溶液制成质量浓度为2.0 mg/mL的溶液,即得。
2.3 供试品溶液制备 将地骨皮粉碎,过4号筛,精密称取粉末约0.2 g,置于50 mL离心管中,加入流动相溶液7 mL,超声(350 W)处理30 min,离心(4 000×g)10 min,取上清液转移至25 mL量瓶中,重复提取2次,残渣用流动相溶液洗涤,合并提取液,用流动相溶液洗涤定容,经0.45 μm微孔滤膜滤过,即得[12]。
2.4 专属性实验 按“2.3”项下方法制备供试品、对照品溶液,在“2.1”项色谱条件下进样,结果见图1。
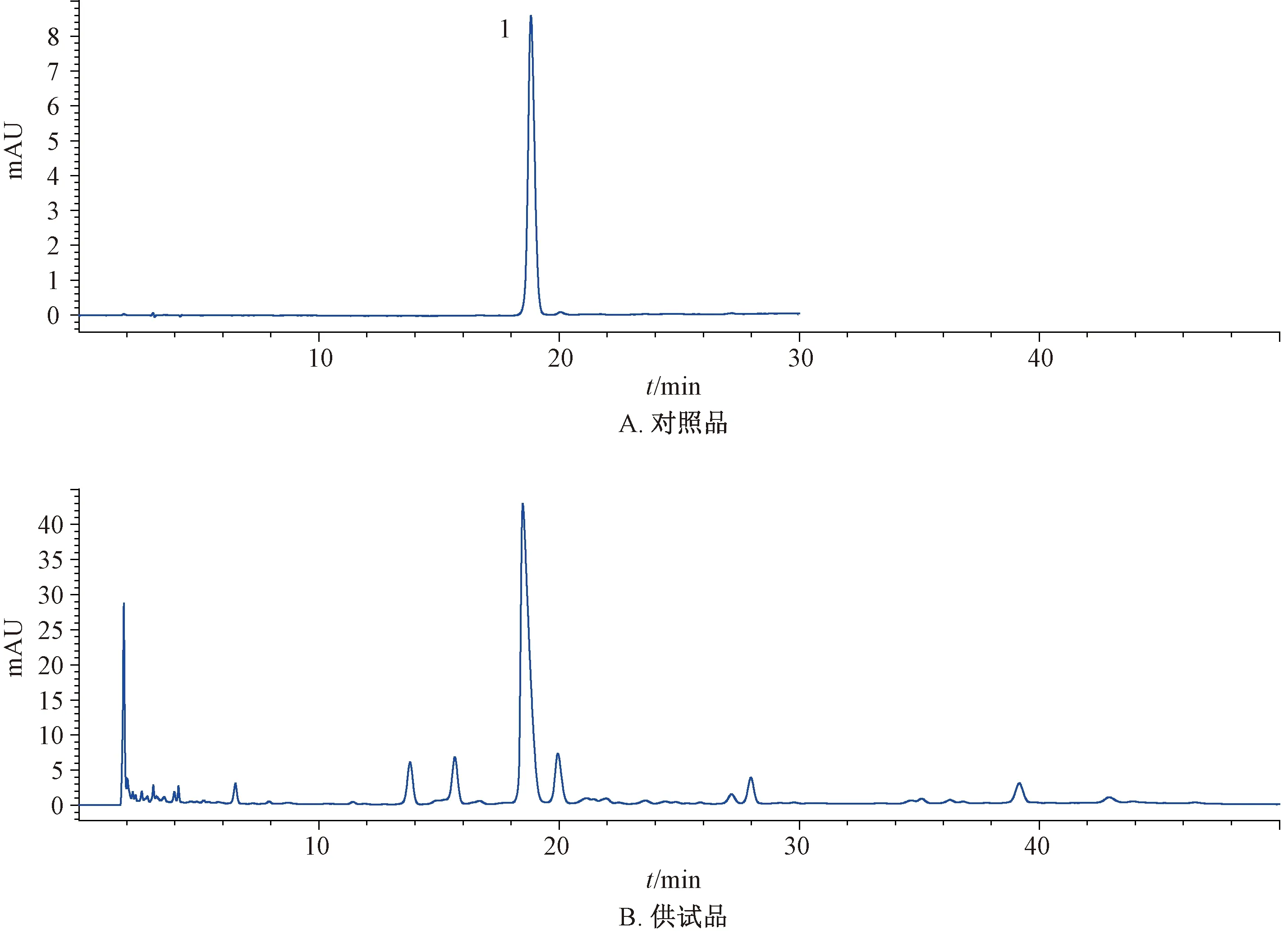
1.地骨皮乙素图1 地骨皮HPLC色谱图
2.5 方法学考察
2.5.1 线性关系考察 取地骨皮乙素母液,以20%甲醇和0.15%磷酸的混合溶液稀释,制备成质量浓度分别为40、80、160、240、480 μg/mL的对照品溶液,精密吸取5 μL,在“2.1”项色谱条件下进样,以地骨皮乙素质量浓度为横坐标(X),峰面积为纵坐标(Y)进行回归,得方程为Y=4.185 4X-1.267 3(r=0.999 97),在40.0~480 μg/mL范围内线性关系良好。
2.5.2 精密度试验 精密吸取上述低、中、高3个质量浓度对照品溶液各5 μL,在“2.1”项色谱条件下进样6次,测得地骨皮乙素峰面积 RSD 为0.27%、0.26%、0.40%,表明仪器精密度良好。
2.5.3 重复性试验 取同一批供试品(批号YC20190101)约0.2 g,精密称定,平行6份,按“2.3”项下方法制备供试品溶液,在“2.1”项色谱条件下进样,测得地骨皮乙素含量RSD为0.78%,表明该方法重复性良好。
2.5.4 稳定性试验 取同一批供试品(批号YC20190101)约0.2 g,精密称定,按“2.3”项下方法制备供试品溶液,于0、2、4、8、12 h在“2.1”项色谱条件下进样,测得地骨皮乙素峰面积RSD为1.69%,表明供试品溶液在室温下12 h内稳定性良好。
2.5.5 加样回收率试验 取9份含量已知的样品(批号YC20190101)约0.1 g,精密称定,分别按80%、100%、120%水平加入对照品溶液,各平行3份,按“2.3”项下方法制备供试品溶液,在“2.1”项色谱条件下进样。测得地骨皮乙素加样回收率95%~105%,平均加样回收率为100.8%,RSD为2.36%。
2.6 地骨皮含量测定 按“2.3”项下方法制备供试品溶液,在“2.1”项色谱条件下进样,结果见表3。由此表明,21批地骨皮中地骨皮乙素含量范围为0.13%~5.24%,建议在2020年版《中国药典》中增加地骨皮含量测定项,即按干燥品计算,本品含该成分不低于1.0%。

表3 地骨皮乙素含量测定结果
3 地骨皮指纹图谱建立
3.1 供试品溶液制备 取各批药材粉末(过4号筛)约0.2 g,精密称定,置50 mL离心管中,精密加入流动相溶液25 mL,超声(350 W)处理30 min,离心10 min(约4 000×g),经0.45 μm微孔滤膜过滤,即得[11]。
3.2 色谱条件 同“2.1”项。
3.3 方法学考察
3.3.1 精密度试验 精密吸取同一供试品溶液(批号YC20190101)5 μL,在“3.2”项色谱条件下进样6次,以共有峰的3号峰(地骨皮乙素)作为内标[13],测得共有峰相对保留时间、相对峰面积RSD分别为0.05%~0.45%、1.22%~2.30%,表明仪器精密度良好。
3.3.2 重复性试验 精密称取同一批样品(批号YC20190101)6份,按“3.1”项下方法制备供试品溶液,在“3.2”项色谱条件下进样,以共有峰的3号峰(地骨皮乙素)作为内标[13],测得共有峰相对保留时间、相对峰面积RSD分别为0.06%~0.32%、1.21%~2.81%,表明该方法重复性良好。
3.3.3 稳定性试验 取同一批供试品溶液(批号YC20190101),于0、2、4、8、12、24 h在“3.2”项色谱条件下进样,以共有峰的3号峰(地骨皮乙素)作为内标[13],测得共有峰相对保留时间、相对峰面积RSD分别为0.05%~1.36%、0.40%~ 2.70%,表明供试品溶液在24 h内稳定性良好。
3.4 图谱生成 取21批供试品溶液,按“3.1”项下方法制备供试品溶液,在“3.2”项色谱条件下进样,色谱图见图2。
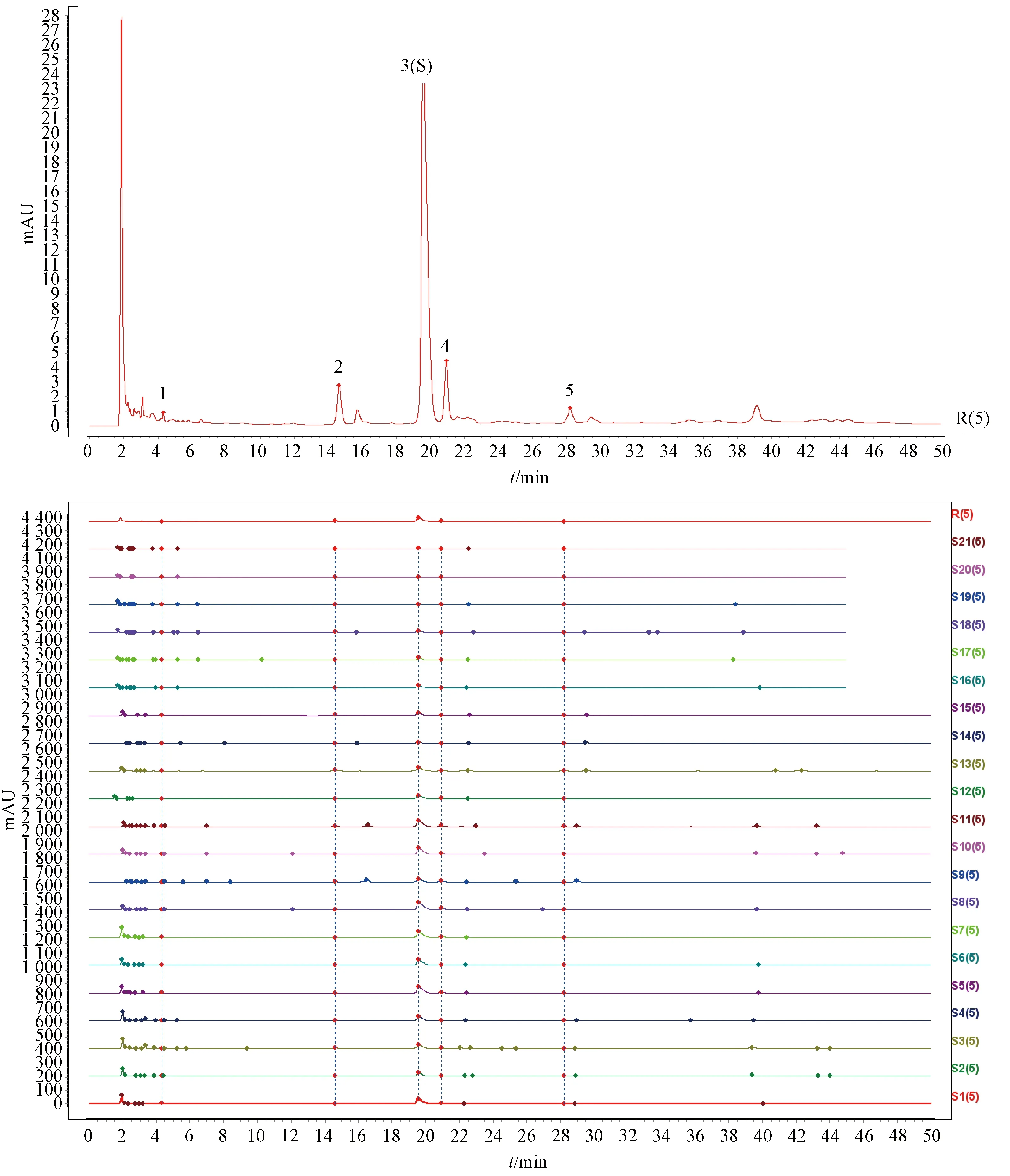
3.地骨皮乙素 4.地骨皮甲素图2 21批样品对照图谱及HPLC指纹图谱
3.5 相似度分析 将各批药材的HPLC色谱图导入“中药色谱指纹图谱相似度评价系统”(2.0版)[13],生成对照图谱(图2),标定了5个特征峰。利用中药指纹图谱相似度评价系统软件进行计算,结果各批样品相似度均大于0.97。张永等[14]在研究肉桂指纹图谱时发现,桂皮醛过高的峰面积使得不同年限肉桂药材的相似度没有明显差别,故本研究剔除最大峰地骨皮乙素重新计算,结果见表4。由此可知,除编号S18、S19相似度小于0.80外,其余各批相似度均大于0.8。

表4 剔除地骨皮乙素后21批样品相似度分析
3.6 聚类分析 聚类分析是以一定分析手段将关系相近的研究对象进行合理的分类的综合性手段之一[15]。将上述21批样品5个特有峰的峰面积导入SPSS 21.0软件,采用组间平均数连接法和夹角余弦对21批样品的5个特征峰进行系统聚类分析,结果见图3,可知结果与相似度分析一致。
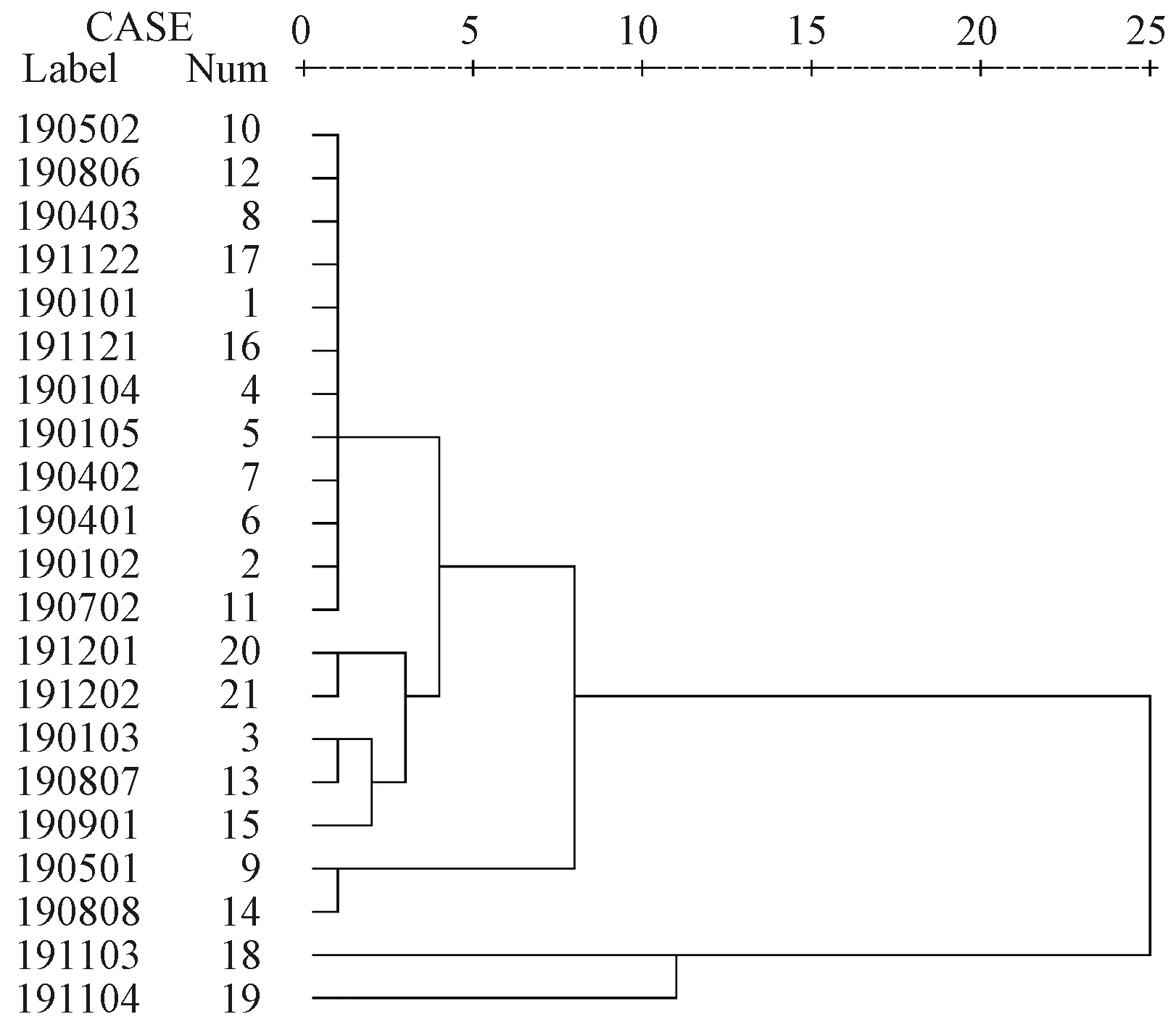
图3 21批地骨皮系统聚类分析图
4 地骨皮灰分检测
总灰分指药材经加热炽灼灰分遗留下的无机物,称定质量,判断是否符合限度规定,它是生理灰分与外来灰分之和[16]。组织中含草酸钙较多的药材,需要测定酸不溶性灰分,可以更准确地反映出外来杂质的量[16]。
灰分测定参照2015年版《中国药典》四部通则测定法进行,取21批药材粉末(过2号筛),每批约4.0 g,精密称定,置于恒定质量的空坩埚中,放入马弗炉中程序升温,灰化完全后取出,冷却后记录数据,复烘0.5 h,直至数据达到恒重的要求,结果见表5。
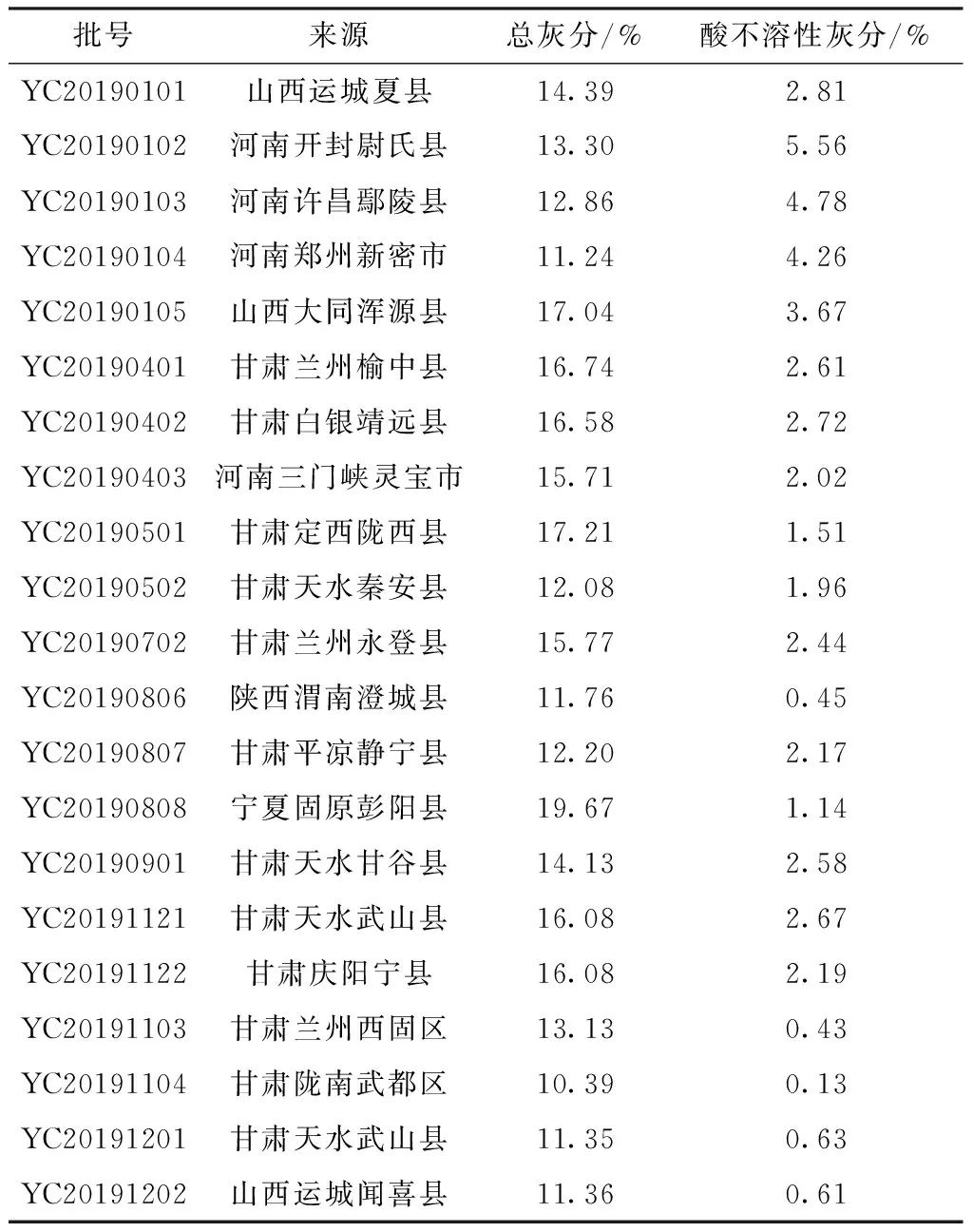
表5 21批样品灰分测定结果
2015年版《中国药典》一部地骨皮项下规定,灰分不得大于11%,酸不溶性灰分不得大于3%[1]。表5显示,20批样品灰分均大于11%,仅1批(YC20191104)合格,但是该批有效成分含量低(0.33%),可能是过度水洗导致。《香港中药材标准》第六册地骨皮项下[12]规定,总灰分不得多于19%,酸不溶性灰分不得多于4.5%;第17版《日本药典》地骨皮项下[17]规定,总灰分不得多于20.0%,酸不溶性灰分不得多于3.0%。地骨皮灰分与有效成分含量的关系,见图4,由S13~S21数据可知,当地骨皮中总灰分和酸不溶性灰分降低时,地骨皮乙素含量显著降低,故建议2020年版《中国药典》对地骨皮灰分限量进行调整,总灰分不超过19.0%,酸不溶性灰分不多于4.5%。
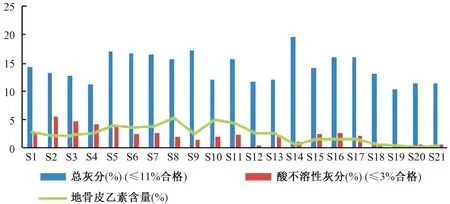
图4 地骨皮灰分与地骨皮乙素含量的关系
5 讨论与结论
本实验选用了甲醇-水、乙腈-水、甲醇-0.1%甲酸、甲醇-0.1%三氟乙酸、甲醇-0.1%磷酸作为流动相进行考察,最终确定“2.1”项下条件,色谱图上各色谱峰分离良好,保留时间适中,峰型对称。
由于2015版《中国药典》上对地骨皮灰分做了控制,但是并没有对其指标性成分进行说明。因为地骨皮外皮具有较厚的糠磷皮,其中有细密的组织小孔及不规则裂纹,很容易吸附灰尘,所以灰分不容易达标,但浸泡或多次洗涤又会显著降低其有效成分含量。本实验建立了地骨皮样品中地骨皮乙素含量测定方法,建议2020年版《中国药典》中增加地骨皮含量测定项,按干燥品计算,本品含地骨皮乙素(C28H42N4O6)不低于1.0%,并对其灰分限量进行调整,总灰分不超过19.0%,酸不溶性灰分不多于4.5%。
本实验建立了地骨皮药材的对照指纹图谱,确定了5个共有峰作为基本特征峰。在相似度分析时,应剔除对指纹图谱贡献率较大的地骨皮乙素峰,以利于指纹图谱的综合评价,根据聚类分析结果,将21批样品划分为2大类,具体分类形成原因有待进一步研究。
