软膏剂水分活度分布规律及在制药行业的应用指导
2021-09-22闵红高翔周志云贺聪莹安凤秋
闵红 高翔 周志云 贺聪莹 安凤秋

[摘要]目的调查目前市面上软膏剂的水分活度( aw )分布状况,为“水分活度测定在非无菌制剂中的应用指导原则”提供数据支撑。方法2019年8月在西安市各大药店采集43家生产企業34个品种共102批次软膏剂,并在25℃下对其 aw 进行检测。结果软膏剂的平均 aw 分布在0.0326~0.9804。去除离群值后,软膏剂平均 aw 的95%置信区间为0.7013~0.7661。结论对高 aw 软膏剂研发提出优化处方原则,提高自我防腐能力;对低 aw 软膏剂提出减少释放检验频次原则,合理微生物控制策略;软膏剂 aw 分布规律为《中国药典》“水分活度测定在非无菌制剂中的应用指导原则”提供坚实的数据支撑。
[关键词]软膏剂;水分活度( aw );微生物安全评价;应用指导原则
[中图分类号] R283.6 [文献标识码] A [文章编号]2095-0616(2021)23-0074-04
Distribution law of water activity of ointment and application guidance in pharmaceutical industry
MIN Hong1,2 GAO Xiang1 ZHOU Zhiyun1,2 HE Congying1,2 AN Fengqiu3
1.Shaanxi Institute for Food and Drug Control, Shaanxi, Xi'an 710065, China;2.Key Laboratory of Pharmaceutical Microbiological Detection Technology, National Medical Products Administration, Shaanxi, Xi'an 710065, China;3.School of Environmental and Chemical Engineering, Xi'an Polytechnic University, Shaanxi, Xi'an 710048, China
[Abstract] Objective To investigate the distribution of water activity (aw) of ointments in the market at present, and to provide data support for "Guiding Principles of Water Activity Determination in Non-sterile Preparations". Methods In August 2019, 102 batches of ointments of 34 varieties from 43 manufacturing enterprises were collected from major pharmacies in Xi'an, and their aw was tested at 25℃. Results The average aw distribution of ointment ranged from 0.0326 to 0.9804. After removing outliers, the 95% confidence interval of average aw of ointment was from 0.7013 to 0.7661. Conclusion The principle of optimizing prescription is put forward for the research and development of high aw ointment to improve self-preservation ability. For low aw ointment, the principle of reducing release test frequency and rational microbial control strategy were put forward. The distribution law of ointment aw provides solid data support for "Guiding Principles of Water Activity Determination in Non-sterile Preparations" in Chinese Pharmacopoeia.
[Key words] Ointment; Water activity (aw); Microbial safety evaluation; Application guidance principles
水分活度( aw )是相同温度下样品中水分的饱和蒸汽压和纯水饱和蒸汽压的比值[1-2]。aw 已经在食品和化妆品行业微生物安全评价方面取得了广泛研究与应用[3-5],但对于制药行业是一个相对崭新的概念。目前,美国药典<1112>章节已收载“非无菌制剂水分活度测定的应用研究”,其内容涵盖了水分活度的概念、水分活度与微生物的关系、代表性微生物生长所需最低 aw、水分活度在制药行业的应用、对代表性剂型药物推荐了微生物控制策略等方面内容[1],而《中国药典》2020年版在 aw 相关内容仍属空白。
本研究调查43家生产企业34个品种共102批次的上市软膏剂的 aw 分布规律。根据软膏剂 aw 分布规律,首先评估软膏剂的潜在污染菌和不可接受微生物,建立软膏剂微生物检测指标;其次,对软膏剂研发提出优化处方原则,提高自我防腐能力;对低 aw 软膏剂提出减少释放检验频次原则,使其微生物控制策略更加合理;对软膏剂包装密闭系统也提出更高要求,为《中国药典》“水分活度测定在非无菌制剂中的应用指导原则”提供坚实的数据支撑。
1材料与方法
1.1材料
仪器:Aqualab 型水分活度仪(美国 Decagon 公司)。试药:2019年8月在西安市各大药店随机采集43家生产企业34个品种共102批次软膏剂,具体药品信息见表1。
1.2水分活度测定方法
首先采用水分活度标准溶液0.25aw、0.50aw、0.76aw 和0.92aw 对仪器进行多点校准。取试样放在一次性塑料样品杯,将样品杯开口置于样品仓中,合上盖子并置于 Read 位置。测定温度为25℃,AquaLab循环读数直到三次连续读数之间小于0.0005aw 时,仪器达到平衡并准确读数。每个样品重复测定3次,取平均值。
2结果
2.1软膏剂aw 分布规律及置信区间
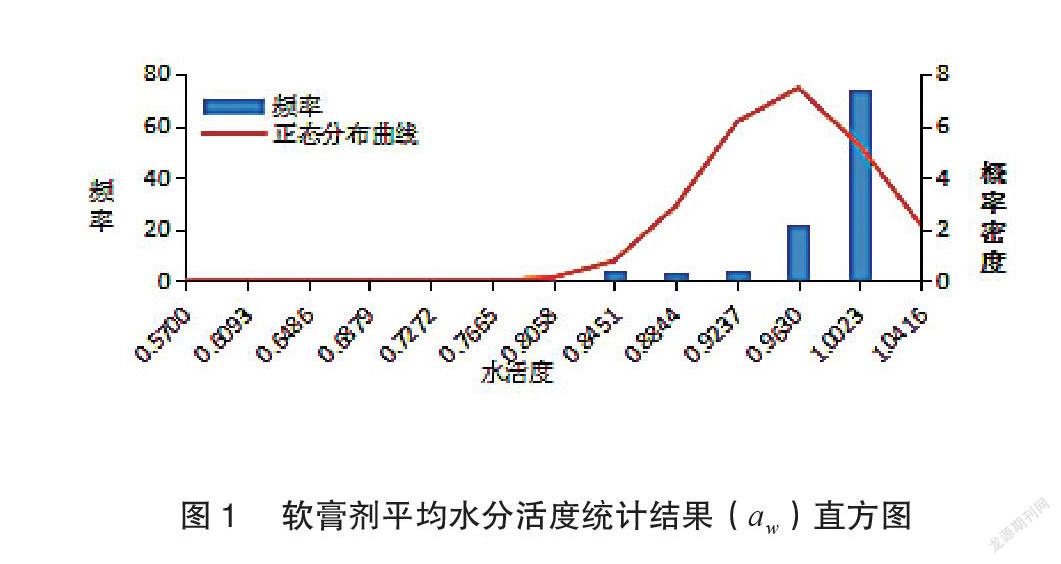
本研究对随机抽取的102批次上市软膏剂(43家生产企业、34个品种)的 aw 进行检测。见图1。软膏剂的平均 aw 分布于0.0326~0.9804,其95%置信区间为0.6179~0.7166,当去除10个离群值后,软膏剂平均 aw 的95%置信区间为0.7013~0.7661。其中,合肥立方制药股份有限公司生产的丹皮酚软膏 aw 值最大,湖北人福成田药业有限公司生产的莫匹罗星软膏 aw 值最小。aw 分布于<0.4000、0.4001~0.5000、0.5001~0.6000、0.6001~0.7000、0.7001~0.8000、0.8001~0.9000和0.9001~1.0000的药剂数分别占总量的9.80%、2.94%、14.71%、32.35%、6.86%、10.78%和22.55%。
2.2不同类型软膏剂aw 分布规律
根据软膏剂功效、主治及药剂类型,可将其分为五类:第Ⅰ类为抗生素类外用制剂,其 aw 分布于0.4850~0.9487;第Ⅱ类具有清热解毒,止痛生肌的作用,主治各种烧、烫、灼伤,其aw 分布于0.5410~0.8490;第Ⅲ类为主治各种皮炎、湿疹、皮癣的化药制剂,其 aw 分布于0.0428~0.9804;第Ⅳ类主治各种皮炎、湿疹、皮癣的中药制剂,其 aw 分布于0.6692~0.9773;第Ⅴ类具有凉血止血、消肿止痛作用,主治内痔、外痔、混合痔,其 aw 分布于0.5543~0.9745。
3讨论
3.1为“水分活度测定在非无菌制剂中的应用指导原则”提供数据支撑
《药品生产质量管理规范》(GMP)是国际公认的药品生产质量管理的准则,强调对药品微生物的源头控制和过程控制[6]。aw 检查是实现对药品微生物源头控制和过程控制的一种安全评价方法。美国药典(USP)<1112>章节中收载了“非无菌制剂水分活度测定的应用研究”,而我国自2018年加入国际人用药物注册技术协调会(ICH)后,要求药品标准进一步与国际接轨,因此亟须制定相应的指导原则,提高国际竞争力。
随机抽取102批软膏剂平均 aw (去除离群值)的95%置信区间为0.7013~0.7661,该值与美国药典(USP)提出的外用软膏剂 aw (0.55)存在一定差异,这可能与中、美在软膏剂生产过程所用原辅料及生产工艺不同相关,该 aw 值为《中国药典》中收载“水分活度测定在非无菌制剂中的应用指导原则”提供了坚实的数据支撑。
3.2建立软膏剂微生物检测指标,降低微生物污染风险
微生物生长与 aw 密切相关,不同类型微生物有所需的最低 aw 要求,当药品 aw 低于该临界值,该类型微生物将无法生长。研究表明,铜绿假单胞菌、大肠埃希菌(G-)的最低 aw 分别为0.97和0.95;金黄色葡萄球菌(G+)最低 aw 为0.86;蜡样芽孢杆菌和枯草芽孢杆菌最低 aw 分别为0.95和0.80;白色念珠菌和黑曲霉 aw 分别为0.87和0.77;甚至最耐高渗酵母和耐旱真菌在 aw <0.60时也不会增殖[1,7]。
软膏剂指原料药物与油脂性或水溶性基质混合制成均匀的半固体外用制剂[8]。本研究结果表明软膏剂 aw 分布于0.0326~0.9804。 aw 分布于0.86~0.98的软膏剂,建议控制需氧菌总数、霉菌和酵母菌总数、金黄色葡萄球菌和铜绿假单胞菌;分布于0.80~0.85的软膏剂,建议控制需氧菌总数、霉菌和酵母菌总数;分布于0.60~0.79的软膏剂,建议仅控制霉菌和酵母菌总数[1,9]。需要注意的是,该 aw 虽不适合微生物生长,但不代表该药品无存活微生物[10-11]。aw 检查仅可作为非无菌制剂微生物控制体系的有力补充,不可取代微生物限度检查。
3.3为软膏剂提供合理微生物控制策略
我国软膏剂的aw 值分布较为广泛,对aw <0.60的软膏剂,由于其不支持微生物生长或孢子萌发,可以通过风险评估后减少微生物限度检查频次,实施跳批次檢查,甚至可取消微生物常规检查,建立符合产品特征的日常微生物控制策略。风险评估需首先审查药品开发、生产、过程验证和常规检查(至少20批次)微生物历史监测数据;其次,证明原材料、制药用水、生产过程、制剂和包装体系的微生物控制策略具有效性[1,12]。
3.4优化软膏剂处方,提高药品自我防腐能力
我国软膏剂 aw 分布范围较为广泛,并且相同类型软膏剂的 aw 也未呈现出规律性,这可能与企业在制剂中添加不同辅料相关,添加白凡士林、黄凡士林、液状石蜡、麻油、蜂蜡等辅料的软膏剂,其 aw 值相对较低。莫匹罗星软膏 aw 值最低,这是因为莫匹罗星软膏中添加大量聚山梨酯400,聚山梨酯400具有较强的吸湿性,适于作为润湿剂和稠度调节剂[13]。
本研究发现84.31%软膏剂 aw 高于美国药典(USP)。因此,对于 aw 值较高的软膏剂,在处方研发过程建议评估后对其处方优化,即通过改变氯化钠、蔗糖、乙醇、丙二醇和甘油等浓度,降低软膏剂aw,从而提高药品自我防腐的能力[14-15]。
3.5对软膏剂的包装系统密闭性提出更高要求
目前,药品容器密封包装系统主要集中于如何防止微生物对药剂的侵入[16],未将有效阻止环境水分子的入侵纳入质控要求。药品 aw 理念的提出,对于软膏剂包装材料的密闭性、稳定性提出更高的要求,即在药品储存过程中,该包装系统既要有效防止微生物又要有效阻止水分子侵入药剂。
[参考文献]
[1]The United States PharmacopieialConvention.United States Pharmacopeia[M].41th Edition.Baltimore:United Book Press,2018:7298-7300.
[2]闵红,杨静,呼延婷婷,等.片剂水分活度迁移规律与载荷微生物生长状况研究[J].中国药业,2019,28(22):21-25.
[3]Juneja VK,Valenzuela-Melendres M,Heperkan D,et al. Development of a predictive model for Salmonella spp. reduction in meat jerky product with temperature, potassium sorbate, pH, and water activity as controlling factors[J].International Journal of Food Microbiology,2016,236:1-8.
[4]杨晓莉,李翠,谢毓华,等.基于水分活度测定的发酵红萝卜浓缩汁细菌检测方法[J].中国食物与营养,2020,26(3):23-26.
[5]张静,谢茵,吴良发,等.水分活度在化妆品微生物控制方面的应用分析[J].中国医药科学,2019,9(16):16.
[6]曹嘉成,张书卉,焦灵利.基于风险管理的药品 GMP 检查发起机制研究[J].药学与临床研究,2020,28(3):229-232.
[7]周志云,杨静,李翠,等.黑曲霉生长最低水分活度研究[J].中国药业,2020,29(17):61-63.
[8]国家药典委员会.中华人民共和国药典2020年版四部[M].北京:中国医药科技出版社,2020:160-176.
[9]戚成,吴雪扬,陈元美,等.肠炎沙门菌的温度、 pH 值和水分活度主参数模型的构建[J].食品科学,2018,39(14):138-144.
[10]Shrestha S,NummerB.Survival of Salmonella spp. In low water activity chicken base paste and powder formulated at different salt levels[J].Food Control,2016,59:663-668.
[11]Osaili TM,Al-Nabulsi AA,Nazzal DS,et al.Effect of storage temperatures and stresses on the survival of Salmonella spp. in halva[J].Letters in Applied Microbiology,2017,65(5):403-409.
[12]绳金房,李辉,马仕洪,等.浅析水分活度测定在非无菌制剂微生物控制中的应用[J].药物分析杂志,2018,38(10):1837-1841.
[13]杨慧萍,王蕴华,侯健,等.聚山梨酯80对多源肥大细胞脱颗粒的影响研究[J].药物评价研究,2019,42(3):472-478.
[14]Turan H,SQnmez G,?elik M.Y,et al.Effects of different salting process on the storage quality of Mediterranean mussel (Mytilusgalloprovincialis L.1819)[J].Journal of Muscle Foods,2007,18:380-390.
[15]聂少勇.水活度测定及其在制药工业的应用[J].中國医药工业杂志,2018,49(12):1710-1715.
[16]Chang LC,Kang JJ,GauCS.Development of the risk-based, phased-in approach for the international harmonization of the regulation of container closure systems for drugs in Taiwan[J].Regulatory ToxicolPharmacol,2016,77:252-256.
(收稿日期:2021-01-07)
