青檀内生真菌高抗氧化活性菌株筛选及其培养条件优化
2021-09-19柴新义李梦宇于士军张微微胡文龙
柴新义,李梦宇,于士军,孙 星,罗 侠,张微微,胡文龙
(1.滁州学院 生物与食品工程学院,安徽 滁州 239000;2.滁州南谯区大柳镇凤胜食用菌生产合作社,安徽 滁州 239000)
1993年,Stierle[1]从短叶红豆衫中分离出能合成抗癌物质的内生真菌,由此关于内生真菌及其活性物质的研究才真正开展起来。近年来,内生真菌的次生代谢物在病害和虫害的生物防治中起到很大作用,可在农业中发挥重大作用,使植物的生长免遭病虫破坏[2-4]。在医药方面,可推进抗生素类药物的研发,治疗各种新型疾病。因此,越来越多的学者研究植物内生真菌[5-6]。关于内生真菌代谢产物中活性物质的研究主要应用在医学方面,如抗癌、抗肿瘤等活性物质药物的研发[7]。真菌方面在对紫薯、麻黄、三尖杉、枸杞等植物内生真菌次生代谢产物及发酵产物的研究中取得了一定的结果,加速了生物活性物质方面的研究进展[8-10]。近年来,对植物内生真菌的研究主要包括裸子植物和被子植物,研究发现,内生真菌具有活性的菌株可为农业方面及抗性药物的研发提供参考依据[11-12]。
青檀是我国特有的古老榆科植物,在植物与其内生真菌长期协同进化的过程中,往往已形成了丰富和稳定的内生真菌菌群,从青檀植物内生真菌资源中筛选出高抗氧化活性的菌株具有巨大的潜力。由此,本研究通过对青檀内生真菌高抗氧化活性菌株的筛选和培养条件的优化,以期为今后的深入研究和工业化生产提供重要参考。该研究不仅有利于保护我国稀有的特有野生树种青檀,而且利于推进抗氧化、抗癌和抗肿瘤等生物药物的研发。
1 材料与方法
1.1 材料
1.1.1 供试菌株
供试菌株分离自安徽琅琊山内我国特有的野生榆科植物青檀健康的枝条内,共30株,由滁州学院生物与食品工程学院微生物学实验室提供。
1.1.2 培养基
液体发酵培养基:葡萄糖20 g/L,蛋白胨2 g/L,K2HPO43.2 g/L,CuSO46.0×10-3g/L,MgSO40.2 g/L,pH自然。
液体菌种培养基:马铃薯200 g/L,葡萄糖20 g/L,KH2PO43 g/L,MgSO43 g/L,VB11.0×10-2g/L,pH自然。
1.1.3 试剂与设备
二苯代苦味肼基自由基(DPPH),75%乙醇,2%次氯酸钠,葡萄糖,蔗糖,乳糖,可溶性淀粉,NH4CL2,(NH4)2SO4,蛋白胨,尿素,K2HPO4,CuSO4,KH2PO4,MgSO4,VB1等。
高压蒸汽灭菌锅,YXQ-LS-75SII,西安常仪仪器设备有限公司;超净工作台,BBS-SDC,济南飞捷医疗设备有限公司;恒温培养箱,LHS-80SC(H),上海印溪仪器仪表有限公司;干燥箱,101-3A,南京实验仪器厂;恒温培养振荡器,DHZ-1112,上海精宏仪器有限公司;电子天平,FA1004,江苏南京设备仪器商城;超速离心机,IEC Multi,美国热电集团;紫外分光光度计,752N,上海精科仪电。
1.2 方法
1.2.1 制备菌丝体发酵粗体液
配制3000 mL液体发酵培养基,按每瓶100 mL装至锥形瓶中,灭菌15 min后在超净工作台中用直径1 cm的打孔器取供试菌株3块,接种至锥形瓶中,然后放入转速150 r/min、25℃的恒温培养振荡器中培养7 d。随后,用8层无菌纱布对上述培养物进行过滤,过滤后的液体置转速5000 r/min的离心机,离心处理20 min,然后用移液枪移取10 mL液体,再用0.45 mm的滤膜过滤,即可获得粗提液。
1.2.2 粗提液抗氧化活性的测定
制备0.065 mmol/L的DPPH自由基溶液,然后取上述离心后的粗提液2 mL,加入1.9 mL的DPPH自由基溶液,将其置于37℃环境中反应30 min,然后再放入离心机中离心5 min,最后利用紫外分光光度计测定样品517 nm处的吸光值,设置空白对照记为Amax,样品溶液吸光值记为A0,样品加DPPH自由基溶液吸光值记为Ai,用公式DPPH=[1-(Ai-A0)/Amax]×100%,计算自由基的清除率。
1.2.3 制备液体菌种
用马铃薯制备液体种子培养基1000 mL。分装灭菌后,接种具有高抗氧化活性的菌株,放入恒温培养振荡器中培养3~4 d,培养物作为发酵培养条件优化研究的液体菌种。
1.2.4 高抗氧化活性菌株培养条件的优化
(1)最适碳源的筛选:以液体发酵基本培养基为基础,分别选择乳糖、可溶性淀粉、葡萄糖、蔗糖为唯一碳源,添加量为20 g/L,接种液体菌种培养基20 mL,放入恒温培养振荡器中25℃下,培养7 d,测定DPPH自由基清除率。每个处理3个重复。
(2)最适氮源的筛选:以液体发酵基本培养基为基础,分别选择蛋白胨、尿素、NH4Cl2、(NH4)2SO4为唯一氮源,添加量为20 g/L,接种液体菌种培养基20 mL,放入恒温培养振荡器中25℃下,培养7 d,测定DPPH自由基清除率。每个处理3个重复。
(3)最适装液量的确定:在250 mL的锥形瓶中分别装入80、100、120、140 mL的液体发酵基本培养基,接种液体菌种培养基20 mL,放入恒温培养振荡器中25℃下,培养7 d,测定DPPH自由基清除率。每个处理3个重复。
(4)最适pH值的确定:以液体发酵基本培养基为基础,分别调节起始pH值为5.0、6.0、7.0、8.0,接种液体菌种培养基20 mL,放入恒温培养振荡器中25℃下,培养7 d,测定DPPH自由基清除率。每个处理3个重复。
(5)最适温度的确定:以液体发酵基本培养基为基础,接种液体菌种培养基20 mL,放入温度分别为25、27、29、31℃的恒温培养振荡器中,培养7 d,测定DPPH自由基清除率。每个处理3个重复。
(6)最适培养时间的确定:以液体发酵基本培养基为基础,接种液体菌种培养基20 mL,放入恒温培养振荡器中,分别培养6、8、10、12 d,测定DPPH自由基清除率。每个处理3个重复。
1.2.5 数据处理
利用公式DPPH=[1-(Ai-A0)/Amax]×100%计算自由基的清除率。利用SAS 9.12软件中GLM模块进行不同处理之间的差异性分析。
2 结果与分析
2.1 青檀内生真菌抗氧化活性菌株的筛选
对供试的30株青檀枝条内生真菌菌株进行DPPH自由基清除率试验,结果表明:有3株内生真菌表现了较强的抗氧化活性,占供试菌株的10%,菌株CZXY0024的DPPH自由基清除率最高,达(79.35±0.09)%,且与CZXY0014和CZXY0027两个菌株之间的DPPH自由基清除率存在明显差异(表1)。因此,选择菌株CZXY0024进行高抗氧化活性菌株培养条件的优化试验。

表1 青檀内生真菌菌株对DPPH自由基清除率试验Tab.1 DPPH radical scavenging activity of endophytic fungi from Pteroceltis tatarinowii
2.2 高抗氧化活性菌株培养条件的优化
2.2.1 单因素试验
(1)最适碳源
实验结果表明,不同碳源对青檀内生真菌发酵液的DPPH自由基清除率的影响不同,且存在显著性差异(图1)。葡萄糖作为碳源时,DPPH自由基清除率最高,为62.07%。可溶性淀粉作为碳源时,DPPH自由基清除率最低,仅为27.32%。因此,选择葡萄糖作为最佳培养碳源。
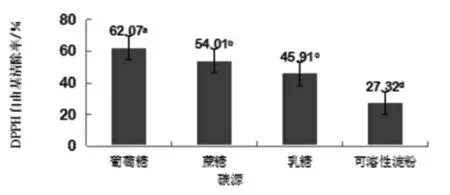
图1 不同碳源对青檀内生真菌发酵粗提液DPPH自由基清除率的影响Fig.1 Effects of different carbon sources on DPPH free radical scavenging efficiency of crude extracts from endophytic fungi from Pteroceltis tatarinowii
(2)最适氮源
实验结果表明,不同氮源对青檀内生真菌发酵液的DPPH自由基清除率的影响不同,且存在显著性差异(图2)。硫酸铵作为氮源时,DPPH自由基清除率最高,为67.71%。氯化铵作为氮源时,DPPH自由基清除率最低,仅为37.82%。因此,选择硫酸铵作为最佳培养氮源。
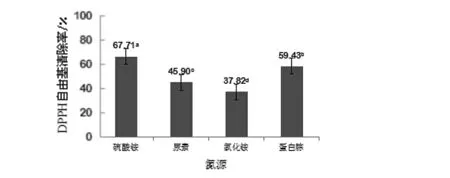
图2 不同氮源对青檀内生真菌发酵粗提液DPPH自由基清除率的影响Fig.2 Effects of different nitrogen sources on DPPH free radical scavenging efficiency of crude extracts from endophytic fungi from Pteroceltis tatarinowii
(3)最适装液量
实验结果表明,不同装液量对青檀内生真菌发酵液的DPPH自由基清除率的影响不同,且存在明显差异(图3)。装液量100 mL时,DPPH自由基清除率最高,达70.32%。因此,选择100 mL/250 mL的装液量作为最佳培养装液量。
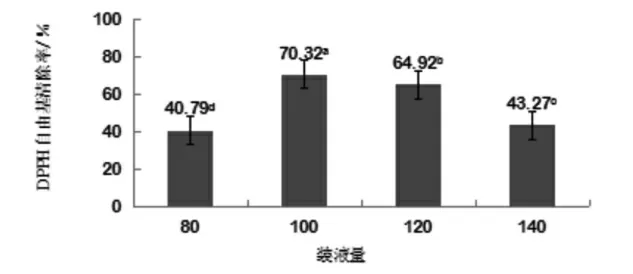
图3 不同装液量对青檀内生真菌发酵粗提液DPPH自由基清除率的影响Fig.3 Effects of different liquid contents on DPPH free radical scavenging efficiency of crude extracts from endophytic fungi from Pteroceltis tatarinowii
(4)最适pH值
实验结果表明,不同起始pH值对青檀内生真菌发酵液的DPPH自由基清除率的影响不同,且存在明显差异(图4)。pH值7.0作为起始pH时,DPPH自由基清除率最高,为56.79%。pH值5.0作为起始pH时,DPPH自由基清除率最低,仅为27.21%。因此,pH值7.0可作为最适起始pH。
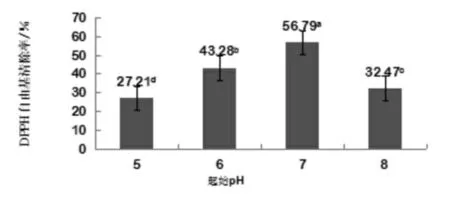
图4 不同起始pH对青檀内生真菌发酵粗提液DPPH自由基清除率的影响Fig.4 Effects of different initial pH on DPPH free radical scavenging efficiency of crude extracts from endophytic fungi from Pteroceltis tatarinowii
(5)最适温度
实验结果表明,不同发酵培养温度对青檀内生真菌发酵液的DPPH自由基清除率的影响不同,且存在明显差异(图5)。培养温度为27℃时,发酵粗体液对DPPH自由基清除率最高,达59.71%。培养温度为31℃时,DPPH自由基清除率最低,仅为29.78%。因此,选择27℃的发酵培养温度作为最适培养温度。
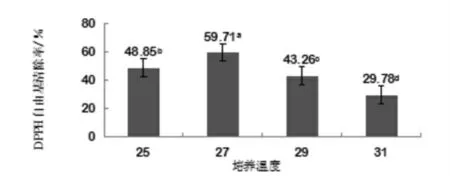
图5 不同培养温度对青檀内生真菌发酵粗提液DPPH自由基清除率的影响Fig.5 Effects of different culture temperature on DPPH free radical scavenging efficiency of crude extracts from endophytic fungi from Pteroceltis tatarinowii
(6)最适培养时间
实验结果表明,不同发酵培养时间对青檀内生真菌发酵液的DPPH自由基清除率的影响不同,且存在明显差异(图6)。培养时间为8 h时,发酵粗体液对DPPH自由基清除率最高,达67.61%。培养时间为6 h时,DPPH自由基清除率最低(43.54%)。因此,选择8h作为最适发酵培养时间。
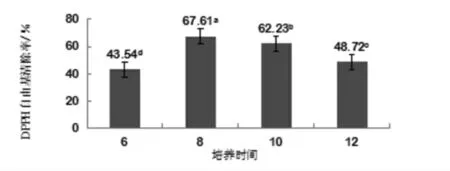
图6 不同培养时间对青檀内生真菌发酵粗提液DPPH自由基清除率的影响Fig.6 Effect of different culture time on DPPH free radical scavenging efficiency of crude extracts from endophytic fungi from Pteroceltis tatarinowii
2.2.2 正交试验
在单因素实验结果的基础上,选取最适装液量、pH、培养温度、培养时间4个因素,每个因素选取3个水平,设计正交试验(表2)。
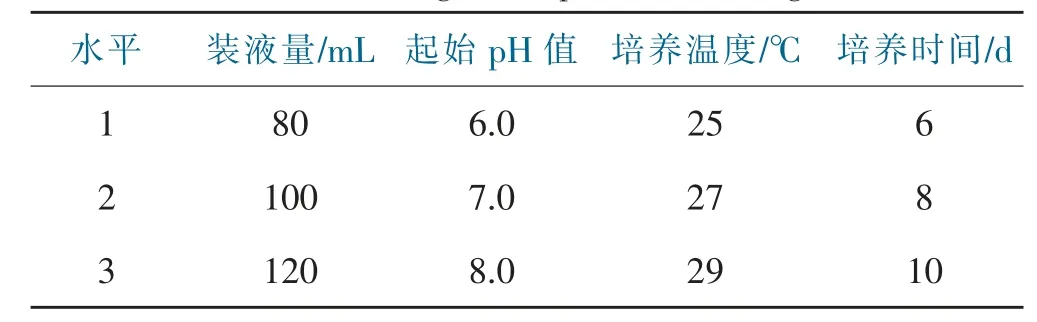
表2 正交试验组合设计表Tab.2 Orthogonal experimental design
正交试验优化结果表明,影响青檀内生真菌发酵粗提液抗氧化活性的因素大小顺序为:起始pH值>培养温度>培养时间>装液量。由此可知,起始pH值对青檀内生真菌发酵粗提液的DPPH自由基清除率影响最大,其次为培养温度和培养时间,装液量的影响最小。因此,青檀内生真菌高抗氧化活性菌株CZXY0024最优发酵培养条件的组合为:葡萄糖20 g/L、(NH4)2SO42 g/L、K2HPO43.2 g/L、CuSO46×10-3g/L、Mg-SO40.2 g/L、最适装液量80 mL、pH 7.0、温度27℃、培养时间8 d,该培养条件下青檀内生真菌发酵粗提液对DPPH自由基清除能力最高,达86.68%(表3)。
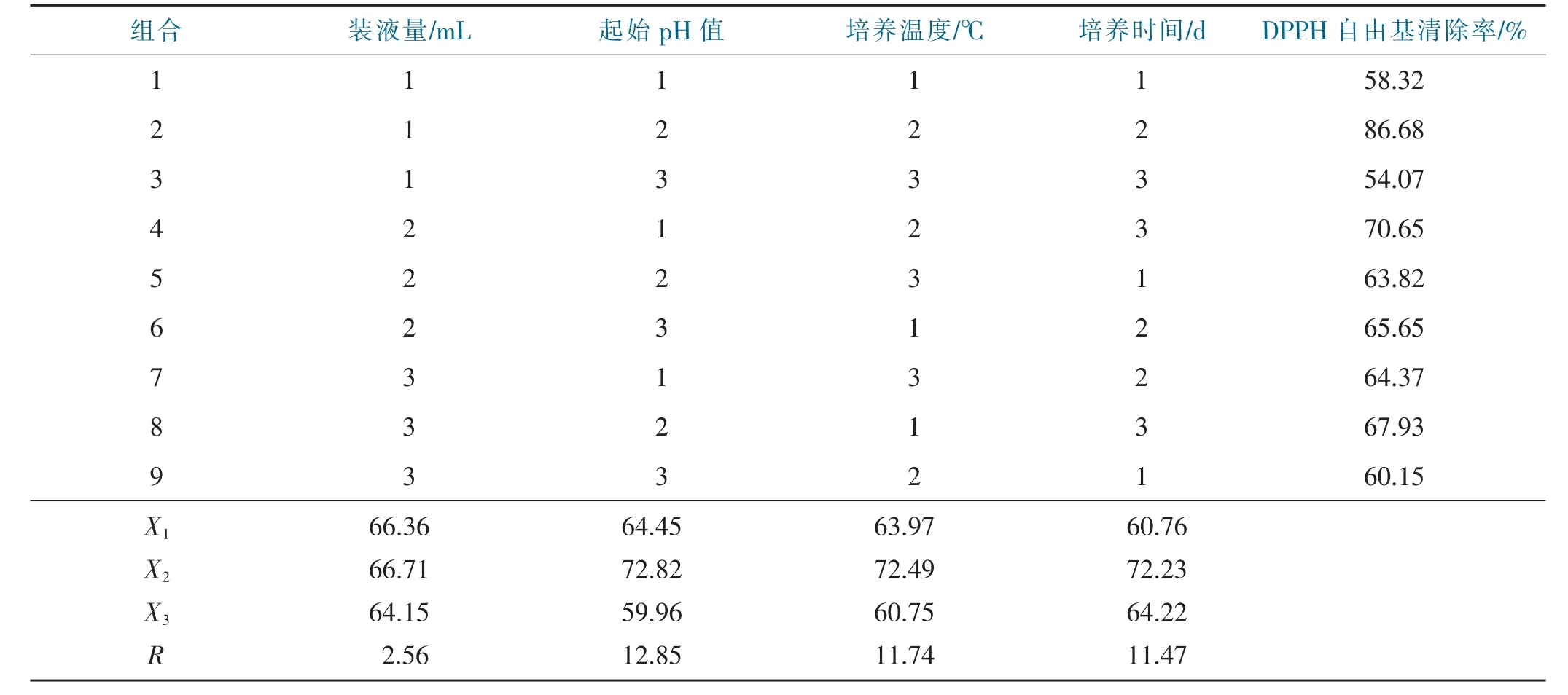
表3 不同正交试验组合对青檀内生真菌发酵粗提液的DPPH自由基清除率的影响Tab.3 Effects of different orthogonal test combinations on DPPH free radical scavenging efficiency of endophytic fungi from Pteroceltis tatarinowii
3 讨论与结论
刘雅莉等[13]对蒺藜内生真菌分别测定了发酵液对DPPH、OH、O2自由基的清除能力,其在21株内生真菌中发现9株具有氧化活性,占42.86%。高强等[14]发现,采集自山东泰安的青檀叶片中的球毛壳具有较高的抗氧化活性。张新国等[15]对从乌头、唐松草、车前草等药用植物中分离出的43株内生真菌进行了抗氧化活性研究,结果发现其中6株具有较好的抗氧化活性,占9.84%,且6株内生真菌对OH自由基具有较强的清除率(>50%)。刘洋等[16]研究发现,5株杜仲叶部内生真菌发酵产物在体外具有较高的清除DPPH自由基能力,同时发现杜仲叶部内生真菌的次级代谢产物对DPPH的清除率具有剂量依赖性。本研究对分离自我国特有榆科植物青檀中的30株内生真菌进行了抗氧化活性的筛选实验,发现其中3株真菌具有较好的抗氧化活性,占供试菌株的10%。由上可见,植物内生真菌是可以作为筛选抗氧化活性菌种的重要资源之一。
曹正等[17]对四种不同灵芝子实体提取物的抗氧化活性进行了研究,结果显示DPPH自由基清除率可达81.88%。刘力等[18]利用从自然发酵的酸浆水中分离的2株淀粉乳杆菌和阿米塞毕赤氏酵母进行发酵豆腐黄浆水以研究其清除DPPH自由基的能力,结果显示在单菌发酵时淀粉乳杆菌发酵黄浆水对DPPH自由基清除能力没有增强作用,而经过阿米塞毕赤氏酵母发酵的豆腐黄浆水清除DPPH自由基的能力得到一定提高,达38.49μmol/mL。张天博等[19]对一株保加利亚乳杆菌突变菌株UV2-6进行发酵条件的优化研究,结果表明在麦芽糖2%,酵母膏3%,复合无机盐0.1%,吐温800.1%,pH值为8.0,接种量3%,42℃培养的条件下,DPPH自由基清除率达81.46%。而本研究中筛选的青檀内生真菌高抗氧化菌株对DPPH自由基清除率可高达86.68%。另外,通过对青檀内生真菌抗氧化活性菌株筛选及其发酵培养条件的研究,有望为今后的生物药物开发和生产提供参考。
青檀内生真菌菌株CZXY0024的最优生产组合为:葡萄糖20 g/L、(NH4)2SO42 g/L、K2HPO43.2 g/L、CuSO46×10-3g/L、MgSO40.2 g/L、最适装液量80 mL/250 mL、pH 7.0、温度27℃、培养时间8 d,该条件下发酵粗提液对DPPH自由基清除能力最高,可达86.68%。
