粒径对吴茱萸次碱混悬凝胶透皮吸收的影响
2021-09-03唐开锋欧水平王玉和张桂悦
唐开锋,欧水平,王玉和,张桂悦,龙 江,王 森
(1.遵义医科大学 药学院,贵州 遵义 563099;2.遵义市第一人民医院 药剂科,贵州 遵义 563000;3.遵义医科大学附属医院 药剂科,贵州 遵义 563099;4.重庆市大渡口区人民医院,重庆 400084)
在已经开发或研究的具有良好生物活性的药物中,难溶或溶解性差的药占比超过40%[1],疏水性强成为这类药物吸收的最大障碍[2]。降低药物粒径已成为改善药物透皮吸收的重要方法之一,随着纳米技术的发展,将药物制备成纳米制剂已经获得广泛的发展,如将药物制备成纳米混悬液、纳米脂质体[3]、纳米乳、纳米囊及纳米粒[4]。在透皮给药系统中,难溶性药物的粒径大小也会影响药物的透皮吸收及皮肤滞留,研究表明,将药物制备成纳米粒径后,其在体外透皮吸收及皮肤滞留量提高2~3倍以上[5-6]。
吴茱萸次碱(Rutaecarpine,Rut))是芸香科植物吴茱萸主要的生物活性成分之一,在心血管、神经、消化、肿瘤等领域都有广泛的药理作用[7],如激动TRPV1受体[8]、抗Ang Ⅱ诱导的心肌细胞肥大[9]等。由于Rut水溶性和脂溶性均较差,口服生物利用低,其油水分配系数logPow为3.2,适宜透皮吸收,其透皮吸收屏障在于从角质层向亲水性活性表皮层的渗透[10]。针对Rut透皮吸收性差的问题,已有采用纳米乳[11]、液晶联用微针[12]等载体技术,添加促渗剂[13]等促进Rut透皮吸收的研究报道,但尚未见将Rut制成纳米混悬制剂促进其透皮吸收的研究报道。本研究将Rut制成Rut微米混悬液(Rut micron suspension,Rut-MS)和Rut纳米混悬液(Rut nanosuspension,Rut-NS),进一步制备成纳米混悬凝胶剂(Rut-nanogel)和微米混悬凝胶剂(Rut-microgel),并进行两者的透皮吸收和皮肤滞留性能比较研究,以考察药物粒径对吴茱萸次碱透皮吸收和皮肤滞留的影响,为Rut纳米混悬凝胶剂的研制提供依据。
1 材料与仪器
1.1 仪器 ME204E分析天平(梅特勒-托多利仪器上海有限公司);AD145S-P超细匀浆机(上海昂尼仪器仪表有限公司);AH-2010 高压均质机(ATS Engineering inc);DL-820D超声仪(上海之信仪器有限公司);90 Plus PALS Zeta电位及粒度分析仪(美国布鲁克海文仪器公司);TGL-16C离心机(上海安亭科学仪器厂);PH700型PH测量仪(EUTECH INSTRUMENTS);RFCD-923电动剃刀(宁波真和电气股份有限公司);平头型数显测厚仪(河南埃维特电子科技有限公司);TK-24BL型透皮扩散试验仪(上海锴凯科技贸易有限公司);1260Agilent高效液相色谱仪(美国安捷伦科技有限公司)。
1.2 试药 吴茱萸次碱对照品(99.70%,成都曼斯特生物科技有限公司);吴茱萸次碱(91%,陕西昊辰生物科技有限公司);卡波姆940(美国路博润公司);吐温 80(重庆江川化工有限公司);泊洛沙姆 188(德国巴斯夫有限公司);三乙醇胺(成都市科龙化工试剂厂);甲醇(天津市富宇精细化工有限公司);聚乙二醇400(成都市科龙化工试剂厂);氯化钠(国药集团化学试剂有限公司);乙腈(HPLC)(上海月旭科技股份有限公司);蒸馏水(自制)。
1.3 动物 SPF级雄性SD大鼠5只,健康SD大鼠,清洁级,雄性,体重180~200 g,购于长沙市天勤生物技术有限公司,许可证号:SCXK(湘)2014-0011。
2 方法
2.1 Rut HPLC测定
2.1.1 色谱条件 色谱柱Ultimate®LP-C18(4.6×250 mm,5 μm);流动相:水—乙腈(30∶70)等度洗脱,流速:1.0 mL/min,检测波长:343 nm,进样量:20 μL,柱温:25 ℃。
2.1.2 对照品溶液配制 精密称取吴茱萸次碱对照品4.87 mg,用甲醇定容到25 mL,超声(40 W)30 min使其完全溶解,以0.22 μm滤膜过滤,即得194.8 μg/mL的Rut对照品储备液。
2.1.3 专属性 分别精密吸取Rut对照品溶液、空白皮肤接收液、空白皮肤滞留液、透皮接收液和皮肤滞留液,按2.1.1项下色谱条件进样测定,记录色谱图。
2.1.4 线性范围 精密吸3.1.2项下对照品储备溶液适量,用甲醇稀释至浓度分别为19.48、9.74、4.87、2.43、1.2175、0.608 7 μg/mL的系列对照品溶液。分别精密吸取上述溶液20 μL,按2.1.1项下色谱条件进样测定。以峰面积为纵坐标,Rut质量浓度为横坐标,进行线性回归,得到标准曲线方程。
2.1.5 精密度和稳定性 精密吸取透皮接收液,按2.1.1项下色谱条件进样6次,记录锋面积,计算Rut峰面积RSD。取同一透皮接收液,分别在0、2、4、8、12、24按2.1.1项下条件进样测定,计算Rut浓度RSD值。
2.1.6 回收率实验 精密取24 h的透皮接收液0.5 mL,分别加入高、中、低3个质量浓度的Rut对照品溶液0.5 mL各3份,混合均匀后用0.22 μm微孔滤膜滤过,弃去初滤液,取续滤液,按2.1.1项下色谱条件精密量取20 μL进样,测定Rut含量,计算回收率。
2.2 Rut-microgel和Rut-nanogel的制备和表征
2.2.1 Rut-MS和Rut-NS的制备称 取泊洛沙姆1 880.5 g、吐温801.0 g,加入100.0 g水,超声至完全溶解,再取Rut 0.24 g,在20 000 r/min高剪切下加入上述溶液中,继续高剪切3 min,即得Rut-MS。Rut-MS再经140 MPa高压均质5 min,制得Rut-NS。
2.2.2 Rut-MS和Rut-NS的粒径测定 分别取Rut-MS和Rut-NS适量,加蒸馏水稀释80倍,超声(40 W)1 min采用90 Plus PALS Zeta 电位及粒度分析仪测定粒径、PDI,测量波长 659 nm、温度25 ℃,入射角度90 ℃,测量次数5次。
2.2.3 Rut-microgel和Rut-nanogel的制备 分别取Rut-MS和Rut-NS 20 g,与0.48%卡波姆940溶液2.4 g混合均匀,加三乙醇胺调节pH约为6.5,即得Rut-microgel和Rut-nanogel。
2.2.4 Rut-microgel和Rut-nanogel的含量测定 分别精密称取2.2.3项下Rut-microgel和Rut-nanogel 0.025 g,加入甲醇稀释100倍,用0.22 μm 微孔滤膜滤过,即得供试品溶液。精密吸取供试品溶液,按2.1.1项下色谱条件进样测定,计算Rut含量。
2.3 体外透皮实验
2.3.1 SD大鼠皮肤的处理 取健康SD大鼠,用电剃刀除去背部鼠毛,将大鼠断颈处死;用剪刀将背部皮肤剪下置生理盐水中,小心除去皮下组织、血管及脂肪,用生理盐水反复冲洗,并检查其完整性;放入-20 ℃冰箱备用。使用时,将皮肤在室温下用生理盐水解冻后,用滤纸吸干,剪至合适大小,并测定其厚度。
2.3.2 体外透皮吸收试验 以SD大鼠皮肤为扩散屏障,采用改良Franz透皮扩散试验仪进行体外透皮实验,将处理好的皮肤剪成2 cm×2 cm大小12份,平均分为两组,两组间总厚度差异为0.026 mm;剪切好的大鼠皮置于扩散池与接收池之间,真皮层面向接受池,用夹子夹紧,防止漏液。接收池中放入磁力搅拌子,并分别加入透皮吸收接收液(30%PEG400-30%乙醇-生理盐水)8 mL,于37±0.01 ℃, 350 r/min的搅拌平衡30 min,弃掉接收液,重新加入接收液8 mL;分别用减量法加入Rut-microgel和Rut-nanogel各6份,每份1.20 g,涂抹均匀,在上述温度和搅拌条件下进行体外透皮吸收试验;在2、4、6、8、10、12、24 h取样2 mL,同时补充相同体积的新鲜接受液,将取出的接收液在10 000 r/min离心10 min,即得透皮接收液。透皮吸收试验结束后取下皮肤,用新鲜接收液清洗表面残留凝胶,滤纸吸干,剪碎后加入甲醇5 mL超声提取2次,每次30 min,取上清液用0.22 μm微孔滤膜滤过,得皮肤滞留液。按2.1.1项下色谱条件进样测定透皮接收液和皮肤滞留液中Rut浓度。
2.4 数据处理和统计分析
2.4.1 透皮吸收参数 按公式(1)计算取样时间t内的累积透过量Qt,将Qt与t作图得透皮吸收曲线,将直线部分进行线性回归,求出直线斜率,即为稳态透皮速率Js,直线与横轴的相交点即为时滞tlag。
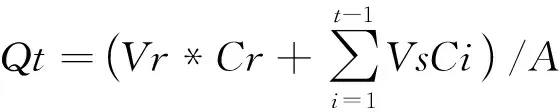
(1)
式中Qt为第n次取样时的累积透过量,Vr代表接收液体积(8 mL),Ct为每个取样点浓度(μg/mL),Vs为取样体积(2 ml),Ci为第i次取样测得的接收液中Rut浓度,A为扩散渗透面积(3.46 cm2)。
2.4.2 皮肤滞留量 按式(2)计算皮肤滞留量QS:
QS=V'C/A
(2)
式中V′为提取皮肤液总体积(6 mL),C为皮肤提取液药物总浓度,A为扩散渗透面积(3.46 cm2)。
3 结果
3.1 Rut HPLC测定方法的建立
3.1.1 专属性HPLC色谱图 结果表明Rut主峰的峰形良好,基线平稳,供试品溶液与对照品溶液的主峰保留时间一致,供试品溶液中其他组分对主峰不产生干扰,专属性良好(见图1)。
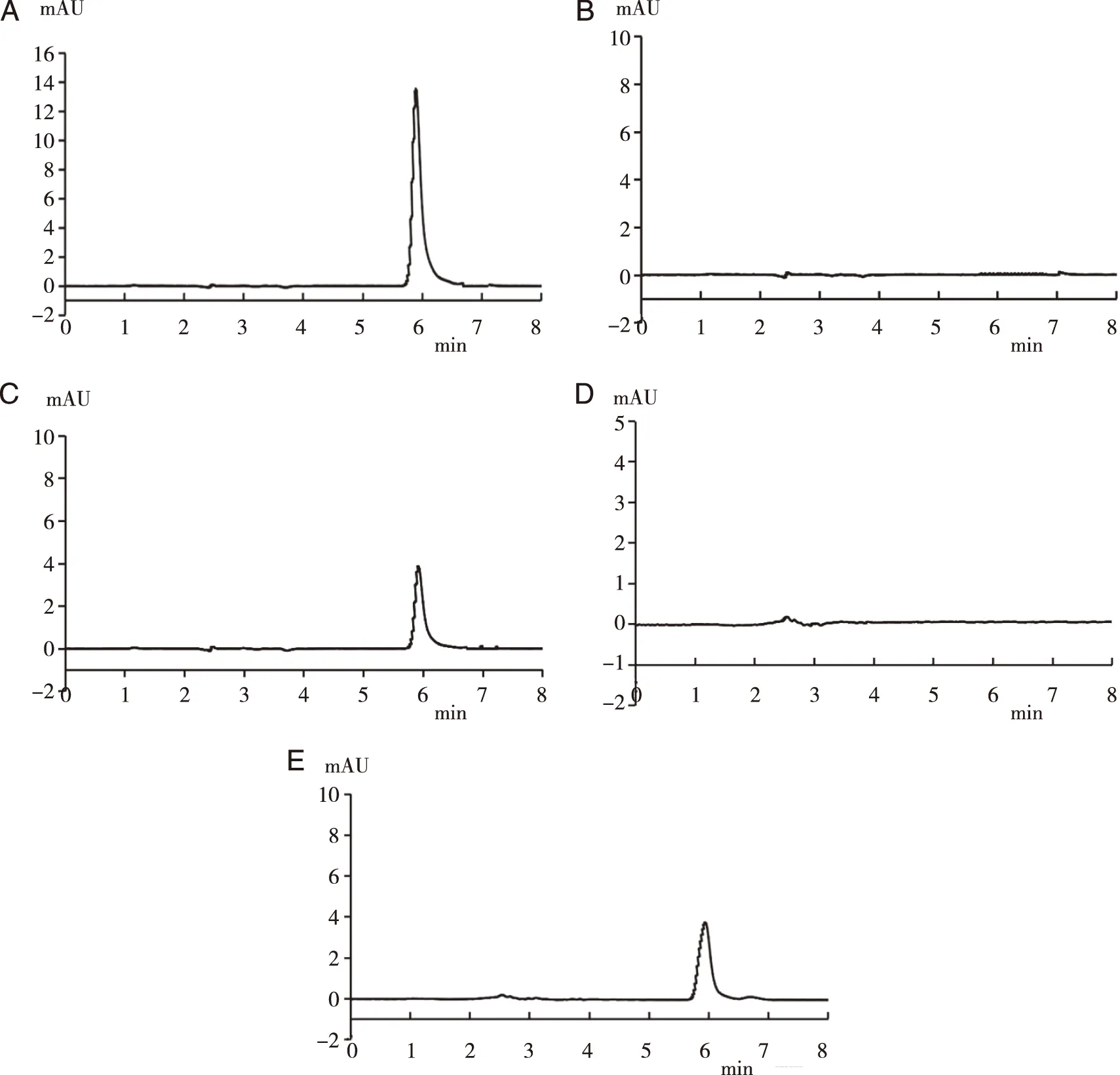
A:Rut对照品溶液;B:空白皮肤接收液;C:皮肤接收液;D:空白皮肤滞留液;E:皮肤滞留液。图1 HPLC色谱
3.1.2 线性范围 Rut标准曲线方程为C=64.5112X+37.1153,R2=0.9996,表明Rut浓度在0.6087~19.48 μg/mL内有良好的线性关系。
3.1.3 精密度和稳定性 按2.1.5记录峰面积,计算Rut峰面积的RSD为0.74%,表明HPLC仪器精密度良好。取同一透皮接收液,分别在2.1.5项下时段进样测定,计算Rut浓度的RSD为1.21%,说明供试品溶液在24 h内稳定。
3.1.4 回收率试验 按2.1.6项下方法,测定Rut含量,计算回收率,结果见表1。结果Rut的回收率90%~130%,各组RSD均<5%,说明本方法的回收率符合生物样品的分析要求。
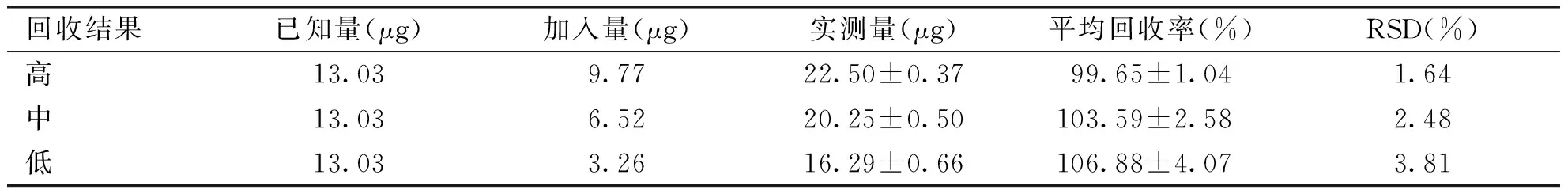
表1 回收率实验结果(n=9)
3.2 Rut-microgel和Rut-nanogel粒径和含量测定Rut-MS和Rut-NS的粒径分别为(1 317.46±107.27、211.66±1.06) nm,PDI分别为0.367±0.029、0.233±0.011,Rut-microgel和Rut-nanogel中Rut含量分别为21.11、20.12 mg/g。
3.3 Rut-microgel和Rut-nanogel透皮吸收和皮肤滞留参数Rut-microgel和Rut-nanogel的透皮吸收和皮肤滞留参数见表2,透皮吸收曲线见图2。结果表明,Rut-nanogel的透皮吸收速度明显高于Rut-microgel,在透皮吸收的前6h内Rut-nanogel吸收呈直线上升趋势,Q24是Rut-microgel的1.62倍,tlag减少6.24min,Js是Rut-microgel的2.12倍,而Rut-microgel的Qs是Rut-nanogel的2.16倍。
表2 透皮吸收参数及皮肤滞留量

图2 Rut-microgel和Rut-nanogel透皮吸收曲线
4 讨论
本研究初步证明了将Rut的粒径从微米级(1 317.46±107.27 )nm降低到纳米级(211.66±1.06) nm,以有限剂量给药在离体大鼠背部皮肤透皮吸收试验中,可有效地提高其透皮吸收速度、累积透过量,有利于Rut外用制剂迅速透皮吸收,发挥局部或全身治疗作用。
研究表明,纳米混悬制剂促进药物透皮吸收和皮肤滞留和以下原理有关:①难溶性药物粒径减小至纳米级后溶解度增加。有研究证实,将Rut粒径从1 μm减少至200 nm后,可大幅增加其溶解度,口服吸收总量增加9倍[14]。②NS皮肤给药以后能使药物在皮肤表面处于过饱和状态,增加了经皮渗透的浓度梯度,加速了药物的透皮扩散。③小于40 nm的药物可以直接进入毛囊后溶解扩散,750 nm以下粒径的药物可以纳米粒的形式渗透进角质层,在毛囊中积累,并在角质层和毛囊中溶解,维持局部的过饱和浓度,促使药物向附近组织渗透扩散[5,15]。Rut-nanogel促进Rut透皮吸收是否与Rut纳米粒更多蓄积在毛囊而持续扩散有关,有待进一步研究Rut-nanogel的透皮吸收途径和在皮肤中的分布。
大量研究证实,纳米混悬液能通常能增加药物的皮肤滞留量,但本次试验的结果却显示纳米混悬液的皮肤滞留量更少,其原因应与本次试验中采用的有限剂量给药(约40 μg/cm2)有关,Rut粒径降低后,溶解性增大,加快了渗透速率,经过24 h的渗透,已经基本完全扩散进入接收液中,使得皮肤滞留量大幅减少,而在普通混悬凝胶中,Rut粒径大,溶解率低,渗透性差,使得药物更容易累积在皮肤中,从两项的累积透过量及时滞时间比较,也能证实了这一原因。有待进一步采用无限剂量给药进行透皮吸收试验,验证减小Rut粒径至200 nm左右是否会增加其皮肤滞留量。
