维持性血液透析患者骨密度情况及发生骨质疏松的影响因素分析
2021-08-31薛劲松杨书平鞠杰王萍方芳
薛劲松 杨书平 鞠杰 王萍 方芳
维持性血液透析(MHD)是治疗终末期肾脏病的重要手段,能够提高患者的生存质量,延长生存期,但患者多伴有程度不一的骨质代谢紊乱,易发生骨质疏松[1]。骨质疏松属于全身性代谢性疾病,以骨微结构破坏、骨量减低、骨脆性增加等为主要特征,可导致患者发生肌肉、骨骼疼痛,增加骨脆性,增加骨折风险,严重影响患者的健康生活[2-3]。骨质疏松会会增加MHD跌倒风险,轻者可引起软组织损伤、肢体疼痛,重则可导致患者失能、骨折、丧失独立能力、恐惧等严重后果,是患者致残、致死的一项重要隐患。若能早期充分了解MHD患者发生骨质疏松的影响因素,指导临床实施针对性的护理干预对策,对减少骨质疏松发生和改善患者预后具有积极意义。故本研究分析MHD患者骨密度情况及发生骨质疏松的影响因素,为临床早期实施相应的预防措施提供参考,报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2018年3月-2020年3月在笔者所在医院行MHD治疗的66例患者临床资料,纳入标准:MHD治疗≥3个月;明确慢性肾脏病史;临床资料完整;病情稳定。排除标准:合并甲状腺疾病、慢性感染、恶性肿瘤等影响骨代谢疾病;骨折或先天性骨骼发育不全;肝肾等重要脏器功能不全。年龄33~86岁,平均(60.12±3.46)岁;男45例,女21例;透析时间3~215个月,平均(52.37±12.32)个月。本研究经医学伦理委员会审核批准;患者或家属签署知情同意书。
1.2 方法
收集入组患者年龄、性别、透析时间、体质量指数(BMI)、合并基础疾病(高血压、冠心病、糖尿病)、原发疾病类型、生化指标[甲状旁腺激素(iPTH)、血磷(P)、碱性磷酸酶(ALP)、白蛋白(ALB)]、骨密度等资料。
1.3 骨密度测定
使用美国GE公司的双能X线吸收骨密度仪测定入组患者腰椎(L1~4)骨密度,用T表示。参考文献[4]骨质疏松及骨矿盐疾病诊疗指南标准判断骨密度情况:T值<-2.5为骨质疏松;T值>-1.0为骨量正常,T值为-2.5~-1.0为骨量减少。
1.4 观察指标
分析MHD患者骨密度情况及发生骨质疏松的影响因素。
1.5 统计学处理
应用SPSS 21.0软件分析数据,计量资料以(±s)表示,采用t检验,计数资料以率(%)表示,采用χ2检验,多因素使用Logistic回归分析,P<0.05为差异有统计学意义。
2 结果
2.1 骨密度情况
66例行MHD治疗患者中骨质疏松22例(33.33%),骨量正常17例(25.76%),骨量减少27例(40.91%)。
2.2 影响因素分析
2.2.1 单因素 骨质疏松组年龄≥60岁、女、绝经女性、透析时间≥50个月、BMI<18.5 kg/m2、iPTH>250 pg/ml比例高于非骨质疏松组,差异有统计学意义(P<0.05);两组合并基础疾病、原发疾病类型、P、ALP、ALB相比,差异无统计学意义(P>0.05),见表1。

表1 MHD患者发生骨质疏松的影响因素单因素分析 例(%)

表1(续)
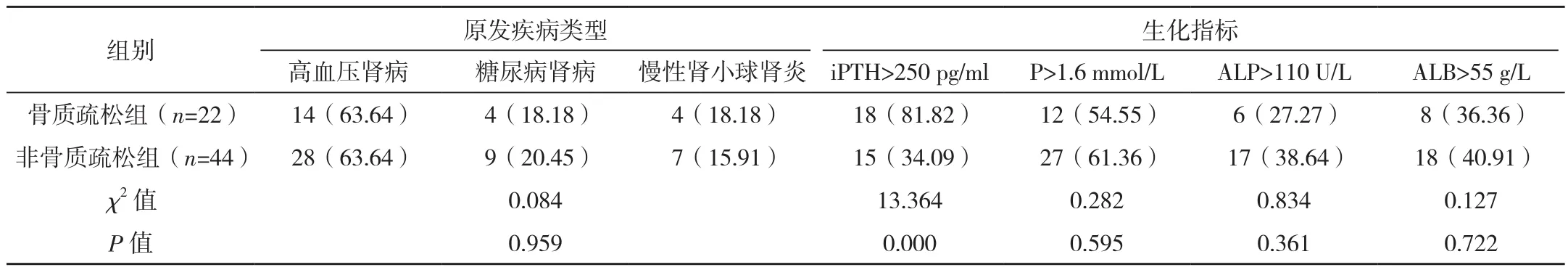
表1(续)
2.2.2 多因素 多因素Logistic回归分析显示,年龄≥60岁、女、绝经、透析时间≥50个月、BMI<18.5 kg/m2、iPTH>250 pg/ml是MHD患者发生骨质疏松的独立危险因素(OR>1,P<0.05),见表 2。

表2 MHD患者发生骨质疏松的影响因素多因素分析
3 讨论
骨质疏松是MHD患者常见的并发症之一,是因机体骨形成低于骨吸收,骨重建呈负平衡状态,引起骨量减少、骨微观结构破坏,诱发全身骨痛、腰背痛、活动受限等,并会增加骨的脆性,增加骨折、脊柱畸形变等严重后果[5-7]。本研究中,66例行MHD治疗患者中骨质疏松22例(33.33%),骨量正常17例(25.76%),骨量减少27例(40.91%),提示MHD患者中骨质疏松发生率较高。分析原因在于长期行MHD治疗能够导致患者发生严重营养不良,减少骨量,降低骨密度,促使骨微观结构发生改变,进而诱发骨质疏松有关。因此,寻求MHD患者发生骨质疏松相关危险因素,指导临床制定相应的预防措施干预对于疾病的恢复至关重要。
张立新等[8]经多因素Logistic回归分析结果显示,性别、年龄、BMI、PTH、碱性磷酸酶(ALP)是MHD并发骨质疏松症的独立危险因素(OR=2.944、2.676、2.324、2.512、2.622,P=0.009、0.023、0.034、0.026、0.025、0.021)。本研究结果显示,年龄≥60岁、女、绝经女性、透析时间≥50个月、BMI<18.5 kg/m2、iPTH>250 pg/ml是MHD患者发生骨质疏松的独立危险因素(OR=4.592、4.667、17.500、5.278、3.383、8.700,P=0.007、0.007、0.000、0.016、0.025、0.001),与上述研究结果相似。(1)老龄。老龄患者多存在营养不足、胃肠吸收功能减弱,减弱激素对机体的刺激作用,减少骨形成,增加骨吸收,诱发骨代谢紊乱;肠道钙吸收减少,增加骨钙流失,减少沉积到骨骼上的钙原子和钙离子,促使骨骼变软,改变骨密度结构,同时老龄患者活动量相对减少,削弱骨骼应力作用,减少骨形成,易发生骨质疏松[9]。(2)女、绝经女性。女性体内性激素水平能够促进骨骼发育,性激素水平降低,尤其雌激素分泌量减少会使股骨细胞对PTH的敏感性提高,促使机体骨质大量流失;激素水平下降还会减低机体对钙质的吸收,破骨细胞活跃,使骨量流失进一步加快,易发生骨质疏松。尤其是绝经女性机体内雌激素水平明显下降,减弱抗氧化体系水平,增加细胞膜NADPH氧化镁,促使过氧化物累积而引起氧化应激,其会损伤DNA、细胞膜脂类、细胞核、线粒体、转录因子等大分子物质,加速成骨细胞、骨细胞凋亡,引起骨重建失衡,降低骨密度和破坏骨微结构,易引起骨质疏松[10-12]。(3)低BMI。人体脂肪能够促进髋骨、股骨等承重骨骼的发育、生长,使骨质流失减少,发挥提升骨密度作用,还能刺激雄激素转化为雌激素,减缓骨质流失速度。低BMI者机体营养状况较差、蛋白摄入少且脂肪含量较低等,易发生骨量减少,增加骨质疏松发生风险。(4)透析时间长。透析时间越长者处于尿毒症状态时间越长,体内蓄积的毒素越多,增加骨矿物质流失,增加骨质疏松发生率。(5)iPTH高。高水平的iPTH能够增加成骨细胞、间质细胞和破骨细胞激活相关基因(RANKL)合成,促进破骨细胞的增殖、分化;直接作用于骨骼系统,增加破骨细胞活跃度;能经Src激酶介导αβ整合蛋白易增强骨吸收,引起骨量流失,诱发骨质疏松[13]。
综上所述,MHD患者易发生骨质疏松,老龄、女、绝经女性、透析时间长、低BMI、iPTH高是MHD患者发生骨质疏松的独立危险因素,临床需加以重视。
