氨基改性MCM-41对阴离子染料酸性品红的吸附研究
2021-08-26曹菊林宋纪双陈晓春
曹菊林,姚 勇,宋纪双,张 更,陈晓春
(1.安徽新力电业科技咨询有限责任公司,合肥 230601;2.国网安徽省电力有限公司电力科学研究院,合肥 230601; 3.合肥离子医学中心,合肥 230088)
前 言
随着我国工业迅猛发展,印染工业也在发展的进程中创造出了巨大的经济效益,但同时又对水资源带来了严重的污染破坏,印染废水已成为我国目前主要的水体污染源之一[1]。相比较各种染料废水的处理方法,吸附法由于设计简单、成本低、操作方便、对有毒物质不敏感等,已成为染料废水处理的理想方法。活性炭是其中最常用的吸附剂,然而由于受到吸附容量和生产原料的制约,以及再生处理费用高昂,通常只用于低浓度废水处理或者深度处理[2],寻求新型廉价的高选择性、高吸附容量的吸附剂成为吸附法研究的重点。
介孔材料是上世纪90年代迅速兴起的新型纳米结构材料,比表面积大、孔隙率高、孔径分布窄、表面富含不饱和基团、孔径易控制等[3],是一种完美的选择性吸附材料,而且在改性后还能表现出更多的特性。由于介孔材料MCM-41 表面带负电,对带正电的染料吸附效果较好,为了提高MCM-41的吸附范围,本文着重研究氨基改性后的MCM-41对阴离子染料废水酸性品红的吸附,并探讨介孔材料去除染料的机理和影响吸附效率的因素。
1 材料与方法
1.1 MCM-41和氨基改性MCM-41的制备
MCM-41采用水热合成法在碱性条件下制备:将一定浓度的NaOH溶液加入到十六烷基三甲基溴化铵(CTAB)的水溶液中,边加边搅拌至完全溶解,调节溶液pH为10左右,再向溶液中缓慢加入正硅酸乙酯(TEOS),继续搅拌直至溶液变为粘稠的白色凝胶状,其中各反应物之间的摩尔比为0.12CTAB∶1TEOS∶0.24NaOH∶66.7H2O。将凝胶转移到聚四氟乙烯反应釜中,在100℃下晶化48h,随后过滤、洗涤、干燥,550℃下焙烧5h,即得到全硅MCM-41介孔分子筛[4]。
NH2-MCM-41的制备是参照Heidari等[5]的研究,具体方法是:准确称取2.5g已干燥的MCM-41和2.5g 3-氨丙基三甲氧基硅烷(APTS),加入到含有50mL正己烷的烧瓶中,常温下冷凝6h,随后过滤,用正己烷多次冲洗,再用烘箱在105℃下干燥24h,冷却后贮存于干燥器中备用。
1.2 MCM-41和NH2-MCM-41的表征分析
使用物理吸附仪测定氮在-194℃下吸附—解吸附等温线,可以获得MCM-41和NH2-MCM-41的BET比表面积、总孔隙容量和密度泛函理论(DFT)孔隙尺寸分布,结果如表1所示。改性后MCM-41的BET比表面积,总孔体积和平均孔径均减小,这是改性官能团-NH2嫁接在MCM-41的孔道内导致的。
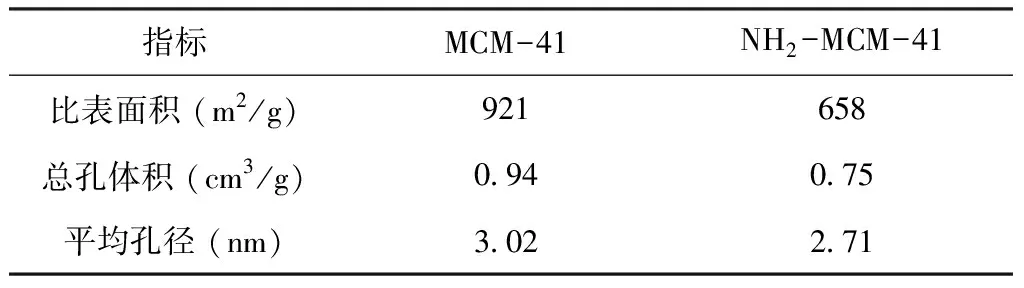
表1 MCM-41和NH2-MCM-41的物理参数Tab.1 Physical parameters of MCM-41 and NH2-MCM-41
利用傅里叶变换红外光谱(FTIR)分析来测定MCM-41表面上的官能团,并检验改性基团是否嫁接成功,结果如图1所示。2 936cm-1代表-CH2反对称伸缩和对称伸缩振动,1 562cm-1是-NH的弯曲振动[6]的特征吸收峰,该两处吸收峰的出现表明了-NH2基团成功地被嫁接在MCM-41表面上了。而且,在3 445cm-1和1 635cm-1附近的吸收峰的强度下降了,说明了改性后MCM-41上大部分-OH被-CH2取代了[5]。
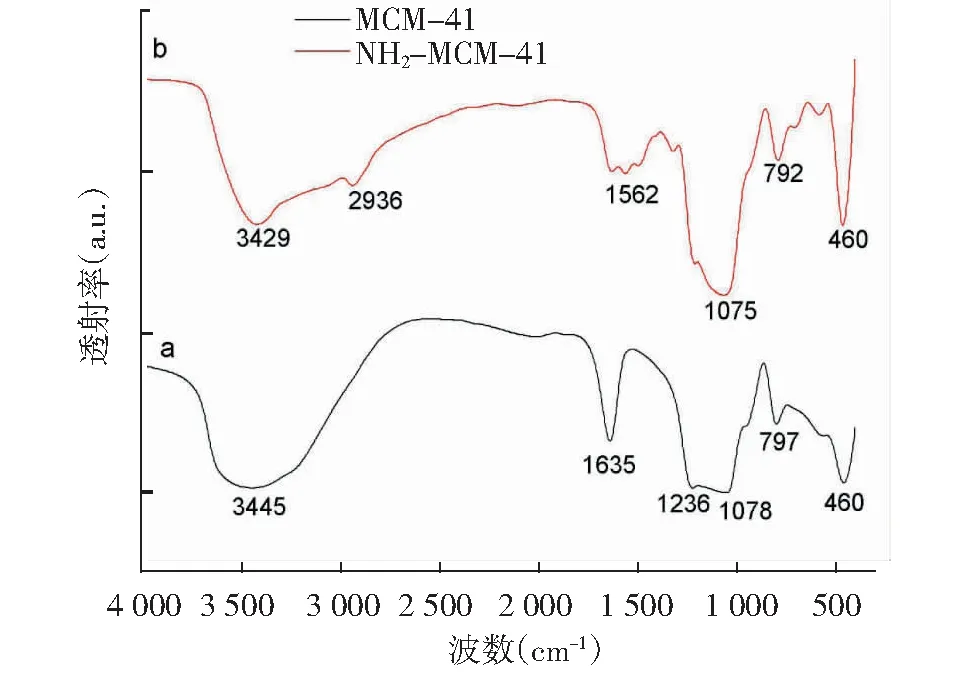
图1 MCM-41(a)和NH2-MCM-41(b)红外光谱图Fig.1 FTIR spectra of MCM-41(a) and NH2-MCM-41(b)
1.3 实验方法和计算公式
染料浓度的测定:实验所用的阴离子染料为酸性品红(AF)(C20H17N3Na2O9S3),配制一定浓度梯度的染料溶液,置于一组50mL比色管中,在最大吸收波长λmax=524nm下,用1cm的比色皿,以蒸馏水作为参比,测定吸光度,绘制出标准曲线。测定样品溶液中染料的剩余浓度时,按此方法在最大吸收波长下测定其吸光度,并作空白校正,再根据标准曲线求得。
吸附实验:配制一定浓度的AF溶液,各取100mL加入到250mL碘量瓶中,分别加入一定量的NH2-MCM-41,用0.1mol/L的HCl和NaOH溶液调节溶液的pH值,将碘量瓶放入水浴恒温振荡器中(180rpm),振荡吸附一定时间后用微孔滤膜过滤,测定剩余染料的浓度。
解吸附-吸附循环实验:向装有1.0g吸附饱和后的NH2-MCM-41的碘量瓶中分别加入100mL 0.1mol/L NaOH、0.1mol/L HCl和乙醇(10%)溶液,在25℃恒温振荡器中振荡,解吸平衡后过滤,测定滤液中剩余染料的浓度,计算解吸率,并将解吸附后的NH2-MCM-41洗涤烘干再用于吸附AF溶液的实验,以此方法循环多次。
染料的去除率η(%)按公式(1)计算:
(1)
吸附剂的吸附量qe(mg/g)按公式(2)计算:
(2)
公式(1)、(2)中C0和Ce分别表示染料溶液的初始浓度和平衡浓度(mg/L);V表示染料溶液的体积(L);M表示吸附剂的质量(g)。
2 结果与讨论
2.1 MCM-41改性前后对阴离子染料的吸附效果对比
通过使用改性前后的MCM-41作为吸附剂对酸性品红溶液进行实验对比,结果得出NH2-MCM-41对AF的去除效果更好,去除率为62.81%,而MCM-41对其去除率只有11.85%,这说明了氨基改性后的MCM-41能够较好地吸附阴离子染料。由于MCM-41表面上含有官能团Si-O和Si-OH因而带有负电荷,只能吸附带正电荷的染料而不能去除带负电荷的染料[7]。在改善MCM-41使其能够吸附特定物质的设计中,对MCM-41进行表面修饰以此来提高吸附能力和吸附选择性是非常有效的,这种修饰是利用吸附剂与被吸附质之间的特殊相互作用[8]。因此,对MCM-41进行氨基改性用于去除阴离子染料是非常有必要的。
2.2 溶液pH值的影响
吸附过程的效率很大程度上取决于溶液的pH值,因为pH值会影响吸附质(染料分子)的电离度,同样还会影响吸附剂的表面性能[9]。从图2中可以发现,随着溶液pH值的增大,AF的去除率和吸附量都急剧下降,在pH值为3.0时最高,去除率和吸附量分别为92.02%、92.02mg/g。
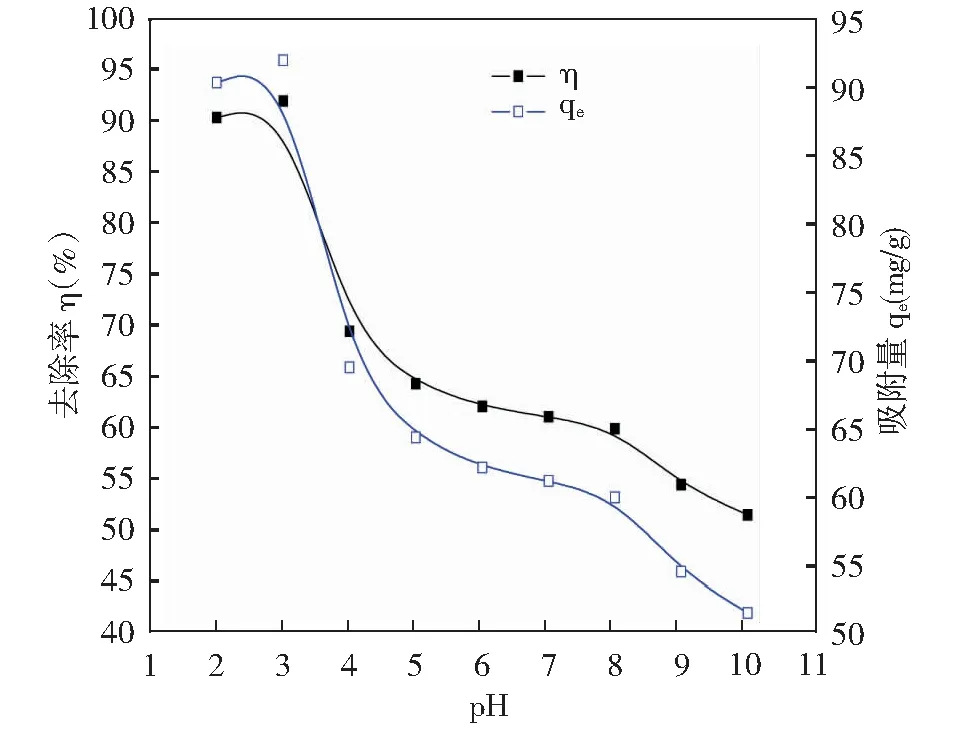
图2 溶液pH对阴离子染料AF吸附效果的影响Fig.2 Effect of solution pH on the adsorption of anionic dye AF
(3)
(4)
公式(3)、(4)中,D、M分别代表AF和NH2-MCM-41结构中的其他部分。
2.3 吸附剂剂量的影响
吸附剂的剂量是测定吸附容量和吸附百分比的重要参数,NH2-MCM-41的剂量对阴离子染料AF吸附效果的影响结果见图3。从图中可以得出当NH2-MCM-41的投加量从0.05g增加到0.2g时,AF的去除率显著提高;当NH2-MCM-41从0.2g继续增加到0.5g时,去除率缓慢上升,故取0.2g作为最佳吸附剂投加量。去除率随着吸附剂的增加而增加是因为吸附剂与吸附质之间有了更大的吸附接触表面积,从而提供了更多的吸附位点来吸附染料[12]。
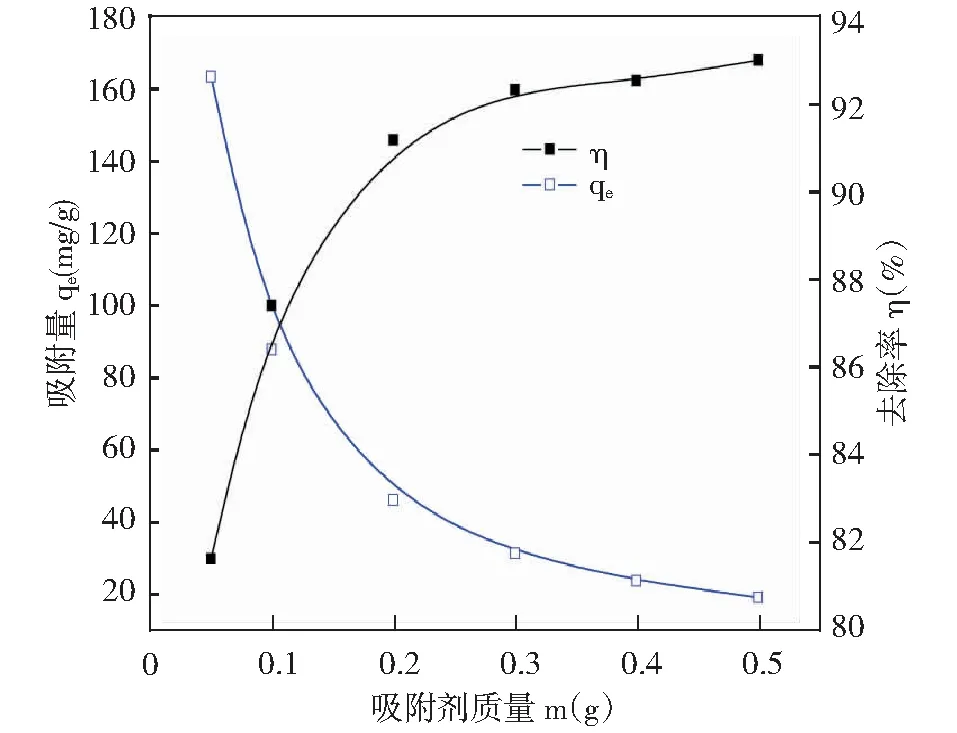
图3 吸附剂剂量对阴离子染料AF吸附效果的影响Fig.3 Effect of adsorbent dosage on the adsorption of anionic dye AF
2.4 吸附时间的影响
污染物与吸附剂之间的平衡时间在吸附法处理污水中是有重大意义的,对任一种高效率的吸附剂而言,需要在较短的时间内能够快速地摄取污染物质和达到平衡状态。从图4中可以得出,AF去除率、吸附量都随着吸附时间的增加而增加,在最初的240min内,去除率和吸附量的增加速率均较快,随后吸附速率下降直到达到饱和,去除率和吸附量基本都不再发生变化。在240min时,AF的去除率已达到90.38%,吸附量为45.19mg/g,故选择240min作为最佳吸附时间。在最开始的吸附过程中,因为溶液中有大量的吸附剂存在,所以吸附速率很快。后面吸附速率的下降可能是因为被吸附到NH2-MCM-41表面上的阴离子染料与溶液中剩余的带同种电荷的染料之间存在静电排斥作用。此外,染料分子进入到NH2-MCM-41内部的小孔扩散速率也较慢[12]。
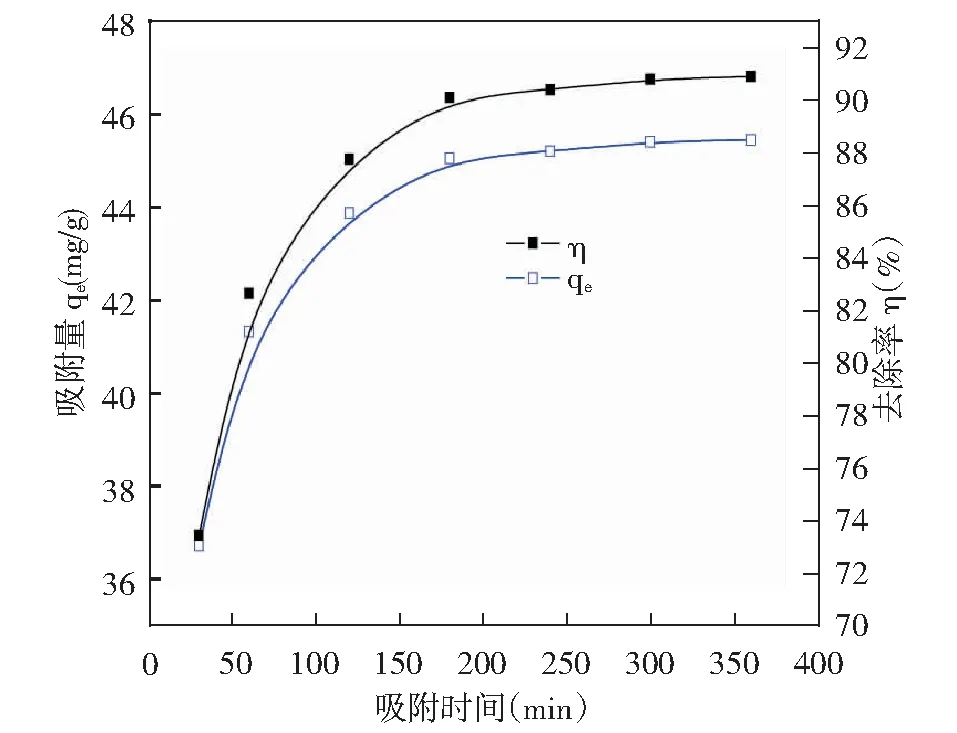
图4 吸附时间对阴离子染料AF吸附效果的影响Fig.4 Effect of adsorption time on the adsorption effect of anionic dye AF
2.5 染料初始浓度的影响
图5为不同的AF溶液初始浓度对吸附效果的影响,可以明显地看出随着染料初始浓度的增加,NH2-MCM-41的吸附量也不断增加,但是染料的去除率却逐渐减小。染料的初始浓度可以提供一种重要的驱动力,用于克服染料在水溶液与固相吸附剂之间的所有传质阻力。当溶液中AF的初始浓度升高时,吸附驱动力也随之升高,促使更多的染料分子吸附到NH2-MCM-41上,从而增加了吸附效果,提高了吸附量[13]。而初始浓度增加时,去除率却下降,这主要是受吸附剂表面上活性位点数量限制的缘故。当溶液中染料分子的浓度较低时,有充足的吸附位点用来吸附AF;但当AF浓度过高时,吸附质的数量远远多于吸附位点的数量,从而导致了去除率下降[14]。
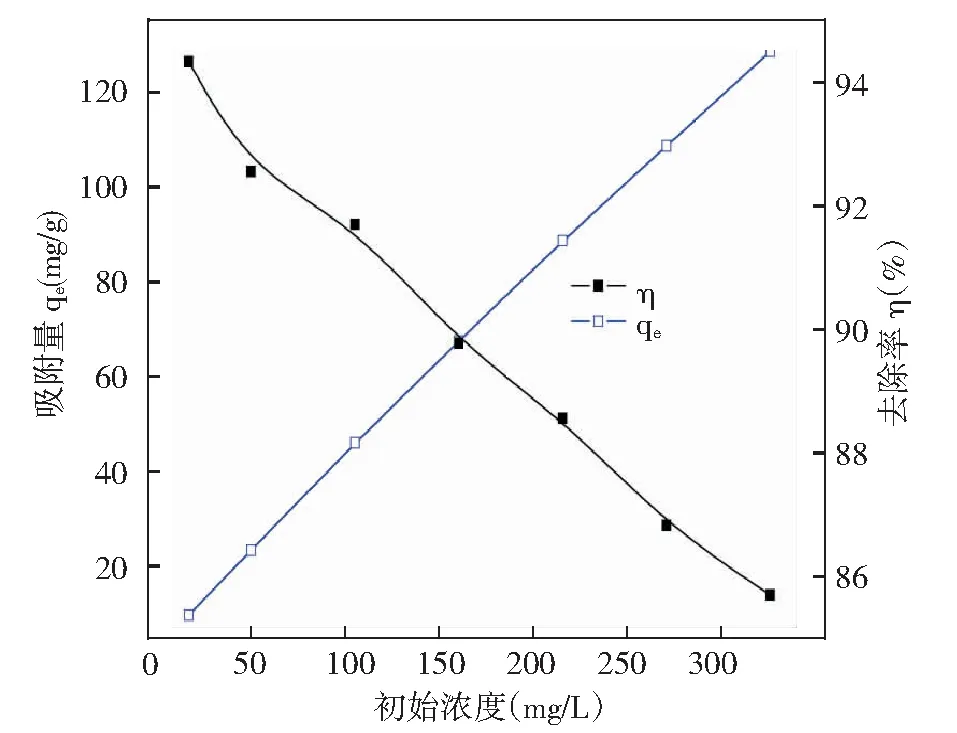
图5 染料初始浓度对阴离子染料AF吸附效果的影响Fig.5 Effect of the initial dye concentration on the adsorption of anionic dye AF
2.6 吸附等温线研究
分别采用Langmuir、Freundlich两种等温吸附模型来拟合不同温度下NH2-MCM-41的平衡吸附量与吸附平衡后溶液中剩余的染料浓度之间的关系。Langmuir模型是一个理想的单分子层吸附模型,它假设:吸附剂有均匀的表面,各处的吸附能相同;分子在固体表面为单层吸附,吸附平衡时,吸附速度与脱附速度相同[15]。Freundlich吸附等温模型是用来描述多分子层吸附的经验模型,适用于吸附剂表面不均匀的条件。
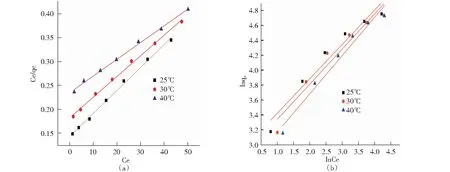
图6 AF的Langmuir模型(a)和Freundlich模型(b)等温拟合Fig.6 Langmuir(a) and Freundlich(b) isotherms for the adsorbtion of AF on NH2-MCM-41
图6为NH2-MCM-41吸附去除AF的Langmuir和Freundlich等温吸附模型拟合结果,所得参数见表2,对比相关系数R2可知NH2-MCM-41对AF的吸附可以更好地用Langmuir模型来描述,说明了该吸附过程更倾向于单层吸附。由Langmuir模型拟合结果可知,在25~40℃的温度范围内,NH2-MCM-41对AF的吸附量随着温度的上升而减小,说明该吸附过程是放热反应。Freundlich模型对AF吸附的拟合效果也较好(R2>0.90),拟合后得到的n值均在1~3之间,这表明NH2-MCM-41对AF的吸附是比较容易进行的[16]。
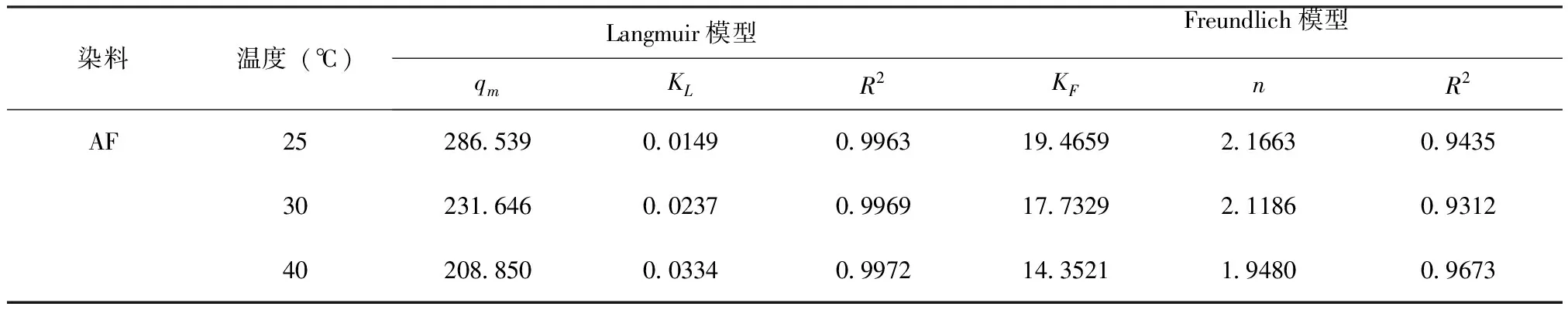
表2 NH2-MCM-41吸附AF等温线拟合参数Tab.2 Isotherm parameters for the adsorption of AF on NH2-MCM-41
2.7 吸附动力学研究
吸附动力学是评价一个吸附过程重要的物理化学因素,采用准一级动力学和准二级动力学模型对实验数据进行非线性拟合。准一级动力学模型假设吸附质占有吸附位点的速率与剩余未被占有的位点数目成正比关系[17]。准二级动力学模型假设吸附质在吸附剂上的吸附是化学吸附或者是利用电子共享或电子得失的化学吸附[18],可以用来预测整个吸附反应过程。
NH2-MCM-41吸附AF的准一级和准二级反应动力学模型拟合结果如图7所示,所得参数及相关系数见表3。比较两种动力学模型的线性相关性,准二级动力学模型对NH2-MCM-41吸附AF的动力学过程拟合效果最好,其相关系数R2值达到了0.999,也说明吸附过程为化学吸附。由准二级动力学模型得到的理论吸附容量为45.231 8mg/g,与由实验所得到的吸附容量45.442 0mg/g非常接近。
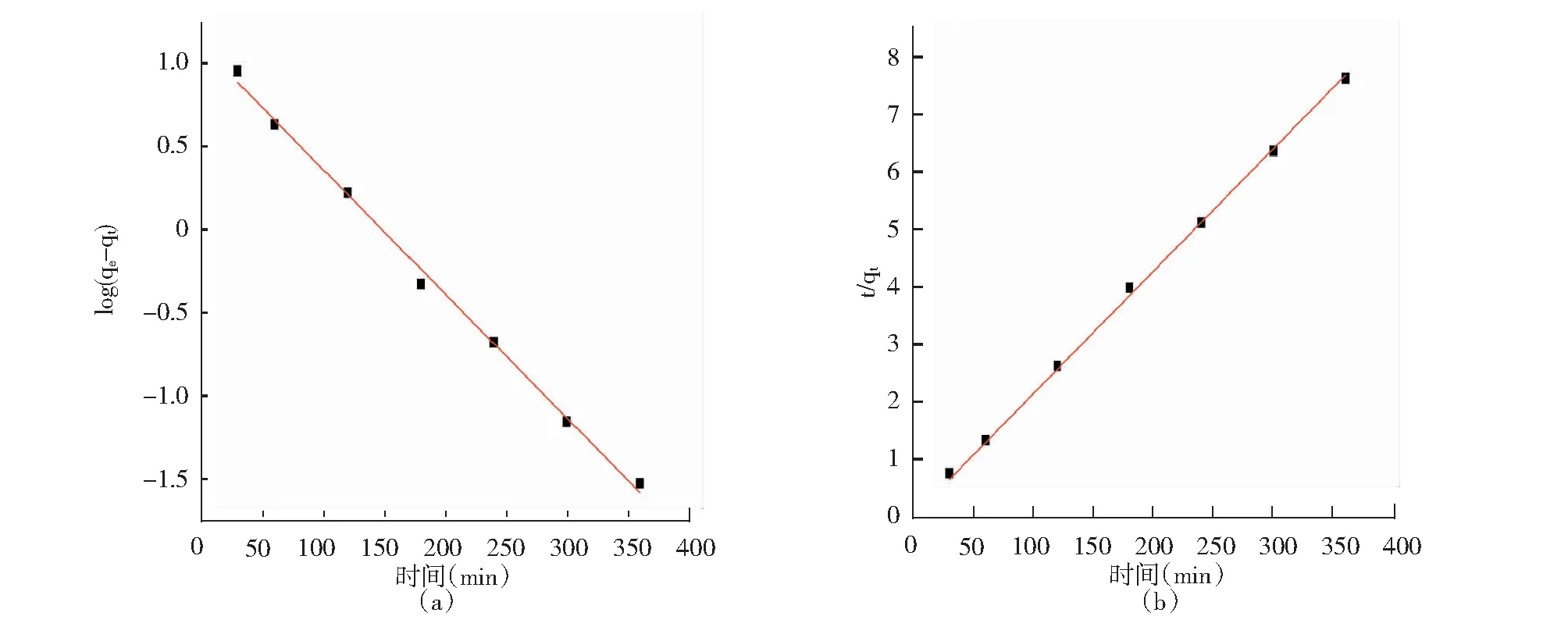
图7 AF的准一级动力学模型拟合(a)和准二级动力学模型拟合(b)Fig.7 Pseudo-first-order kinetic model(a) and Pseudo-second-order kinetic model(b) for the adsorption of AF on NH2-MCM-41
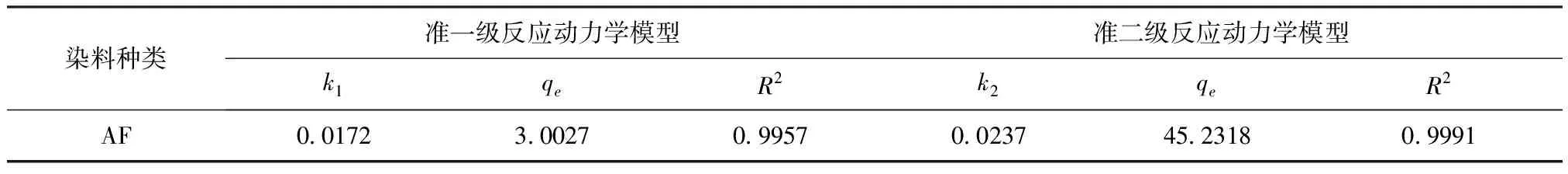
表3 NH2-MCM-41吸附AF动力学拟合参数Tab.3 Kinetic parameters for the adsorption of AF on NH2-MCM-41
2.8 解吸附研究
良好的可再生性能和重复使用率是吸附剂的一个重要指标,图8为NH2-MCM-41循环解吸附后吸附AF的去除率变化。实验得出NaOH溶液对AF的解吸效果较好,解吸率为72%,而HCl和乙醇溶液的解吸效果较差。由此可得出溶液的pH值对于解吸过程有重大影响。因为NaOH溶液中有大量的OH-,而带负电荷的AF与NH2-MCM-41
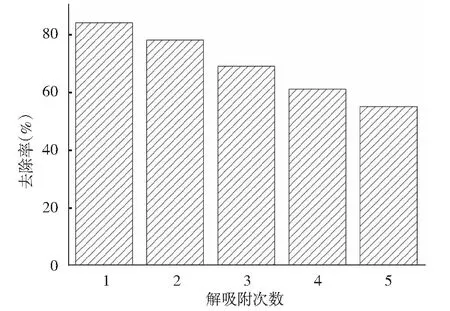
图8 NH2-MCM-41解吸附循环实验的吸附去除率Fig.8 Adsorption removal rate of NH2-MCM-41 in serial recycle tests
表面官能团的亲和力不如OH-的亲和力强,导致已吸附在NH2-MCM-41上的AF被OH-置换出来[19],从而有了较好的解吸效果。NH2-MCM-41在NaOH溶液中解吸附后,对AF的去除率呈下降趋势,这可能是在解吸附过程中吸附剂孔道内的AF未被完全洗脱下来导致的,在循环5次使用后去除率仍保持在50%以上,表明NH2-MCM-41具有较高的重复使用价值。
3 结 论
介孔材料MCM-41是一种具有良好吸附性能的新型纳米结构材料,但对于阴离子染料废水AF的吸附效果不佳,通过对MCM-41进行氨基官能团修饰改性后,可以大大提高其对AF的去除效果。在溶液pH值为3.0时,去除率和吸附量达到最大,分别为92.02%和92.02mg/g。吸附剂质量、反应时间的增加都可以提高染料的去除率,吸附平衡时间为4h。Langmuir比Freundlich等温线模型对吸附行为拟合效果更好,说明NH2-MCM-41吸附AF的反应倾向于单层吸附,动力学数据符合准二级动力学模型,吸附过程为化学吸附。NaOH溶液对吸附饱和后的NH2-MCM-41有良好的解吸附效果。NH2-MCM-41可以作为一种新型廉价高效的吸附剂用来去除AF废水,并且具有较好的再生性能和较高的重复使用价值。MCM-41在水处理领域有广泛的发展前景,并可以通过表面官能团修饰来提高吸附能力和改变吸附选择性,为加强MCM-41在印染废水治理方面的实际应用提供理论基础。
