3D 打印定制一体化半骨盆假体治疗髋臼周围原发恶性骨肿瘤短期疗效的评估
2021-08-26闵理王杰张瑀琦卢敏勋周勇张闻力罗翼王一天唐凡段宏屠重棋
闵理 王杰 张瑀琦 卢敏勋 周勇 张闻力 罗翼 王一天 唐凡 段宏 屠重棋
功能性重建骨盆肿瘤切除后残留的巨大骨缺损是骨肿瘤外科医生必须面对的巨大挑战。自 20 世纪 70 年代开始,多种非假体重建方式应运而生,包括髋关节旷置,髂 - 股骨融合或假关节重建,结构性同种异体骨重建,自体股骨重建 + 髋关节置换以及自体瘤骨灭活回植。这些方案虽然在部分患者中取得了较好的术后功能,但均存在不可避免的缺陷,比如术后长时间制动,双下肢不等长,深部感染,来源有限,骨不愈合,肿瘤复发等。
近年来,半骨盆假体重建因其初始稳定性较好、外形更易被接受以及功能恢复相对较快等因素,逐渐占据骨盆恶性肿瘤治疗的主导地位[1]。迄今为止,已知的半骨盆假体类型主要有马鞍式 (saddle) 假体、冰激凌锥形 (icecream cone) 假体、组配式 (modular) 假体和定制式 (custom-made) 假体。马鞍式假体未与宿主骨形成稳定的骨性连接,整体功能较差,并且并发症发生率较高[2-5]。冰激凌假体与宿主骨的连接更加紧密,但不适合骨盆 Ⅰ 区大部分切除的骨缺损,不能重建完整骨盆环[6-10]。组配式半骨盆假体组装灵活,且可进行骨盆环完整重建,但其安装技术要求高,假体组件间存在断裂风险,不匹配的假体与宿主骨锚定将直接影响骨整合,最终易导致松动[1,11-15]。
自 1971 年第一例定制化半骨盆假体投入临床应用起,其设计理念及方法一直在快速发展[17]。随着 3D 打印技术的应用以及假体设计进一步改良,定制化半骨盆假体的预后已经得到了长足进步[18-27]。但这种假体的设计仍存在可以改善的地方,比如一体化设计以及重建完整骨盆环。一体化设计可从整体考虑假体力学分布及传导,重建完整骨盆环可获得骨盆三维稳定进而增强假体稳定性,避免后期的假体移位、松动及断裂[21,28]。目前来看,具备这两种性质的定制假体仅由 Wong 等[29]报道过,但其应用仅为 1 例骨缺损较小的病例,并且骨盆连续性尚未被完全破坏。
因此,笔者自主设计研发了 3D 打印定制一体化半骨盆假体,并应用于临床治疗。本研究通过单中心回顾性队列研究实施 en-bloc 切除联合 3D 打印定制一体化半骨盆假体重建术治疗原发性髋臼周围恶性骨肿瘤患者,并评价其疗效。目的在于: (1) 阐述假体的设计理念;(2) 介绍相关手术技巧;(3) 评价并讨论该假体治疗原发性髋臼周围恶性骨肿瘤的早期疗效。
资料与方法
一、纳入和排除标准
1. 纳入标准:(1) 2016 年 10 月至 2017 年 5 月,我院行 en-bloc 切除联合 3D 打印定制一体化半骨盆假体重建术治疗的原发性髋臼周围恶性骨肿瘤患者;(2) 18~70 岁患者;(3) 原发性髋臼周围恶性骨肿瘤患者;(4) 接受 en-bloc 切除联合 3D 打印定制一体化半骨盆假体重建术者;(5) 随访资料完整者。
2. 排除标准:(1) 无法接受 3D 打印定制一体化半骨盆假体及其相关并发症者;(2) 合并其它严重疾病或全身评估不能耐受手术者;(3) 伴有关节内感染或其它部位活动性感染者;(4) 对金属植入物过敏者;(5) 伴有严重骨质疏松者;(6) 患侧肢体肌肉力量严重减退者;(7) 心理或精神障碍不能配合治疗者;(8) 患侧下肢其它关节 (膝、踝) 存在明显功能受损影响下肢功能评估者;(9) 随访资料不完整者。
二、一般资料
本研究经由四川大学华西医院伦理委员会批准。所有患者均签署知情同意书。
本研究共纳入 11 例,男 5 例,女 6 例;年龄为 31~65 岁,平均 45.6 岁。本组 11 例均为初治,其中累及骨盆 Ⅰ、Ⅱ 区 3 例,累及骨盆 Ⅰ、Ⅱ、Ⅲ 区 8 例,Enneking Ⅱb 级 8 例,Enneking Ⅲ 级 3 例[17,30]。
本组 11 例均以髋部疼痛伴活动受限入院,无病理性骨折患者。体格检查:患者骨盆及髋关节区 域无或稍肿胀,局部压痛明显,髋关节活动度明显降低。
所有初治患者均活检证实为原发性髋臼周围恶性骨肿瘤,其中软骨肉瘤 6 例,骨肉瘤 1 例,去分化皮质旁骨肉瘤 1 例,尤文氏肉瘤 1 例,血管肉瘤 1 例,纤维肉瘤 1 例。并完善骨盆的 X 线片、三维 CT、磁共振,双下肢站立位 X 线片,全身骨显像或 PET-CT 以及胸部薄层 CT 扫描 (图 1a,图 2a)。其中 3 例术前诊断为肺部转移。
术前通过 HHS (harris hip score) 评分系统与 MSTS (musculoskeletal tumor society scores) 评分系统进行评估[31-32]。
三、围术期处理
1. 3D 打印定制一体化半骨盆假体设计和制造:本研究中涉及假体均由华西医院骨与软组织肿瘤中心临床团队设计,并由北京春立正达医疗器械有限公司制造。个性化模拟正常的尺寸和外观是假体设计和制造的主要原则。将 CT 数据导入 Mimics V20.0 (Materialise Corp,Leuven,Belgium) 中建立虚拟三维模型,此后,利用图像融合技术将 MRI 数据整合至虚拟三维模型中用以显示肿瘤边界 (图 1b,图 2b)。术前模拟确定切除范围:软骨肉瘤边缘以外 10 mm,其它高度恶性肿瘤边缘以外 30 mm。共设计 11 个 3D 打印定制一体化半骨盆假体。其中,8 例骶髂关节无法保留,3 例骶髂关节保留,8 例耻骨上支部分保留,3 例耻骨上支完整保留。并由此共设计 4 种类型假体 (图 3)。
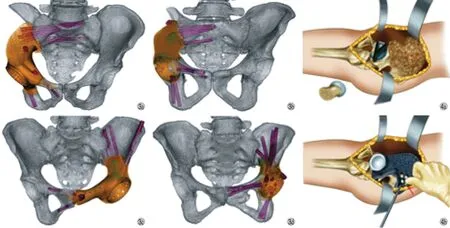
图3 针对不同骨缺损设计四大类假体 a:Ⅰ 型假体针对骨缺损累及骶髂关节但保留部分耻骨;b:Ⅱ 型假体针对骨缺损累及骶髂关节但未累及耻骨;c:Ⅲ 型假体针对骨缺损未累及骶髂关节但累及部分耻骨;d:Ⅳ 型假体针对骨缺损未累及骶髂关节及耻骨图 4 术中示意图 a:在充分暴露骨盆肿瘤后,股骨颈截骨暴露髋臼,根据术前计划使用髋臼截骨导板辅助精准截骨;b:安放假体时,优先固定耻骨后,再复位假体,行髂骨或骶骨螺钉固定Fig.3 Four types of prostheses were designed for different bone defects a: Type Ⅰ prosthesis for bone defects involving the sacroiliac joint; it will preserve part of the pubis; b: Type Ⅱ prosthesis for bone defects involving the sacroiliac joint but not the pubic bone; c: Type Ⅲ prosthesis for bone defects involving the pubis but not the sacroiliac joint; d: Type Ⅳ prosthesis for bone defects only involving the acetebulumFig.4 Intraoperative schematic diagram a: Acetabular osteotomy guide was used to assist the precise osteotomy according to the preoperative plan after acetabulum exposure following femoral neck osteotomy; b: Prosthesis should be reduced and fixed with sacrum screws after pubic bone fixation as placing
假体主体由髂骨翼缩小简化而来,髂后上下棘及坐骨棘均被移除。假体由实心结构和类骨小梁多孔结构组成。实心结构包括沿弓状缘延伸的“弧形”支撑结构,螺钉孔,髋臼和耻骨支。类骨小梁多孔结构特征为 600 μm 孔径和 70% 孔隙率。众多缝线孔沿假体嵴分布用以重建臀肌及髂肌。截骨导板固定在肿瘤侧。
所有假体在近端通过平整类骨小梁多孔表面连接切除后残留髂骨或骶骨,并用松质骨螺钉固定。在远端,3 例假体通过类骨小梁多孔半球面与残余髋臼连接,8 例假体通过类骨小梁多孔耻骨柄或者耻骨帽与残余耻骨连接。坐骨支重建由坐骨结节的保存情况决定。
假体通过电子束熔融技术生产,同时假体模型及截骨导板采用光固化技术进行生产 (图 1c,图 2c)。假体设计 (2 天)、制作 (3 天)、后处理 (2 天) 以及运输 (3 天) 共 10 天左右。
2. 手术方法:本组 11 例患者的手术均由同一名资深外科医生完成。患者均取摇摆侧卧位髂后入路联合 Smith-Petersen 入路,视肿瘤范围决定是否附加腹股沟切口。在分离过程中,髋关节周围肌肉起止点被尽可能保留。骨表面软组织被尽量分离以放置截骨导板辅助截骨。截骨完成后使用塑料模型验证截骨精确,并采用脉冲水枪反复冲洗及应用聚维酮碘浸泡术野。假体植入前,对于保留的骶髂关节面使用咬骨钳显露松质骨,对于保留的髋臼采用髋臼挫或其它方式处理骨面使骨面与假体相应部分匹配。假体在接触面处理完成后一次植入,优先固定耻骨后再复位假体行髂骨或骶骨固定。在坐骨保留的情况下,通常最后进行固定。在骨盆重建完成后,使用骨水泥将聚乙烯超半径内杯以增加 (5°~10°) 前倾角的方式固定至髋臼内,并完成股骨侧的安装及髋关节的复位。在尽可能重建肌肉前,再次采用脉冲水枪反复冲洗及应用聚维酮碘浸泡术野。手术完成后记录术中时长及术中失血量。
3. 术后处理:术后患肢处于旋转中立位,15°~25° 外展,15° 髋关节屈曲位和 15° 膝关节屈曲位,并辅以梯形枕和防旋鞋维持体位。术后 3 天内,通过 2 项测试评估髋臼周围肌力及稳定性。第一个测试是检查患者髋关节周围稳定性:患者主动保持患肢髋关节外展 15°~25°,屈曲 60°~80°,膝关节屈曲 90° 姿势的能力。第二个试验为在髋关节外展 15°~25°,屈曲 20°~30°,膝关节屈曲 30°~45° 情况下主动伸膝并维持。
若患者均顺利通过两个测试,则认为髋关节稳定性及伸膝肌力良好,符合早期康复的条件。这类患者在术后 1 周内继续同测试方案相同的锻炼方式加强髋部肌肉的力量和平衡。术后 2 周内,进行站立不负重屈髋训练。术后 2 周,患肢的负重从 10 kg 逐渐增加直到与健肢受力相等 (持续时间一般为 2 周)。术后 4 周,允许患者进行髋关节外展、内收、后伸训练,并配合助行器练习行走。
若患者难以完成任一测试,则认为髋关节稳定性差或缺乏肌肉力量,此时采用骨盆 - 大腿支具固定是必要的 (15°~25° 外展,15° 髋屈曲,15° 膝关节屈曲)。该两项测试在患者术后 2~3 周内作为日常床上训练进行。术后 3 周,患者可行站立不负重屈髋训练。术后 4 周,逐渐从 10 kg 开始负重直到增加至全重 (持续时间一般为 2 周)。术后 6~8 周行髋部外展、内收、后伸训练,并采用助行器练习 行走。
术后前 3 个月,患者睡眠情况下均需 T 型枕及防旋鞋辅助。此后,所有患者都被鼓励在没有拐杖的情况下行走,并被告知开始为期 1 周的翘二郎腿和下蹲训练 (图 1d,图 2d)。在此训练完成后患者可以不需要辅助器械行走并屈髋 ≥ 90°。
四、术后随访及疗效评价标准
手术边界由我院病理科评定并报告,用以确定肿瘤的 en-bloc 切除。
骨盆 X 线片,术后及术后前 3 个月每月 1 次,此后每 3 个月 1 次。骨盆正位片用于评价患者双下肢长度和髋臼高度、偏心距及外展角。下肢长度测量标准为,术后同侧小转子最低处与骨盆坐骨结节连线或经对侧坐骨结节与中轴线垂线的距离。髋臼高度测量标准为,同侧髋臼顶点与坐骨结节连线或对侧坐骨结节与中轴线垂线的距离。承重力臂 (bodyweight moment arm) 测量标准为髋臼中心到中轴线的距离。髋臼外展角,髋臼外侧最高点与最低点连线和中轴线之间的夹角。
骨盆三维 CT 用于评价患者髋臼假体前倾角,术后当即 1 次,以后每 3 个月检查 1 次。
评价标准为,在髋臼最大横断面图片上,以髋臼缘最前点与最后点连线和身体水平面垂线之间 夹角。
断层融合成像技术 (tomosynthesis-shimadzu metal artefact reduction technology,T-SMART) 检查用于评估骨整合情况,术后当即 1 次,以后每 3 个月检查 1 次。
肿瘤学评估记录包括局部复发、转移和死亡。功能学评估采用 MSTS 评分和 HHS 评分。并发症评估记录包括感染、脱位、松动、假体断裂、假体周围骨折等 (图 1e、f,图 2e、f)。
五、统计学处理
统计学分析采用 IBM SPSS 25.0 数据处理软件 (IBM SPSS,Armonk,NY)。术前与术后 MSTS 评分及其分项和 HHS 评分以±s形式表示,使用配对t检验用于连续变量统计学检验,检验水准 α 值取双侧 0.05。
结 果
经术后病理结果确认,术中所有患者在截骨导板辅助下获得 R0 切除。所有患者按术前计划行 3D 打印定制一体化半骨盆假体重建,术中行髋关节前屈 90°、后伸 30°、前屈 45°、外展 45° 测试,未见脱位。软组织重建中,9 例臀中肌获得重建,2 例无法重建;臀大肌,髂腰肌,缝匠肌及股直肌均良好重建。手术时间 170~540 min,平均 (287.27±109.72) min,术中出血量 900~8200 ml,平均 (3527.27±2162.53) ml。
所有患者均获平均 (27.82±1.75) 个月的随访。无肿瘤复发及死亡。术前 Enneking 分期 Ⅲ 级的患者中,1 例接受肺部转移瘤切除术,术后无肺部新发肿瘤;1 例接受化疗,在一线化疗及二线化疗均耐药后接受阿帕替尼靶向治疗,现肺部转移瘤稳定;1 例拒绝肺部手术、化疗及靶向等后续治疗,现局部未复发,肺部转移灶处于进展中。余患者无肺转移。
末次随访时,11 例均获得良好骨整合 (图 1f,图 2f)。术后双下肢长度方面,健侧小转子最低处与骨盆坐骨结节连线或经对侧坐骨结节与中轴线垂线距离为 (6.22±2.78) mm,患侧为 (6.78± 3.85) mm,双侧对比差异无统计学意义 (t= -0.691,P= 0.505)。术后髋臼高度测量方面,健侧髋臼顶点与坐骨结节连线或对侧坐骨结节与中轴线垂线的距离为 (85.26±11.52) mm,患侧为 (86.55± 12.85) mm,双侧对比无统计学意义 (t= -1.419,P= 0.186)。术后承重力臂方面,健侧髋臼中心到中轴线距离为 (98.75±3.99) mm,患侧为 (97.62± 4.28) mm,双侧对比差异无统计学意义 (t= 1.106,P= 0.294)。所有患者双下肢长度、髋臼偏心距、髋臼前倾角、髋臼外展角与术前相同。双下肢长度评价标准为,对比术前术后患侧小转子最低处与骨盆坐骨结节连线关系。髋臼高度测量标准为,以腰椎棘突连线作为中心线,以髋臼顶端向该中心线做垂线,比较双侧垂线高度差。髋臼偏心距,由髋臼中心向中心线做垂线,比较双侧垂线长度。髋臼外展角,髋臼外侧最上点与最下点连线和中心线之间的夹角。
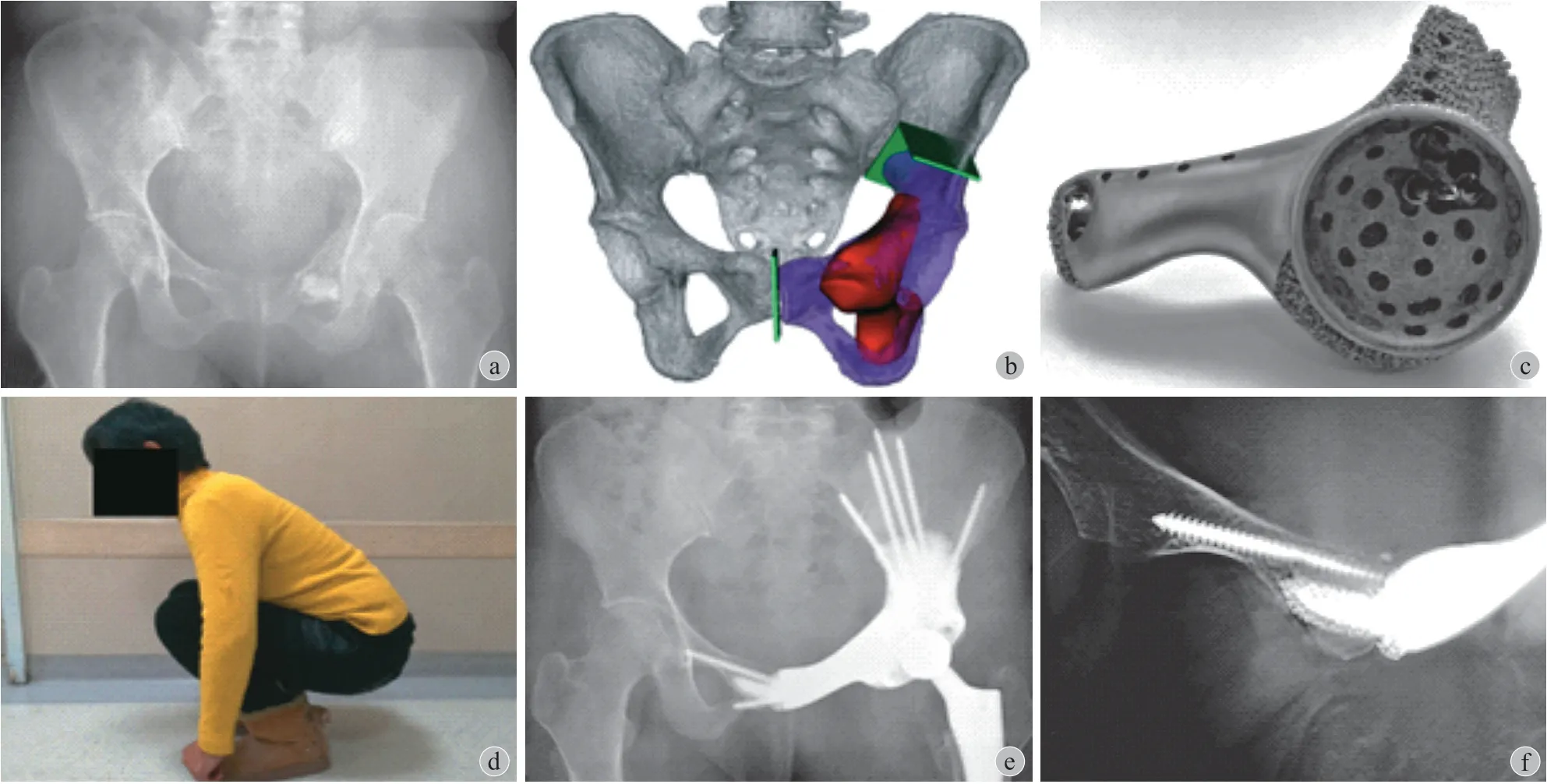
图1 a:53 岁女性骨肉瘤,术前骨盆 X 线片;b:术前手术模拟,图中可见患者左耻骨及髋臼受累;c:假体侧位观;d:该患者下蹲功能良好;e:Ⅲ 型 3D 打印半骨盆定制假体置换术后 X 线片;f:术后 2 年 T-SMART 展示良好骨整合Fig.1 a: Preoperative pelvic X-ray of a 53-year-old osteosarcoma woman; b: Preoperative surgical simulation, the left pubic bone and acetabulum were involved; c: Lateral view of the prosthesis; d: Good squatting functions; e: Postoperative X-ray image of the type Ⅲ 3D-printed hemipelvis prosthesi; f: T-Smart showed good osseointegration 2 years after surgery
骨盆三维 CT 用于评价患者髋臼假体前倾角,术后及术后每 3 个月 1 次。在横断面图片上,以 髋臼缘最前点与最后点连线和身体水平面垂线之间夹角。
本组 11 例术后患肢髋关节功能均获得明显改善,末次随访时 9 例无辅助行走,2 例扶手杖行走。术后 MSTS 评分及其相关分项 (疼痛、功能、行走、行走辅助、情感接受度、跛行) 与术前比较,其差异有统计学意义。术后 HHS 评分与术前比较,其差异有统计学意义 (表 1)。
本研究中,1 例脂肪坏死引起伤口延迟愈合,经清创一期缝合后伤口愈合。未见深部感染、假体脱位、假体或螺钉断裂等其它并发症。
讨 论
一、假体创新设计利于精准重建三维骨盆环,为骨整合提供必要条件
自 20 世纪 70 年代以来,定制化假体以其形态重建的精准化逐步成为主流。但以往的定制化假体以减材制造为主,涂层覆盖甚至于抛光的假体表面导致假体骨界面骨整合不良,进而不可避免地出现假体机械性失效[18,20,22]。得益于增材制造 (3D 打印) 技术的纵深发展和对于骨整合理论的深入理解,近期,3D 打印类骨小梁多孔结构定制化假体已被成功运用于临床[21,28-29,33-36]。然而,即便在假体骨界面获得较为满意的骨整合,组配式假体多关节连接方式依旧存在松动甚至断裂可能性。另外,骨盆肿瘤在切除后,整个骨盆环将呈现纵向与横向的移位,部分假体会以牺牲 Ⅲ 区连接来使假体植入更为便捷,但完整的骨盆环重建不仅可以增加半骨盆假体的三维稳定和改善假体重建后骨盆的力学传导,更是避免患者术后并发症的必要措施。
笔者设计并制作了一系列具有类骨小梁结构多孔表面结构的定制一体化半骨盆假体,并应用于 11 例原发性髋臼周围恶性骨肿瘤患者。
假体置换的长期目标是为了患者重返社会提供持久的静力支持。假体强度和界面骨整合能力便成为关注焦点。为了增强假体整体强度,假体内部由实心结构构成,将弓状缘支撑结构、髋臼、螺钉孔、耻骨等在内的连续于一体。骨整合能力与界面结构、初始稳定性和应力刺激有关。本研究中的假体界面均采用已被证实具有促进骨形成能力的多孔结构[37-43]。在术中,尽可能显露宿主骨小梁结构连接假体界面,辅以股骨头自体骨移植以促进骨整合。假体耻骨部分采用耻骨柄或耻骨帽等设计增大假体与残余耻骨的接触面。充分的初始稳定性可以通过设计良好的螺钉方向和三维解剖重建骨盆环实现[21]。术后康复期宜早期进行适当负重锻炼,通过适当应力刺激进一步促进假体界面骨整合,增强假体稳定性。
二、重视术前精准方案设计与围术期个性化康复利于患者功能重建
此前,采用定制化半骨盆假体临床研究显示术后患者平均 MSTS 得分在 11~22 分[18,20-22,24-25]。本研究中,MSTS 评分平均为 22 分,HHS 评分平均为 77.6 分,所有患者均能行走,其中 9 例不需要任何辅助措施。其原因包括:(1) 骨盆肿瘤通常处于较深位置,要获取良好视野需要分离众多肌肉及软组织,术前对手术入路的精确分析确定最佳手术入路可以尽可能地减少额外的肌肉损伤,从而保证保留更多的功能;(2) 术中手术导板应用减小不必要的切口暴露、减少周围正常肌肉损害的情况下达到 en-bloc 切除;(3) 完整骨盆环及原位髋臼重建保证了骨盆三维稳定及正常应力传导,为术后早期功能锻炼提供坚实基础。同时,早期负重促进骨整合,更有利于重建骨盆稳定,最终提升术后功能恢复水平[44];(4) 术中尽可能保留肌肉附着点骨组织,在重建缝合肌肉止点时,以骨 - 金属重建替代肌腱 - 金属重建,加强稳定性,利于早期锻炼;(5) 个性化术后康复计划最大化利用留存肌肉能力,从而达到较好的功能恢复。
三、注重术前手术模拟与实际手术操作利于并发症防治
定制假体重建治疗骨盆恶性肿瘤最常见的并发症包括复发 0%~33%、感染 0%~30% 和脱位 0%~20%[18-26]。
以往定制型假体研究中,术后平均复发时间为 10~22.2 个月[18-19,21-23,25-26]。本研究采用基于 CT 并融合 MRI 数据的多模态图像融合技术,生成虚拟三维图像,精准显示肿瘤范围,并通过精确的肿瘤边界分析,仔细的手术模拟,精准的手术导板设计以及严格按照计划的手术操作,最终达到良好的局部肿瘤控制。同时,对于肿瘤骨切除边界而言,在软骨肉瘤中采用了文献报道的中位切除边界 10 mm[29,36,45-46]; 而在高级别恶性肿瘤中采用了较为激进的 30 mm 作为切除边界以最大限度的控制局部复发[47]。
本研究中,伤口延迟愈合是目前惟一并发症。为了减少深部感染,本组在假体设计和围术期处理实施了 3 个步骤:(1) 该假体具有仿生流线型形态和粗糙表面多孔结构,为软组织长入提供必要条件,可有效减少术后死腔;(2) 截骨导板和塑料模型的应用,显著减少了手术和假体暴露时间; (3) 在肿瘤切除后和假体植入前,反复的脉冲水枪冲洗和聚维酮碘浸泡避免了创面感染。
为减少脱位,术前进行了对髋臼位置及方向精准设计,术中借助截骨导板精准切除及按计划重建,在适当增加前倾角情况下安置限制型聚乙烯内杯,并调整了恰当的肌肉软组织张力。
目前看来,3D 打印定制一体化半骨盆假体治疗髋臼周围原发恶性骨肿瘤早期疗效显著,使之成为骨盆恶性肿瘤重建的可靠方式。假体表面类骨小梁多孔结构有助于假体骨整合,定制一体化设计极大方便了手术时假体的精准植入。术前模拟、术中操作以及术后康复计划的注重,将进一步促进患者功能恢复以及控制术后并发症。当然,希望随着时间的推移,该假体应用于更多患者后,更确切印证该假体与宿主骨之间骨整合与其长期生物稳定性的相关性。
