液质联用法测定食品中氯酸盐和高氯酸盐
2021-08-25王浩张旭张杉于晓瑾张文超巴冬梅
王浩,张旭,张杉,于晓瑾,张文超,巴冬梅
国家食品质量安全监督检验中心(北京 100094)
含氯消毒剂是指溶于水中具有杀灭微生物的次氯酸的消毒剂,经常用于食品加工设备的消毒,因此食品中可能存在高浓度氯酸盐残留。高氯酸盐是一种环境微量污染物,除了对饮用水的直接或间接污染外,高氯酸根离子还污染环境,并经土壤-植物、水-水生生物系统进入食物链,逐级富集累积后对农产品和食品安全构成威胁。两者均可抑制人体甲状腺对碘离子的吸收,干扰其正常功能,进而影响代谢和发育,尤其是婴幼儿大脑组织的发育,引发学习障碍、发育迟缓、多动症等症状。2020年5月25日,欧盟委员会发布(EU)2020/685号条例,修订高氯酸盐在部分食品中的最大残留限量。其中,婴儿配方奶粉、婴儿食品、水果蔬菜、加工谷类食品和茶叶中高氯酸盐的最大残留限量依次为0.01,0.05,0.01和0.75 mg/kg。目前,测定氯酸盐和高氯酸盐残留的文献比较多,方法主要是离子色谱法[1-2]、离子色谱-质谱法[2-4]、高效液相色谱-质谱法[5-10]等。但是离子色谱法存在灵敏度不高、易产生假阳性等问题。离子色谱-质谱法虽然去除了干扰,提高了定性与定量的准确性和灵敏度,但流动相多为无机酸碱,不适合直接进入质谱,需先经过抑制器转换成水,检测成本较高,不利于方法的推广。液相色谱-质谱联用仪在全国基层实验室已经普遍使用,由于其对痕量残留物质精准的定性定量能力,符合目前食品安全标准所追求的高效、准确、普及的要求。该方法前处理简单,灵敏度高,适合于各类食品中氯酸盐和高氯酸盐残留的准确定性、定量分析。
1 材料与方法
1.1 材料
1.1.1 样品来源
样品,国家食品质量安全监督检验中心。
1.1.2 主要仪器与试剂
Agilent 6470A型串联三重四极杆质谱仪,配Agilent1290Ⅱ型液相色谱仪,美国Agilent公司;离心机;超声波清洗仪;去离子水发生器;涡旋混匀器。
乙腈,色谱纯(重蒸),德国Fisher公司;氯酸盐和高氯酸盐标准溶液(1 mg/mL):北京振祥公司;氯酸盐-18O3(200 μg/mL)、高氯酸盐-18O4(100 μg/mL)标准溶液:美国剑桥公司;PRiME HLB固相萃取柱(200 mg/6 mL,美国Waters公司)。
1.2 方法
1.2.1 标准溶液的配制
分别准确量取100 μL 1 mg/mL氯酸盐和高氯酸盐标准溶液,用超纯水稀释至100 mL,制成氯酸盐、高氯酸盐质量浓度分别为1 μg/mL的混合标准中间液,于4 ℃保存。使用时用水逐级稀释成0.50,1.00,2.00,5.00,10.0,20.0和50 ng/mL的标准工作液。其中,标准工作液中氯酸盐同位素内标溶液质量浓度为5.0 ng/mL,高氯酸盐同位素内标溶液质量浓度为2.0 ng/mL,现配现用。
1.2.2 样品前处理
包装饮用水:称取1.00 g(精确至0.01 g)试样,加入10.0 μL同位素内标中间液,涡旋振荡10 s,供液相色谱-串联质谱仪测定。
液态样品:称取1.00 g(精确至0.01 g)试样,加入50.0 μL同位素内标中间液,用乙腈定容至5 mL,具塞后剧烈振摇片刻,超声提取10 min,吸取1 mL上清液,过PRiME HLB固相萃取柱,弃去前5滴,过0.22 μm有机滤膜,供液相色谱-串联质谱仪测定。
固态样品:称取1.00 g(精确至0.01 g)试样,置于250 mL玻璃离心管中,加入100.0 μL同位素内标中间液,再加入10.0 mL 70%乙腈水溶液,涡旋30 s,超声提取40 min,吸取1 mL上清液,过PRiME HLB固相萃取柱,弃去前5滴,过0.22 μm有机滤膜,供液相色谱-串联质谱仪测定。
乳粉:准确称取1 g(精确至0.01 g)试样,置于10 mL玻璃离心管中,依次加入100.0 μL同位素内标中间液和2.0 mL 50 ℃左右热水,涡旋10 s,用乙腈定容至刻度,具塞后剧烈振摇片刻,使蛋白质沉淀,超声提取10 min,吸取1 mL上清液,过PRiME HLB固相萃取柱,弃去前5滴,过0.22 μm有机滤膜,供液相色谱-串联质谱仪测定。
茶叶:准确称取1 g(精确至0.01 g)试样,置于250 mL玻璃离心管中,加入200.0 μL同位素内标中间液,再加入20.0 mL 70%乙腈水溶液,涡旋30 s,超声提取40 min,先取2 mL上清液于玻璃离心管,在4 ℃和10000 r/min条件下离心5 min,取1 mL离心液过PRiME HLB固相萃取柱,弃去前5滴,过0.22 μm有机滤膜,供液相色谱-串联质谱仪测定。
1.2.3 仪器条件
色谱条件:色谱柱为资生堂PC HILIC柱(150 mm× 2.0 mm,5 μm);流速0.22 mL/min,柱温25 ℃,进样量1 μL,流动相为乙腈+20 mmol/L乙酸铵水溶液(25∶75,V/V)。
质谱条件:负离子模式扫描,雾化气压力413.8 kPa;干燥气温度350 ℃,干燥气流速10 L/min。
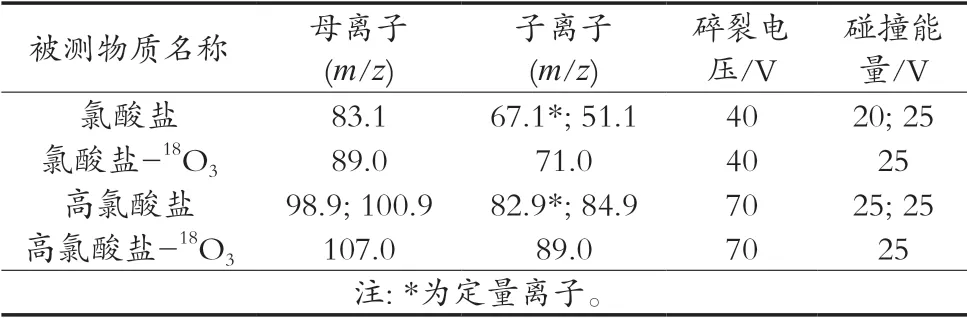
表1 氯酸盐和高氯酸盐的质谱参数
2 结果与讨论
2.1 样品前处理条件选择
氯酸盐和高氯酸盐都是常见的环境污染物,溶于水和乙醇。因此,该法首先用水溶解乳粉样品,然后再用有机试剂去除蛋白。分别比较乙醇、乙腈、丙酮、氯仿有机试剂的除蛋白效果,结果发现乙腈能有效去除样品中蛋白质,其余几种去除蛋白效果不好。比较超声时间对阳性样品提取效率的影响,采用建立的检测方法测定婴幼儿营养米粉,当超声时间为10,20,30,40和50 min时,氯酸盐的测定值分别为25.1,31.5,36.7,40.6和41.3 μg/kg,高氯酸盐的测定值分别为10.4,13.6,19.5,25.7和26.2 μg/kg。试验证明,固态样品超声处理40 min能充分提取出目标化合物。因为高氯酸盐为环境污染物,很多溶剂(甲醇、乙腈等)均可能存在,所以试验中使用的乙腈需要重蒸处理。
分别对比PRiME HLB(6 mL/200 mg)固相萃取柱、Oasis HLB(6 mL/200 mg)固相萃取柱、安杰尔C18(6 mL/200 mg)固相萃取柱、安杰尔 PCX(6 mL/ 200 mg)固相萃取柱中的净化效果,结果发现PRiME HLB(6 mL/200 mg)固相萃取柱效果比较好,其能吸附非极性干扰物质而不影响目标化合物的回收率,特别是对基质中脂肪和磷脂,去除效率高达95%以上。同时,其操作简便,无需活化平衡,可以直接过柱;试验发现:当提取液中乙腈含量低于50%时,氯酸盐内标和高氯酸盐内标过PRiME HLB(6 mL/200 mg)固相萃取柱时会被部分吸附,从而造成定量不准确,因此选择70%乙腈水溶液为样品的提取溶液。
2.2 同位素内标选择
基质效应是指样品中除目标分析物以外的其他成分对待测物测定值的影响,抑制或者增强目标化合物响应的现象。比较目标化合物在基质中与纯溶剂中的标准曲线的斜率来评价氯酸盐和高氯酸盐在各种食品基质(包装饮用水、乳粉、米粉、牛奶、茶叶、苹果等)中的基质效应,目标化合物在基质中与纯溶剂中斜率比值小于1,表明基质对其具有电离抑制作用;比值大于1,表明具有电离增强作用。试验发现:除包装饮用水外,氯酸盐和高氯酸盐在其他基质中均为电离抑制作用,比值均低于0.80(包装饮用水除外)。同时,在实际检测过程中,较难获取全空白基质进行基质加标或基质匹配定量,因此有必要采用同位素内标法来弥补前处理过程中差异对于检测定量结果影响,提高方法定量的准确性。试验选择氯酸盐-18O3和高氯酸盐-18O4为内标物质。
2.3 分析性能
用标准系列工作液,分别进样2 μL,测定结果经线性回归(y为峰面积;x为浓度,μg/L),同时用空白样品,定量添加标准溶液,按照方法中介绍的步骤操作,当所得谱图的信噪比大于3时,将此添加量定为最低检出限;当信噪比大于10时,将此添加量定为最低定量限,结果见表2。

表2 氯酸盐和高氯酸盐的线性方程、线性范围、相关系数、方法定量限及检出限
2.4 方法的回收率和精密度
分别选取具有代表性的样品进行回收率与精密度试验。准确称取包装饮用水、茶叶、液体乳、饮料、饼干、鱼肉、番茄、苹果、婴幼儿配方乳粉、婴幼儿营养米粉及婴幼儿果泥等典型样品,各6份,每份1.0 g,共3组,分别定量加入氯酸盐和高氯酸盐标准物质。考虑到很难找到阴性样品,为了更好考察方法的回收率与精密度,加标水平分别设定为10,20和50 μg/kg,按样品前处理进行测定。结果表明,不同浓度平均加标回收率为80.1%~119.5%,平均相对标准偏差为2.1%~9.9%(n=6)。
2.5 实际样品检测
使用该方法对市售的100份食品进行检测,共检出97份阳性样品,含量在0.51~817 μg/kg,检出率达98.0%,其中茶叶残留量较高。上述结果表明,我国食品中确实存在氯酸盐和高氯酸盐残留,其对消费者健康存在的风险,应当引起重视。

表3 婴幼儿配方乳粉样品氯酸盐和高氯酸盐的加标回收率 单位:%

图1 含氯酸盐和高氯酸盐的阳性样品MRM色谱图
3 结论
采用固相萃取技术结合液相色谱-串联质谱法,建立一种高效检测食品中氯酸盐和高氯酸盐的检测方法。优化前处理方法,样品不需要固相萃取柱活化等繁琐步骤,样品提取液可以直接通过固相萃取柱净化。该方法能够进行准确的定性与定量,前处理简单,准确性和灵敏度均能满足食品中氯酸盐和高氯酸盐的测定要求。该方法可为相关执法监督和食品生产企业质量控制提供科学依据,为我国的食品质量安全工作给予技术支持。
