液相色谱-串联质谱法测定食品接触材料及制品中新戊二醇迁移量
2021-08-24李泽荣郭旭东凌光耀陈意光熊小婷郭培春刘德云吴晓纯谢文缄黄晓钢
李泽荣,郭旭东,凌光耀,陈意光,熊小婷,李 露,郭培春,刘德云,吴晓纯,谢文缄,黄晓钢
(广州质量监督检测研究院,国家包装产品质量监督检验中心(广州),广东 广州511447)
新戊二醇(又名2,2-二甲基-1,3-丙二醇,简称NPG),是一种无色无味的结晶或结晶性固体,具有吸湿性,易溶于水以及低级醇、低级酮、醚、芳烃化合物等,不易溶于脂肪烃和脂肪族烃[1]。NPG的分子结构中在对称位置有2个伯醇羟基,因此具有良好的反应性能,其中心碳原子上连接4个碳原子而无α氢原子的特点,使其衍生产品具有良好的耐水、耐热和耐光性能[2-3]。目前,NPG主要用于生产不饱和聚酯树脂、饱和聚酯树脂、醇酸树脂、聚氨酯和聚合物增塑剂等,此外在医药、农药生产等领域也有重要用途[4-8]。然而,NPG具有一定毒性,人体一旦摄入过量会对健康造成危害,如可能对中枢神经系统产生刺激性,引起呕吐、疲倦、昏睡、呼吸困难、震颤等症状,此外也可能引起肾脏充血和出血、肝脏脂肪病变、闭尿、支气管炎和肺炎等症状,严重者甚至导致死亡。
在食品接触材料及制品领域,NPG主要用于塑料材料及制品、涂料、涂层以及粘合剂的生产中。如果原料、配方、生产工艺等生产要素的质量控制不严,NPG可能残留在产品中,并迁移进入食品,进而影响人体健康和安全。因其潜在危害性,欧盟和我国食品接触材料及制品的相关法规和标准中均对其限量做出了明确规定。欧盟法规(EU)No.10/2011[9]和我国标准GB 9685-2016《食品安全国家标准食品接触材料及制品用添加剂使用标准》[10]中均明确规定NPG的特定迁移限量(SML)为0.05 mg/kg。
目前,针对NPG的检测研究主要集中于反应体系和原料中NPG的含量和纯度分析方面,主要有气相色谱法、差示扫描量热法和化学分析方法[11-15]。近年来,随着GB 9685-2016等食品接触材料及制品相关食品安全国家标准的实施,相关风险物质的迁移量检测研究报道越来越多[16-18],为该类产品的质量控制提供了技术支持,同时也为相关检测方法标准的制订提供了数据支持和方法参考。相关法规和标准对于食品接触材料及制品中的NPG迁移量虽有限量要求,但尚无相应的检测方法标准,也尚未见相关检测研究报道。因此,针对食品接触材料及制品中的NPG迁移量开展检测方法研究具有重要意义。本文建立了食品接触材料及制品中NPG迁移量的液相色谱-串联质谱测定方法,所建方法包括水、4%(体积分数)乙酸、乙醇溶液(体积分数分别为10%、20%、50%、95%)和橄榄油等食品模拟物,检出限满足欧盟和我国相关法规与标准的限量要求。
1 实验部分
1.1 仪器与试剂
TSQ Quantiva高效液相色谱-串联质谱仪(美国Thermo Fisher公司);Milli-Q超纯水器(美国Millipore公司),分析天平(感量为0.1、0.01 mg)。
新戊二醇标准品(CAS No.126-30-7,纯度98%,美国Panphy公司);甲醇、乙腈、乙醇(色谱纯,美国Spectrum公司);甲酸(色谱纯,上海安谱实验科技股份有限公司);乙酸(分析纯,广州化学试剂厂);橄榄油(分析纯,上海麦克林生化科技有限公司);实验用水为超纯水。
1.2 标准溶液的配制
准确称取适量NPG标准品(精确至0.01 mg),用甲醇配制成质量浓度约为1 000 mg/L的标准储备溶液,于-20℃下保存。
1.2.1水基、酸性、乙醇类模拟物工作溶液的制备准确移取适量标准储备溶液于100 mL容量瓶中,用水配制成质量浓度为1 mg/L的标准中间溶液,于4℃下保存。使用时以10%乙醇溶液稀释成质量浓度分别为10、20、50、80、100 μg/L的标准工作溶液。
1.2.2 油基模拟物工作溶液的制备准确移取适量标准储备液于100 mL容量瓶中,用10%乙醇溶液配制成质量浓度为1 mg/L的标准中间溶液,于4℃下保存。
分别称取(2.00±0.01)g橄榄油于6个10 mL比色管中,依次加入0.000、0.020、0.040、0.100、0.160、0.200 mL标准中间溶液,涡旋混匀,得到含量分别为0、10、20、50、80、100 μg/kg的标准工作溶液。分别在上述比色管中加入2.00、1.98、1.96、1.90、1.84、1.80 mL 10%乙醇溶液,涡旋混合5 min,以1 000 r/min离心5 min,取下层清液过0.22 μm水性滤膜后待测。
1.3 样品前处理
1.3.1 迁移试验按照GB 5009.156-2016[19]及GB 31604.1-2015[20]的要求,对样品进行迁移试验,迁移液置于4℃冰箱中避光保存。进行下一步处理前先将迁移液恢复至室温。
1.3.2 迁移液前处理对于水、4%乙酸、10%乙醇迁移液,取约1 mL过0.22 μm水性滤膜后待测;对于20%乙醇、50%乙醇、95%乙醇迁移液,取5.0 mL于10 mL比色管中,45℃氮吹浓缩至体积分别约为4、2.5、0.5 mL,放至室温后用水重新定容至5 mL,涡旋混匀后取约1 mL过0.22 μm水性滤膜,待测;对于橄榄油迁移液,称取(2.00±0.01)g(精确至0.01 g)样品于比色管中,加入2 mL 10%乙醇溶液,涡旋混合5 min,以10 000 r/min离心5 min,取水层约1 mL过0.22 μm水性滤膜,待测。
1.4 实验条件
1.4.1 色谱条件色谱柱:ACQUITY UPLC®BEH C18柱(50 mm×2.1 mm,1.7 μm)。流动相:0.01%甲酸溶液(A)-乙腈(B),梯度洗脱:0~1.5 min,8%B;1.5~1.6 min,8%~90%B;1.6~5.0 min,90%B;5.0~5.1 min,90%~8%B;5.1~9.0 min,8%B。流速:0.25 mL/min;柱温:室温;进样量:5 μL。
1.4.2 质谱条件离子源:电喷雾离子源(ESI);扫描模式:正离子模式;检测模式:多反应监测(MRM);喷雾电压:4 000 V;鞘气(N2):40 Arb;辅助气(N2):25 Arb;吹扫气(N2):3 Arb;气化温度:350℃;离子传输管温度:350℃;质谱参数如下:保留时间为1.12 min,定量离子对为m/z105>45.1,定性离子对为m/z87>45.1,对应的碰撞能量分别为16、10 eV,透镜电压均为30 V。
2 结果与讨论
2.1 色谱柱的选择
NPG属于强极性小分子化合物,因此选择反相色谱柱作为分析柱。考察了可兼容100%水性流动相的Accucore AQ(50 mm×2.1 mm,2.6 μm)和ACQUITY UPLC HSS T3(50 mm×2.1 mm,1.8 μm)色谱柱,以及应用范围较广的ACQUITY UPLC®BEH C18(2.1 μm×50 mm,1.7 μm)3种不同类型色谱柱对NPG的分离效果(见图1)。结果显示,NPG在Accucore AQ柱上的保留较弱,易受到杂质干扰;在HSS T3和BEH C18柱上均可获得较好的保留。考虑到C18柱在日常检测中使用较广泛,本文选择BEH C18作为色谱分析柱。
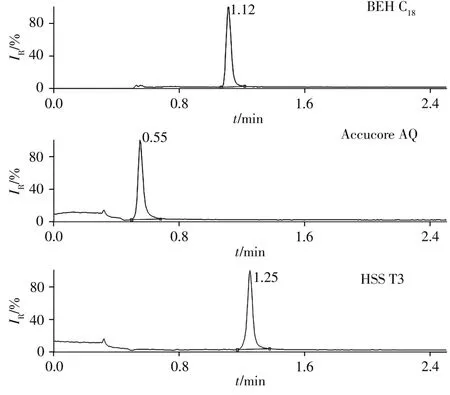
图1 NPG在3种色谱柱上的色谱图Fig.1 Chromatograms of NPG on three different columns
2.2 流动相的选择
对比考察了甲酸溶液-乙腈、甲酸溶液-甲醇作为流动相对NPG色谱分离效果和质谱响应的影响。结果显示,采用甲酸溶液-甲醇作为流动相时,NPG的基线较高,而采用甲酸溶液-乙腈作为流动相可获得较好的保留,且基线较低,因此选择甲酸溶液-乙腈作为流动相。进一步对比了甲酸溶液-乙腈流动相中甲酸含量分别为0.005%、0.01%、0.1%时的影响,结果显示,采用0.01%甲酸溶液时NPG的响应最高。因此最终选择0.01%甲酸溶液-乙腈作为流动相。
2.3 前处理条件的选择
采用水、4%乙酸和10%乙醇进行迁移试验后的迁移液较澄清,无明显基质效应,过滤后可直接测定。采用20%乙醇、50%乙醇、95%乙醇进行迁移试验后的迁移液也较澄清,但直接测定会产生溶剂效应,且乙醇浓度越高,溶剂效应越明显,因此,本研究采用氮吹方式去除大部分乙醇后,重新用水定容,以降低溶剂效应。橄榄油迁移液采用10%乙醇提取1次即可得到理想的提取回收率,且基质效应小,可满足分析要求。
2.4 质谱条件的优化
NPG是具有典型新戊基结构的二元醇,易得到H形成[M+H]+的母离子(m/z105),因此选择在电喷雾源正离子模式下进行分析。进行一级质谱扫描时发现,除了m/z105的峰外,m/z87的峰响应强度也很大,可能原因为[M+H]+在源内发生裂解,产生了脱去1个水分子的离子,即[M+H-H2O]+(m/z87)。对m/z105和m/z87的母离子进行二级质谱分析,结果显示,两个母离子均只有m/z45.1的子离子可得到较好的响应强度,因此选择m/z105>45.1和m/z87>45.1作为监测离子对,其中m/z105>45.1作为定量离子对。对监测离子对的碰撞电压等质谱参数进行进一步优化,优化后NPG的多反应监测色谱图见图2。

图2 NPG的多反应监测色谱图Fig.2 Multiple reaction monitoring chromatograms of NPG
2.5 方法的线性范围与检出限
分别取“1.2.1”和“1.2.2”配制的工作溶液,在“1.4”实验条件下测定。以NPG的质量浓度(x)为横坐标,相应峰面积(y)为纵坐标,绘制标准曲线,得到NPG的线性范围、线性方程和相关系数。结果表明,对于水基、酸性、乙醇类模拟物,NPG在10~100 μg/L质量浓度范围内线性关系良好,线性方程为y=3 823x+5 359,相关系数为0.999 7,检出限(LOD,S/N≥3)可达5 μg/L,定量下限(LOQ,S/N≥10)可达10 μg/L;对于油基食品模拟物,NPG在10~100 μg/kg范围内线性关系良好,线性方程为y=3 896x-2 667,相关系数为0.999 9,LOD为5 μg/kg,LOQ为10 μg/kg(由于工作溶液制备方式不同,采用的浓度单位与其他模拟物不同)。NPG在不同食品模拟物中的检出限和定量下限均低于相关法规和标准中规定的限量值,可满足检测需求。
2.6 方法精密度及回收率
选取塑料、涂层、橡胶3种典型食品接触材料及制品的空白样品,分别用水、4%乙酸(AcOH)、10%乙醇(EtOH)、20%乙醇、50%乙醇、95%乙醇和橄榄油作为食品模拟物,按照“1.3.1”进行迁移试验,分别向迁移液中添加低、中、高3个浓度水平的标准溶液,按“1.3.2”进行前处理后测定,每个添加浓度平行测定6次(见表1)。结果显示,在3个加标水平下,NPG的加标回收率为92.8%~117%,相对标准偏差(RSD)为0.90%~8.6%,可满足NPG迁移量的测定要求。
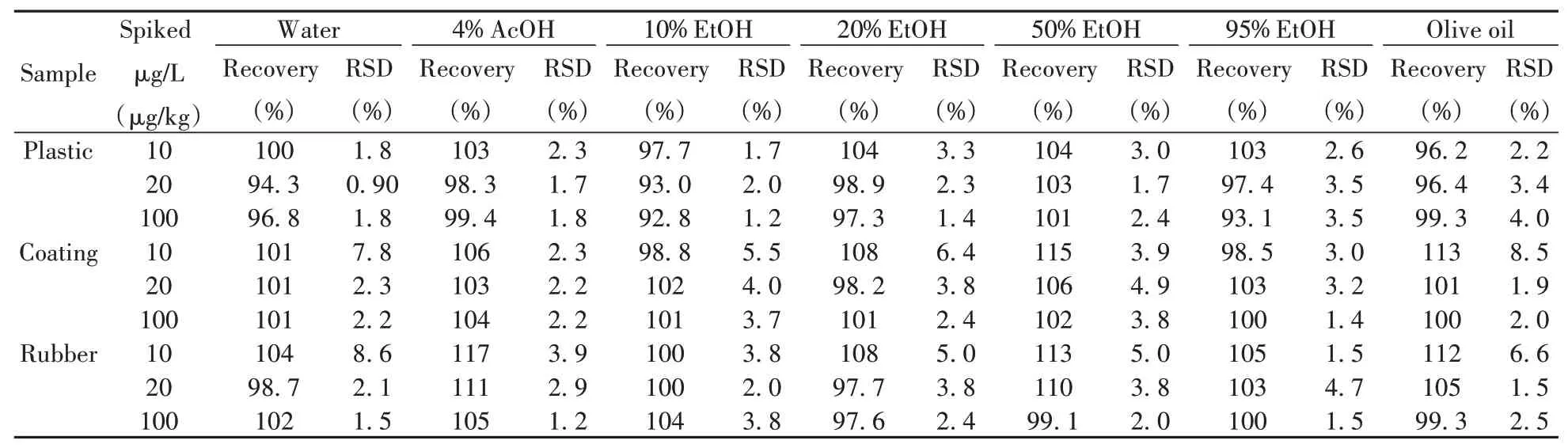
表1 NPG的回收率及相对标准偏差(n=6)Table 1 Recoveries and RSDs of NPG(n=6)
2.7 实际样品检测
本文采用建立的方法对30份不同材质的食品接触材料样品进行测定,样品类型包括塑料食品包装、有内涂层的食品金属罐、橡胶制品等。检测结果显示,30份样品中均未检出NPG。
3 结论
本文建立了一种食品接触材料及制品中NPG迁移量的液相色谱-串联质谱分析方法。所建方法操作简单易行,基本包括了相关标准涉及的食品模拟物类型,检出限低于法规和标准中NPG的特定迁移限量,具有较强的适用性,可为相关产品质量监控提供科学依据和技术支持。
