多学科协作诊疗模式在救治凶险性前置胎盘中的应用>
2021-08-20胡燕钱惠勤季璇史天一王丽平乔东艳朱光宇李嘉刘松乔孙杰于红
胡燕,钱惠勤,季璇,史天一,王丽平,乔东艳,朱光宇,李嘉,刘松乔,孙杰,于红>
(1.东南大学附属中大医院 妇产科,江苏 南京 210009; 2.东南大学附属中大医院 介入科,江苏 南京 210009;3.东南大学附属中大医院 超声科,江苏 南京 210009; 4.东南大学附属中大医院 重症医学科,江苏南京 210009; 5.东南大学附属中大医院 麻醉科,江苏 南京 210009)
自2016年二胎政策实施以来,凶险性前置胎盘(pernicious placental previa,PPP)患者呈明显递增趋势,PPP是引起孕妇致命性术中出血、育龄期妇女子宫切除及严重术中、术后并发症的主要原因[1]。对于产科医生来说,减少术中和产后出血、保留子宫和减少并发症是一个巨大的挑战。PPP目前尚无标准的诊疗模式,我院利用自身学科优势,于 2016年成立多学科协作诊疗(multidisciplinary diagnosis and treatment,MDT)团队,针对PPP患者从术前讨论评估、术中协作及术后管理制定个体化诊疗方案,取得了良好的临床应用效果。本研究回顾性分析46例PPP患者的临床资料,旨在探讨MDT在PPP处理中的临床意义。
1 资料与方法
1.1 一般资料
选择我院 2016年1月至2020 年12月收治的前置胎盘孕妇138例,年龄27~44岁,平均(32.43±4.00)岁;孕周21+5周~39+3周,平均(34.21±3.77)周。其中通过彩色多普勒超声或MRI 检查明确诊断为PPP和术中发现为胎盘植入共计46例,发生率为33.33%(46/138)。见表1。
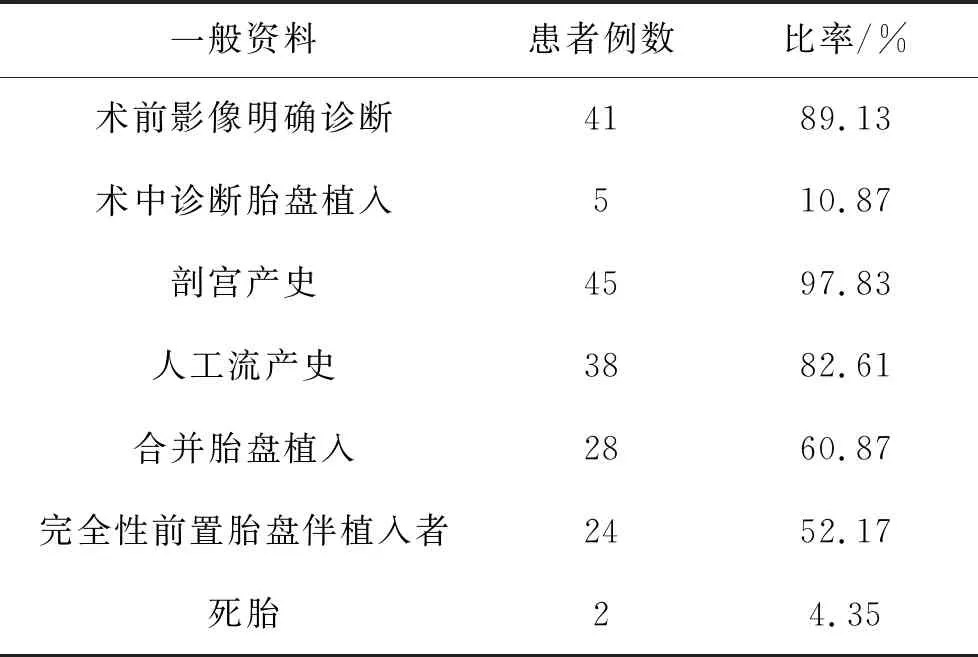
表1 PPP患者临床信息
1.2 救治策略与方法
由医务处和产科牵头组织重症医学科(Intensive Care Unit,ICU)、新生儿重症监护病房、麻醉科、手术室、输血科、泌尿外科、影像科、介入血管科等多学科联合讨论制订计划、手术分级、相关人员配备,做好各科室之间衔接协调,各科室医务人员提前做好抢救母婴准备,备好应急处理方案。
1.2.1 入院管理 (1) 仔细核对孕周。(2) 完善检查:① 实验室检查:血型、血细胞分析、尿常规、纤溶功能、生化全套、病毒8项;② 影像学检查:产科高危超声、胎盘植入评分、B超(肝、胆、胰、脾、双肾、输尿管、膀胱)、盆腔3.0核磁共振成像(Nuclear Magnetic Resonance Imaging,MRI)平扫(测量双侧髂内动脉直径)、心电图、心脏彩超。(3) 术前处理:① 铁剂,维持Hb≥110 g·L-1;② 促进胎儿肺成熟:无症状者于妊娠34~36 周予地塞米松[2];有反复出血及早产征象者在妊娠34周前促胎肺成熟。(4) 分娩时机:① 病情稳定者建议在妊娠34~36+6周择期手术终止妊娠[2];② 发生持续性出血、子痫前期、先兆早产、胎膜早破、胎儿并发症或孕妇病情恶化等威胁母儿生命的情况,应提前终止妊娠[2]。
1.2.2 术前管理 (1) 组建MDT团队,具体如下:① 产科或母胎医学科:孕期诊断咨询,进行产前评估、产时和产后的管理;② 麻醉科:术前评估决定麻醉方式,术中管理生命体征及大出血;③ 影像科:超声和MRI诊断,明确胎盘位置及植入深度和广度,明确腹主动脉、髂总动脉及盆腔血管的宽度;④ 介入科:术前、术中放置球囊及术后介入栓塞;⑤ 输血科:血制品和(或)自体输血管理;⑥ ICU:术后病人的监护管理;⑦ 新 生儿病房:处理早产儿和急诊手术高危儿;⑧ 泌尿外科:术前决定是否放置输尿管支架,术中修复输尿管、膀胱损伤;⑨ 其他科室:如血管外科行血管损伤修复[2]。(2) 术前任务分配:① 充分沟通,详细告知母儿结局;② 再次核对实验室及影像检查结果,完善疑难病例讨论、术前讨论及医务科重大手术审批手续。(3) 人员分配,手术台上下3~5名医师:① 联系血库充足备血(悬浮少白红细胞∶去病毒灭活血浆∶血小板比例为1∶1∶1,如术中出血超过1 500 ml可考虑自体血过滤后回输);② 备好急查采血管(血常规、纤溶功能、生化+电解质);③ 记录紧急联系电话(检验科、介入科、输血科、ICU、新生儿病房、产房等);④ 联系产房准备围手术期所用物品(缩宫素、欣母沛、卡贝缩宫素、麦角新碱、米索前列醇、宫腔球囊、填塞纱条);⑤ 联 系手术室准备止血带及直针,备好自体血回输装置。
1.2.3 术中管理 (1) 血管球囊预置:根据超声及MRI显示的胎盘植入程度合理选择:完全胎盘植入和穿透性胎盘植入者术前至介入科行髂内血管球囊预置术,术中每次阻断时间最长60 min,释放时间5~10 min。如出血较少,可抽空球囊,保留球囊导管在髂内动脉并继续观察3~24 h,如有出血随时充盈球囊;如出血仍较多,则在髂内动脉继续留置充盈的球囊导管,若无继续出血,24 h内可根据情况在病房拔除球囊导管及导管鞘。剖宫产术后在股动脉穿刺点局部血管封堵后加压包扎,如术中及术后仍然无法有效止血,可在患者生命体征平稳的情况下至数字减影血管造影(digital subtraction angiography)手术室行双侧子宫动脉栓塞术(uterine artery embolization, UAE)。(2) 麻醉管理:麻醉方式可为蛛网膜下腔及硬膜外阻滞联合麻醉和经气管全身麻醉,具体方式应根据患者胎盘植入程度、估计出血量、手术治疗方案及手术时间综合考虑[3]。(3) 体位:患者取“大”字位平躺,臀下铺引流袋,便于术中观察阴道出血。(4) 产后出血防治办法:① 三部曲:使用宫缩剂、按压腹主动脉、控制性牵拉脐带,必要时延迟断脐;② 辅助措施:宫腔填塞、子宫压迫缝合、U型缝合术及子宫、髂内动脉结扎术等。(5) 胎盘处理:① 胎盘剥离:胎盘粘连或胎盘植入者可在子宫血流暂时阻断情况下谨慎剥离,或行部分胎盘和(或)部分子宫壁切除,剥离面出血部位缝合,必要时行子宫下段环行缝扎术,然后行子宫缝合和(或)子宫重建[3]。② 胎盘原位保留:无明显出血的胎盘植入或穿透性胎盘植入者,且满足患者要求保留生育功能,具备及时输血、紧急子宫切除、感染防治等条件的可选择胎盘原位保留[4]。(6) 子宫切除术指征:产前或产时子宫大量出血、保守治疗效果差或保守治疗过程中出现严重出血及感染[5];子宫破裂修补困难;其他因素需切除子宫。(7) 异体输血联合自体回输血。(8) 手术时间>3 h和(或)出血量>3 000 ml,术中应加用抗感染药物,必要时放置腹盆腔引流管。
1.2.4 术后管理 (1) 经导管动脉栓塞:保守治疗无效、生命体征平稳,术后可于介入科进行血管栓塞。(2) 术后必要时转ICU支持治疗。(3) 对胎盘原位保留的患者应密切监测,必要时行子宫切除术,以防止出血、感染等并发症的发生。
1.3 统计学处理
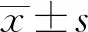
2 结 果
46例患者无一例死亡,5例患者切除子宫:术前3例行超声评分分别为8、9、12分,1例行MRI示胎盘植入,1例示胎盘粘连,术后病理检查均显示胎盘植入。手术时间最长为250 min,最短60 min,平均时间为(121.1±53.7)min。术中术后失血最多者5 000 ml,最少300 ml,平均失血量为(1 680.4±1 194.2)ml,5例切除子宫患者平均失血量为(4 460.0±826.0)ml。所有患者术后住院(7.5±2.7) d,新生儿Apgar 1 min初评平均(9.0±2.2)分。见表2。
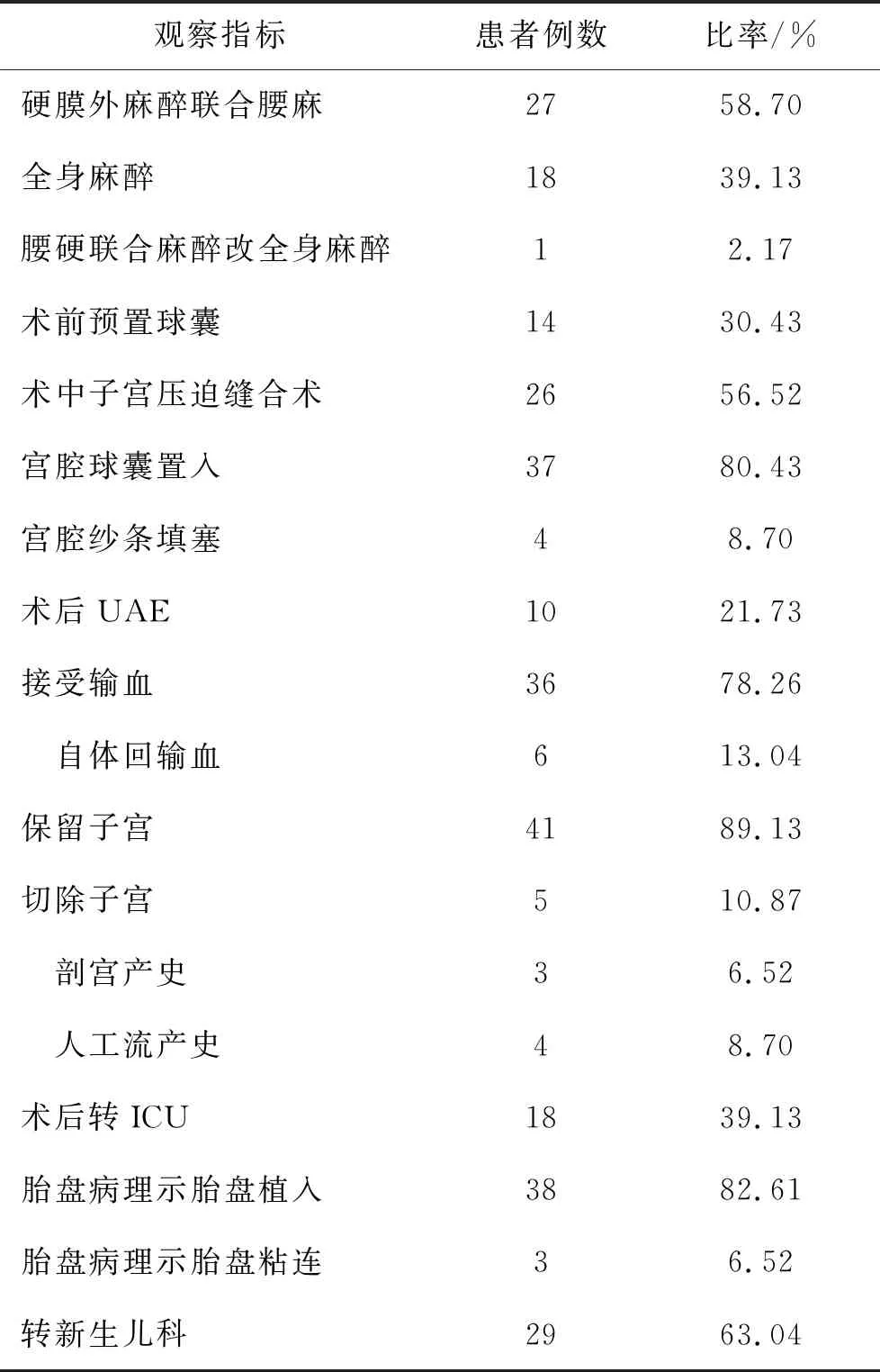
表2 临床指标和结局
3 讨 论
3.1 MDT
MDT最先应用于肿瘤外科[3],随之在其他临床学科也取得了显著成效。作为一种跨学科协同处理模式,MDT能够提供有效、安全的近远期治疗方案,保障病人生命安全[3]。前置胎盘合并穿透性胎盘植入是当今产科领域面对的巨大难题,胎盘植入常侵蚀膀胱、直肠等邻近器官,专科诊疗模式术前对胎盘植入评估不足、准备不充分、手术技术局限、手术方案单一,容易造成危及母儿安全的不良结局[4]。跨学科团队合作能提供准确诊断、协作计划,为更安全的手术提供有效保障,改善临床结局[5]。本研究中46例患者均在MDT模式下得到成功救治,母儿均预后良好,从术前、术中、术后及远期康复各方面进行评估干预,有效地保证了孕产妇的生命安全和围生儿的良好结局。
3.2 前置胎盘+胎盘植入、PPP
PPP的概念于20世纪 90 年代提出[6],指有剖宫产分娩史,此次妊娠诊断为前置胎盘,并且胎盘附着于子宫瘢痕部位者,常伴有胎盘植入[7]。胎盘植入根据植入程度分为胎盘粘连、胎盘植入和穿透性胎盘3类[8]。据统计,很多国家的胎盘植入发生率都在增加[9]。在过去的40年里,世界各地的剖宫产率从不足10%上升到30%以上,同时胎盘植入类疾病增加了10倍[10]。胎盘植入的风险随着既往剖宫产次数增加而增加[11]。在我国,由于剖宫产率、人工流产率一直居高不下及二孩政策的开放,剖宫产后再次怀孕女性增加,使得PPP和胎盘植入发病率升高。本组46例患者中45例均有≥1次剖宫产,38例有人工流产史,既往手术操作造成子宫内膜损伤,或存在子宫蜕膜原发性发育不良现象,导致PPP或胎盘植入。
3.3 术前评估
根据对高危孕妇的怀孕风险评估,PPP属于“红色”风险,应建议尽快到三级医疗机构接受评估,以确定是否可以继续妊娠,如答案肯定,应由市级及以上孕产妇危急重症救治中心进行孕产期保健服务及住院分娩。本研究患者多为外院或外地转诊至本院进行救治。
胎盘植入诊断主要依据病史及影像学检查(首选为有胎盘植入诊断经验的超声医师)[2]。超声是目前最主要的诊断方式,按照胎盘位置及厚度、胎盘后低回声带是否消失、膀胱线是否连续、胎盘陷窝性状、胎盘基底部血流信号、宫颈形态是否完整、宫颈是否存在血窦以及剖宫产史等9项,每项评0、1、2分,计算总分[12],<6分为无植入或粘连型,6~9分为植入型,≥10分为穿透型。此评分系统已在临床广泛应用,本组46例患者均于术前进行超声检查,提示胎盘粘连或植入,与术后病理诊断符合。但是超声的准确性还存在偏倚,其可靠性也与检查医生的水平相关,超声表现的缺失不能排除胎盘植入[2]。
MRI是另一种用于胎盘植入诊断的有效方法,在子宫后壁植入、超声难以诊断及评估穿透性胎盘等情况时更具价值[5]。改良MRI征象评分系统对胎盘植入的总体诊断符合率达89.9%[13]。本研究中患者有39例进行MRI检查,其中30例确定胎盘植入,并于术中或病理确诊,诊断符合率为76.92%,原因可能与操作人员经验不足有关。MRI由于设备和人员的要求检测费用昂贵,基层医院难以完成,限制了其应用[14],可能会造成漏诊。
3.4 术中处理
PPP最常见的并发症是术中及术后严重出血。最常用的止血方法是子宫压迫缝合术,包括经典的B- Lynch缝合、Cho缝合、Hayman缝合等[15]。本研究中患者采用子宫压迫缝合术26例,宫腔球囊置入 37例,宫腔填塞 4例,证实机械压迫止血作为临床常用方法切实有效、简便可行。
随着介入医学的发展,介入放射学技术也广泛用于产科出血的救治,包括双侧髂内动脉内球囊阻断术(balloon occlusion of internal iliac artery, BOIIA)、双侧髂总动脉内球囊阻断术(balloon occlusion of common iliac artery, BOCIA)、腹主动脉内球囊阻断术(balloon occlusion of abdominal aorta, BOAA)、UAE(包括卵巢动脉栓塞术)等[16- 21]。本研究中的患者采用的介入方式包括术前BOIIA、BOCIA、BOAA和术后UAE共计14例,其中仅1例切除子宫,其余恢复良好。但介入方法各有利弊,BOCIA和BOAA因同时阻断了下肢血供,有潜在发生缺血- 再灌注损伤的风险,球囊阻断时间有限,如操作不熟练或各科室缺乏配合,可能增加血栓形成的风险[16]。此外,术前预置球囊患者需接受辐射,BOCIA栓塞对宫颈以下止血效果不佳,UAE单独用于产后出血由于卵巢动脉血供持续止血不彻底等,所以临床处置时应结合出血特点酌情应用。
指南推荐紧急手术终止妊娠时行子宫全切,择期手术时子宫次全切可以减少出血和并发症,缩短手术时间,但宫颈有植入或穿透性胎盘植入时需子宫全切[15]。子宫切除是治疗胎盘植入的常用方法,但会导致产妇丧失生育能力,所以对于有生育要求的产妇需要评估胎盘植入深度和面积,结合实际情况保留子宫。本研究中5例患者切除子宫,其平均失血量明显多于总体平均失血量,其原因为穿透性植入或植入面积大等原因,其余41例患者在综合评估和有效处理后均得以成功保留子宫。
麻醉方式:局部麻醉在安全性、减少失血和病人的接受程度等方面好于全身麻醉,然而也需做好全身麻醉的准备[21]。本研究患者硬膜外麻醉联合腰麻27例,1例术中改为全身麻醉,显示硬膜外麻醉联合腰麻能够满足大部分手术的需求。
血液管理:对于确诊患者术前备血,术中注意评估患者失血的情况并及时输血,动态检测HGB、电解质,进行血气分析以及评估凝血功能或血容量的变化,实时了解患者所需的输血量。大量输血方案(massive transfusion protocol)可参考产后出血常用推荐方案为红细胞∶血浆∶血小板以1∶1∶1的比例输入[22],有条件的医院可采用自体血过滤回输[15]。本研究中36例患者因失血量大接受输血,其中6例患者采用自体回输血,均无不良反应。
3.5 术后管理
术中大量的失血及输血、输液以及术后可能出现的腹腔或盆腔持续性出血、复苏后的容量超负荷容易导致术后血流动力学异常,易致产妇出现严重并发症,甚至死亡。因此,在患者术后早期通常需要在ICU进行密切监测和处理,以确保循环稳定[15]。本研究中患者术后转ICU者18例,原因为出血量多、生命体征不稳定等,于ICU期间须预防重要器官损伤和输血相关的肺损伤等,观察有无活动性出血和各项指标,积极预防感染,术后平均住院7.5 d,恢复良好后出院。
MDT模式的构建旨在推动多学科交叉发展,使其对疾病的诊疗策略更加规范化、专业化,同时合理优化配置医疗资源,进一步提高亚专业的技术水平。产科将MDT模式应用于PPP可减少产时产后出血及输血量,缩短剖宫产时间,降低子宫切除风险,维持患者围手术期的生命体征平稳,有效地改善救治结局,减少母儿并发症,从而降低孕产妇死亡率。
