引导骨再生术辅助正畸治疗关闭中切牙缺牙间隙的应用
2021-08-14陈露祎黄忞吴佳奇罗俊
陈露祎 黄忞 吴佳奇 罗俊
1.南昌大学附属口腔医院正畸科 江西省口腔生物医学重点实验室,南昌330006;2.深圳市口腔医院儿童口腔科,深圳518001;3.南昌大学附属口腔医院种植科,南昌330006;4.南方医科大学深圳口腔医院正畸科,深圳518001
对于个别牙长期缺失的患者,种植修复或正畸移动邻牙关闭缺牙间隙是常见的两种治疗方法,但长期缺牙处的牙槽骨常伴有不同程度的吸收,增加了治疗难度,此时可结合引导骨再生术(guided bone regeneration,GBR)增加牙槽骨量,从而得到更加稳定的临床效果。
本文报道1例GBR辅助正畸治疗关闭缺牙间隙,取得良好效果的病例。
1 病例报告
患者,女,18岁,2014年8月因“门牙缺失影响美观”于南昌大学附属口腔医院正畸科就诊。现病史:5年前因外伤致上门牙缺失,当地医生建议成年后进一步处理,遂来就诊。既往史:有根管治疗及拔牙史,否认全身系统疾病史。
1.1 检查
左右面部基本对称,鼻唇角小,凸面型,张口度三横指,张口型正常,双侧颞下颌关节无弹响无杂音;口内检查:11、21牙缺失,双侧磨牙远中关系,双侧尖牙远中关系(拍左侧像时下颌有前伸),上颌牙弓卵圆形,下颌牙弓尖圆形,36、46牙面可见充填物。上前牙区间隙8 mm,下牙弓拥挤度5 mm,前牙覆2 mm,口腔卫生良好(图1)。

图1 治疗前面像及口内像Fig 1 Extraoral and intraoral view before treatment
全景片及锥形束CT(cone beam computed tomography,CBCT)三维重建影像显示:上前牙区缺牙处骨质薄,牙槽骨呈凹陷状,12、13、22、23牙牙冠近中倾斜,牙根周围紧贴密质骨,牙根根型明显;35、45牙根尖近中侧可见高密度影像;36牙根管治疗完善(图2、3)。侧位片示骨性Ⅲ类,均角生长型(图4、表1)。诊断:安氏Ⅱ类错畸形,骨性Ⅲ类,均角生长型。

表1 术前术后头影测量值Tab 1 The cephalometric measurements of pretreatment and posttreatment (°)
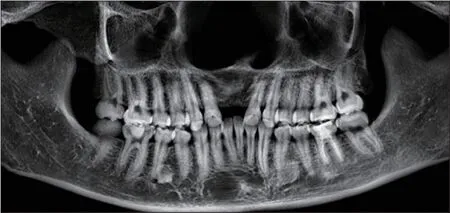
图2 治疗前全景片Fig 2 Pretreatment panoramic radiograph
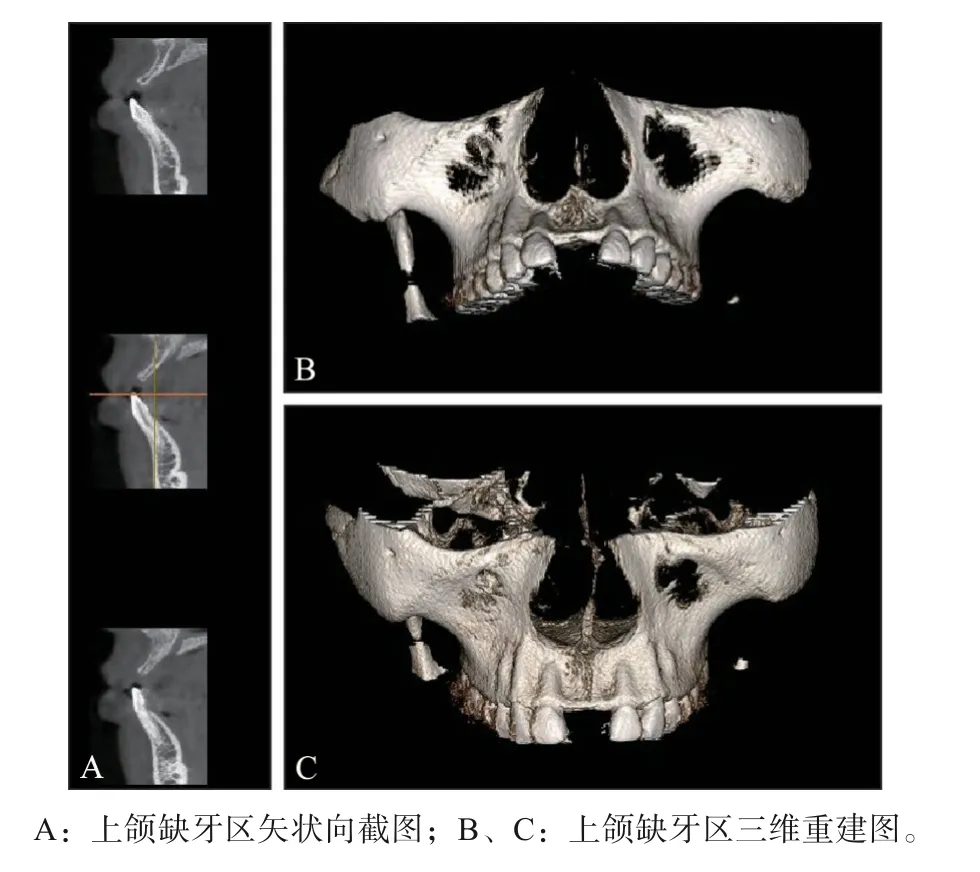
图3 治疗前CBCT三维重建Fig 3 3D reconstruction image of CBCT before treatment
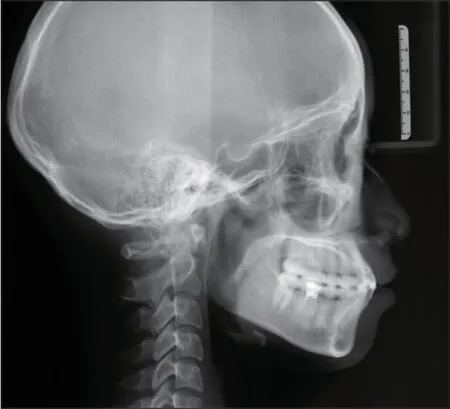
图4 治疗前侧位片Fig 4 Pretreatment lateral cephalogram
治疗目标:关闭缺牙间隙,达到稳定咬合关系,尽量改善侧貌。
1.2 治疗
方案一:拔牙矫治,术前拔除14、24、34、44牙,开拓上前牙修复间隙,矫治过程中结合GBR获得足够骨支持后内收前牙,解除下颌拥挤,使双侧磨牙及尖牙达到安氏Ⅰ类关系,改善侧貌,术后种植修复11、21牙。该方案的优点是:可以达到上下颌牙列良好的尖窝锁结关系;而缺点包括:需要拔除4颗正常牙,矫治全程上前牙区有缺隙,不利于美观,后期种植修复价格昂贵等。
方案二:拔牙矫治,术前拔除34、44牙,矫治过程中结合GBR获得足够骨量后,近中移动邻牙替代缺失牙,并预留邻牙修复改形间隙,解除下颌拥挤,改善侧貌。该方案的优点是:只需拔除2颗正常牙,后期无需种植修复;但缺点是:上前牙仍需改形以达到美学标准及获得正常的前牙覆覆盖。
与患者沟通协商,综合各种因素考虑,患者最终选择了方案二。
治疗过程:2014年9月初,装新亚固定直丝弓矫治器,上下颌使用0.016英寸镍钛圆丝进行排齐,随后逐步更换至0.018英寸澳丝摇椅弓打开咬合,并为GBR手术后关闭间隙做准备。矫治第8个月,于南昌大学附属口腔医院种植科行上前牙区GBR手术,此时上下颌为0.018英寸澳丝,术区部分弓丝截断(图5)。
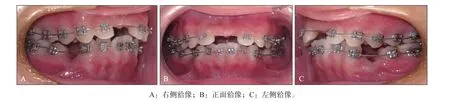
图5 初期排齐阶段Fig 5 Initial alignment stage
GBR过程:术前含漱0.2%氯己定1 min,0.5%碘伏棉球进行消毒,上前牙区用2%含肾上腺素(1∶100 000)甲派卡因进行局部浸润麻醉,行角形切口,翻全厚瓣,将上中切牙位点唇侧牙槽骨去皮质骨化,植入2枚2 mm×10 mm钛合金螺钉以支撑成骨空间,填充Bio-oss骨粉,覆盖Bio-Gide胶原膜,行软组织减张后严密缝合(图6)。术后1周内嘱患者含漱氯己定,口服3 d抗炎药,10 d后拆线,创面愈合良好,上颌重新安装0.018英寸澳丝。

图6 GBR手术过程Fig 6 GBR procedure
GBR术后1月:上颌在0.018英寸澳丝上使用弹性橡皮链施以轻力(约60 g)关闭缺牙间隙,2个月后使用0.017英寸×0.025英寸镍钛方丝进行过渡,随后在0.018英寸×0.025英寸不锈钢方丝上继续关闭间隙,同时控制前牙转矩及牙轴;下颌在此阶段使用0.018英寸澳丝摇椅弓进一步打开咬合,并滑动法关闭拔牙间隙。
矫治第14个月时,取出术区的微螺钉手术(图7)。矫治第16个月,上颌更换为0.018英寸澳丝,下颌去除第二前磨牙托槽,继续使用0.018英寸澳丝打开咬合(图8)。矫治期间预留上前牙修复间隙,但患者强烈要求继续关闭间隙,最终于第24个月拆除矫治器,制作并佩戴压膜保持器进入保持阶段。
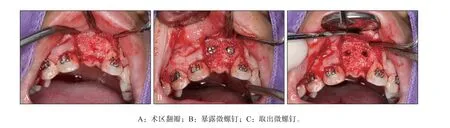
图7 微螺钉取出过程Fig 7 Microscrew removal process
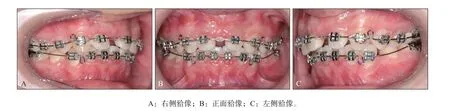
图8 剩余间隙关闭阶段Fig 8 Remaining gap closure phase
治疗结果:上前牙区缺牙间隙关闭,脸型改善,微笑弧稍差,患者对矫治结果满意(图9)。治疗后全景片及CBCT三维重建影像显示:上颌侧切牙牙根位于骨松质中,唇侧可见厚度约2 mm的高密度影像(图10~12)。
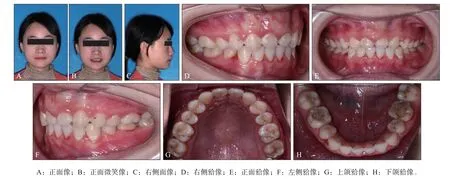
图9 治疗后面像及口内像Fig 9 Extraoral and intraoral view after treatment
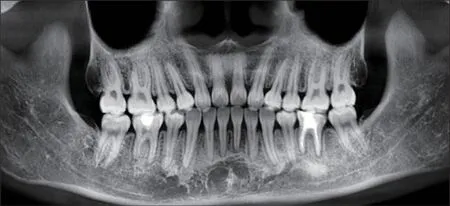
图10 治疗后全景片Fig 10 Posttreatment panoramic radiograph
疗程共计24个月。
2 讨论
长期缺牙会导致牙槽嵴不同程度的吸收、变窄变平,对正畸关闭缺牙间隙会有较大影响[1],此时,正畸医生应考虑邻牙形态及骨皮质的血液供应、生理反应的特点施以轻力,使其适应性改建,尤其是成人,治疗时间相对较长,如若施力不当,会导致牙槽骨进一步吸收,发生骨开裂或骨开窗,最终导致牙齿无法合理移动[2-3]。本病例中,该患者选择了正畸关闭缺牙间隙的治疗方案,但是由于上颌中切牙长期丧失,牙槽嵴吸收,常规关闭间隙困难,正畸术中结合GBR辅助治疗,降低了正畸移动牙齿的风险。
GBR作为骨增量的一种方式,通常与屏障膜、骨替代材料联合应用。由于骨组织生长相对缓慢,成纤维细胞和上皮细胞会优先占据骨缺损空间并形成软组织,所以GBR的生物学机制就是利用屏障膜阻止这些优势生长的细胞长入,而允许来源于骨组织的细胞增殖并长入屏障膜下方的隔离空间内,确保骨缺损区的成骨过程不受上皮组织的干扰[4-5]。GBR除了需要利用屏障膜形成成骨细胞生长的空间外,还需借助骨替代材料,如Bio-oss骨粉,以便成骨细胞爬行长入;此时骨或骨替代材料还将起到支撑屏障膜,支撑膜下成骨空间的作用[6]。该患者术后CBCT检查显示,术区唇侧存在一个接近2 mm左右厚度的高密度团块,对于这部分组织,Araújo等[7]的动物实验研究检查发现,GBR术区形成的组织主要由矿化骨23%±3%、结缔组织57%±11%和残留的生物材料20%±11%组成。Garaicoa等[8]的研究表明,在上颌前牙区通过GBR进行水平骨增量时,成骨效果与唇侧骨板的凹陷度呈正相关,距离牙槽嵴顶9 mm处凹陷较大的根尖区域,术后6个月可获得(4.39±2.65)mm的骨宽度增加。该患者上颌缺牙区同样存在较大的凹陷,术中利用2枚暂时性微螺钉获得了稳固的支撑,有效稳定了骨替代材料,结合黏骨膜瓣减张缝合,减轻了软组织对术区的压迫,防止膜塌陷,有利于后期获得尽可能多的成骨量。
正畸牙移动的生物学基础是颌骨的可塑性、牙骨质的抗压性及牙周膜内环境的稳定性,矫治力作用于牙齿后,压力侧牙周膜受挤压收缩从而产生较多破骨细胞,张力侧牙周膜受牵拉产生更多成骨细胞,最终达到新的稳定状态[9]。关于正畸牙移动至GBR区是否会引起牙周膜变化,Araújo等[10]曾移动犬牙至GBR区,随后在压力侧牙周膜内发现了Bio-oss颗粒,但其未与牙根直接接触,而是与富含成纤维细胞胶原蛋白的组织或多核破骨细胞样细胞接触,且此时的牙周膜厚度与常规正畸牙相比,两者无明显差异。这说明,GBR术区形成的骨质不会阻碍牙齿移动,矫治力作用于牙齿后,牙周膜最终可以达到新的稳定状态。
关于GBR术后正畸加载力的时间,目前研究[11]尚有争议。Araújo等[10]曾将1颗牙齿移动到3个月前用Bio-oss进行GBR的区域,发现张力区出现大量成骨,压力区部分成骨,因此该学者认为,在GBR术后3月内进行牙齿移动均有利于成骨,这与Liou等[12]的研究结果类似,即牙槽骨手术后3~4个月内为正畸牙快速移动期,此阶段内移动牙齿有利于成骨。Attia等[13]研究则认为,GBR术后即刻正畸加力,可最大程度增加骨量。本例患者在GBR术后第二个月开始正畸加力,但即刻加载力是否可以缩短矫治时间,形成更多的骨量,尚待进一步研究。
有研究表明,Bio-oss的存在不会妨碍牙齿的移动,牙齿的移动也不会妨碍GBR术后成骨[14],GBR与正畸联合应用不仅可以促进骨再生[15-16],还可以使牙周组织再生,为种植创造良好条件[17]。故本例患者GBR手术时机选择在正畸术中,结合术后CBCT可发现,GBR区高密度影在1年半的时间内都稳定在2 mm左右,未见明显的吸收。笔者认为,这是由于该患者GBR术区原牙槽嵴凹陷度较大,且正畸术中行GBR可以使正畸所造成的牙齿微量移动,激活牙槽骨的血运改建,增加其成骨与破骨活性,恰好与GBR相辅相成。
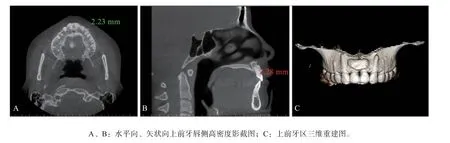
图11 治疗后CBCT三维重建Fig 11 3D reconstruction image of CBCT after treatment
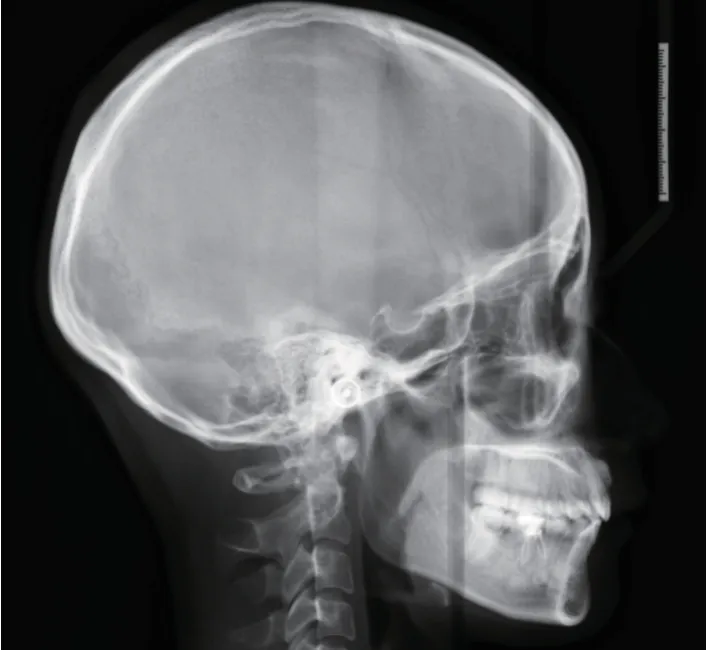
图12 治疗后侧位片Fig 12 Posttreatment lateral cephalogram
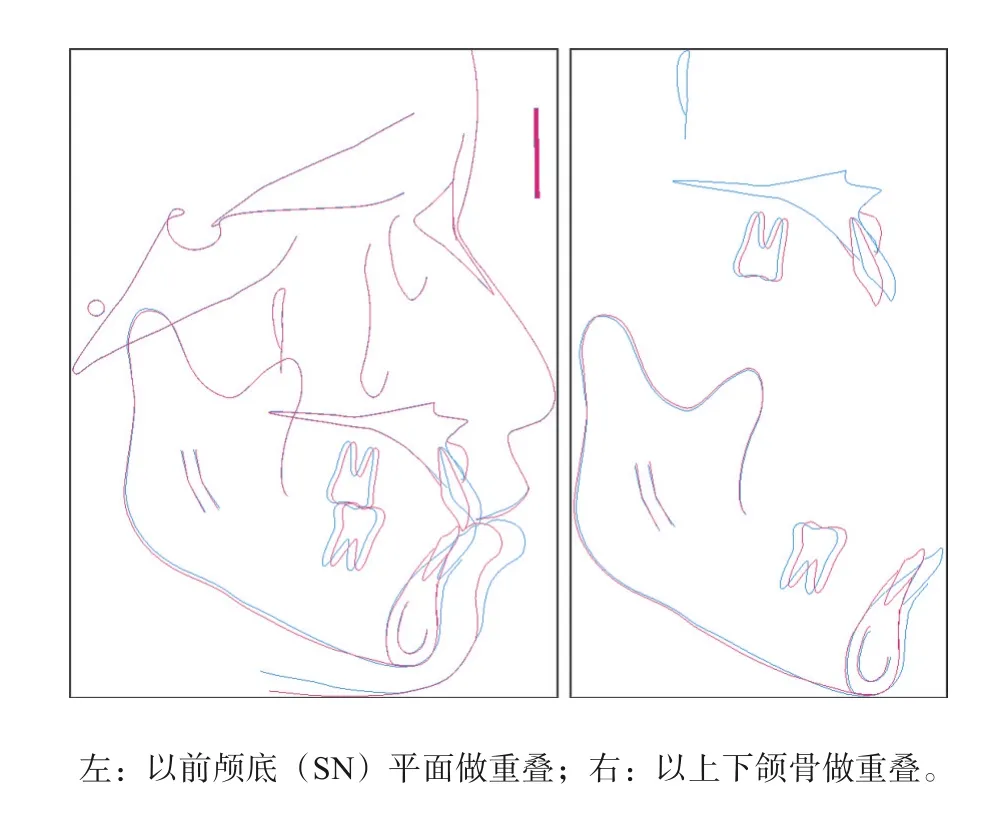
图13 治疗前后头影测量描记重叠图Fig 13 Superimposed cephalometric tracings of pretreatment and posttreatment
关于植骨效果的稳定性,自体骨由于良好的骨诱导性、成骨特性和骨传导特性,依然是牙槽嵴重建的金标准,远期植骨效果相对GBR稳定[18],但需开辟第二术区,手术创伤相对较大,而GBR不需开辟第二术区,术后反应相对较小,两者各有优势与不足。
利益冲突声明:作者声明本文无利益冲突。
