好氧堆肥对猪骨中磷元素赋存形式的影响
2021-08-12徐彦胜冯玉寒胡国全朱能敏
徐彦胜, 黎 霞, 冯玉寒, 胡国全,朱能敏
(农业农村部沼气科学研究所,农业农村部农村可再生能源开发利用重点实验室,四川 成都 610041)
我国是养殖大国也是畜禽肉制品消费大国,每年产生的畜禽粪污和动物骨质等废弃物量高达25亿吨[1],给脆弱的乡村生态环境带来了巨大威胁。好氧堆肥和厌氧发酵是目前技术水平下最适宜稳定化处理畜禽粪污等大宗农业废弃物的工艺技术[2-3]。但从固体废弃物资源化和无害化角度而言,厌氧发酵产生的大量沼渣和沼液仍须进行二次处理以最大程度削弱其对环境容量的压力[4],而好氧堆肥终产物为腐熟稳定化的固体有机质,并没有体积数倍于固体产物的沼液产生。因此,从减量化角度考虑,好氧堆肥是较为经济适宜的处理大宗畜禽粪污的实用技术[5]。畜禽骨质如猪蹄骨富含氮、磷、钙和钾等作物生长的大量和微量元素[6]。但是畜禽骨质中的氮、磷等元素为非有效态,必须通过物理、化学或者生物等方法转化为能被作物吸收的有效态才能成为有机肥料的组成部分[7-8]。好氧堆肥过程中好氧微生物以有机质为底物进行呼吸营生的同时释放出大量的热量导致堆体快速升温至60℃~75℃并维持3~5天,同时结构复杂的大分子有机质被分解成小分子有机物、二氧化碳和水[9-11]。有研究发现高温蒸煮能显著促进猪骨中非有效态磷转变为有效态磷[12-13]。因此,好氧堆肥产生的物理高温和化学小分子有机酸对畜禽骨质中的氮、磷等营养元素应具有一定溶出作用,这使畜禽粪污与畜禽骨质联合堆肥制备高品位有机肥料成为可能。
本研究以养殖场猪粪为原料、稻草秸秆为碳氮调理剂、猪蹄骨为磷源进行混合好氧堆肥,通过测定堆肥与骨质中磷元素含量并关联堆体温度和有机酸产量等过程指标揭示猪蹄骨中磷元素转化特性,为以动物骨质为辅料通过好氧堆肥生产富含氮、磷的高品位有机肥提供理论依据。
1 材料与方法
1.1 材料
猪粪来源于成都邛崃市某集约化生猪养殖场经过干稀分流后的固相粪污,其基本理化性质见表1,表中显示猪粪含水率和碳氮比偏离了好氧堆肥的最适范围[14]。因此,通过添加稻草秸秆调节原料碳氮比和含水率,保证堆肥快速启动并获得腐熟度较好的堆肥产品。猪蹄骨取自成都市某餐饮店餐厨废弃物,经温水洗涤去残渣后自然晾干破碎成1 cm左右的小段用于堆肥实验。稻草秸秆取自成都天府新区水稻收割后的新鲜稻草,经清洗风干切碎至3~5 cm小段备用。试剂除特别说明外均为分析纯或更高纯度级别且不经过任何预处理,实验用水来自密理博(Millipore)纯水仪出水(18.2 MΩ cm-1)。

表1 猪粪基本理化性质
1.2 试验方法
实验采用槽式堆肥,将猪粪、猪蹄骨与稻草秸秆(m猪粪:m猪蹄骨:m稻草= 10∶1∶2)混合均匀后铲进堆肥槽(L170 cm × W120 cm × H200 cm),逐层均匀铺设,直到堆体高度为1 m为止,然后在堆体中央和边缘插入电偶式温度计记录堆体温度。根据堆肥腐熟过程,前期每隔3天翻堆、间隔5天取样,30天之后每隔5天翻堆、间隔10天取样,样品保存在4℃冰箱备用。
1.3 分析方法
总磷、总氮、总钾、速效氮、速效磷和速效钾按照土壤农化分析方法测定[15],挥发性脂肪酸利用气相色谱仪分析(GC112A,上海仪电,中国),堆肥产物官能团和晶相结构分别采用傅立叶红外光谱仪(Nicolet2000, USA)和X射线衍射仪(Ares, Malvern Panalytical, UN)分析,pH值利用电位法测定。
2 结果与讨论
2.1 堆肥过程中温度变化
由图1和图2知,是否添加猪骨对堆体温度影响不显著,这可能与猪骨用量小或猪骨碳含量较低有关,因为好氧堆肥过程中温度的上升主要是微生物代谢碳源释放热量导致[16]。堆体温度在10天左右达到峰值(55℃~58℃),维持5天后逐渐降低直到与环境温度接近。堆体维持40℃及以上高温的时间约10~12天,该时间段微生物生理代谢活动旺盛,猪粪中有机质快速分解生成小分子有机物,而氮、磷、钾等元素也最可能在该时段内发生形态改变。30天后堆体温度降至30℃以下,表明大部分易分解有机物已被微生物代谢,堆体产生的热量逐渐减少导致其与环境温差减小。但直到70天,堆体与外界环境依然存在5℃的温差,这说明堆肥后期微生物依然能够通过呼吸活动产生少量热量,80天后猪粪已腐熟稳定,堆体与环境温差基本消失。
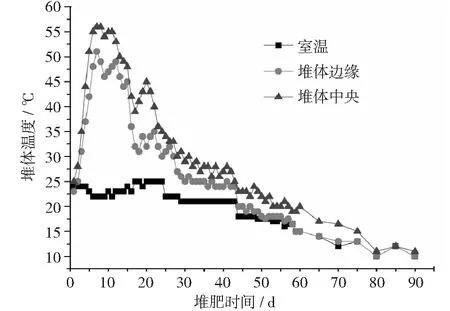
图1 添加猪骨堆肥温度变化
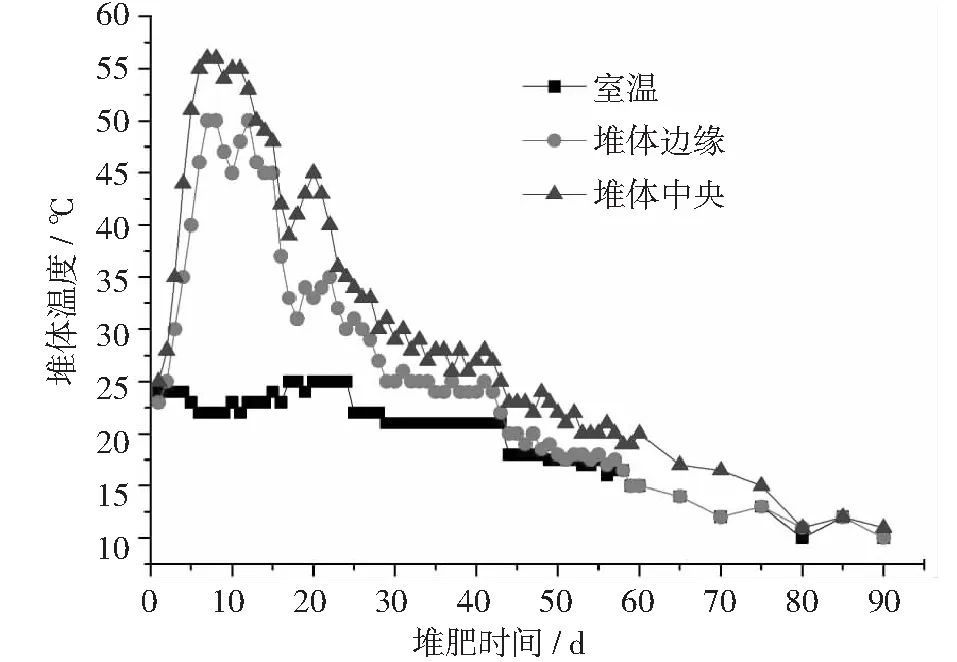
图2 未添加猪骨堆肥温度变化
2.2 堆体pH值及有机酸变化
由图3和图4可知,添加猪骨对堆体pH值变化无显著影响。在堆肥初始阶段(<10天),堆体pH值由初始的8.3左右急剧下降至第5天的7.5左右,然后缓慢上升。在25天~30天之间,添加猪骨头和未添加猪骨头堆体的pH值都达到峰值(8.1),之后pH值又经历了缓慢下降和上升的过程,但都在8.0附近波动。堆体pH值在30天后的小幅波动表明堆体已经进入腐熟稳定化阶段,堆体中生物化学反应已基本结束[17]。pH值变化也说明了堆体产生大量有机酸主要集中在堆肥前20天,这也是堆体温度急速上升的阶段。
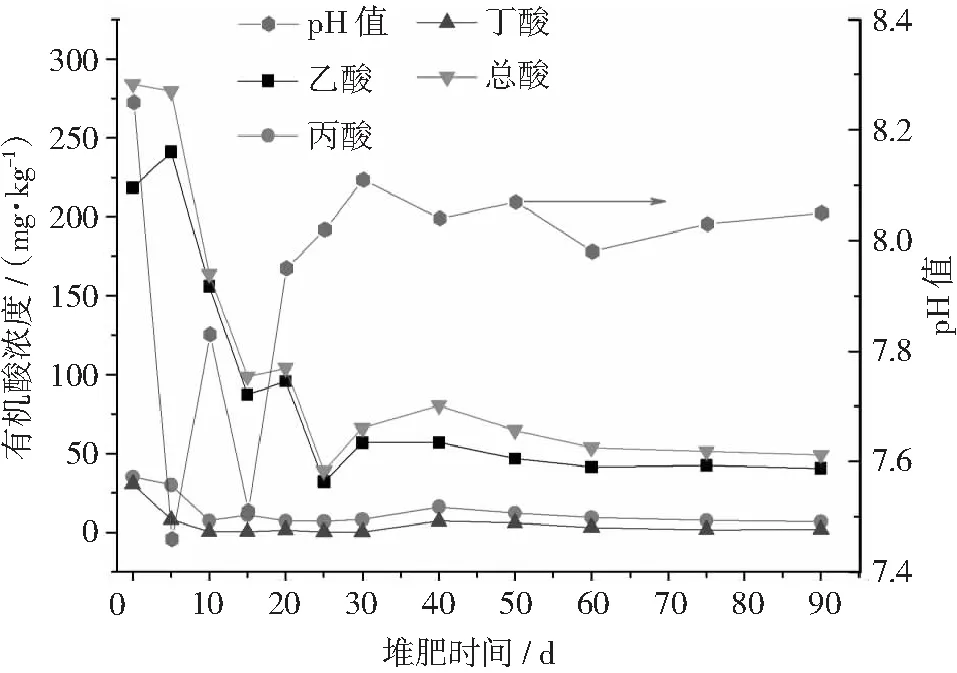
图3 添加猪骨的堆体pH值及有机酸变化
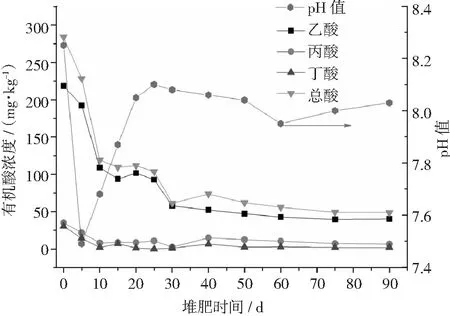
图4 未添加猪骨的堆体pH值及有机酸变化
2.3 堆肥固相产物红外光谱特征
图5~6和表2显示,添加猪骨头与否对堆肥产物官能团结构影响并不显著。新鲜猪粪在3417 cm-1,2924 cm-1,2850 cm-1,1650 cm-1,1049 cm-1和655.7 cm-1处出现了较为明显的特征峰。随着堆肥的进行,874 cm-1-655.7 cm-1之间出现了强度不大的吸收峰,说明猪粪被分解产生了新的官能团。随着堆肥时间的进一步延长,2924 cm-1,2850 cm-1,655.7 cm-1处的吸收峰逐渐变弱,表明脂肪类或者糖类被分解[19]。就1430 cm-1峰而言,其峰强度先增加(10天)然后逐渐降低,90 d堆肥结束其峰强已几不可见。因为1430 cm-1归属于木质素和脂肪族化合物的特征峰,该峰强的变化表明在堆肥过程中木质素是在高温阶段缓慢分解的。

表2 堆肥固相产物红外光谱特征峰归属[18]
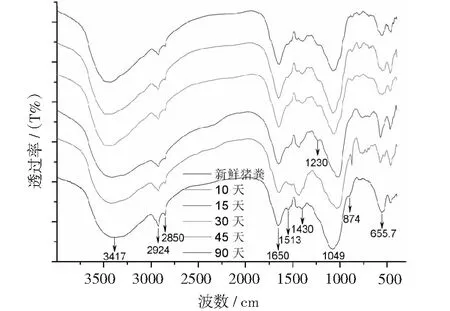
图5 添加猪骨的堆体固相产物红外光谱特征变化
2.4 堆肥固相产物总氮、磷、钾变化
氮、磷、钾是猪粪和猪粪堆肥中的主要作物营养元素,对作物生长具有明显的促进作用。图7和图8显示,新鲜猪粪中总氮和总钾含量高达15 g·kg-1,而总磷只有9 g·kg-1。猪粪中氮、磷和钾主要来源于饲料在猪消化系统中的代谢产物。磷和钾在好氧堆肥过程中不会被分解成可挥发性物质,在没有外加磷源的条件下二者绝对质量浓度理论上不会发生变化。但由于堆肥过程中部分碳、氮元素转变成为二氧化碳、氨气等挥发性气体导致堆体总质量减小,因此,总磷和总钾质量浓度在堆肥过程中有小幅上升,这在未添加猪骨的对比实验中表现得较为明显。本研究中,总氮在堆肥过程中呈现与总钾相似的变化趋势——质量浓度小幅上升,这说明氮元素转化为气体的挥发量小于碳元素转化为气体的挥发量。就本研究而言,添加猪骨与否对堆肥总磷的影响非常显著。添加猪骨后,堆肥中总磷质量浓度在堆肥前期快速增长,在前30天,其浓度由最初的9 g·kg-1快速增加到12.5 g·kg-1,增加了38.89%,随后基本保持稳定,而未添加猪骨堆肥中总磷最终质量浓度为9.5 g·kg-1。由于堆体温度前30天一直保持在40oC左右,因此可以推断,猪骨中磷元素在高温及有机质分解产生的有机酸的共同作用下从骨质中溶出进入堆肥中,导致堆肥总磷含量显著上升。同时,好氧堆肥中某些好氧菌还能通过代谢活动将猪骨中磷元素转化成自身细胞的组成部分,也间接导致堆肥中总磷浓度的升高[11]。从总磷变化趋势可以看出,猪骨中磷元素在堆肥过程中是能够溶出并进入堆肥中从而提升肥料品质的,这无疑为大量动物骨质的资源化利用提供了一条新途径,对提升传统堆肥产品中的磷含量也具有一定现实意义。

图6 未添加猪骨的堆体固相产物红外光谱特征变化
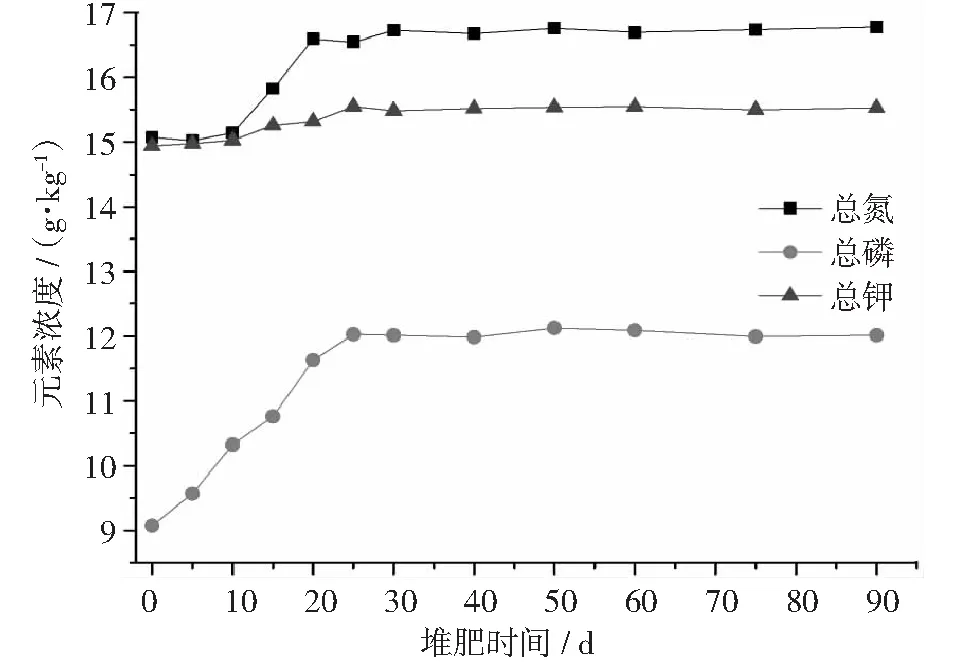
图7 添加猪骨的堆体总氮、总磷、总钾变化
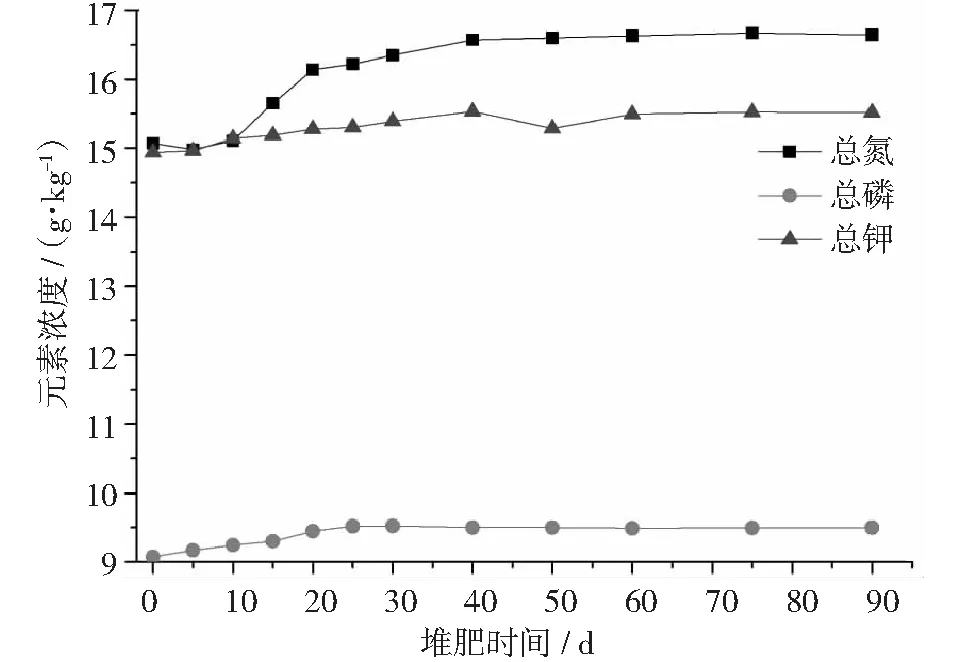
图8 未添加猪骨的堆体总氮、总磷、总钾变化
2.5 堆肥固相产物速效氮、磷、钾变化
作为肥料,速效氮磷钾才是决定堆肥品质的关键指标。图9和图10显示,速效钾浓度随着堆肥时间的延长呈现上升态势,最终浓度达到15000~16000 mg·kg-1,而速效氮浓度呈现先上升后下降的变化趋势,但二者的最终浓度与添加猪骨与否关系不大,即猪骨的添加对速效氮、速效钾在堆体中的含量影响不显著。但添加猪骨后,速效磷在堆肥前10天浓度由初始的1200 mg·kg-1迅速上升至3800 mg·kg-1左右,涨幅达3.2倍。而未添加猪骨堆肥中,速效磷浓度10天后小幅上升到1300 mg·kg-1,之后基本保持不变。显然,添加猪骨堆体中速效磷浓度的显著上升与总磷的显著增加都是猪骨中磷在堆肥过程中释放溶出导致的。这进一步说明动物骨质中的磷元素能够通过好氧堆肥转变成速效磷,从而提高堆肥速效磷含量。对比图7和图9可以发现,速效钾占总钾的95%以上,而有效氮却只占总氮的20%左右,速效磷占总磷的33%左右。速效氮、速效磷和速效钾占总氮、总磷和总钾百分比的显著差异说明,钾元素对有机固体的亲和力明显弱于氮和磷元素,其存在形式主要由钾元素的化学性质决定,而氮和磷元素的存在形式主要由元素和环境基质特性等共同决定。换言之,堆肥对猪粪中钾元素形态影响并不显著,但对氮、磷元素的影响相对明显。
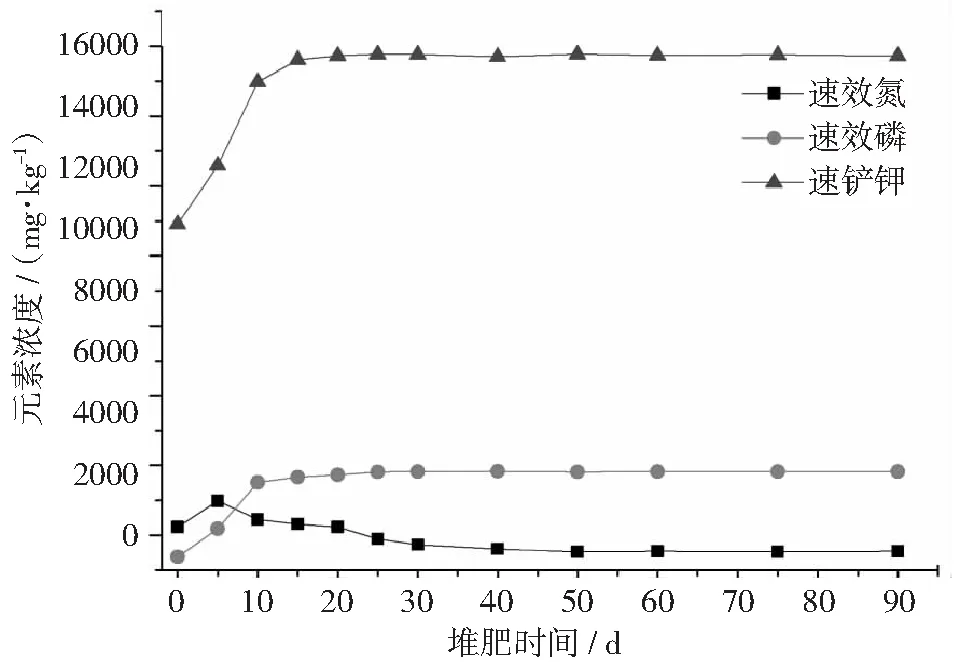
图9 添加猪骨的堆体中速效氮磷钾变化

图10 未添加猪骨的堆体中速效氮磷钾变化
3 结论
(1)添加骨质对堆体升温速率、温度峰值以及固相产物有机官能团结构并无显著影响。
(2)堆肥对猪骨中磷元素溶出进入堆体成为堆肥有效成分具有明显的促进作用,但猪骨中元素氮和元素钾堆肥溶出效应并不明显。
(3)堆肥过程中产生的有机酸、热量导致的堆体升温是猪骨中磷元素溶出释放转化为有效磷的主要原因。
