基于生物模板制备二氧化碳加氢反应的Cu/ZnO催化剂
2021-07-24蔡中杰田盼黄忠亮黄猛黄加乐詹国武李清彪
蔡中杰,田盼,黄忠亮,黄猛,黄加乐,詹国武,李清彪,3
(1 厦门大学化学化工学院,福建厦门351100; 2 华侨大学化工学院,福建厦门361021; 3 集美大学食品科学与工程学院,福建厦门361021)
引 言
近年来,二氧化碳(CO2)的大量排放引起了世界各国的广泛关注,目前大气中CO2浓度高达413×106,高浓度CO2会引起温室效应进而导致严重的气候和环境问题[1]。我国的CO2排放量持续增高已超过全球排放量的20%,每年排放量约为120 亿吨,为实现2060 年碳中和的目标,我国的减排和CO2资源化任务尤为艰巨[2-3]。因此,必须加快构建清洁低碳的能源体系,其中将CO2通过加氢反应转化为液体能源(如甲醇)受到研究学者的广泛关注[4-5]。甲醇是一种非常活泼的C1化合物,可以作为能源转化的中枢平台,通过甲醇制烯烃(MTO)和甲醇制芳烃(MTA)等反应可将CO2直接转化为具有高附加值的化学产品[6]。此外,甲醇还可以通过电解制取绿氢,再经过CO2加氢制取甲醇,达到“零碳排放”的能源体系。这一经济循环过程将拓展新能源、降低碳排放、实现碳循环等效果[7]。因此开发高性能和高稳定性的CO2加氢制甲醇催化剂具有重要的意义。
目前CO2加氢制甲醇的催化剂主要以Cu 基与Pd 基催化剂为主[8-10],与Pd 基催化剂相比,Cu 基催化剂由于Cu 产量丰富、价格低廉,已被广泛研究。但是单独Cu 位点对CO2几乎没有吸附与活化作用,所以大量研究通过改变Cu 与金属氧化物载体的相互作用来调控Cu的电子结构、催化剂表面的氧空位和CO2的吸附量,从而提高催化活性与甲醇选择性[11-13]。目前工业上CO2加氢制甲醇的催化剂以Cu/ZnO/Al2O3为主,由于逆水煤气反应(CO2+ H2CO+H2O)的存在导致了甲醇的选择性普遍较低,而且反应中副产物H2O会导致铜颗粒的快速烧结和失活[14-15]。目前关于Cu/ZnO催化剂的本征活性位点还存在很大的争议,一方面认为Cu和ZnO之间密切协同作用所形成的Cu-ZnO 界面是CO2加氢反应的活性位点,其中ZnO 能直接活化反应物分子并具有一定的储氢能力[16-17];另一方面认为,金属与载体间的强相互作用(SMSI)所形成CuZn 合金是反应活性位点,其中ZnOx覆盖在Cu(211)的表面形成的堆叠位错结构有利于含氧中间体的稳定[18]。另外目前关于副产物H2O 在整个CO2加氢反应中的作用也具有争议性,Sun 等[19]以碳纳米管等碳材料为载体,利用其表面的疏水性促进水的解吸与甲醇的生成。Wang等[20-21]通过制备具有三维有序大孔结构的Cu/ZnO/Al2O3催化剂,发现H2O可以促进关键中间体(HCO3*)的水解反应并生成甲醇,有效提高催化剂稳定性与甲醇选择性。因此,对催化剂的构效关系的研究十分重要。
生物模板法是指利用具有多层次、多维空间结构的天然生物质为模板制备具有多级孔结构的纳米材料,这不仅符合绿色环保的理念,而且通过简单制备方法实现了复杂多孔复合材料的制备[22-24]。近年来。以植物生物质为模板制备金属氧化物实现了氧化物材料的碳、氮元素自掺杂,有效改善传质以及特殊的多层次空间结构赋予催化剂优异的催化性能,在非均相加氢反应中具有广泛的应用[22]。本课题组[25]先前的研究通过植物提取液制备了三维多孔的钙钛矿型LaCoO3催化剂,实现了CO2高效加氢制甲烷反应。Li等[26]利用丝瓜与稻谷壳为模板制备bio-ZSM-5 分子筛催化剂并用于CO2加氢制二甲醚。Jiang等[27]用油菜花粉为模板制备多孔TiO2催化剂用于1,3-丁二烯选择性加氢反应等。基于此,本文围绕Cu/ZnO 催化剂进行CO2加氢制甲醇反应研究,借助油菜花粉作为生物模板制备具有多孔结构的ZnO,来研究催化剂的多孔结构、表面性质与催化性能之间的关系,并与化学沉积沉淀法所制备的Cu/ZnO 催化剂相比,探讨影响铜基催化剂稳定性和甲醇选择性的关键结构因素。
1 实验材料和方法
1.1 材料
无水乙醇、甲醇、二水合乙酸锌、六亚甲基四胺(HMT)、聚乙烯吡咯烷酮(PVP,K30)、三水合硝酸铜、硼氢化钠等试剂均来自国药集团化学试剂有限公司。油菜花粉购自五台山蜂业有限公司。本实验用水均为去离子水,电阻为16 MΩ。
1.2 催化剂的制备
本文涉及的载体和催化剂的制备流程如图1所示。
采用生物模板制备的ZnO 标记为bio-ZnO:将2.0 g 花粉分散于50 ml 混合溶液(乙醇/水体比1∶1)中,超声30 min 混合均匀后置于油浴锅中加热至80℃,待温度均匀后加入2.0 g Zn(Ac)2·2H2O,搅拌1 h 后加入0.94 g HMT 沉淀剂,继续反应2 h 后冷却至室温,离心分离后在50℃下干燥24 h。在马弗炉中焙烧(升温速率:2℃·min-1,2 h),改变样品焙烧温度为500、600、700℃,即得目标产物,分别命名为bio-ZnO-X(X=500、600、700,与焙烧温度对应)。
无生物模板制备的ZnO 标记为chem-ZnO:将2.0 g Zn(Ac)2·2H2O 溶于50 ml 去离子水中,超声20 min 使其混合均匀后向溶液加入0.94 g HMT 沉淀剂,放入100℃烘箱中水热反应6 h 后经离心、干燥即得chem-ZnO。
Cu-ZnO 催化剂:将上述制备的0.25 g bio-ZnO与0.25 g chem-ZnO 样品分别加入40 ml 甲醇中,再加入40 mg PVP 及0.25 g Cu(NO)2·3H2O,超声10 min使其混合均匀,室温搅拌1 h 后向混合溶液中再加入NaBH4的甲醇溶液[n(NaBH4)=5n(Cu)],继续搅拌2 h 后用乙醇离心洗涤,在80℃条件下干燥12 h,随后在350℃焙烧(升温速率:2℃·min-1,3 h)条件下得到最终的催化剂。
1.3 催化剂性能评价
催化剂的活性和稳定性评价是在固定床反应器中进行的。简要步骤如下:将250 mg 粉末催化剂与400 mg 石英砂放入固体研钵中研磨,然后装入石英棉支撑的石英管中。在200℃、常压下通入10%H2/Ar(30 ml·min-1)对催化剂进行还原处理2 h,将处理气切换为原料气(CO2∶H2=1∶3,体积比),反应条件为250℃、3.0 MPa,空速条件为3600 ml·g-1·h-1。反应后的产物经减压后由在线气相色谱检测,通过色谱出峰面积及校正因子计算出CO2的转化率与相应产物的选择性。二氧化碳的转化率、甲醇选择性及时空产率的计算公式如下:

1.4 催化剂表征
催化剂的形貌表征主要通过德国ZEISS 公司的Sigma 扫描电镜(SEM)进行表征;催化剂的微观结构由美国FEI 公司的TECNAI F30 透射电镜(TEM)进行观察。
X 射线粉末分析(XRD)由日本理学Rigaku ⅣXRD 进行表征,光源为Cu Kα(λ= 1.54 Å,1 Å =0.1 nm),扫描速率为10(°)·min-1,扫描范围为10°~80°。
X 射线光电子能谱(XPS)采用美国Thermo Fisher ESCALAB 250 xi 型号仪器进行表征。光源为Al Kα单色射线(hν=1486.6 eV),所有数据都经过C 1s在284.8 eV处的结合能校正。
催化剂比表面积通过N2物理吸脱附法测定,采用Micromeritics 公司Tristar Ⅱ3020 型比表面积分析仪器。
氢气程序升温还原(H2-TPR)实验,先将100 mg催化剂在纯He(30 ml·min-1)条件下200℃预处理2 h,接着将气体调至5%H2/Ar气氛(30 ml·min-1)进行还原,还原温度由室温升至700℃(升温速率:5℃·min-1),通过在线热导检测器(TCD)检测出口尾气的H2浓度。
通过电感耦合等离子体发射光谱法(ICP-OES,安捷伦,5100 SVDV)测定催化剂样品中的Cu含量。
2 实验结果与讨论
2.1 催化剂的形貌表征
原始花粉和不同焙烧温度下获得的bio-ZnO 样品的SEM 表征结果如图2 所示。花粉模板整体呈9µm×10µm 椭球形,而且粒径大小分布均匀,表面具有丰富的网状孔结构且大孔直径约为500 nm。通过改变bio-ZnO 样品的焙烧温度可以得到不同形貌与结构的ZnO 载体。如图2(d)~(f)所示,当焙烧温度为500℃时ZnO 能完整复制出花粉模板的形貌,但是其尺寸与原始花粉相比略小,而且表面网状大孔的直径也缩小至400 nm。推测这是由于花粉内部结构在焙烧后会呈现一定程度的体积收缩,可以清楚观察到bio-ZnO 表面清晰的大孔结构与ZnO 微小晶粒。随着焙烧温度升高至600℃原有的花粉模板多孔结构逐渐塌陷[图2(g)~(i)],当焙烧温度高达700℃后多孔结构消失[图2(j)~(l)]。另外,从图2 中焙烧后样品的颜色可以看到,bio-ZnO-500 样品的颜色为黑色;bio-ZnO-600 为灰色;bio-ZnO-700 为白色,随着焙烧温度的增加,样品颜色越来越淡,这表明bio-ZnO-500的多级孔结构是由花粉模板中未焙烧完全的生物碳组成。在相同条件下,利用化学沉积沉淀法制备的ZnO 呈边长为3µm 的正六面体结构(图3)。

图2 原始花粉的扫描电镜图[(a)~(c)];不同焙烧温度下制备的bio-ZnO的扫描电镜图:500℃[(d)~(f)],600℃[(g)~(i)],700℃[(j)~(l)][其中图(d)、(g)、(j)中插图分别为该焙烧后样品的照片]Fig.2 Representative SEM images of the original pollen[(a)—(c)]and bio-ZnO obtained at the calcination temperature of 500℃[(d)—(f)],600℃[(g)—(i)],and 700℃[(j)—(l)][Insets in(d),(g),and(j)are photos of the calcined samples]
2.2 催化剂的理化性质表征

图3 沉积沉淀法制备的chem-ZnO的扫描电镜图Fig.3 Representative SEM images of chem-ZnO support prepared by deposition precipitation method

图4 不同样品的氮气吸脱附曲线(内插图为孔径分布)(a);红外谱图(methanol表示甲醇洗涤样品)(b);ZnO载体的XRD谱图(c);负载Cu后催化剂的XRD谱图(d)Fig.4 N2 physisorption isotherms of different samples(inset shows corresponding pore size distribution curves)(a);FTIR spectra(b);XRD patterns of ZnO support samples(c);XRD patterns of catalyst samples(d)
图4(a)是不同焙烧温度下得到的bio-ZnO 样品的氮气吸脱附曲线,所得bio-ZnO-500、bio-ZnO-600、bio-ZnO-700 样 品 的BET 比 表 面 积 分 别 为14.6、8.2、5.7 m2·g-1。根据国际纯粹与应用化学联合会(IUPAC)定义,图中bio-ZnO-500 的吸脱附曲线含H3 型迟滞环,为介孔材料。同时,插图中基于吸附数据的孔径分布图中显示介孔大小集中在10 nm 左右。在较高的相对压力(P/P0=0.80~0.99)范围内有迟滞环出现,结合SEM 表征也可证实大孔结构的存在,以上分析结果证明bio-CZ-500 具有多级孔结构。结合BET 结果分析,bio-ZnO 具有较高的BET比表面积,随着制备过程中焙烧温度的提高,bio-ZnO 样品的比表面积也随之减少,证明未焙烧完全的生物碳组成了bio-ZnO的多级孔结构。从图4(b)的红外谱图可知,利用花粉生物模板所制备的ZnO在400~600 cm-1的范围内都出现了O—Zn—O 的特征峰,文献[27]中指出在3500 cm-1以上属于花粉杂质K+、Ca2+的特征峰,样品在焙烧处理后依然存在灰分。同时发现通过甲醇洗涤,可以除去表面残留的K+、Ca2+等生物灰分,因此在后续实验中采用甲醇处理以避免生物灰分对催化剂活性的影响。将XRD[图4(c)、(d)]的结果与无机晶体库中标准PDF 卡片进行对比,发现bio-ZnO 晶型主要为六方晶相(JCPDS#65-3411),而且与沉积沉淀法制备的chem-ZnO 相比,bio-ZnO 样品的衍射峰峰宽较窄,推测采用生物模板法所制备的bio-ZnO 颗粒较小且分布均匀。通过ICP-OES 测量催化剂中Cu 含量,发现bio-CZ-500催化剂中Cu实际含量为12.60%,chem-CZ中Cu的实际负载量为12.67%,说明Cu 实际负载量基本一致。图4(d)显示焙烧后样品中都出现了比较明显的CuO 的衍射峰,说明CuO 已经负载在ZnO 载体表面。图5 为未焙烧Pollen-ZnO 样品的热重分析(TGA),当焙烧温度为500℃时所获得的bio-ZnO 内仍含有约25%(质量)的生物碳。因此,bio-CZ-500中Cu/Zn 的实际摩尔比为0.25;而chem-CZ 中Cu/Zn实际摩尔比为0.19。下文将继续探究Cu/Zn 摩尔比对催化剂活性的影响。

图5 未焙烧Pollen-ZnO样品的热重图Fig.5 TGA profile of the uncalcined Pollen-ZnO sample
2.3 催化剂的性能评价
首先,对催化反应的最优反应条件进行探究。考虑到二氧化碳加氢制甲醇为放热反应,催化剂对反应温度十分敏感,分别选取210、230、250、270℃四个不同反应温度对两种催化剂进行活性评价,结果如图6(a)所示,随着温度的升高,chem-CZ 催化剂的CO2转化率不断增加,相反甲醇选择性不断降低至39%。bio-CZ-500 催化剂也呈现相似的规律,但是整体的选择性依然远高于chem-CZ。当温度升至270℃后,两者的甲醇选择性与产率均呈现下降趋势。综合考虑CO2转化率与甲醇产率,最终确定3.0 MPa、250℃、空速30 ml·min-1为最优反应条件。如图6(b)所示,考虑到Cu/Zn摩尔比对催化剂的活性也有影响,进一步对bio-CZ-500 催化剂中铜的负载量进行考察,发现随着Cu/Zn 摩尔比的增加,CO2的转化率先增加后减少,甲醇的选择性也呈现相似的规律,这是因为随着Cu负载量的增加其暴露面积也相应增加,更易引起催化剂表面Cu 颗粒的团聚失活[21]。对4 个催化剂(bio-CZ-500、bio-CZ-600、bio-CZ-700、chem-CZ)在最优反应条件下进行催化活性评价,发现存在明显不同的催化活性(CO2转化率与产物分布方面)。从图6(c)可以看到bio-CZ-500催化剂活性最好,CO2单程转化率为5%,甲醇的选择性达到81%,而其他3 个催化剂甲醇的选择性都不足50%。推测bio-ZnO-500 中特有的多孔结构是其优异活性的主要原因。碳是一种疏水性(或弱亲水性)材料[19],其疏水性有助于促进副产物H2O 在催化剂表面的脱附。对以上4种催化剂进行了水接触角测试,发现甲醇的选择性与催化剂表面的水接触角呈正相关,即接触角越大,甲醇的选择性越高。为进一步探究催化剂的多孔碳结构与稳定性之间的关系,分别选取0.50 g 的bio-CZ-500 与chem-CZ催化剂进行100 h的稳定性评价[图6(d)]。在反应起始阶段,chem-CZ 催化剂对甲醇的选择性较低产物主要为CO,使得整体CO2的转化率较高。由于bio-CZ-500中含有25%的生物碳成分,在反应过程中活性组分诱导活化所需时间较长[28],待活性稳定后,CO2的转化率以及甲醇的选择性等性能依然是优于chem-CZ 催化剂的。另外,bio-CZ-500 催化剂在运行100 h 后催化剂的活性与选择性基本不变,同时甲醇的时空产率可达到60 mg·h-1·g-1;相反chem-CZ催化剂在反应12 h后活性便开始下降,甲醇的时空 产 率(41 mg·h-1·g-1)也 远 低 于bio-CZ-500 催化剂。
2.4 催化剂的反应前后的对比表征
如图7 所示,尽管bio-CZ-500 与chem-CZ 催化剂均采用浸渍还原法负载Cu颗粒,但是两种催化剂中Cu 颗粒却显示出不同的粒径:bio-CZ-500 催化剂中Cu 粒度为(14.4±2.6)nm,而chem-CZ 催化剂中Cu 粒度为(16.2±3.8)nm。由于bio-ZnO 具有多级孔结构且BET 比表面积较大(14.6 m2·g-1),所以CuO 颗粒的分散度比较均匀,同时也观察到小颗粒的ZnO纳米颗粒。相比之下,由于chem-ZnO 的BET 比表面积较小(2.1 m2·g-1),而且ZnO 载体颗粒较大,导致负载在chem-ZnO上的Cu颗粒分散度较差[29-30]。

图6 反应温度对两种催化剂活性的影响(内插图为催化剂相应的模型)(a);Cu/Zn摩尔比对bio-CZ-500催化性能的影响(b);四种催化剂的活性评价结果(c);bio-CZ-500与chem-CZ催化剂的稳定性评价结果(图中实心图例代表bio-CZ-500,空心图例代表chem-CZ)(d)Fig.6 Effect of reaction temperature on the catalytic performance of bio-CZ-500 and chem-CZ(insets are the structure model)(a);The effect of different molar ratios on the catalytic performance of bio-CZ-500(b);Comparisons of catalytic performance of four catalysts(c);Long-term stability test of bio-CZ-500 and chem-CZ catalysts during 100 h on stream(the soild symbols represent bio-CZ-500 and hollow symbols represent chem-CZ)(d)
反应后催化剂的TEM表征数据如图8所示。反应进行100 h 后,统计bio-CZ-500 催化剂上Cu 颗粒的粒径为(15.2±2.8) nm,与反应前Cu 的粒径相比几乎不变,说明在反应过程中Cu 与ZnO 颗粒之间存在一种稳定的Cu-ZnO 活性界面能够抑制Cu 颗粒的团聚增大,使得催化剂呈现较好的稳定性。相反,chem-CZ 催化剂在反应后,Cu 颗粒粒径增加至(19.5±2.1)nm,使得Cu 在ZnO 表面的分布更不均匀,而且从高分辨TEM 图中发现了CuZn(200)合金相的形成[15]。另外副产物H2O 在ZnO 载体表面的沉积会导致合金颗粒的团聚,这些结果证明chem-CZ 催化剂快速失活的主要原因是Cu 颗粒的烧结团聚。
2.5 催化剂的构效关系讨论
采用XPS对反应前后催化剂表面Cu、Zn元素的化学结构与电子性质进行表征。如图9(a)中,932.5~935.0 eV 范围内对应的是Cu 2p3/2的光电子峰,940~945 eV 处是其卫星伴峰[31],说明反应前催化剂中Cu主要以Cu2+的形式存在。反应前的bio-CZ-500 催化剂中Cu2+的结合能(933.8 eV)略大于标准Cu2+结合能(933.6 eV)。一般来讲这是由于周围Zn2+的影响[32],Zn2+的电负性大于Cu2+,使得Cu 整体电子云密度降低,结合能增加,证明bio-CZ-500 催化剂中CuO 与ZnO 的高度分散性。chem-CZ 催化剂Cu2+的结合能为933.6 eV,表明反应前chem-CZ 催化剂中Cu 主要为CuO[33]。通过对比反应后的催化剂,CuO经过H2还原后形成了大量的Cu0。由于在催化剂制样表征过程中单质铜极易氧化,因此观察到反应后催化剂XPS 谱图中存在部分的Cu2+。通过对出峰位置进行拟合并计算谱图峰面积之比发现,chem-CZ中Cu0的含量依然远高于bio-CZ-500,这说明反应过程中chem-CZ 产生了大量的CuZn 合金(该物种不易被氧化)。

图7 反应前的bio-CZ-500催化剂的透射电镜图[(a)~(c)];反应前的chem-CZ催化剂的透射电镜图[(d)~(f)];[其中图(b)、(e)中内插图为Cu颗粒的粒径分布]Fig.7 Representative TEM images of fresh bio-CZ-500 catalyst[(a)—(c)]and fresh chem-CZ catalyst[(d)—(f)][Insets in(b),(e)show the particle size distributions of Cu nanoparticles]

图8 反应后的bio-CZ-500催化剂的TEM图[(a)~(c)];反应后的chem-CZ催化剂的TEM图[(d)~(f)][其中图(b)、(e)中的内插图为Cu颗粒的粒径分布]Fig.8 TEM images of spent bio-CZ-500 catalyst[(a)—(c)]and spent chem-CZ catalyst[(d)—(f)][Insets in(b),(e)show the particle size distributions of Cu nanoparticles]
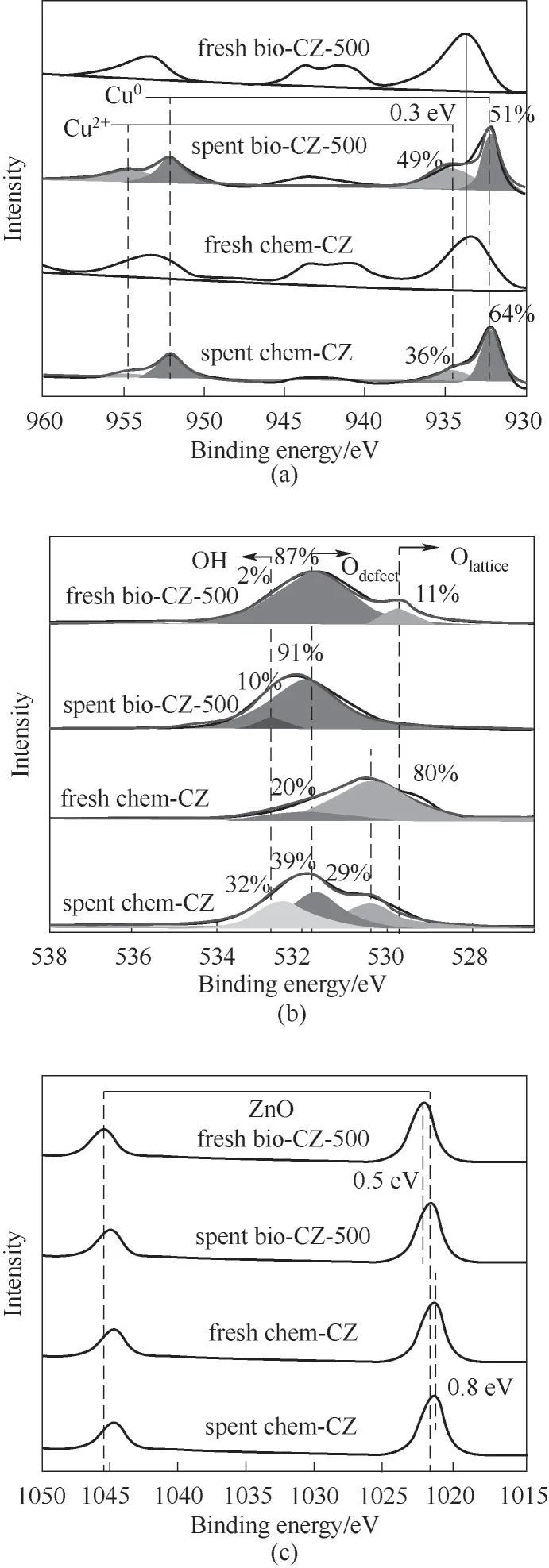
图9 反应前后bio-CZ-500与chem-CZ催化剂的XPS谱图Fig.9 XPS spectra of bio-CZ-500 and chem-CZ catalysts before and after the catalytic reaction
如图9(b)所示,结合能在526~538 eV 之间为O 1s 的能谱范围,结合能在529.7 eV 处的光电子峰代表ZnO 中的晶格氧;结合能在530.6 eV 处的光电子峰代表ZnO 表面的缺陷氧;结合能在531.6 eV 处的光电子峰为OH-的特征峰。通过拟合并计算谱图峰面积之比,发现反应前bio-CZ-500 催化剂中表面缺陷氧的浓度高达87%,同时含有10%的晶格氧[8];相反,反应前chem-CZ 催化剂中缺陷氧的浓度只有20%,晶格氧浓度高达80%。经过100 h 的反应后,bio-CZ-500 催化剂中的缺陷氧升高至91%,同时OH-的浓度升高,这说明仅少部分副产物水残留在催化剂表面。反应后chem-CZ催化剂表面的OH-浓度升高至32%,说明副产物水在chem-CZ 催化剂表面的扩散速率低。另外,与chem-CZ 催化剂相比,bio-CZ-500 表面丰富的氧空位更有利于催化剂对CO2的吸附与活化[34]。
图9(c)中1015~1050 eV 区间范围内对应的是Zn 2p 的能谱[32]。结合能1021.8 eV 处为Zn2+的标准光电子峰,对于反应前bio-CZ-500 催化剂,Zn 2p 谱图向高结合能方向偏移。这是因为bio-CZ-500 催化剂中ZnO 粒径大小与分散度都比较好,同时Cu2+的高度分散也会导致Zn2+的化学环境发生变化。所以当CuO 在反应中被还原为Cu0后,反应后bio-CZ-500 催化剂中Zn 2p 谱图的结合能又恢复到ZnO 的标准出峰位置。这证明了bio-CZ-500 催化剂在反应过程中存在稳定的Cu-ZnO 活性界面使得两者保持原有的元素性质。相反,反应后的chem-CZ 催化剂中Zn 2p 谱图与反应前chem-CZ 催化剂中Zn2+相比往低结合能方向偏移,说明在反应过程中产生了CuZn合金[32],这与图9(a)的Cu 2p光电子谱所得结论相吻合。
为了揭示bio-CZ-500 催化剂具备较高活性原因,通过H2程序升温还原实验考察两种催化剂的还原能力(图10)。从H2-TPR 谱图可以看到,两种催化剂中的还原性能存在差异。其中bio-CZ-500 在160.4℃的还原峰归属于CuO 的还原,205℃处的还原峰表明部分CuO 与ZnO 形成了稳定的Cu-ZnO 界面需要更高的还原温度将其转化为Cu0[35],500~600℃范围内的还原峰为ZnO 的特征还原峰。在chem-CZ 催化剂中只出现一个位于182.6℃处的还原峰,比bio-CZ-500中CuO 的特征峰要高。一方面是因为在程序升温过程中,bio-CZ-500 中CuO 粒径小且分散较好易被还原;另一方面是由于chem-ZnO中CuO由于分散度较差,高温下容易团聚变大,需要较高的还原温度[31]。对于ZnO 来说也是如此,由小颗粒堆积而成的bio-CZ-500 中ZnO 远小于chem-ZnO,因此其还原温度也低。另外,从H2消耗量的角度来看,bio-CZ-500 也远高于chem-CZ,可进一步增强催化剂对CO2的加氢效率。
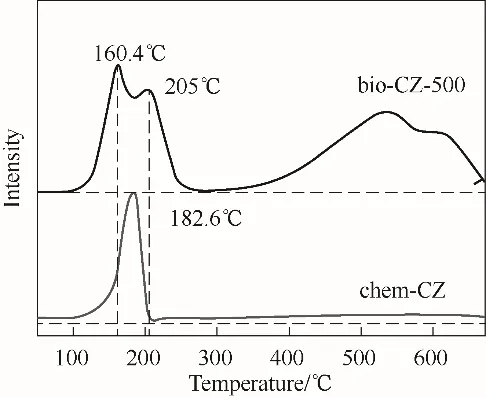
图10 bio-CZ-500与chem-CZ催化剂的H2程序升温还原谱图Fig.10 H2 TPR profiles of bio-CZ-500 and chem-CZ catalysts
综合上述反应前后催化剂的表征结果,提出了两种Cu/ZnO 催化剂中结构与性能之间的关系。如图11所示,由花粉为生物模板而合成的bio-Cu/ZnO催化剂具有多级孔结构,高度分散的Cu与ZnO所形成Cu-ZnO界面是其活性位点[36],甲醇的选择性高达81%,且碳骨架的弱亲水性也促进了副产物水在催化剂表面的脱附,赋予了催化剂更好的稳定性。相反化学沉积沉淀法合成的chem-Cu/ZnO 为正六面体结构,不具有多孔结构,Cu 颗粒主要分散在ZnO外表面,在反应过程很容易产生CuZn 合金,对氢气吸附效率降低,有利于逆水煤气反应(RWGS)的进行,导致甲醇的选择性低于50%。此外,副产物水在chem-Cu/ZnO 催化剂表面脱附速率过慢,引起Cu颗粒的团聚,导致催化剂快速失活。

图11 Cu/ZnO催化剂的结构与催化活性之间的构效关系Fig.11 The structure-performance relationship of Cu/ZnO catalysts
3 结 论
本文采用花粉为生物模板制备多层次空间结构的ZnO 载体及Cu/ZnO 催化剂,并研究CO2加氢制甲醇的催化性能,得出以下结论。
(1)通过一系列表征手段揭示了bio-CZ-500 催化剂能够完整复制出花粉的多级孔结构,同时通过控制焙烧温度部分保留生物模板的多孔碳结构。与化学沉积沉淀法制备的chem-CZ 催化剂相比,bio-CZ-500化剂在CO2加氢制甲醇反应中具有较高的活性与良好的稳定性。
(2)通过研究催化剂结构与性能之间的构效关系,发现生物模板独特的多维、多层次空间结构具有“一举两得”的作用:一方面多级孔结构有利于提高Cu的分散度和中间产物扩散;另一方面碳骨架的弱亲水性也促进了反应副产物水的脱附,从而提升催化剂的稳定性。
(3)bio-CZ-500 催化剂中高度分散的Cu 纳米颗粒与ZnO 颗粒所形成的活性Cu-ZnO 界面是促进甲醇高选择性(81%)的主要原因。化学沉积沉淀法制备的chem-CZ 催化剂由于CuZn 合金的存在,对H2的解离吸附效率低,其强亲水性表面易导致副产物水在催化剂表面的堆积,引起催化剂的失活。这一工作为制备高效稳定的Cu 基工业催化剂提供新思路。
符 号 说 明
GHSV——反应空速,ml·g-1·h-1
MMeOH——MeOH的摩尔质量,g·mol-1
nCO2,in——反应器进口CO2气流量,mol
nCO2,out——反应器出口CO2气流量,mol
SMeOH——产物MeOH选择性,%
STYMeOH——产物时空产率,mg·h-1·g-1
VCO2——原料气中CO2的体积分数,%
XCO2——CO2转化率,%
