磁共振模拟定位影像及磁共振诊断影像与定位CT融合的精准性比较
2021-07-21张策
张策
湖北省黄冈市团风县人民医院 (湖北黄冈 438000)
放射治疗是治疗恶性肿瘤患者的主要方式。随着近年来医疗科技的发展,精确放射治疗在临床上的优势逐渐凸显,可以在满足理想的治疗效果基础上,减轻患者放射治疗的痛苦,提升患者的治疗依从性[1]。精确放射治疗的实现主要依靠影像学技术精确的定位能力。CT 技术作为放射治疗计划的基础,具有操作简单、可重复性高等优势,但软组织分辨力较差,对于中枢神经系统、软组织部位的肿瘤需联合MRI 技术满足治疗需求,可在MRI 诊断影像(magnetic resonance diagnostic imaging,MRIdiag) 与CT 模拟定位影像上勾画靶区,但受扫描方式及患者体位的影响,精准性存在一定局限性[2-3]。近年来,放射治疗专用MRI 模拟定位机在肿瘤治疗中的应用频率逐渐增加,可行多种体位扫描,但是否有利于提升精准性仍鲜有研究。为此,本研究探究MRI 模拟定位影像(magnetic resonance simulated localization imaging,MRIsim)及MRIdiag 与定位CT 融合的精准性,评价MRIism 的应用价值,现报道如下。
1 资料与方法
1.1 一般资料
选取2019年1月至2020年9月我院收治的29例患者,其中男18例,女11例;年龄7~81岁,平均(58.68±11.35)岁;脑胶质瘤10例,前列腺癌19例。本研究经医院医学伦理委员会审核批准。
纳入标准:经病理组织学检查确诊;患者及家属均对本研究知情同意。排除标准:其他颅内肿瘤、头颈部肿瘤、腹部肿瘤、盆腔内肿瘤;精神障碍难以有效沟通交流。
1.2 方法
模拟定位:(1)CT 模拟定位,依据定位部位固定患者体位,脑胶质瘤患者采用头架固定,前列腺癌患者采用体部固定架固定,制作热塑膜,使用3D 激光灯确定参考位点,选择美国通用公司CT590大孔径模拟定位机以十字交叉法标记体表位点行CT 模拟定位,扫描层厚为2.5 mm,脑胶质瘤患者扫描范围为头顶至1椎体,前列腺癌患者扫描范围为腰4椎体下缘至会阴下2 cm,患者下床,CT 定位过程结束;(2)MRI 模拟定位,CT 模拟定位完成后1~2 d,采用飞利浦Ingenia 3.0T MR-RT 以CT 扫描所标记位点行MRI 模拟定位,扫描层厚及扫描范围均与CT 模拟定位一致,患者下床,MRI 定位过程结束。所有患者均采用美国CIVICO 公司提供的CT 和MRI 兼容的固定装置及3D 方法但不设置角度进行扫描,其中脑胶质瘤患者的2片Flex 灵活线圈贴于热塑膜外,前列腺癌患者的体部线圈放置在线圈桥架上。
图像融合:由1名高年资的影像学医师完成图像融合,采用刚性匹配办法将CT 模拟定位影像、MRIsim 及医院影像归档和通信系统网络中的MRIdiag 上传至Pinnacle 9.0计划系统进行影像融合,影像融合时先将两个影像手动粗略匹配,然后行基于算法的全图像自动融合,观察各个解剖器官的重叠情况,最后以手动调整为主将感兴趣区域设置在肿瘤区域进行微调,当肿瘤区域的解剖结构最大程度地匹配时融合工作完成。
危及器官(organ at risk,OAR)及靶区勾画:基于CT模拟定位影像、MRIsim 及MRIdiag 勾画OAR,选择勾画容易、生理性运动小以及勾画者主观因素影响小的OAR 进行比较;同时基于CT 模拟定位影像和MRIsim 的融合影像(fusion image of CT simulated localization image and MRIsim,F_CTMsim)以及CT 模拟定位影像和MRIdiag 的融合影像(fusion image of CT simulated localization image and MRIdiag,F_CTMdiag)勾画靶区,前列腺癌患者仅照射前列腺及精囊腺靶区。
计划设计:依据基于CT 模拟定位影像勾画的OAR 以及基于融合图像勾画的靶区为原则设计治疗计划,脑胶质瘤计划选择眼球、脑干、全脑,设计5~7野共面或非共面计划;前列腺癌计划选择骨盆,设计7野共面计划。所有计划均依据QUANTEC 限量要求来限制OAR 的剂量。
1.3 观察指标

1.4 统计学处理
采用SPSS 24.0统计软件进行数据分析,符合正态分布的计量资料以±s表示,组间比较采用t检验,计数资料以率表示,组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 OAR 体积
脑胶质瘤患者基于CT 模拟定位影像、MRIsim 及MRIdiag 勾画的体积比较,差异均无统计学意义(P>0.05);前列腺癌患者基于CT 模拟定位影像勾画的盆骨体积均大于MRsim、MRIdiag,差异有统计学意义(P<0.05);前列腺癌患者基于MRIsim 和MRIdiag 勾画的盆骨体积比较,差异无统计学意义(P>0.05),见表1。
表1 OAR 体积(cm3,±s)
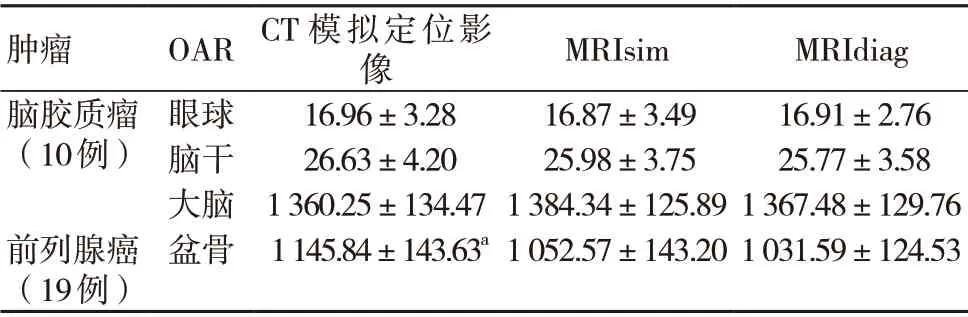
表1 OAR 体积(cm3,±s)
注:OAR 为 危 机 器 官,MRIsim 为MRI 模 拟 定 位 影 像,MRIdiag 为MRI 诊断影像;与基于MRIsim、MRIdiag 勾画饭盆骨体积比较,aP<0.05
肿瘤 OAR CT 模拟定位影像MRIsim MRIdiag脑胶质瘤(10例)眼球 16.96±3.28 16.87±3.49 16.91±2.76脑干 26.63±4.20 25.98±3.75 25.77±3.58大脑 1 360.25±134.47 1 384.34±125.89 1 367.48±129.76前列腺癌(19例)盆骨 1 145.84±143.63a 1 052.57±143.20 1 031.59±124.53
2.2 OAR 剂量学
脑胶质瘤及前列腺癌患者基于CT 模拟定位影像、MRIsim 及MRIdiag 勾画的OAR 剂量学比较,差异均无统计学意义(P>0.05),见表2。
表2 OAR 剂量学(cGy,±s)
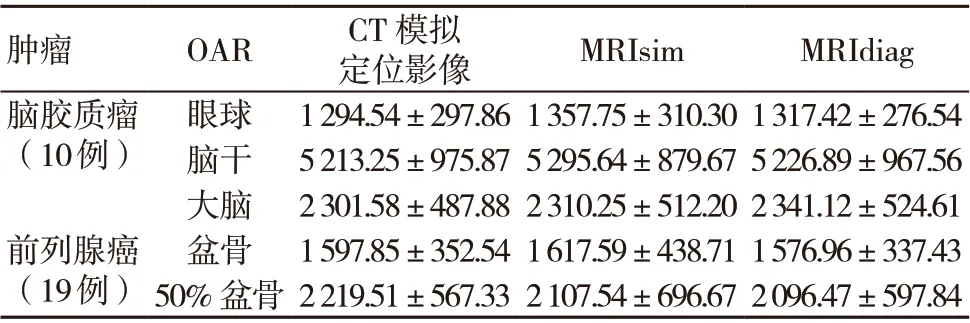
表2 OAR 剂量学(cGy,±s)
注:OAR 为 危 机 器 官,MRIsim 为MRI 模 拟 定 位 影 像,MRIdiag 为MRI 诊断影像
肿瘤 OAR CT 模拟定位影像 MRIsim MRIdiag眼球 1 294.54±297.86 1 357.75±310.30 1 317.42±276.54脑干 5 213.25±975.87 5 295.64±879.67 5 226.89±967.56大脑 2 301.58±487.88 2 310.25±512.20 2 341.12±524.61前列腺癌(19例)脑胶质瘤(10例)盆骨 1 597.85±352.54 1 617.59±438.71 1 576.96±337.43 50%盆骨2 219.51±567.33 2 107.54±696.67 2 096.47±597.84
2.3 OAR 轮廓的一致性和相似性
脑胶质瘤患者及前列腺癌患者CT 模拟定位影像与MRIsim 比较的S大于CT 模拟定位影像与MRIdiag 比较的S,差异有统计学意义(P<0.05);脑胶质瘤患者及前列腺癌患者CT 模拟定位影像与MRIdiag 比较的S和MRIdiag 与MRIsim 模拟定位影像比较的S差异无统计学意义(P>0.05),见表3。
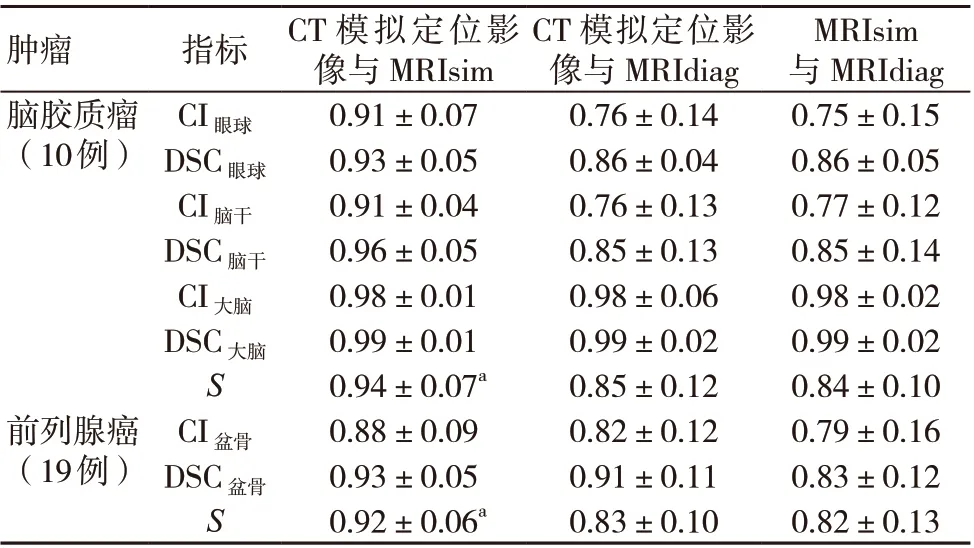
表3 OAR 轮廓的一致性和相似性
2.4 靶区体积、剂量学、一致性和相似性
脑胶质瘤及前列腺癌患者基于F_CTMsim、F_MRIdiag勾画的靶区体积及剂量学比较,差异均无统计学意义(P>0.05);脑胶质瘤及前列腺癌患者基于F-CTMsim、F-CTMdiag勾画的靶区CI、DSC分别为0.97、0.98;其中脑胶质瘤临床靶体积(clinical target volume,CTV)为0.93、0.97 cm3,计划靶体积(planning target volume,PTV)为0.95、0.98 cm3;前列腺癌患者CTV为0.95、0.98 cm3,PTV为0.97、0.98 cm3。
3 讨论
放射治疗模拟定位为肿瘤放射治疗治疗基础环节[4]。目前,临床在放射治疗模拟定位中以CT 为基础,与传统X 线定位技术相比,CT 三维成像技术更有利于提供丰富的解剖学信息及电子密度信息[5-6]。但因CT 三维成像技术在软组织、盆腔、脊髓等组织中应用效果不佳,在放射治疗定位中存在一定局限性。张扬子等[7]在对低位直肠癌术前放射治疗靶区勾画研究中发现,与CT 定位相比,MRI 技术在软组织恶性肿瘤定位中效果更为理想。而相关研究表示,为保证放射治疗精准性,将MRI 技术与CT 技术融合,效果更为理想[8-9]。MRIsim 的出现,将MRI 定位与放射治疗体位精准对接,进一步提升了靶区定位精准性,同时解决了既往患者放射治疗中托架无法安放问题[10-11];而此种技术将磁场强度由低场提高到中高场,图像质量显著提升,有利于提升定位精准性[12]。但目前关于MRIsim 与CT 融合是否可在此基础上进一步提升定位精准性仍鲜有研究。
本次危及器官体积及剂量学结果比较中,29例患者均行MRIdiag、MRIsim 技术扫描,并分别与CT 图像刚性匹配融合,在对2种类型恶性肿瘤患者的4个危及器官进行体积、剂量比较中,CT 模拟定位影像勾画的盆骨体积较大,但在其他危及器官勾画中,三者勾画体积与剂量水平均相近,说明除盆骨外,三种技术在其他器官放疗定位效果良好,但就具体数据而言,MRIsim、MRIdiag 技术效果稍强,考虑原因与以上两种技术可提升靶区准确度及图像质量相关,与龚修云等[13]研究结果相近。
在危及器官轮廓一致性和相似性比较中脑胶质瘤患者及前列腺癌患者CT 模拟定位影像与MRIsim 比较的S大于CT 模拟定位影像与MRIdiag 比较的S,考虑原因为,MRIsim 技术可避免手工数据转移形成的转译错误,在对头颈部、下腹部及四肢区域扫描中,这些区域组织对高能射线更为敏感,肿瘤异质性更明显,因此MRIsin 与CT 融合匹配精准性更为理想;同时其放疗体位及固定系统精准性提升,可有效减少运动伪影对图像质量的影响,对后续靶区勾画、制定治疗方案、修正MRI 适应性计划具有积极意义[14]。顾莹等[15]学者对脑胶质瘤、鼻咽癌、前列腺癌放射治疗患者定位研究中发现,除盆腔外,鼻咽癌患者全脑MRIdiag 勾画体积较CT、MRIsim 小,说明在对恶性肿瘤患者定位期间,单一应用CT、MRIdiag 技术可能存在指标异常情况,考虑原因可能与患者固定期间分次摆放头颈部位置不确定性、头颈部固定性相对较差等因素相关;同时在其研究中发现MRIsim 与CT 融合定位精准性更为理想,本研究结果与其相近,证实MRIsim 与CT 融合定位优势。综上所述,与MRIdiag 相比,MRIsim 与CT 模拟定位影像融合可以提升图像匹配的精准性,且并未明显改变所勾画靶区剂量学,效果更为理想。
