饲料蛋白质含量测定改良方法的稳定性及其消煮时间的研究
2021-07-21卢锦斌张利敏
卢锦斌,张利敏
(1.西北农林科技大学 动物科技学院,陕西 杨凌 712100;2.陕西华秦农牧科技有限公司,陕西 杨凌 712100)
饲料原料蛋白质含量测定是饲料生产过程中的重要环节。目前测定饲料原料及产品中蛋白质含量的方法主要有凯氏定氮法和近红外光谱法[1-2]。尽管近红外光谱分析技术具有检测速度快、无损、不消耗试剂、前处理简单以及可同时检测多种成分等多方面的优势,但凯氏定氮法仍然是检测饲料蛋白质含量的重要方法。传统的凯氏定氮法存在一个明显的弊端,即耗时过长,仅消煮样品就需3~3.5 h,既影响工作效率又消耗能量。因此,通过改良缩短凯氏定氮法的消煮时间具有较大的应用价值。
消化环节的改良通常从催化剂和消化液两个方面入手。传统凯氏定氮法的催化剂为CuSO4·5H2O与K2SO4(1:15)混合催化剂。浓H2SO4与混合催化剂组合法消化充分,但由于消泡问题未得到解决,无法实现快速分解。早期有不少研究报道,利用H2O2与浓硫酸发生的剧烈反应消化样品可极大地缩短消化时间,原因是H2O2有助于消泡,且适当加大H2O2的量可促样品快速分解,且减少电能消耗[3-5],这种改良的凯氏定氮法也被称为双氧水测定法。但不同研究报道中H2O2添加量以及消煮时间并不统一,且该方法测定值与凯氏定氮法测定值并不相等,各报道也没有验证不同饲料原料用该方法与用凯氏定氮法测定的蛋白质含量值的比值是否相同,以及同一类型原料不同来源的样品该比值是否相同。这些问题没有解决导致该方法不能得到推广应用。鉴于该方法对原料的快速消化特点,有必要对其进一步研究,以便在实际生产中能够利用其优势。本研究通过系列试验,确定H2O2的添加比例以及消煮时间,并分析讨论该方法的稳定性。在此基础上,通过比较和分析不同饲料原料凯氏定氮法(即国标法)和改良凯氏定氮法蛋白质含量测定值的比值,探讨将该方法应用于饲料原料蛋白质含量测定的可行性。
1 材料与方法
1.1 饲料原料
玉米、麸皮、豆粕、棉粕、DDGS、玉米蛋白粉、鱼粉均由本地企业提供。
1.2 方法
1.2.1 样品处理和试验设计 以四分法采集所需样品,置于65 ℃风干后,经粉碎机粉碎,过40目筛后保存。每次试验所有样品都同时采用改良方法和传统凯氏定氮法同时进行测定,每个样品每种方法均设计3个重复。
1.2.2 试验方法 首先利用H2O2完全替代凯氏定氮法中的混合催化剂(即H2O2直接催化法)进行消化。设定H2O2与浓硫酸的比例为1:1,选取常规凯氏定氮法中常用的浓硫酸添加量12 mL,因此 H2O2的添加量也为12 mL。由于H2O2只对焦化后的有机物进行氧化,因此,测定时先称取0.5 g样品于消化管中,再加入12 mL浓硫酸,静置几分钟待样品焦化后,缓慢加入等体积的H2O2,样品在浓硫酸与H2O2的作用下被分解消化,然后再进行蒸馏定氮和滴定。
H2O2替代部分混合催化剂测定法(即H2O2-混合催化剂法)具体操作如下:0.5 g样品添加7.5 mL H2O2,H2O2与浓硫酸比例仍为1:1,同时添加4 g混合催化剂(为凯氏定氮法添加量的1/2)。测定时,先称取0.5 g样品和4 g混合催化剂于消化管中,再加入7.5 mL浓硫酸,置于已预热好的消化炉中消化约5 min待样品焦化后缓慢加入7.5 mL的H2O2,然后置于消化炉消化20 min左右,最后再进行蒸馏定氮和滴定。
1.2.3 统计分析 采用SPSS 18.0软件中的单因素方差分析,其余数据使用SPSS软件中的成对样本t检验进行差异显著性检验,P<0.05表示差异显著,P<0.01表示差异极显著。
2 结 果
2.1 H2O2直接催化法测定结果
首先选取低蛋白含量的玉米和高蛋白含量的豆粕进行测定。凯氏定氮法在消化阶段耗时3~3.5 h,而利用H2O2直接催化法可以看到在H2O2与浓硫酸的剧烈反应下,样品迅速消化,随着反应的进行,消化液颜色逐渐变淡直至透明,5 min内溶液基本澄清,10 min内反应趋于平静,但为充分消化,共消化20 min。将凯氏定氮法所测值与12 mL H2O2直接催化法所测值进行比较分析,结果如表1所示。用H2O2完全替代催化剂配合浓硫酸对样品进行消化,测定的样品蛋白质含量低于凯氏定氮法测定的蛋白质含量。其中,玉米凯氏定氮法所测值与H2O2直接催化法所测值的比值均值为1.240,而豆粕凯氏定氮法所测值与H2O2直接催化法测值的比值均值为1.189,比值差异极显著(P=0.005)。但两种原料测定值比值组内RSD (relative standard deviation, RSD)均小于3%。
为了检测不同原料两种方法蛋白质测定值比值是否都不相等,又选取4种不同蛋白含量原料的样品进行验证。结果如表2所示,每种原料不同重复比值RSD<1%,但不同原料两种方法测定值的比值都不相同,蛋白质含量越高的样品,两种测定值的比值越大,显示该方法消化并不充分。不同原料H2O2直接催化法测定值与凯氏定氮法测定值的比值存在极显著的差异(P<0.01)。

表 1 玉米和豆粕蛋白质含量凯氏定氮法与H2O2直接催化法测定值比值Table 1 The ratios of protein content in corn and soybean mealdetermined by Kjeldah method and H2O2 direct catalysis method

表2 凯氏定氮法与H2O2直接催化法测定不同原料的蛋白质含量Table 2 Determination of protein content in different samplesby Kjeldah method and H2O2 direct catalysis method
2.2 H2O2-混合催化剂法测定结果
上述结果显示单独使用H2O2原料消化不充分。为使原料成分充分消化,试验调整了催化剂的配方,采用H2O2-混合催化剂法进行测定,结果见表3。

表3 样品蛋白质含量H2O2-混合催化剂法测定值与凯氏定氮法测定值及其比值Table 3 Protein content of samples determined by H2O2-mixed catalyst method and Kjeldah method and their ratio
由表3可知,各组样品H2O2-混合催化剂法与凯氏定氮法测定值的比值RSD均<3%,显示比值大小稳定,但不同原料该比值仍然不相等,不同原料比值大小与其蛋白质含量无关。其中DGGS该比值最低,接近1;豆粕和鱼粉该比值相近(P>0.05),分别为1.062和1.056,而玉米和玉米蛋白粉比值最高,且两种原料的该比值接近(P>0.05),分别为1.129和1.126。
在凯氏定氮法中,样品的消化温度在360~410
℃之间,低于360 ℃样品中的氮消化不完全,高于410 ℃则容易造成氮的损失,因此在该法中设定的温度为360 ℃,符合要求范围。消化时间是影响消化效果的另一关键因素,为探究在H2O2-混合催化剂法中消化时间对于测定结果的影响,本试验接下来选取蛋白质含量适中、在上述两类方法中表现都较为稳定的豆粕作为样品,以H2O2-混合催化剂法进行试验,消化时间分别设定为5、10、15、20、25、30 min。由图1可以看出,消化时间在5~20 min内,豆粕中蛋白质含量随着消化时间的延长而提高,但从20 min至30 min,蛋白质含量测定值没有变化。因此可以推测在H2O2-混合催化剂法中,当消化温度为360 ℃、总消化时间为20 min时,样品蛋白质含量的测定值可以达到最高值,说明不同原料两种方法测定结果比值不相等的原因并非消化时间不充分所致。
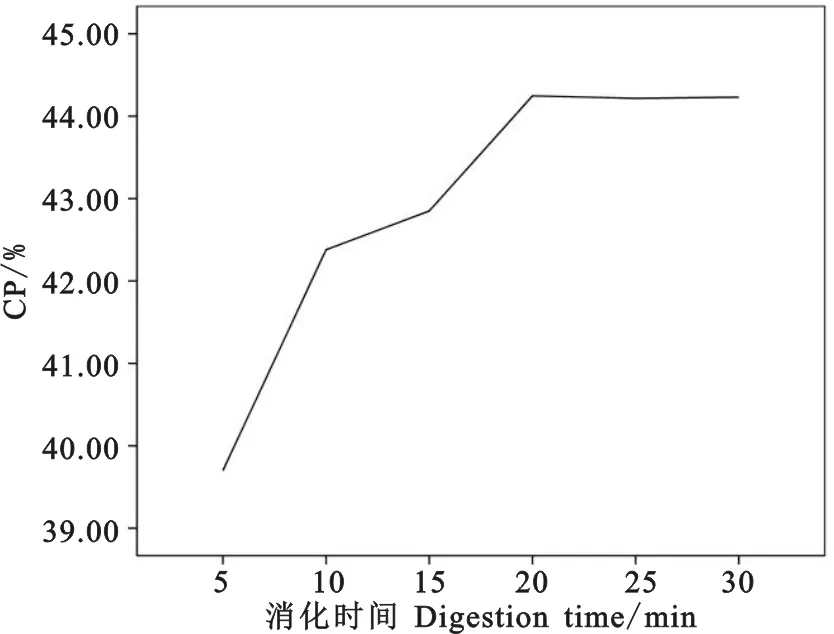
图1 不同消化时间对混合催化剂法测定结果的影响Fig. 1 Effects of different digestion time on thedetermination results of mixed catalyst method
为了检测不同来源同种原料H2O2-混合催化剂法与凯氏定氮法测定值比值是否稳定,在前述结果的基础上,又测定了3种来源玉米和3种来源DDGS,其结果见表4,不同来源玉米H2O2-混合催化剂法与凯氏定氮法测定值比值接近(RSD=0.22%)。同样,不同来源DDGS的H2O2-混合催化剂法与凯氏定氮法测定值比值也很接近(RSD=0.30%)。

表4 不同来源同种饲料蛋白质含量H2O2-混合催化剂法与凯氏定氮法测定值及其比值Table 4 Protein content of the same feed with different sources determined by Kjeldah method and H2O2-mixedcatalyst method(HMC)and their ratio
3 讨 论
本试验结果表明,H2O2直接催化法虽然比凯氏定氮法节省了大量的时间和能源,但其测定值与凯氏定氮法测定值相差较大,蛋白质含量越高的原料,两种方法的比值相差越大,显示H2O2直接催化法消化不充分。H2O2完全替代催化剂的H2O2直接催化法所测值虽然小于凯氏定氮法测定值,但对于同一样品而言,每种原料不同重复比值RSD<2%,说明该方法测定值的比值是稳定的,因为统计学上认为某组数据RSD<3%时即可认为该组各数值稳定。与赵德志等[5]报道的结果不一致的是,玉米两种测定方法比值与豆粕两种方法测定比值差异极显著,说明不能根据H2O2直接催化法测定结果、再根据同一比值去推算其他检测样品的凯氏定氮法测定值。
由于使用H2O2直接催化法测定蛋白含量时原料消化不充分,参考苗雪原[6]报道,本试验又采用H2O2-混合催化剂法进行测定,所测CP含量与凯氏定氮法所测CP含量仍然存在差异,但与H2O2直接催化法测定值相比,该方法测定值更接近凯氏定氮法所测值,而且每种原料两种测定方法的比值大小与原料蛋白质含量没有相关性。蛋白质含量最低的玉米凯氏定氮法与H2O2-混合催化剂法测定值比值反而高于鱼粉和豆粕,而玉米蛋白粉该比值与玉米该比值相等。这些结果说明,该比值与蛋白质含量无关,而与原料种类有关。导致这一现象的原因可能是因为不同原料细胞壁结构等不同,使得蛋白质消化程度不同。
本试验最后检测了不同来源的玉米与DDGS样品H2O2-混合催化剂法与凯氏定氮法测定的蛋白质含量,结果显示,不同来源的玉米和不同来源的DDGS,两种测定方法的比值都非常稳定,再次证实H2O2-混合催化剂法与凯氏定氮法测定值的比值大小与原料种类有关。本结果为利用H2O2-混合催化剂法测定单一原料蛋白质含量的可靠性提供了证据。
4 小 结
同一种原料蛋白质含量用H2O2直接法和H2O2-混合催化剂法测定时,均极大地缩短消化时间,但其测定值均低于凯氏定氮法测定值,H2O2-混合催化剂法测定结果更接近凯氏定氮法,且消化20 min可获得稳定的测定值。不同原料H2O2-混合催化剂法与凯氏定氮法测定值的比值不相等,但不同来源同种原料样品该比值稳定,说明不同原料未充分消化或氮损失部分与原料蛋白质含量无关,而与原料种类有关。因此,不能根据某种原料的H2O2-混合催化剂法与凯氏定氮法蛋白质测定值的比值来推测其他原料的该比值,但可以通过建立不同单一原料凯氏定氮法蛋白质测定值与H2O2-混合催化剂法蛋白质测定值的比值数据库,利用H2O2-混合催化剂法快速测定单一饲料原料的蛋白质含量。
