铝炭微电解去除废水中重金属的效果研究
2021-07-16刘鹏宇王晓琴刘晓波
刘鹏宇,王晓琴,刘晓波
(兰州交通大学 环境与市政工程学院,兰州 730070)
随着现代工业的快速发展,矿山、冶金、电镀、机械制造、农药、医药、油漆、纸业等工业在生产过程中均会排放大量的重金属废水,其重金属离子主要包括铬、铜、铅、镉、镍、锌等[1].重金属废水由于毒性大、难降解、残留时间长且可通过食物链在有机体内富集等特点,其任意排放对生态环境安全和人类健康均存在很大的隐患[2].目前,水体中重金属的处理方法主要有化学沉淀法、吸附法、离子交换法、电解法等.但是这些方法均存在一定的局限性,例如化学沉淀法存在污泥产量大,沉淀物降解性能差,易产生二次污染等缺点[3-5].吸附法吸附剂使用寿命短,再生困难,去除效果易受pH值、杂质离子的影响等[6-8].离子交换法对水质要求高,难以应对实际工艺中的水质波动[9-11].电解法能耗高,且产生的副产物也会影响重金属离子的回收[12].微电解技术因其投资少、处理费用低的特点而受到重点关注.
微电解法简单易行、低廉有效,其原理是利用阳极金属与阴极炭之间的电极电位差,自发形成微小原电池,通过氧化还原、絮凝、吸附共沉淀作用对废水进行处理,具有经济、实用、高效和操作简单等优点[13-15].目前常用的微电解技术大多以金属铁为阳极,即铁炭微电解,原电池反应如下:
阳极(Fe):Fe-2e-→Fe2+E0=-0.44 V
(1)
阴极(C):2H++2e-→2H·→H2E0=0 V
(2)
电极反应生成活性物质,与废水中部分物质发生氧化还原作用;铁溶解后产生大量的Fe2+、Fe3+,在碱性条件下发生一系列反应形成络离子及Fe(OH)2、Fe(OH)3胶体,通过吸附、凝聚作用将废水中的污染物净化去除[16-19].林国俊等[20]、于艳杰等[21]、肖宏康等[22]利用铁炭微电解法处理重金属废水,研究表明,在适宜的铁炭投加量、反应时间和pH值条件下均能取得很好的效果.
但是铁炭微电解处理重金属废水,铁溶出量大,出水有颜色,增加了后续处理工艺的负担[23],为此,提出了以金属铝为阳极,活性炭为阴极的铝炭微电解.铝炭微电解原理与铁炭相似,但是铝炭微电解的pH适用范围更广,且铝炭的电极电位差(E(Al3+/Al)=-1.667 V)也高于铁炭微电解法.从理论上对比两种微电解方法,铝炭微电解在处理工业废水方面占据更大的优势.采用铝炭和铁炭微电解在同等条件下对比处理含铬废水,在适宜的条件下,铝炭微电解处理重金属废水效果要远远高于铁炭微电解[24].
本研究以废水中常见的4种重金属离子为对象,采用铝炭微电解对其进行处理,考察反应时间、初始pH值、铝炭质量比、震荡速度、震荡时间等因素对模拟废水中的铜、铅、镍、镉四种重金属离子去除效果所产生的影响.分别利用SEM和 EDS表征铝屑、活性炭在反应前后的表面物理形貌及物质组成变化,研究铝炭微电解对废水中各种重金属离子的去除机理.
1 实验材料及方法
1.1 实验材料
实验仪器:美国瓦里安原子吸收分光光度计(220F型);美国奥立龙pH测试仪(Orion828型);大地磁力加热搅拌器(CJJ78-1型);常州普天数显水浴恒温振荡器(SHA-82A型);泰斯特电热鼓风干燥箱(101-IAB型);日本光学低真空扫描电子显微镜(JSM-5600LV型);英国牛津X射线能量色散谱仪.
试剂:氢氧化钠(NaOH);盐酸(HCl);氯化铜(CuCl2·2H2O);硝酸铅(Pb(NO3)2);氯化镉(CdCl2·21/2H2O);氯化镍(NiCl·6H2O).以上试剂均为分析纯.
1.2 实验方法
1.2.1 活性炭处理
筛分活性炭(1~3 mm粒径)以自来水洗净后置于烘箱内烘干(105 ℃);分别用浓度为100 mg/L的Cu(Ⅱ)、Pb(Ⅱ)、Ni(Ⅱ)、Cd(Ⅱ)水样浸泡活性炭24 h,期间12 h换一次水样,使其吸附饱和,消除活性炭吸附作用对实验的影响;最后将其烘干后备用.
1.2.2 铝屑的前期处理
每次实验前分别用质量分数为5%的NaOH溶液和体积分数为3%的HCl浸泡铝屑(1~3 mm粒径)10 min,去除其表面油分和氧化物,并冲洗干净.为消除因铝屑表面暴露于空气中形成氧化膜对实验效果的干扰,铝屑必须现处理现用.
1.2.3 铝炭微电解实验
加入一定质量比的铝屑和活性炭于150 mL锥形瓶中,使其混合均匀,用pH仪精确控制水样pH值为3.0~7.0(含Pb(Ⅱ)水样pH值为3.0~5.0)后,取20 mL模拟水样,静置(或震荡)5~80 min后,用取样管吸取上清液进行测试分析.研究所用模拟水样初始质量浓度均为100 mg/L.
1.2.4 分析方法
用原子吸收分光光度计测定Cu(Ⅱ)、Pb(Ⅱ)、Ni(Ⅱ)、Cd(Ⅱ)剩余浓度,并计算得到去除率;采用SEM分析铝屑、活性炭表面形貌,EDS分析物质组成.
2 结果与讨论
2.1 反应时间的影响
配制浓度为100 mg/L的模拟废水,调节其初始pH值为3.0.称取质量比为1∶1的铝炭6.0 g,研究不同反应时间(震荡速度为0 r/min)和震荡时间(震荡速度为100 r/min)对含不同重金属模拟水样中去除率的影响,结果如图1和图2所示.
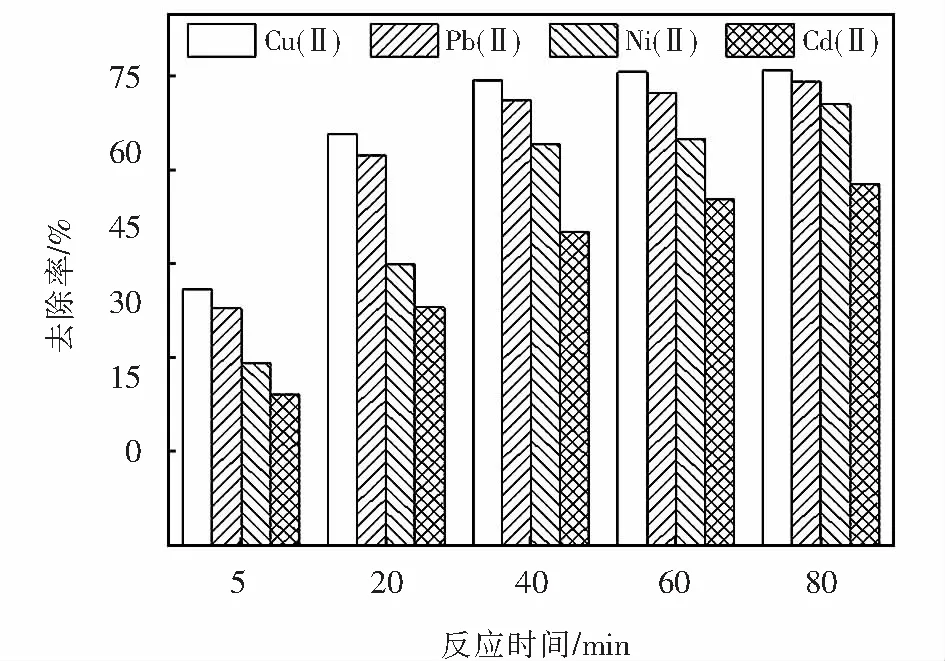
图1 反应时间的影响Fig.1 Effect of reaction time

图2 震荡时间的影响Fig.2 Effect of oscillation time
微电解过程中要实现氧化还原反应发生的离子必须满足吉布斯自由能小于零.根据吉布斯自由能和原电池电动势的关系(ΔrGm=-nFE),可得到当E>0时会自发发生离子的还原反应.而铝炭微电解中各反应标准电极电动势如下:
E=E(Cu2+/Cu)-E(Al3+/Al)=0.342 V +1.667 V=2.009 V
E=E(Pb2+/Pb)-E(Al3+/Al)=-0.126 V+1.667 V=1.541 V
E=E(Ni2+/Ni)-E(Al3+/Al)=-0.246 V+1.667 V=1.421 V
E=E(Cd2+/Cd)-E(Al3+/Al)=-0.407 V+1.667 V=1.26 V
因此溶液中铜、铅、镍、镉离子都能自发的在标准状态下进行阴极还原作用.由图1可知,在静置条件下,四种金属离子去除率随着时间的增加均呈现上升趋势,在40 min之后趋于平稳.其原因是随着反应时间的增加,体系中大部分金属离子被还原为单质,同时,铝阳极上被氧化的Al3+的絮凝作用去除部分金属离子[25],还有部分金属离子形成氢氧化物沉淀从而有效去除.反应时间过长也会导致活性炭表面被沉淀物所覆盖包裹,并且析出的金属单质也会附着在铝屑表面阻碍反应进行,使金属离子的去除率增加不明显[26-27].从图2中可以看到,震荡时间为20 min时,Cu(Ⅱ)、Pb(Ⅱ)去除率已经达到最佳,说明震荡作用可增加待处理水样中的溶解氧,在有氧条件下原电池阴阳两极电位差增大,其氧化还原作用增强,原电池反应在早期迅速发生,使金属离子在短时间内被去除[28].而Ni(Ⅱ)、Cd(Ⅱ)去除率则到40 min以后才趋于平稳,这是因为Ni(Ⅱ)、Cd(Ⅱ)的电极电位不高,在铝炭微电解过程中需要更长的时间才能去除.综合考虑,确定铝炭微电解处理重金属废水的反应时间为40 min.
2.2 铝炭质量比的影响
配制初始pH值为3.0,浓度为100 mg/L的模拟水样作为待处理水样,在反应时间为40 min,震荡速度为0 r/min,铝炭总质量为6.0 g的条件下,考察铝炭质量比对含不同重金属模拟水样去除率的影响,结果见图3.
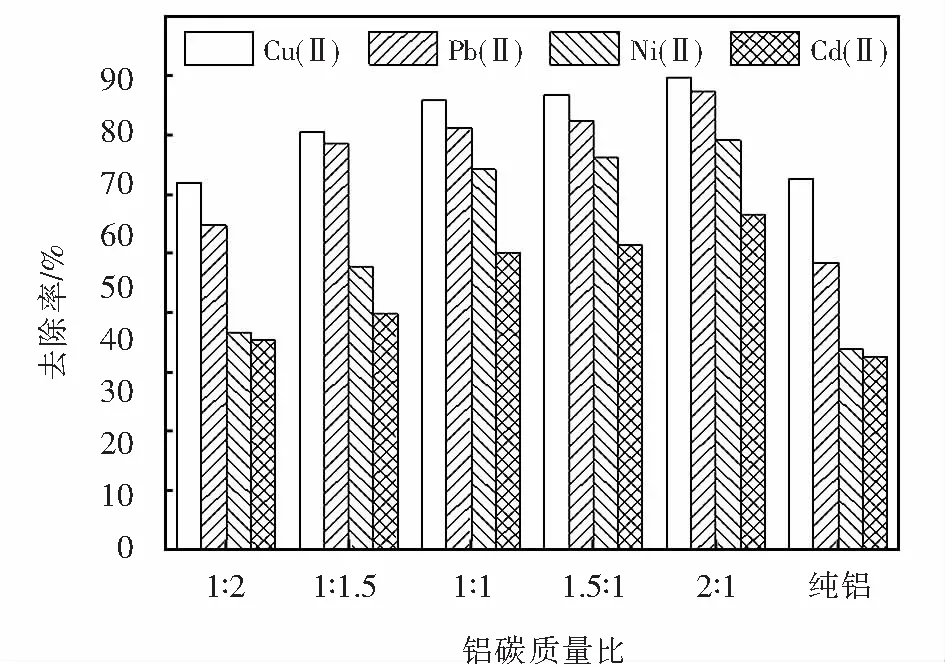
图3 铝炭质量比的影响Fig.3 Effect of aluminum-carbon mass ratio
铝屑和活性炭颗粒构成微小原电池从而发生微电解反应,当铝炭总质量一定时,反应中添加铝屑与活性炭的质量比例对反应的进行程度具有不同的影响.当电极电位较高的金属接触铝炭时,其离子化过程发生在铝屑表面,电子从阳极铝转移至阴极炭发生还原作用导致金属离子被还原为单质从而产生置换作用.置换完全程度和置换速度会受到发生置换作用的两种金属的电极电位差的影响[29].在纯铝条件下,重金属离子的去除主要通过铝与其发生置换反应,因ECu>EPb>ENi>ECd>EAl,故这四种金属离子的去除率依次呈现下降趋势.金属离子因置换作用致其析出而浓度不断降低,在平衡电位等于稳态电位时停止析出[30],故铝的置换作用对金属离子的去除率不高.当加入活性炭时,以铝屑为阳极,活性炭为阴极,铝屑和活性炭形成微电池,体系中形成电子流向.金属离子作为电子受体随着体系中电子的多向流动,在铝炭接触表面得到电子的机率增加,反应速度也随之增加.故微电解反应速度受体系中原电池的数量影响发生变化[31].质量比等于2∶1的铝炭对金属离子去除效果达到最佳,此时Pb(Ⅱ)、Ni(Ⅱ)、Cd(Ⅱ)、Cu(Ⅱ)去除率为77.45%、69.15%、56.67%、79.73%,而后随着铝炭质量比降低,活性炭投加量不断增加,导致活性炭大量堆积,阻碍铝屑、活性炭与废水的充分接触,使铝炭电极表面失衡,反而抑制了原电池的电极反应[32],导致金属离子去除率呈现下降趋势.综合考虑经济性,确定适当的铝炭质量比为1∶1.
2.3 初始pH值的影响
配制浓度100 mg/L的四种含不同重金属模拟废水.称取质量比为1∶1的铝炭6.0 g,在反应时间为40 min,震荡速度为0 r/min时考察初始pH值(考虑到pH值≥5.5时会出现Pb(OH)2沉淀物,pH值范围取3.0~5.0)对模拟废水中不同重金属离子去除作用的影响,图4表明反应结果.

图4 初始pH值对去除率的影响Fig.4 Effect of initial pH on treatment efficiency
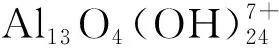
2.4 震荡速度的影响
配制浓度100 mg/L的四种含不同重金属模拟废水,调节其初始pH值为3.0.称取质量比为1∶1的铝炭6.0 g,研究震荡时间为40 min震荡速度对含不同模拟废水中四种重金属离子去除率的影响,图5表明反应结果.
图5表明,震荡速度增大导致铜、铅、镍、镉四种重金属离子去除率先上升后下降.震荡速度为100 r/min时达到最佳去除效果,铜、铅、镍、镉去除率分别为92.52%、91.71%、85.88%、79.58%.原因是附着在铝屑和活性炭表面的絮状物在适度震荡产生的摩擦作用下脱落,铝屑和活性炭表面不断更新,使得微电解反应持续发生,故体系中的重金属离子的阴极还原作用会随着震荡速度的增加而升高[36];过大的震荡速度不仅会导致形成气泡包裹在铝屑和活性炭表面,不利于铝炭微粒形成微电池,还会使氢氧化铝的吸附共沉淀作用减弱导致重金属离子去除率降低.
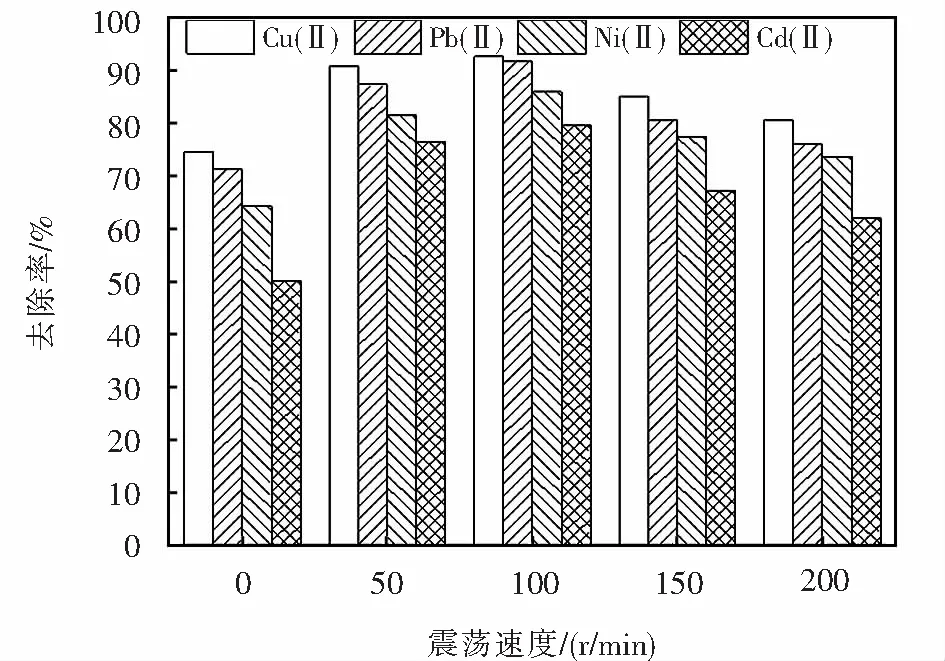
图5 震荡速度的影响Fig.5 Effect of oscillation speed
2.5 表面特征分析
表面特征分析利用SEM和EDS对铝屑和活性炭表面反应前后的表面形貌及物质组成进行表征,如图6和图7结果.所取铝屑和活性炭均为最佳条件下反应后的样品.

图6 铝屑及活性炭反应前后表面形貌对比Fig.6 Appearance of surface of aluminum and activated carbon before and after the reaction

图7 铝屑及活性炭反应前后表面能谱分析对比Fig.7 EDS of surface of aluminum and activated carbon before and after the reaction
从图6中可以清楚的观察到反应前的铝屑表面平整,而反应后的铝屑表面凹凸不平,与铜发生反应的铝屑表面被大量的块状物覆盖,且带有大量裂痕;与铅反应后的铝屑表面腐蚀坑较多且块状物相对较少,但表面附着白色颗粒物或絮状物;与镍反应后的铝屑表面同样出现腐蚀洞坑并附着颗粒物;与镉发生反应的铝屑则表面平整,存在大量的块状物质.电化学反应在铝屑表面产生了电化学腐蚀效应,以及置换和吸附共沉淀作用.另外可以清楚地观察到与铜、铅、镍、镉反应过的铝屑表面附着物依次减少.反应前的活性炭表面孔道横截面清晰可见,在与重金属反应后则表面覆盖了一层白色絮状物,微孔结构被破坏,尤其是和铜、铅反应后的活性炭表面孔结构大部分被覆盖,而与镍、镉反应后的活性炭表面白色絮状物较少.由于反应后的铝屑和活性炭表面结构复杂,形貌差异较大,为进一步考察其形貌和元素组成,对此进行能谱分析.
对比反应前后的铝屑表面,铝含量明显降低,且反应后的铝屑表面检测到了相对应的金属元素.根据各离子与铝氧化还原电动势及金属活动顺序,可得到在标准状态下,阴极会自发进行Cu(Ⅱ)、Pb(Ⅱ)、Ni(Ⅱ)、Cd(Ⅱ)的还原.由EDS结果分析,铝屑表面的Cu(Ⅱ)、Pb(Ⅱ)、Ni(Ⅱ)含量远高于活性炭表面,结合金属活动顺序分析,对Cu(Ⅱ)、Pb(Ⅱ)、Ni(Ⅱ)有主要去除作用的氧化还原和置换反应主要发生在铝屑表面,而Cd(Ⅱ)在活性炭表面的含量却高于铝屑表面,其原因可能是镉与铝的电极电位差较前几种金属小,置换反应速度也随之下降,铝炭微电解反应过程中铝屑被不断腐蚀,形成Al3+进入水溶液,之后形成氢氧化铝附着于活性炭或者沉于反应容器底部,并通过絮凝共沉淀作用将部分Cd(Ⅱ)去除.
此外活性炭表面有微量Na、K、Ca、Si元素分布,这是因为待处理水样中的各种杂质离子被活性炭少量吸附,另外活性炭表面铝元素含量均高于其他金属元素,结合微电解原理,可以推断活性炭表面是金属离子絮凝共沉淀的主要场合.由于微电解过程中产生的絮体及颗粒物会覆盖在铝屑和活性炭表面,使其与体系内的离子接触,进而阻碍了微电解反应的进行,这也是随着反应时间增加,金属离子的去除率不再增加的原因.
3 结论
1) 铝炭微电解法处理重金属废水中Cu(Ⅱ)、Pb(Ⅱ)、Ni(Ⅱ)、Cd(Ⅱ)时,在震荡速度为40 min,铝碳质量比为1∶1,初始pH值为3.0,震荡速度为100 r/min的条件下,铝炭微电解的处理效果最佳,Cu(Ⅱ)、Pb(Ⅱ)、Ni(Ⅱ)、Cd(Ⅱ)的去除率分别可达92.52%、91.73%、85.88%、79.58%.
2) 金属离子的氧化还原电位会极大地影响铝炭微电解的处理效果,使得在相同条件下Cu(Ⅱ)、Pb(Ⅱ)、Ni(Ⅱ)、Cd(Ⅱ)去除率依次下降.
3) 震荡作用会提供一定的溶解氧,使得铝炭微电解在早期迅速进行,大大缩短了铝炭微电解处理重金属废水的反应时间,另外适度的震荡速度还可以促进铝炭表面更新,减缓铝屑钝化.
4) 铝屑和重金属离子发生的置换作用、原电池阴极还原作用以及氢氧化铝的吸附共沉淀作用是铝炭微电解对废水中重金属离子的主要去除机理.
5) 结合SEM和EDS表征分析得出,氧化还原和置换作用主要发生在铝屑表面,絮凝共沉淀作用则主要发生在活性炭表面.
