新型偕胺肟基改性β-环糊精聚合物对Pb(Ⅱ)、Cu(Ⅱ)的吸附 *
2021-07-12赖志文徐梦雅胡志鹏江洪流
赖志文,徐梦雅,胡志鹏,江洪流
(南昌航空大学 材料科学与工程学院, 南 昌330063)
0 引 言
重金属在纺织、皮革、化妆品和造纸行业这些行业的染色过程中被大量用作媒染剂。长期饮用水受铅(Pb),铜(Cu)和镉(Cd)等重金属污染会导致心血管、肺部、免疫、神经、内分泌失调和癌症[1]。到目前为止,大量的水处理技术已经开发并用于去除重金属(HM),包括离子交换(IE)[2]、膜过滤[3]、凝结-絮凝-沉降(CFS)[4]和吸附[5]。在这些方法中,吸附是最广泛使用的方法,因为它易于安全地进行,具有高效率并且低成本。因此,研究开发新型吸附材料对于重金属离子污染的治理具有重要的意义。
β-环糊精(β-CD)由淀粉在酶解作用下产生的,7个α-连接D-吡喃葡萄糖单元的环状低聚糖,环糊精分子表现出“外亲水,内疏水”的特性,当用作吸附剂时,β-CD可以在水溶液中封装污染物,形成明确的主客体络合物[6],由于这些特点,在众多吸附剂中,β-CD在去除废水中污染物方面有巨大潜力。然而,β-CD在水中的有一定程度溶解并容易形成水合物,是其单独用作吸附剂的障碍。Alaaeddin Alsbaiee等[7]合成的多孔β-环糊精聚合物(P-CDP)衍生自四氟对苯二腈(TFPN)的β-环糊精羟基的亲核芳族取代,它能够快速地隔绝各种有机微量污染物。P-CDP中的腈基也可以转化为多种其他化学结构,程艳霞等[8]用偕胺肟基改性聚丙烯腈纤维,吸附高氟高铀废水;Bekir Satilmis等[9]用盐酸羟胺对于四氟对苯二腈聚合的PIM-1(5,5′,6,6′-四羟基-3,3,3′,3′-四甲基-1,1′-螺双茚满的羟基与TFPN交联反应所得本征微孔聚合物)进行化学改性已显示主要产生偕胺肟基结构并且这些产物表现出对铀酰离子具有选择性。Ren等人[10]用盐酸羟胺改性聚丙烯腈纤维表现出对阴离子染料甲基橙和重金属离子Cu(Ⅱ)和Pb(Ⅱ)的吸附效果。
在这项研究中,用β-环糊精的羟基与交联剂四氟对苯二腈进行亲核芳族取代,使用羟胺改性β-环糊精聚合物(CDP-CN)上的腈基,制备了有良好性能的重金属离子吸附剂,并探究了初始浓度和pH的对吸附的影响、吸附动力学、吸附等温线、吸附热力学以及吸附-解吸循环再生。
1 实 验
1.1 材料和仪器
1.1.1 主要试剂及材料
β-CD、四氟对苯二腈(> 98%),四氢呋喃(THF,99.9%,超干,带分子筛,用BHT稳定,水≤30×10-6(按K.F.),N,N-二甲基甲酰胺(DMF,99.9%,超干,含分子筛,水≤30 ×10-6(按K.F.计),羟胺(NH2OH,50%水溶液),Pb(NO3)2和Cu(NO3)2·3H2O,无水碳酸钾(K2CO3),二氯甲烷(AR,CH2Cl2),四氢呋喃(THF,AR),铜试剂(AR),二甲酚橙(AR),六次甲基四胺(CP)。
1.1.2 主要仪器
傅里叶红外光谱(FT-IR),德国Bruker公司;固态核磁共振波谱仪(13C NMR),日本电子公司;马尔文纳米粒度电位仪,英国马尔文公司;水浴恒温振荡器,金坛市易晨仪器制造有限公司;热重/差热综合热(TG)分析仪,美国Perkin-Elmer公司;紫外分光光度计,日本岛津有限公司;X射线光电子能谱(XPS),日本岛津公司;物理气体吸附性能测试(BET),美国麦克公司。
1.2 实验方法
1.2.1 β-环糊精聚合物(CDP-CN)的制备
向干燥的100 ml两口烧瓶中加入β-CD(0.94 g),四氟对苯二腈(0.5 g)和K2CO3(1.43 g),通N2然后用注射器加入THF(36 mL)和DMF(4 mL)(VTHF∶VDMF=9∶1),在85 ℃回流冷凝,并以500r/min搅拌,持续2天。将橙色悬浮液冷却,然后过滤,通过用0.1 mol/L HCl洗涤固体除去残留的碳酸钾直至停止释放CO2。回收的淡黄色固体,并通过H2O,THF(2次×100 mL)30 min和CH2Cl2(1次×50 mL)15 min来分离和活化。反应方程式如图1(a)。
1.2.2 偕胺肟改性β-CD聚合物(CDP-AM)的制备
参考Satilmis B[9]改性PIM-1的方法,将CDP-CN粉末(220 mg)在氮气惰性气氛下用加入无水四氢呋喃(60 mL)、10 mL羟胺,N2保护,并将反应混合物在设定温度65 ℃下连续搅拌30 min。将反应温度升高至69 ℃进行,24 h后冷却样品至室温,滤出沉淀物,并加入乙醇((5次×30 mL)洗涤,真空干燥,得到偕胺肟-β-环糊精聚合物(CDP-AM)。反应方程式如图1(b)。

图1 (a)CDP-CN聚合物和(b)偕胺肟改性β-CD聚合物的合成Fig 1 Synthetic route of CDP-CN and amidoxime modified β-CD polymer
1.3 分批吸附试验
选择Pb(Ⅱ),Cu(Ⅱ)作为代表污染物,研究CDP-AM聚合物的吸附性能。吸附实验在保证控制单一变量系统中进行。用去离子水,Pb(NO3)2和Cu(NO3)2·3H2O制备了Pb(Ⅱ),Cu(Ⅱ)储备液,背景液中含有0.01 mol/L NaNO3和5 mL HNO3,具有较高的水离子强度以防止水解。通过将储备溶液稀释至某些浓度(1~200 mg/L)获得Pb(Ⅱ)和Cu(Ⅱ)的工作溶液。通过0.1 mol/L HNO3/NaOH溶液、NH4Cl-NH3缓冲液和六次甲基四胺缓冲液控制工作溶液的所需pH值。
1.3.1 接触时间对吸附的影响以及吸附动力学
为研究接触时间对吸附平衡的影响以及吸附动力学实验,通过在30 ℃,pH=6吸附剂用量10 mg、C0为100 mg/L和150 mg/L和HMs体积25 mL的条件下,然后以150 r/min摇动,将Pb(Ⅱ)、Cu(Ⅱ)在预定时间内滤出,同时移取上清液并通过0.22 μm孔隙四氟乙烯膜过滤分离,以测定剩余的HMs浓度。
平衡吸附容量(qe,mg/g)和吸附百分比(%)由以下等式[11-12]计算:
(1)
(2)
其中C0和Ce(mg/L)是HMs溶液的初始和最终平衡浓度,V(mL)是溶液的体积,m(mg)是吸附剂的质量。
1.3.2 pH对吸附的影响
为了研究pH对HMs去除的影响,吸附剂用量10 mg、吸附温度30 ℃、C0为100 mg/L和150 mg/L和HMs体积25 mL的条件下。将HMs溶液的pH从1调节至6然后将150 r/min在下振荡24 h,移取上清液并通过0.22 μm孔径的膜过滤分离,加入显色剂,用紫外分光光度计确定剩余的HMs浓度(λmaxCu=452 nm、λmaxPb=582 nm)。
1.4 重复再生实验
为了研究吸附剂的再生,使用1% HNO3作为再生溶液。将吸附后的吸附剂用100 mL 0.1 mol/L的HNO3溶液和乙醇多次洗涤浸泡以解吸。为避免吸附剂在循环过程中的损失影响实验准确性,每一次循环吸附剂不少于三组平行试样收集滤液,在60 ℃下真空干燥以进行下一个吸附循环。进行5次连续的吸附-解吸循环以探究吸附剂再生。在每个循环后,收集滤液进行Uv-vis测试,计算去除效率。
2 结果与讨论
2.1 β-环糊精聚合物的表征
2.1.1 红外表征
图5为CDP-CN,β-CD单体、TFPN和CDP-AM的FT-IR光谱。TFPN的FT-IR在2 235 cm-1处的吸光度为腈基伸缩振动,在1268 cm-1处为C—F拉伸振动[12]。β-CD单体在2 930 cm-1为脂肪族C—H键、1 030 cm-1处的强烈C—O伸展和3423 cm-1处羟基伸缩振动[13-15]。CDP-CN的显示出1 268 cm-1的C—F拉伸振动,3 427 cm-1处的羟基[16],以及1 487 cm-1苯环上的C—C,2 938 cm-1、1 024 cm-1分别是亚甲基的C—H和C—O—C的伸缩振动,结果证明了CDP-CN的形成。对于CDP-AM偕胺肟基的一些重要振动是3 482和3 340 cm-1处的谱带,可以指定为反对称和—NH2基团的对称拉伸模式。将3 170 cm-1的带分配给O—H的伸缩振动。1656和923 cm-1处的谱带分别被指定为肟基的C—N拉伸模式和N—O拉伸模式[10]。
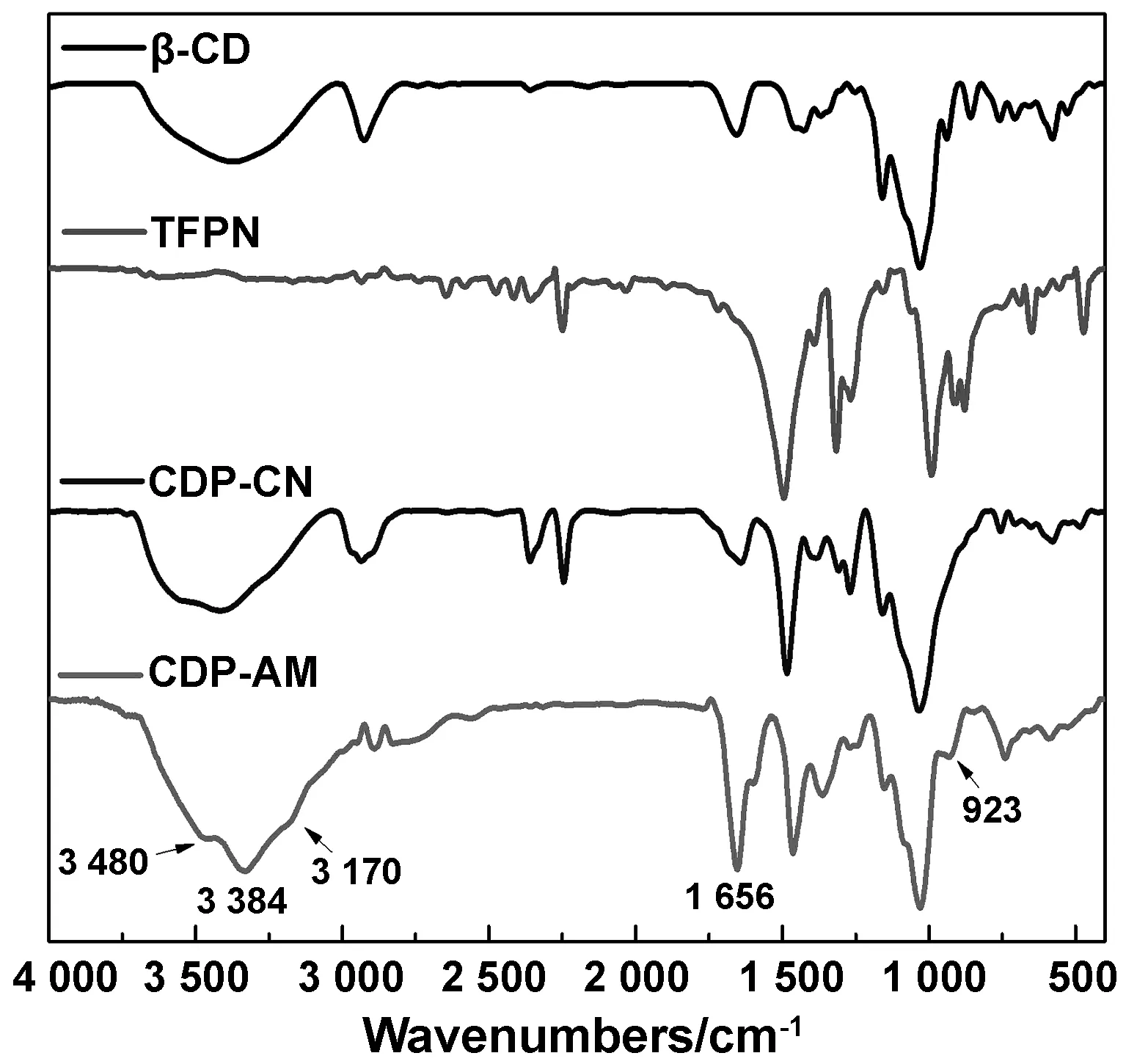
图2 TFPN、β-CD、CDP、CDP-AM的红外光谱Fig 2 Infrared spectra of TFPN, β-CD, CDP, CDP-AM
2.1.2 ζ电位分析
为了研究CDP-AM聚合物的质子化程度,测量了不同pH值下CDP-AM聚合物的ζ电位,如图3所示。随着pH值增大,ζ电位值降低。当pH值<4时,β-CD聚合物被质子化并携带较多正电荷;当pH值>4时,ζ电位值急剧下降,此时HMs离子带正电荷而CDP-AM聚合物带负电荷,利于HMs吸附。

图3 CDP-AM和CDP-CN聚合物在不同pH值下的ζ电位Fig 3 The zeta potential of CDP-AM and CDP-CN polymers at different pH values
2.1.3 热重分析
如图4所示,110 ℃时质量损失7.97%归因于吸附水的蒸发[17-19]。110~200 ℃时,TGA曲线保持稳定。此外,因为DMF在该温度范围内蒸发,但此范围无DMF的质量损失,说明成功除去DMF溶剂[20]。温度超过200 ℃时,质量损失为43.68%,这归因于β-CD单体和四氟对苯二腈的分解,在高于500 ℃的温度下,仍然存在18.06%的质量损失,这可能是由于碳链的分解造成的[21]。CDP-AM在第一阶段失重11.2%源于水分损失,其中100~380 ℃之间显示质量损失36.6%,200~380 ℃归因于偕胺肟基损失引起的[9]。100~450 ℃损失率41.5%。CDP-AM聚合物分解的第二阶段皆归因于聚合物网络的损失。

图4 (a)CDP-CN和(b)CDP-AM的热重分析结果Fig 4 TGA results of CDP-CN and CDP-AM
2.1.4 BET分析
氮吸附-解吸等温线在100 ℃下脱气不少于6 h,结果见图5中表明,CDP-CN的BET表面积为72.5 m2/g,平均孔径为3.54 nm,这证实了CDP-CN的BET表面积较大。而经过改性后的CDP-AM比表面积相对较小,仅有15.3 m2/g,孔径有所增大,所以BET图中吸附-脱附曲线发生交叉现象,这是由于样品比表面积较小所致,同时通过SEM图片也可以看出,CDP-AM表面存在少部分微孔,说明吸附过程中存在少量网络捕获作用。
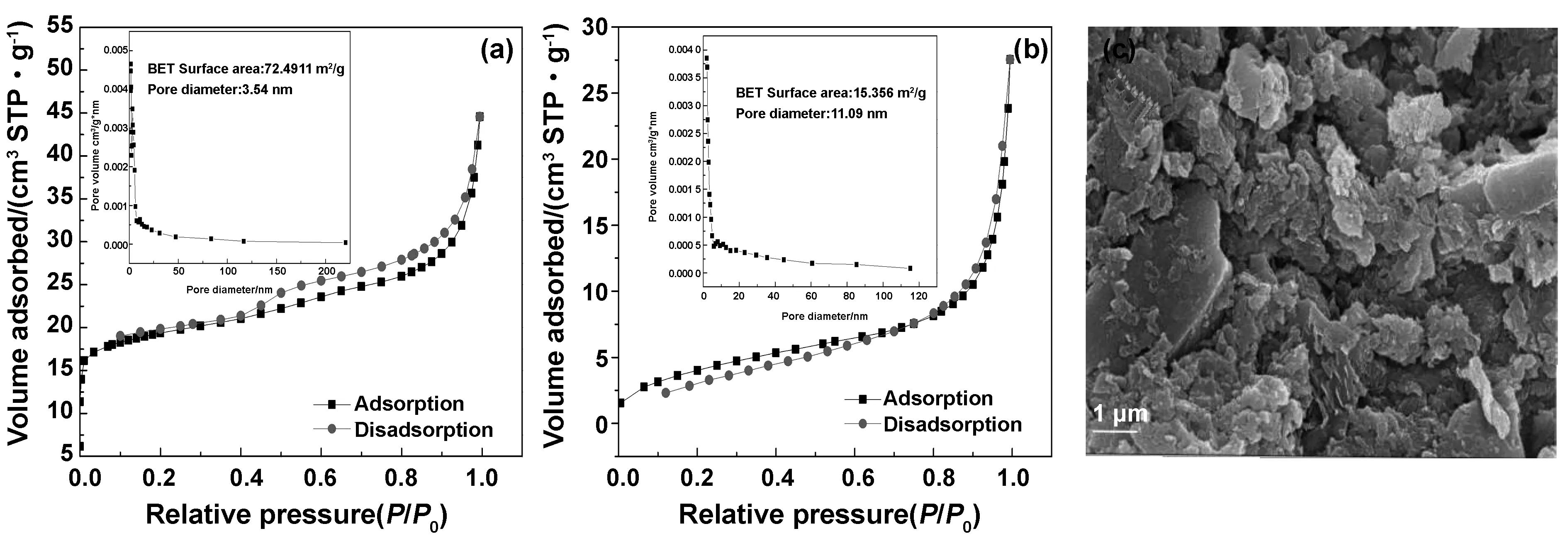
图5 (a)CDP-CN和(b)CDP-AM的氮吸附-解吸等温线,(c)CDP-AM的扫描电镜图像Fig 5 Nitrogen adsorption-desorption isotherm of CDP-CN and CDP-AM and SEM image of CDP-AM
2.1.5 固体核磁表征
图6给出了CDP-CN,CDP-AM的13C NMR结果。103×10-6(C1),74 ×10-6(C2,C3和C5),84 ×10-6(C4)和60 ×10-6(C6)处为环糊精自身结构,95×10-6和140 ×10-6时的共振(标记为7和2)分别对应于CDP-CN中新形成的烷氧基和芳香碳[12];在CDP-AM中112.6 ×10-6(标记为8)对应于新形成的C=N键,150.89 ×10-6(标记9)对应于新形成的C-NH2键[22],证明新形成了偕胺肟基。
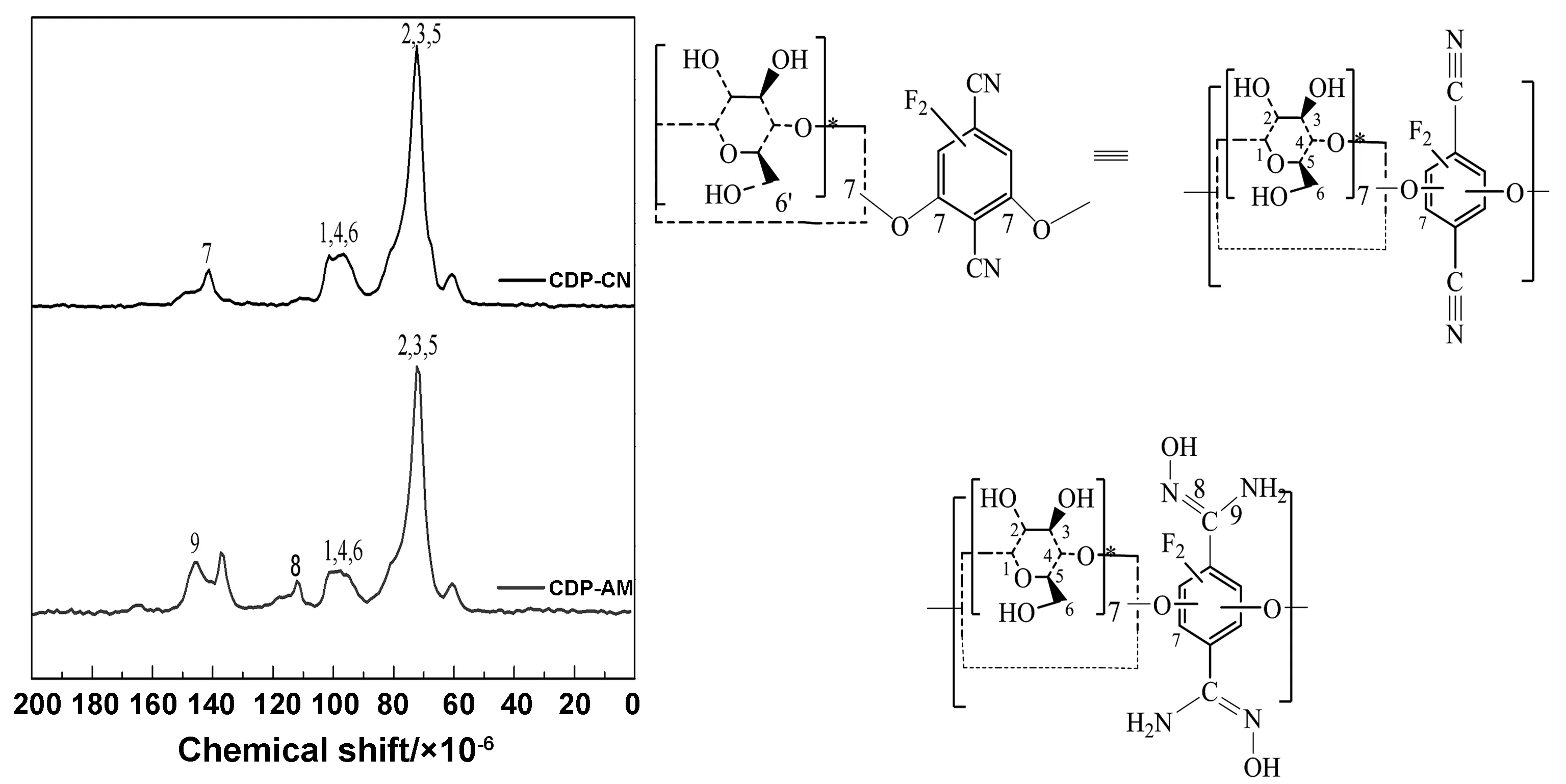
图6 CDP-CN和CDP-AM固态13C NMR光谱Fig 6 13C NMR results of CDP-CN and CDP-AM
2.1.6 XPS表征
还通过XPS表征证实了偕胺肟的功能化。CDP-AM的C1s,O1s和N1s以及总谱能级谱如图7所示。C1s谱已解析为284.2 eV(C—O—C/CH),286.7 eV(C—N/C—N)和287.6 eV(O—C—O)子峰值和292.2 eV(C—F)。N1s光谱显示两个峰,分别被胺和质子化的胺基拆分为399.8 eV(C—NH2)和401.7 eV的胺和质子化的胺基。O1s光谱可拆分为对应于C—O(531.5 eV),偕胺肟基中N—OH和环糊精结构中的C—O—C(532.9 eV)和C—O(533.9 eV)。

图7 CDP-AM的C1s,N1s,O1s以及CDP-CN和CDP-AM全谱扫描Fig 7 C1s, N1s, O1s and CDP-CN and CDP-AM full spectra scans of CDP-AM
2.2 分批吸附结果
2.2.1 接触时间对吸附的影响以及吸附动力学
CDP-AM对HMs的吸附如图8所示,考察了C0为100和150 mg/L的HMs溶液,尽管在早期还没有达到吸附平衡,但是根据不同的吸附系统,随着吸附剂和HMs之间接触时间的增加,不同吸附系统的吸附平衡可以在4~5 h内缓慢达到,吸附容量较可观,尤其对于Pb(Ⅱ)的吸附效率可以接近80%,>270 mg/g。
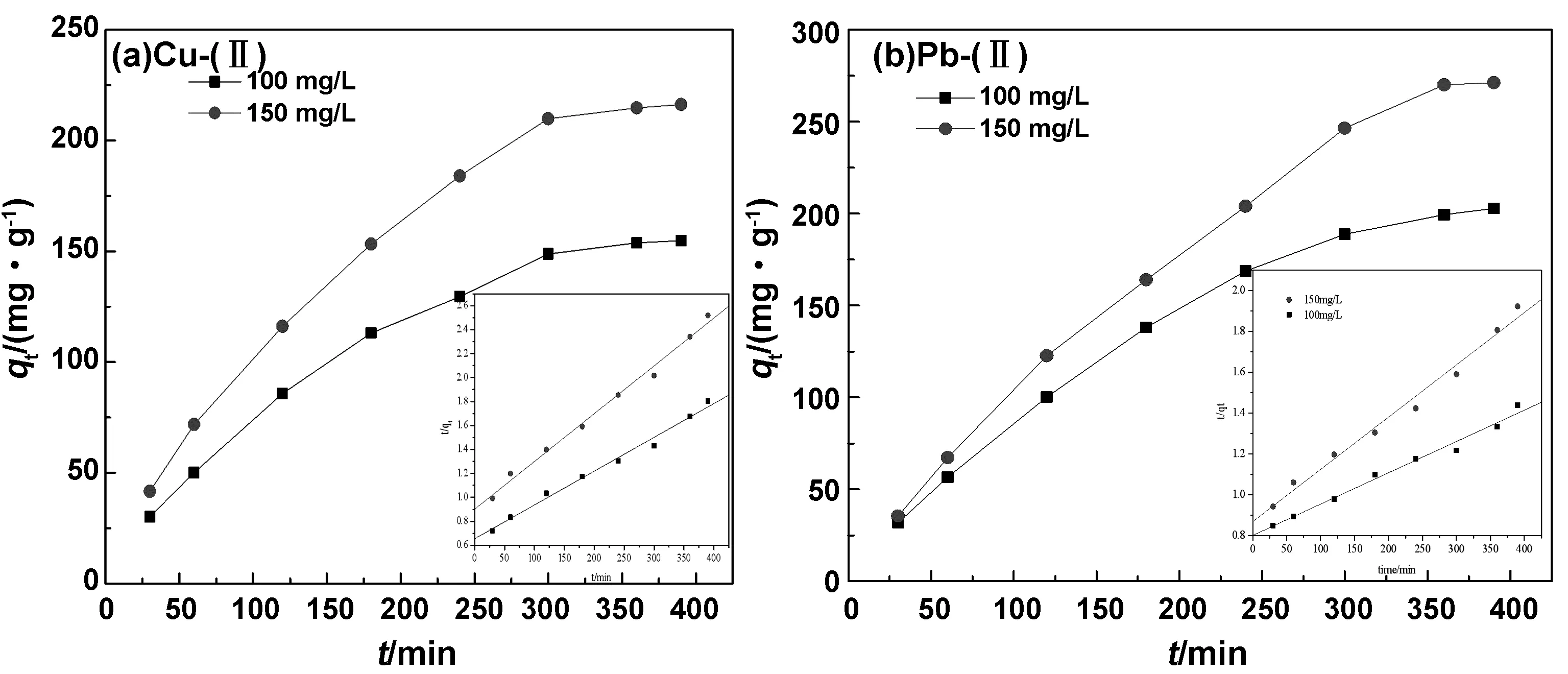
图8 接触时间对CDP-AM吸附Cu(Ⅱ)和Pb(Ⅱ)的影响,(a)(b)中插图为对应的二阶动力学拟合Fig 8 Effect of contact time on the adsorption of Cu (Ⅱ) and Pb (Ⅱ) by CDP-AM. The inset in (a, b) is the corresponding second-order kinetic fitting
动力学实验进一步评估吸附过程随时间的变化,动力学实验数据通过伪一级如图7和伪二级模型如图7进行模拟。伪一级动力学[23]和伪二阶动力学模模型[24](3)和(4)一般表示为:
ln(qe-qt)=ln(qe)-K1t
(3)
(4)
其中k1(min-1),k2(g/(mg min))分别是伪一级反应和伪二级反应的速率常数,qe(mg/g)和qt(mg/g)是该量在平衡和时间t分别的吸附容量。
Pb(Ⅱ)、Cu(Ⅱ)吸附的动力学参数如表1所示。Pb(Ⅱ)、C(Ⅱ)的伪二阶模型的相关系数远高于伪一阶模型。高相关系数值表明Pb(Ⅱ)、Cu(Ⅱ)吸附有利于伪二阶过程,化学吸附是主要控制步骤[25]。
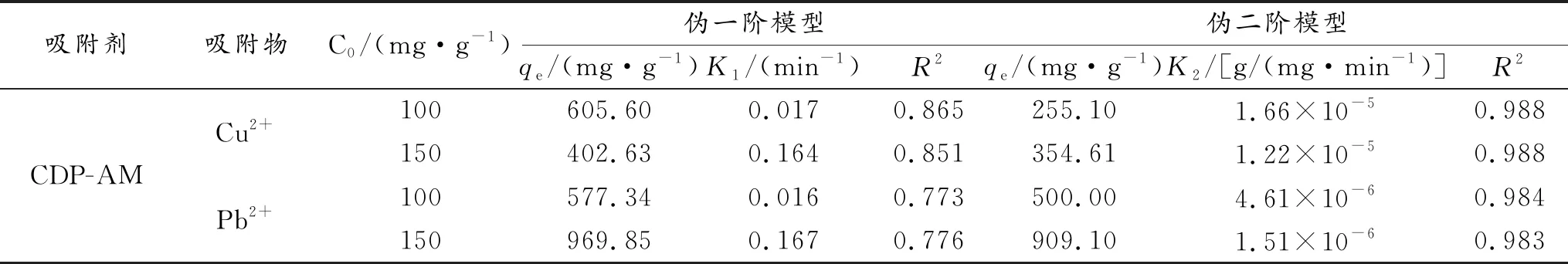
表1 CDP-AM吸附HMs的动力学参数
2.2.2 pH对吸附的影响
pH对Pb(Ⅱ)、Cu(Ⅱ)吸附的影响如图9所示,吸附去除效率随着pH值增大而增大,然而Pb(OH)2(s)的沉淀平衡常数为1.2×10-15,Cu(OH)2(s)的沉淀平衡常数为2×10-20[26]。碱性条件下Pb(Ⅱ)、Cu(Ⅱ)会产生沉淀,本实验pH值为1~6,pH误差±0.1,温度30 ℃。

图9 pH对CDP-AM吸附Cu(Ⅱ)和Pb(Ⅱ)的影响Fig 9 Effects of pH on Cu(Ⅱ) and Pb(Ⅱ) adsorption by CDP-AM
pH对Pb(Ⅱ)、Cu(Ⅱ)吸附的影响是由Pb,Cu物种的静电相互作用和分布引起的。酸性较强时,偕胺肟基中碱性的胺基高度质子化[11],具有阳离子的特征,而在随着pH值升高,吸附容量较低。当pH逐渐增大,同时Zeta电位数据也予以证明,体系携带大量负电,与重金属离子之间存在静电作用。重金属离子首先被吸引到CDP-AM表面,然后进行螯合,因此吸附容量大。
2.3 吸附等温线及热力学
2.3.1 吸附等温线
在这项研究中,在吸附等温线测试中,所有HMs的pH值为6±0.1,初始浓度依次为25,50,75,100,125,150 和200 mg/L,在303,313和323 K 3个温度下测试吸附性能。使用了两个常用的吸附等温模型,即Langmuir等温模型[27]和Freundlich等温模型[28],其中Langmuir等温模型可分为线性(请参见公式(5))和非线性(请参见公式(6))进行数据分析,其表示如下:
(5)
(6)
其中Ce是水溶液中HMs的平衡浓度(mg/L),qe是吸附剂上吸附的HMs的量(mg/g),qm是每单位重量吸附剂吸附形成完整单层的HMs的最大量。在表面上,KL表示吸附焓,应随温度变化,是Langmuir平衡常数。
对于Freundlich等温模型也可分为线性(请参见公式(7))和非线性(请参见公式8)进行数据分析,其表示如下:
(7)
(8)
其中Ce是水溶液中HMs的平衡浓度(mg/L),qe是吸附剂上吸附的HMs的量(mg/g),qm是每单位重量吸附剂吸附形成完整单层的HMs的最大量。KF和n分别是与吸附容量和吸附强度相关的Freundlich常数。
由图10对等温曲线的拟合并对比表2和表3的的模型参数数据,可以发现,Langmuir等温线模型无论线性还是非线性整体优于Freundich等温模型,线性Langmuir等温线模型的拟合结果具有最高的相关系数(R2)值,均大于0.99。通过对R2值的判断,属于单层吸附机理的线性Langmuir等温线模型较好地解释了CDP-AM对Pb(Ⅱ)和Cu(Ⅱ)的吸附过程。
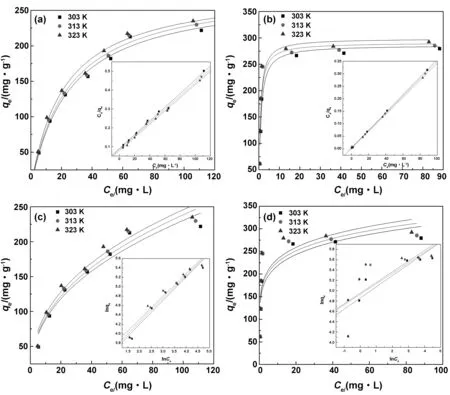
图10 三种不同温度下CDP-AM吸附Cu(Ⅱ)和Pb(Ⅱ)的等温线,图中(a)(b)及插图为Langmuir线性及非线性等温模型,(c)(d)及插图为Freundich线性及非线性等温模型Fig 10 Isotherms of Cu (Ⅱ) and Pb (Ⅱ) adsorbed by CDP-AM at three different temperatures. (a, b) Illustration are Langmuir linear and nonlinear isotherms. (c, d) Illustration are Freundich linear and nonlinear isothermal models
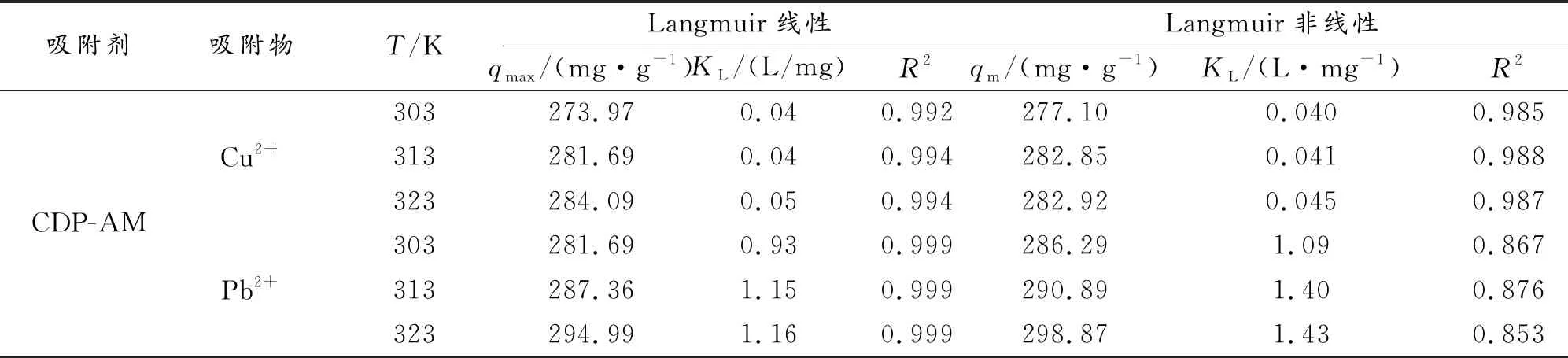
表2 CDP-AM对Cu(Ⅱ)和Pb(Ⅱ)的Langmuir等温线模型参数
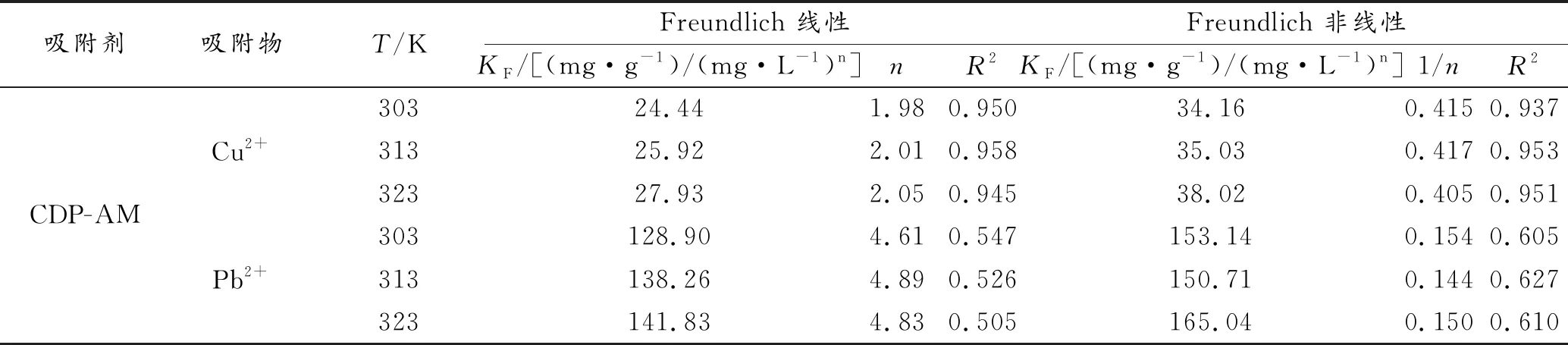
表3 CDP-AM对Cu(Ⅱ)和Pb(Ⅱ)的Freundich等温线模型参数
2.3.2 吸附热力学
研究了温度对303、313和323 K时的吸附行为的影响,CDP-AM的吸附过程是吸热还是放热,自发或非自发的,计算了Pb(Ⅱ)和Cu(Ⅱ)吸附的热力学参数。通过吸附等温线获得的数据通过Vant’Hoff方程计算,以评估包括焓变的热力学参数(ΔH0),熵变(ΔS0))和吉布斯自由能变化(ΔG0)。Van’t Hoff方程[29-30]可表示为公式(9)和(10):
(9)
(10)
其中R是通用气体常数(8.314 J/(mol·K),T是以开尔文为单位的温度。K0是吸附平衡常数。
通过绘制lnKd(Kd=qe/Ce),Y轴的值是lnKd0的值,1/T为X轴,我们可以得到ΔG0的值。表4显示了Pb(Ⅱ)和Cu(Ⅱ)在、303、313和323 K时的lnK0和ΔG0值。在298、303、313和323K在CDP-AM上的吸附,lnKd0与1/T的线性关系图11所示,通过线性拟合可以计算出ΔS0和ΔH0的值。所有热力学参数如表4所示。正的ΔH0值表明CDP-AM表面的吸附是一个吸热过程。负ΔG0值表明HMs在CDP-AM上的吸附是一个自发过程。

图11 拟合吸附热力学参数的ln Kd对1/T关系图Fig 11 ln Kd versus 1/T relationship for fitting thermodynamic parameters

表4 CDP-AM吸附的热力学参数
2.4 吸附机理
偕胺肟基具有双亲结构,偕胺肟基中碱性的胺基高度质子化体系带大量正电荷。在酸性较强的情况,由于与H+的竞争,胺基对重金属离子络合能力减弱,吸附量较小。随着pH值增大,导致H+的竞争能力减弱,酸性羟基将会解离,胺基对重金属离子的配位和螯合能力增强;并且肟羟基解离程度加大,产生氧负离子,此时Zeta电位数值急剧下降为负值,体系带有大量负电,由于静电作用,重金属离子首先被吸引到CDP-AM表面,然后进行螯合,由于静电作用和螯合作用的协同效应, 形成如图12所示五元环,同时五元环的稳定作用使金属通过从亚氨基羟胺形式转变为氨基肟形式而被强烈螯合[31]。

图12 CDP-AM的假想HM吸附机理Fig 12 Hypothetical HM adsorption mechanism by CDP-AM
2.5 重复再生实验
图13是重复再生实验的数据。CDP-AM对于Pb(Ⅱ)和Cu(Ⅱ)吸附第一次移除率虽然只有70%左右,但在重复循环四次实验去除效率仍旧可以保持在65%左右。表明了CDP-AM吸附Pb(Ⅱ)和Cu(Ⅱ)很好的再生性、可重复性,通过含NaOH和乙醇的混合溶液洗涤、浸泡、再生得到的产物可实现多次循环吸附,并且吸附能力损失不大,这些特点使得该吸附剂有很大的应用前景。

图13 再生CDP-AM对于Cu (Ⅱ) 和 Pb (Ⅱ)重复去除率Fig 13 Removing efficiency of Cu (Ⅱ) and Pb (Ⅱ) by regenerated CDP-AM
3 结 论
本实验制备了偕胺肟基改性的β-CD聚合物,通过红外光谱、扫描电镜、XPS等对其结构进行了表征和分析,并首次将改性的聚合物用于除去Pb(Ⅱ)、Cu(Ⅱ),得到如下结论:
(1)通过对Pb(Ⅱ)、Cu(Ⅱ)吸附的动力学分析,吸附过程属于伪二阶过程,化学吸附是控制吸附的主要步骤。
(2)在不同的pH值下,pH对Pb(Ⅱ)、Cu(Ⅱ)吸附的影响是由Pb,Cu物种的静电相互作用和偕胺肟基螯合作用引起的。
(3)根据Langmuir等温线线性拟合,Pb(Ⅱ)、Cu(Ⅱ)在30 ℃时的最大吸附容量分别为273.97和281.69 mg/g。在CDP-AM聚合物表面上的HM吸附过程被证明是吸热和自发过程。经过循环重复实验,发现可以在多个吸附-解吸循环后,仍然保持较高去除效率。
