核心素养视角下的试题评析——以2021年广东省适应性测试化学试题18题为例
2021-07-08广东钟国华
广东 钟国华
1 背景介绍
《普通高中化学课程标准(2017年版2020年修订)》将化学学科的核心素养凝练为“宏观辨识与微观探析”“变化观念与平衡思想”“证据推理与模型认知”“科学探究与创新意识”“科学态度与社会责任”五个方面。学生学科核心素养的发展需在课堂教学中落实,而素养的达成情况需在相关测评中得以检测。近年来高考的命题立意已由知识立意过渡到能力、素养立意,这就引导广大教育工作者对学科核心素养进行研究与思考。
2021年广东省适应性考试化学试题是广东省新高考的前奏,分析本次适应性测试旨在促进教师更好地了解试题与素养的关系,积极发挥“指挥棒”的导向作用,从而增强复习的有效性。
2 试题评析
化工流程题是历年高考化学试题的常见题型,以真实工艺流程为背景,将工业生产的主要阶段以框图形式抽象出来,创设陌生的问题情境,考查学生从陌生情境中识别信息、提取信息并解决问题的能力。此类试题综合性强,对学生能力要求高,能够很好地把化学素养高的学生选拔出来。
2.1 2021年广东省适应性测试18题呈现
综合利用炼锌矿渣(主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4)获得3种金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如下:
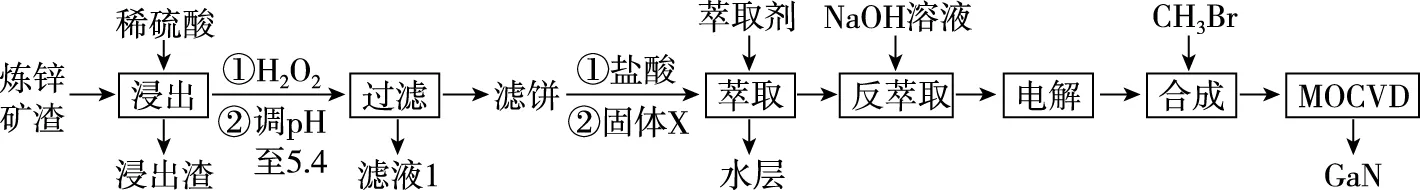
已知:①常温下,浸出液中各离子的浓度及其开始形成氢氧化物沉淀的pH见表1。
②金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表2。
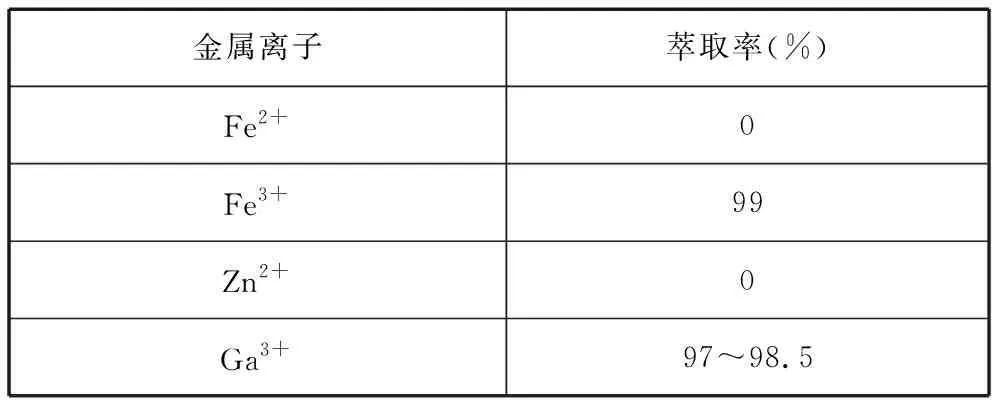
表2 金属离子的萃取率
(1)Ga2(Fe2O4)3中Ga的化合价为________,“浸出”时其发生反应的离子方程式为________________。
(2)滤液1中可回收利用的物质是________,滤饼的主要成分是________;萃取前加入的固体X为________。
(3)Ga与Al同主族,化学性质相似。反萃取后,镓的存在形式为________(填化学式)。
(4)电解过程包括电解反萃取液制粗镓和粗镓精炼两个步骤。精炼时,以粗镓为阳极,以NaOH溶液为电解液,阴极的电极反应式为____________________。
(5)GaN可采用MOCVD(金属有机物化学气相淀积)技术制得:以合成的三甲基镓为原料,使其与NH3发生系列反应得到GaN和另一种产物,该过程的化学方程式为________________。
(6)滤液1中残余的Ga3+的浓度为________mol·L-1(写出计算过程)。
2.2 内容分析
从试题素材背景来看,氮化镓(GaN)是一种具有优异光性能的材料,常用镓盐制备。本题利用炼锌矿渣为原料通过一系列化学、物理过程制得,充分体现化学学科的价值功能。
从试题核心价值来看,本题依托真实复杂的问题情境,要求学生调用已有的必备知识和关键能力,运用正确的价值取向、思想方法与观念,在问题解决过程中体现学生化学学科核心素养的高低。本题各小问考查的核心素养维度见表3。
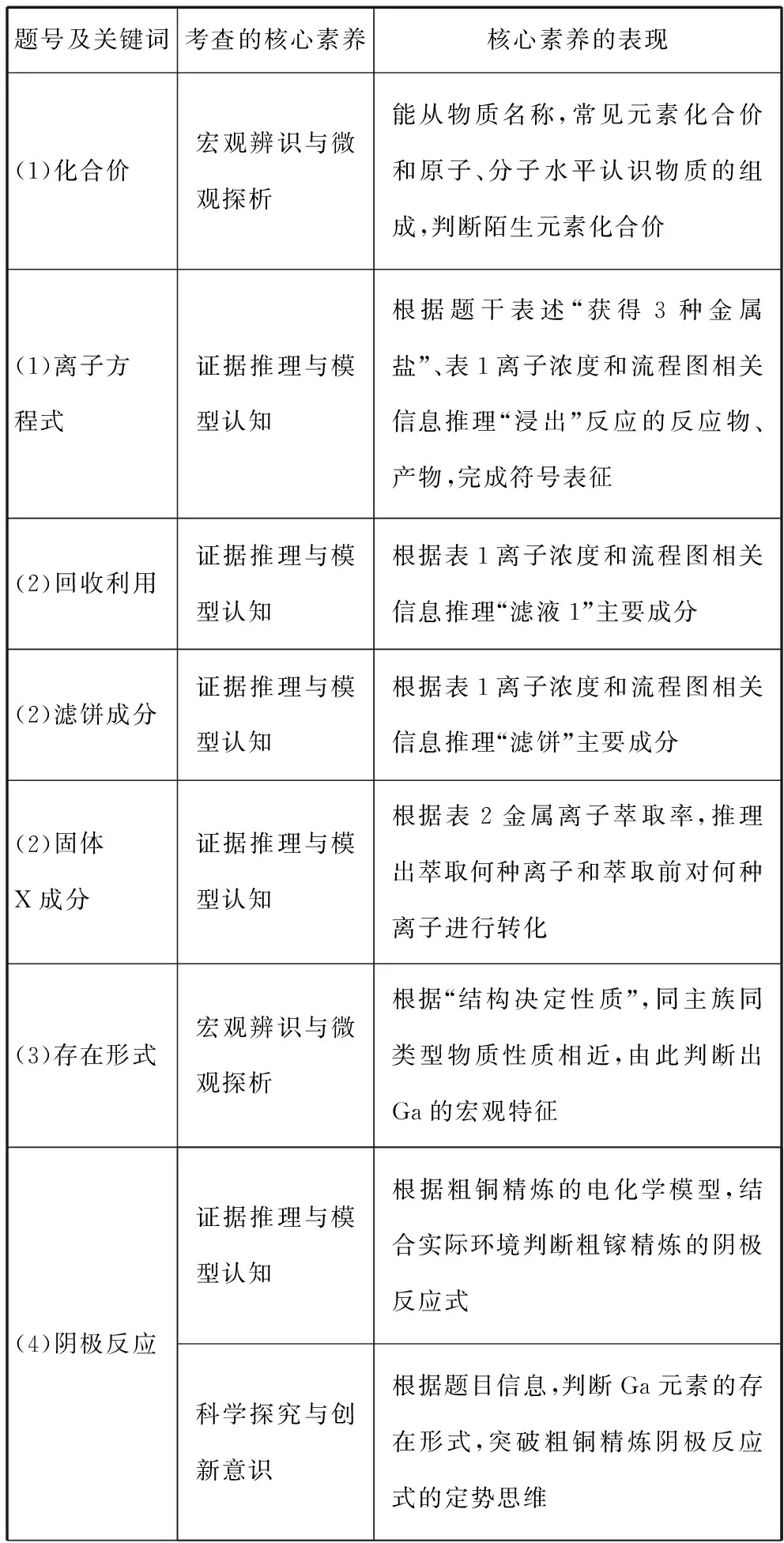
表3 本题各小问核心素养维度
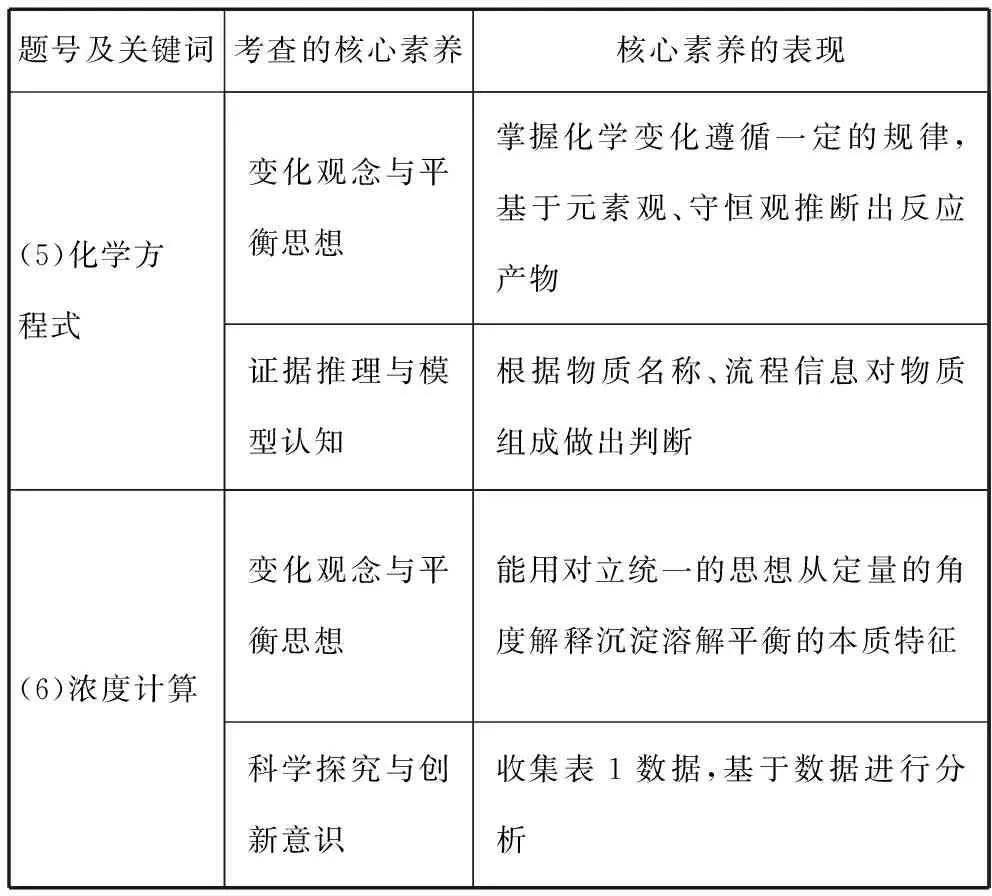
续表
本题与近年全国卷流程题风格基本一致,即通过陌生的工艺流程情境由浅入深,层层推进,从而区分学生化学核心素养的高低。
3 教学启示
“宏观辨识与微观探析”是化学核心素养的学科特征,主要考查涉及化学表征的问题和“结构决定性质”的核心观念;“变化观念与平衡思想”是依靠化学反应原理进行考查的化学核心素养的另一学科特征,主要涉及化学方法及分析能力和定量计算能力;“证据推理与模型认知”是重要的化学学科思维方法,是历年化工流程题考查比重最大的化学核心素养。主要涉及化学语言及应用能力、化学方法及分析能力、基于证据和化学模型进行分析评价逻辑推理的能力。
因此,课堂教学应该提供大量情境,让学生结合宏观现象、微观图表、定量数据、已有模型不断进行推理分析,最终实现问题解决。“三元整合策略”是符合该要求的高思维容量课堂教学策略。
3.1 三元整合策略的定义与主张
“三元整合策略”是指教师以某种元素为核心的一系列物质设计整合型情境,将化学实验、物质性质和基本原理进行整合学习。
三元整合策略主张基于学生在化学实验、物质性质、基本原理三大版块的已有知识创设认知冲突,以“认知冲突”作为课堂教学的研究线索贯穿始终,以知识、方法、能力和素养为教学暗线,围绕驱动问题不断提出解释和修正解释,结合真实实验强化学生有序观察现象的能力和建立有效解决问题的思维。通过三重表征教学提高学生的逻辑思维与语言表达能力,在应用已有知识对外输出过程中培育学生宏观辨识、微观探析、变化观念、证据推理、实验探究等核心素养。
3.2 三元整合策略指导下的案例实施
下面以教育部优课《基于“实验-性质-原理”三元整合策略的钠及其化合物复习专题》为例,探讨高三微专题复习课的高效开展。本课时的教学活动由6个环节展开,主要教学内容如下所述。
3.2.1 环节一:提出问题
开篇引课:在复习指导书中提出利用CaCl2溶液能区分Na2CO3溶液与NaHCO3溶液,其中现象如何,原理如何,我们本节课将进行详细探讨。首先预测向一定量NaHCO3溶液中滴加几滴CaCl2溶液的现象,说出判断依据,并相互讨论。
3.2.2 环节二:预测判断
(1)学生结合已有知识进行预测。
(2)学生说出预测结果和判断依据。
3.2.3 环节三:实验验证
(1)播放验证实验视频。
(2)学生记录实验现象。
3.2.4 环节四:解释推理
(1)推理产生认知冲突的原因和推理反应后期现象。
①上述实验现象中,白色沉淀的成分最可能是什么?结合化学平衡相关知识解释产生该白色沉淀的原因。
②除了产生白色沉淀外,预计还会有哪些现象?说出判断依据。
(2)宏微结合,符号表征:结合上述现象,用离子方程式表示向NaHCO3溶液滴加CaCl2溶液的总反应。
3.2.5 环节五:建立程序
(1)反思评价,拓展迁移
稀释NaHCO3溶液后滴入几滴CaCl2溶液,预计现象与上述是否一致?说出判断依据。
(2)实验验证
①现场演示实验:将NaHCO3溶液稀释2倍和20倍,分别进行实验。
②学生记录实验现象。
(3)建立产生沉淀的思维模型
沉淀的生成、溶解、转化都是Qc和Ksp的大小比较问题,这也是反应进行方向的判断依据。所以,思考程序为成分分析→微观行为→定量判断→符号表征。
3.2.6 环节六:对外输出
(1)举一反三:向CaCl2溶液中通入过量CO2,预计过程会有怎样的现象并说出推测依据。
(2)课后反思:实验室制备乙炔时,硫酸铜溶液的作用是什么,反应后该溶液有何变化?这种变化与CO2通入CaCl2溶液一致吗?请说出判断依据。
该课利用学生熟悉的“NaHCO3和CaCl2能否反应”为实验情景,创设驱动任务,在问题解决的过程中再次通过实验创设问题情境,逐步增大思维难度,迫使学生突破知识板块的限制,主动实现碳酸钠和碳酸氢钠的性质、离子检验、弱电解质的电离、盐类水解等物质性质、化学实验和反应原理三个知识板块的大融合。课堂中既有宏观现象的预测,又有对粒子的微观行为进行分析;既有通过控制浓度控制反应发生与否,又有从电离平衡、水解平衡、沉淀溶解平衡的角度分析;既有基于现象证据、数据证据进行推理,又有基于平衡移动原理的模型分析;既有要从问题和假设出发设计实验的科学探究,又有面对异常现象敢于提出自己见解的创新意识。

