建立解题思维模型 突破有机实验难点
2021-07-08吉林王永波
吉林 王永波
随着新课程改革的推进,高考试题的考查方向逐渐趋近于发展化学学科核心素养,其中,有机实验类综合题在一定程度上体现了学生的关键能力和必备品格,因而近几年在高考试题中频繁出现,是高考试题的难点,主要考查有机物的制备、分离提纯和计算能力等。解决此类问题的关键即在备考过程中积累必备知识,培养关键能力,建立解题思维模型。学生要具有证据意识,能基于有机物官能团的性质,通过分析推理认识有机反应原理,从教材中的有机实验常见问题中辩证地分析不同物质之间的相互区别和联系,建立解题思维模型,运用模型突破有机化学实验试题中涉及的难点。在备考过程中笔者发现该类试题存在几个难点问题:陌生实验原理的确定、实验发生装置的选择、有机产物的分离提纯等。下面是针对以上难点问题逐一进行梳理,运用模型认知的方法解决此类问题,以期对师生有所帮助。
模型一、陌生实验原理的确定
有机实验题中涉及的反应原理通常不是教材中出现的原型,如何确定反应原理呢?下面以三个考题为例,分析反应原理,写出相应的化学方程式。
考题1:化学小组采用类似实验室制乙烯的原理,用环己醇和浓硫酸混合加热至85℃制备环己烯。
考题2:乙酸丁酯是具有果香味的香精,利用实验室制取乙酸乙酯的原理可进行乙酸丁酯的合成。
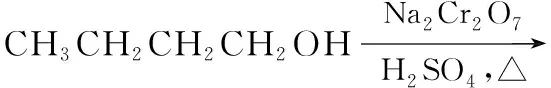
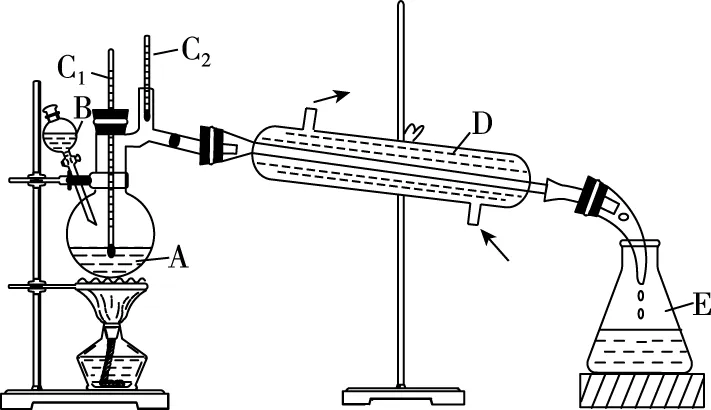
图1
请回答:实验过程中可能生成的副产物是什么?为什么将Na2Cr2O7酸性溶液放入仪器B中,将正丁醇放入仪器A中,二者能否调换,为什么?
【分析】官能团是代表有机物特殊性质的原子或原子团,因此要依据官能团的性质及其常见的反应类型并结合信息进行综合分析。
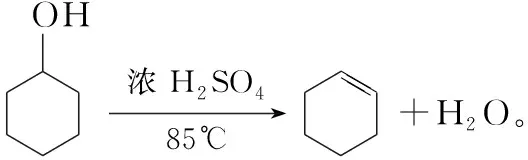
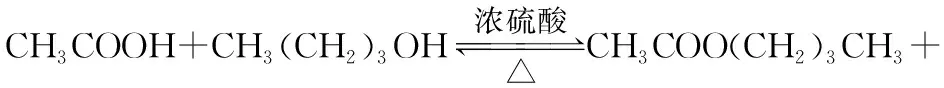
考题3的原理题目中已经给出,但并不是教材中经常出现的化学方程式,而是乙醇催化氧化生成乙醛的变形,氧化剂不是氧气,而是强氧化剂酸性重铬酸钾溶液,因此考生要有一定的知识迁移能力,联想到醇的氧化反应的思维模型。
关于副产物的确定:题干中出现浓硫酸,考生很容易联想到醇发生消去反应生成烯烃或发生取代反应生成醚,但是浓硫酸的体积只有5 mL,且被30 mL Na2Cr2O7溶液稀释,因此,浓H2SO4只能起到酸化Na2Cr2O7溶液以提高其氧化性的作用,并不能使正丁醇发生消去反应或取代反应。已知乙醇能被酸性Na2Cr2O7溶液等强氧化剂氧化为乙酸,由此类推正丁醇也能被氧化为正丁酸,因此副产物为正丁酸。
关于正丁醇和强氧化剂分别盛放在哪个容器中,要依据官能团的性质进行分析。醛比醇更易发生氧化反应,因此,要将酸性Na2Cr2O7溶液滴入正丁醇中,否则正丁醛还未被蒸馏出体系就会被氧化。
由此可见,无论是反应原理的书写还是副产物的确定,都需依据官能团的性质进行判定,熟练掌握官能团的性质和有机物间的转化关系十分必要。笔者总结出如下思维模型。
【思维模型】根据官能团分析有机物的结构和性质,恰当运用题目信息,进行类比和知识迁移,从而得出结论。
模型二、实验发生装置的选择
确定实验原理后,依据题目信息中有机物的物理性质参数,正确选择发生装置。下面结合教材中的重要液态有机物制备实验进行分析。表1列举了实验室制备溴苯、硝基苯和乙酸乙酯的发生装置。
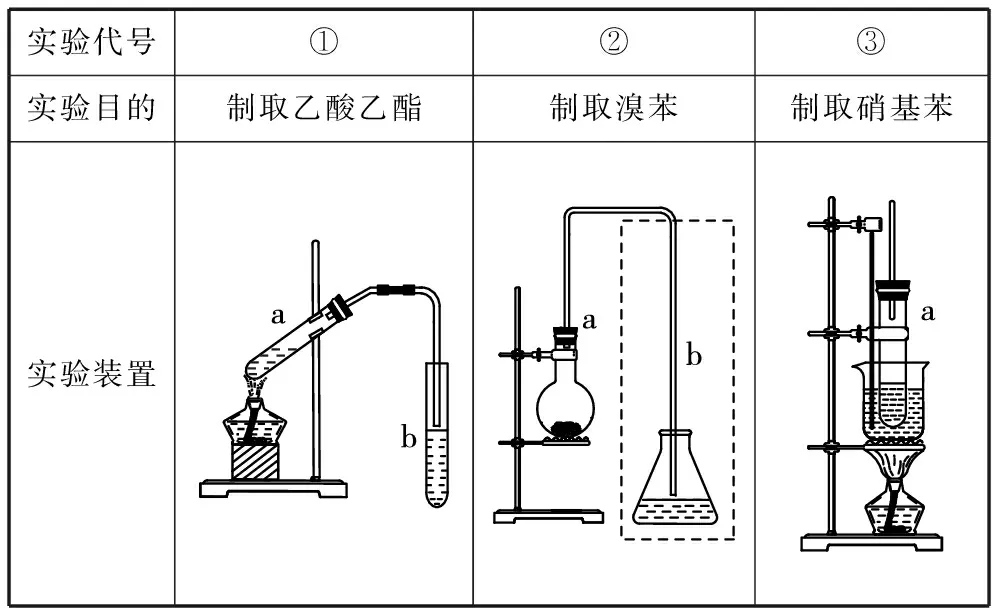
表1
实验①中有机产物乙酸乙酯在加热条件下被蒸馏到仪器b中,离开试管a;实验②和实验③的有机产物溴苯和硝基苯一直存在于发生装置a中。因此可根据产物是否离开发生装置将以上三个实验的发生装置可分为两类:一类是以实验①为代表的蒸馏式,另一类是实验②和实验③为代表的回流式。如何区分两种发生装置呢?大多有机反应需要加热,有机物的沸点低,容易汽化,因此要通过分析反应物和生成物的沸点差异选择发生装置。表2列举了溴苯和乙酸乙酯制备实验中部分物质的沸点:

表2
由表2数据可知溴苯的沸点高于苯和溴单质的沸点,反应过程中需要将挥发的反应物冷凝回流到发生装置中继续反应,因此必须用回流式,以提高反应物的利用率。实验③中硝基苯的沸点远高于反应物苯和硝酸的沸点,因此其发生装置也采用回流式。实验①中乙酸乙酯的沸点低于反应物乙醇和乙酸的沸点,且酯化反应为可逆反应,故需要将沸点低的有机产物乙酸乙酯蒸馏出来,让其离开体系,因此必须用蒸出式,减少生成物的浓度使平衡正向进行,提高反应物的转化率。
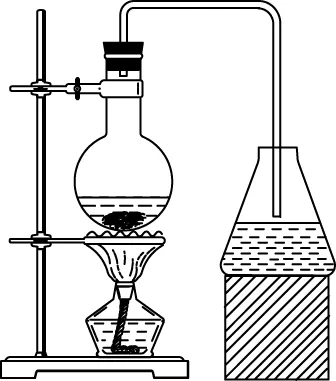
甲
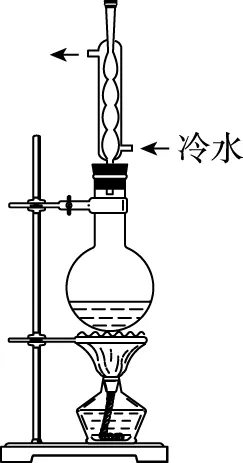
乙
由以上分析不难得出选择制备液态有机物的发生装置的关键,即区分有机产物和反应物的沸点关系,因此可建立如下思维模型。
【思维模型】制备液态有机物常见发生装置的选择
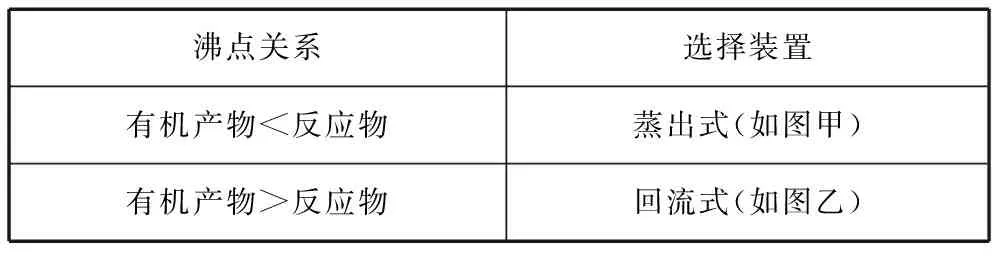
沸点关系选择装置有机产物<反应物蒸出式(如图甲)有机产物>反应物回流式(如图乙)
利用以上思维模型,可准确快速地确定陌生有机反应的发生装置,例如:结合表3数据分析实验室制取乙酸丁酯的发生装置。

表3
【分析】制取乙酸丁酯的装置应选用回流式,因为乙酸丁酯的沸点高于反应物乙酸和丁醇的沸点,利用此装置可将反应物回流,提高原料的利用率。
模型三、产物分离提纯过程
有机反应相对复杂,并伴随着副反应的发生,产物中所含杂质较多,因而分离提纯产物的步骤也较为复杂。若制备常温呈气态的有机物,如乙烯、乙炔等,由于气体沸点低,为得到纯净的产物只需要选择合理试剂进行洗气即可。若制备常温呈液态的有机物,分离过程相对复杂,下面以硝基苯的制备为例进行分析。
硝基苯的制备采取回流式,因此反应物和生成物都存在于发生装置中,所得混合体系中主要有两类,一类为含有溶于水的浓硫酸和浓硝酸的混合溶液,一类为难溶于水的苯和硝基苯。分离时,首先进行水洗分液,洗去混酸,再用碱液洗涤后分液,洗去剩余的少量混酸,然后进行水洗分液,除去可溶性的无机离子,最后加入无水氯化钙等无水盐作干燥剂,过滤,蒸馏,即可得纯品目标产物。溴苯和乙酸乙酯的分离提纯过程基本同上,基于以上操作步骤,进行总结,可得如下思维模型。
【思维模型】液态有机物分离提纯的一般过程:

分离过程中用到的分离方法主要有分液和蒸馏,其中,主要的实验仪器有分液漏斗、蒸馏烧瓶、冷凝管等,常见的干燥剂有氯化钙、硫酸镁、硫酸钠等无水盐。

