借“防”突破无机制备类实验综合题的“难点”
2021-07-08湖南周学兴
湖南 周学兴 王 静
实验题是高考必考题型,得分率较低,究其根本原因是“实验体验少”。制备类实验是高考化学常见的一个类型,主要分为有机制备、无机制备,其中无机制备又分为气体参与制备类、溶液制备类等。
1 高考背景
教育部网站2月19日发布《教育部关于做好2021年普通高校招生工作的通知》指出深化考试内容改革。2021年高考命题要坚持“立德树人”,加强对学生德智体美劳全面发展的考查和引导。优化情境设计,增强试题开放性、灵活性,充分发挥高考命题的育人作用和积极导向作用。实验创新试题的呈现方式种类多,探究题以新实验的探究过程为主,制备类实验则以陌生物质的制备为主等,陌生物质的制备会给予该物质的信息,这些信息主要是命题者针对该物质的获取进行有选择性的提供。
近五年高考化学真题中制备类实验题的考查载体与考点,见表1。
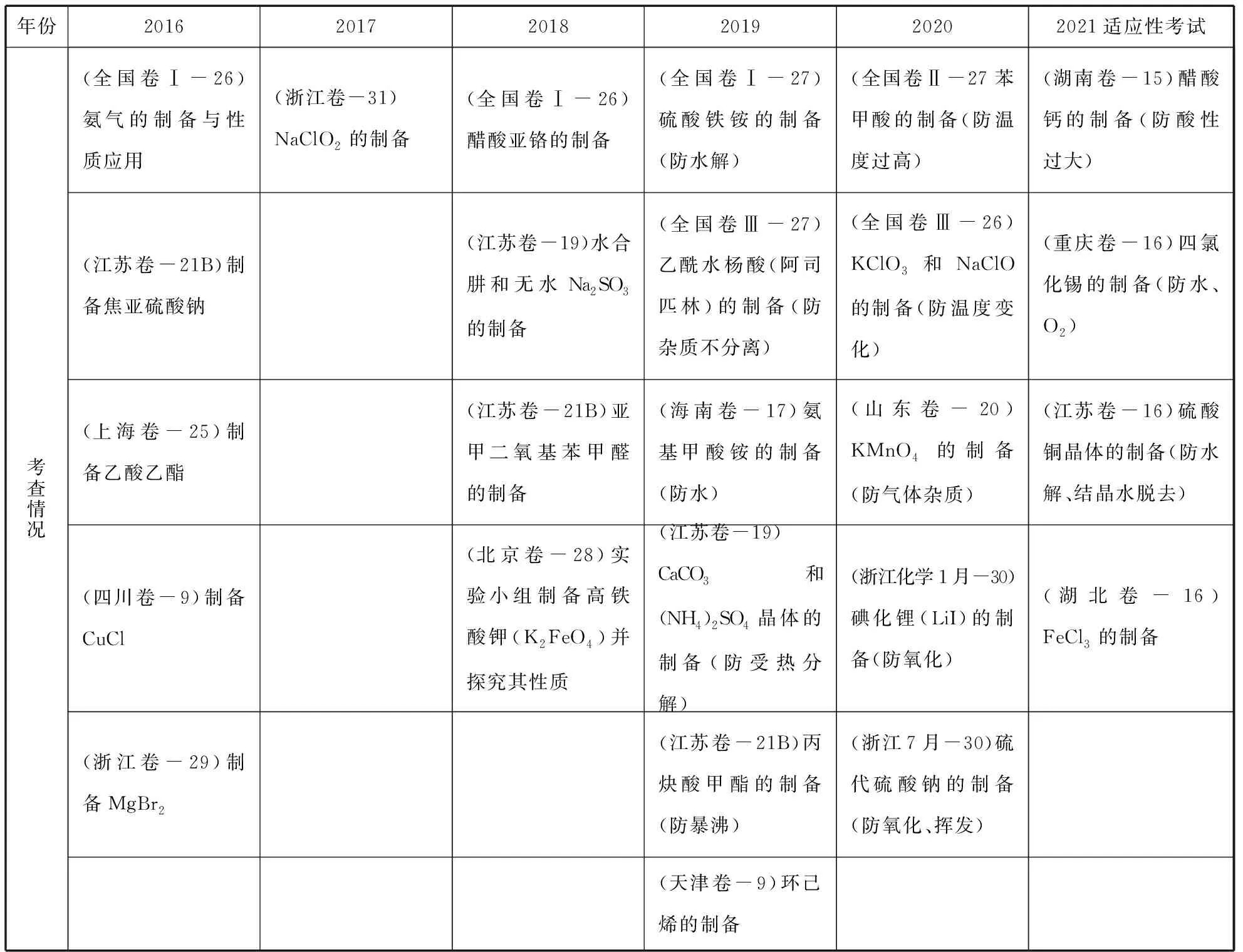
表1 近五年制备类实验题的考查情况汇总
不难发现制备类实验题在高考化学中属于高频考题,为了更好地制备更多的纯净产品,需要进行各种“防”,比如防氧化、防水解、防温度过高、防杂质气体的干扰等。
2 解题模型
首先将实验综合题进行分类,若是制备类,则应通过产品的性质和反应物的性质思考是否有“防”的对象。
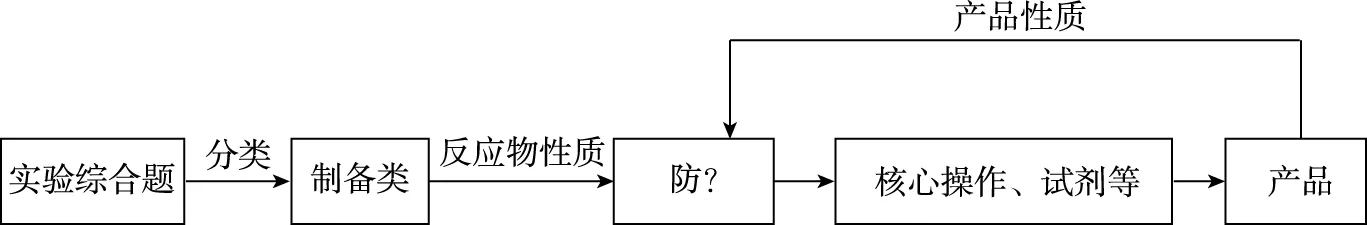
先思考需要“防”的对象,然后积累各种“防”所需要注意的试剂选择和实验操作,有助于从“宏观”上快速突破制备类实验综合题,尤其是气体参与类和溶液型无机制备类实验综合题。
2.1 小试牛刀
【例1】(2021·重庆市适应性考试·16)四氯化锡(SnCl4),常温下为无色液体,易水解。某研究小组利用氯气与硫渣反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。
硫渣的化学组成
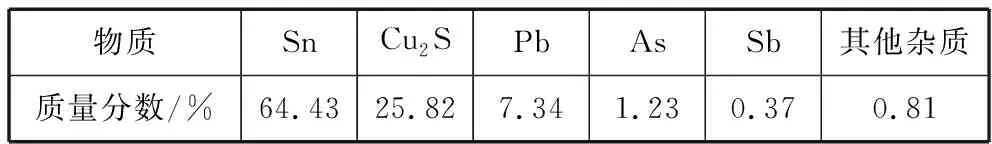
物质SnCu2SPbAsSb其他杂质质量分数/%64.4325.827.341.230.370.81
氯气与硫渣反应相关产物的熔沸点
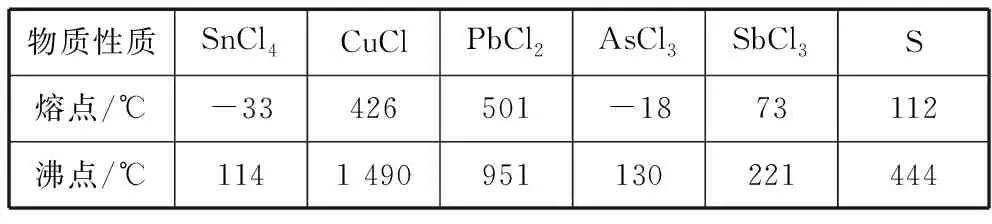
物质性质SnCl4CuClPbCl2AsCl3SbCl3S熔点/℃-33426501-1873112沸点/℃1141 490951130221444
请回答以下问题:
(1)A装置中,盛浓盐酸装置中a管的作用是________,b瓶中的试剂是________。
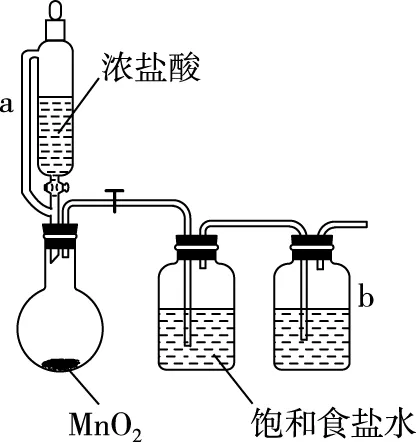
A
(2)氮气保护下,向B装置的三颈瓶中加入适量SnCl4浸没硫渣,通入氯气发生反应。
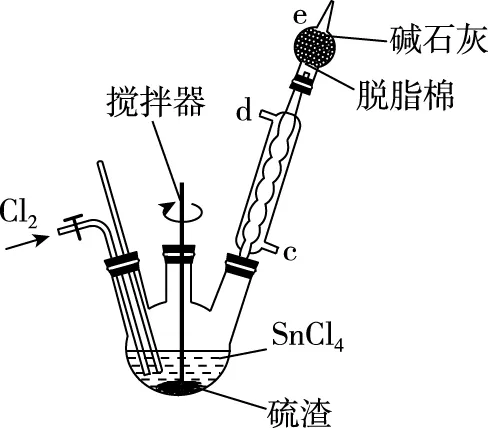
B
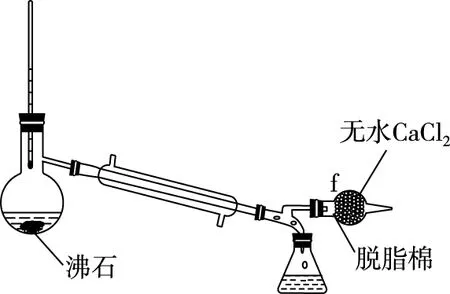
C
①生成SnCl4的化学反应方程式为________;
②其中冷凝水的入口是________,e中试剂使用碱石灰而不用无水氯化钙的原因是________;
③实验中所得固体渣经过处理,可回收的主要金属有________和________。
(3)得到的粗产品经C装置提纯,应控制温度为________℃。

【解题模型】
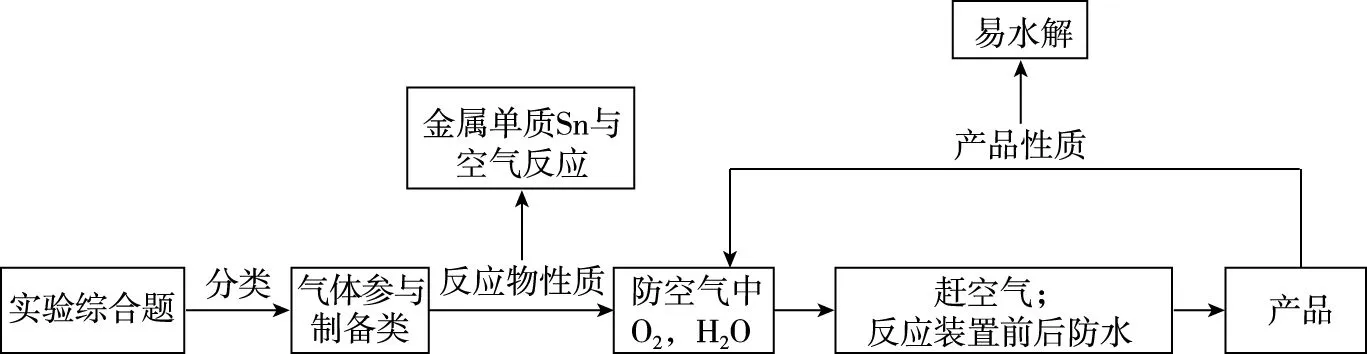
根据分析可知装置e的作用是防止外界空气中的H2O进入反应装置,致使SnCl4水解,同时吸收尾气Cl2。故b瓶中试剂应为浓硫酸,防止Cl2带入水蒸气,引起产品水解。“潜在”考查方向“应先通一段时间Cl2将空气赶尽,再发生反应”,本题采用N2作保护气。
【例2】(2018·全国卷Ⅰ·26)醋酸亚铬[(CH3COO)2Cr·2H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图1所示。回答下列问题:
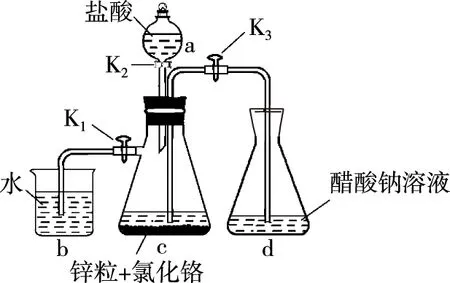
图1
(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是____________________。仪器a的名称是________。
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置。打开K1、K2,关闭K3。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为________________;
②同时c中有气体产生,该气体的作用是____________________。
(3)打开K3,关闭K1和K2。c中亮蓝色溶液流入d,其原因是________;
d中析出砖红色沉淀。为使沉淀充分析出并分离,需采用的操作是________、________、洗涤、干燥。
(4)指出装置d可能存在的缺点________。
【解题模型】
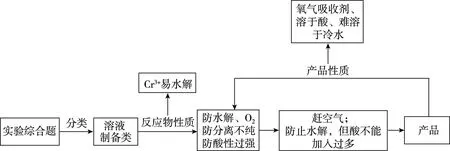
通过该解题模型可快速分析出难点设问的“(4)(5)问”。分离出醋酸亚铬可采取降温结晶,过滤、洗涤干燥。装置存在的缺陷,必然是相对实验目的而言的,即得到产品可能不够“好”——未防止O2的干扰。
综上所述,通过产品性质、反应物性质,抓住“防”字要领,可迅速突破无机制备类实验综合题。故应该对常见需要“防”的对象进行系统总结,可提高解题的效率。
2.2 “防”字汇总
纵观历年高考试题,深挖外在信息和内在信息,抓住无机制备类需要“防”的方向,突破实验操作、试剂作用等难点。其中外在信息指的是直接指明物质性质的信息,内在信息指的是该物质为常见物质,比如“Fe3+”需“防水解”,再如“Fe2+”需“防被氧化”。具体总结归纳,见表2。

表2 常见信息与“防”的对象的关系
3 原创试题
通过上述分析与总结,让原创试题命制过程中对“考点”的设置更加有理有据。比如为了凸显“防”温度过高的原因分析,笔者命制了两道实验综合题,命题过程如下。
首先,实验综合题常考类型题有制备类、性质探究类、定量类、原理探究类等,最终选择无机溶液制备类实验。
其次结合社会、生活等领域的重要化学用品,选择含氯消毒剂NaClO2溶液的制备和SiCl4的制备,分别考查对“防”温度影响和“防”空气和水的影响及产品冷凝易堵塞的难点。
最终命制两道原创试题如下:
【原创试题1】亚氯酸钠(NaClO2)是一种高效含氯消毒剂和漂白剂,主要用于自来水、污水等水环境的杀菌消毒,也常用作纸浆、砂糖、油脂的漂白剂。图2为生产亚氯酸钠的流程之一,所得NaClO2具有纯度高的优点。
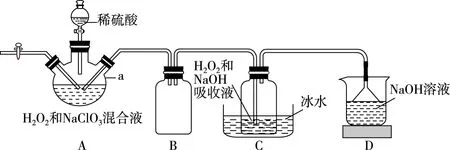
图2
已知:NaClO2饱和溶液低于38℃时析出NaClO2·3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
试回答下列问题:
(1)仪器a的名称为________。
(2)装置A用来制取ClO2,反应的离子方程式为____________________。
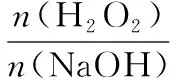
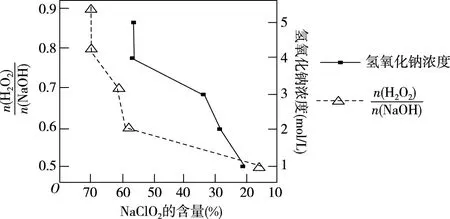
图3
(4)C装置采用“冰水浴”的目的是________。
(5)充分反应后,从产品溶液获取NaClO2晶体的操作是:55℃恒温减压蒸发结晶、趁热过滤、________℃水洗涤、干燥。

【答案】(1)三颈瓶(或三颈烧瓶或三口烧瓶)
(3)4 0.8 还原
(4)防止温度过高,NaClO2分解成NaClO3和NaCl,H2O2受热易分解
(5)38~55(区间任一温度均给分)
在试题设置“难点”考查时,选择分离提纯和“冰水浴”两个角度来考查“防”温度过高的重要信息,通过测试发现第(5)问有较高的区分度。同时凸显了日常生活中化学试剂起到的重要作用,体现了化学学科价值,渗透了社会责任与科学态度的核心素养。
【原创试题2】“中国芯”的发展离不开单晶硅先进制造工艺,四氯化硅是重要中间产物。实验室制备四氯化硅的装置如图4所示:
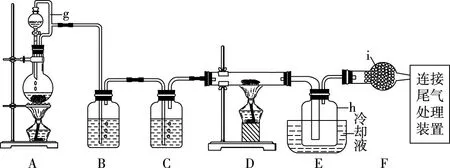
图4
已知:

②四氯化硅遇水极易水解;
③粗硅含铁、铝、磷等杂质,在高温下均能与氯气直接反应生成相应的氯化物;
④有关物质的物理常数见下表:

物质SiCl4AlCl3FeCl3PCl5沸点/℃57.7—315—熔点/℃-70.0———升华温度/℃—180300162
请回答下列问题:
(1)写出装置A中发生反应的离子方程式:________________,仪器i的名称为________,其作用为________。
(2)当观察到________________现象时,点燃装置D的酒精灯。装置B中的试剂为________,若是去掉装置B,带来的危害是________。
(3)有同学认为装置D右端相连的导管为粗导管,其理由是________。
(4)装置E中集气瓶收集到的粗产品除SiCl4外,还含有少量AlCl3、FeCl3、PCl5,可通过________(填分离提纯方法)可得到高纯度产品以及少量残留物。
(5)为了分析残留物杂质中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,某同学称取5.0 g残留物后,经预处理后在容量瓶中配制成100 mL溶液,取25.00 mL试样于锥形瓶中,消耗1.000×10-2mol/L KMnO4标准溶液20.00 mL,则残留物中铁元素的质量分数是________。

(2)D(E)中充满黄绿色气体 饱和食盐水 HCl与Si反应产生H2,与Cl2反应发生爆炸
(3)细导管 容易出现堵塞现象
(4)蒸馏(精馏)
(5)4.480%
该题以硅元素相关物质的制备为载体,考查仪器的使用、实验控制条件、实验数据的处理等。本题通过“防”字要领的理解,可快速突破难点——“(2)(3)问”的分析。
4 结束语
无机物制备是实验综合题考查的主要方向,在高三化学复习备考中,抓住“防”字要领,不仅可以提高“难点”的分析与突破,还节约了分析和思考时间,大大地提高了解题效率。同时结合笔者命制试题的一般过程,抛砖引玉,为广大教师提供一定的命题思路。
