运动预适应减轻一次性运动力竭大鼠心肌凋亡及其机制研究
2021-07-07王永园
吕 磊,李 瑶,王永园,金 涛,钟 勇
0 引 言
大强度超负荷运动可诱发心肌缺血缺氧。近年研究发现,运动预适应可以通过反复短暂、高强度的间歇性运动诱发机体产生内源性保护作用,从而使心肌对后续长时间的缺血、缺氧产生耐受,减轻心肌损伤。研究证实,运动预适应能减少缺血后心梗面积,改善缺血后心功能,减少心律失常,还可能改善心肌细胞能量代谢[1]。既往研究表明,细胞凋亡参与了运动性心肌损伤,运动预适应能通过上调凋亡相关基因Bcl-2和下调Bax的表达,减少动脉硬化大鼠急性心肌缺血所致的心肌细胞凋亡[2]。一氧化氮(NO)能改变线粒体通透性,阻断含半胱氨酸蛋白水解酶(caspase)的激活,减少凋亡信号的释放,从而减少细胞凋亡[3]。然而,运动预适应对力竭运动所致心肌细胞凋亡的作用及其具体机制尚未明确。本研究观察运动预适应对一次性运动力竭大鼠心肌形态改变、氧化应激水平、心肌细胞凋亡和内皮型一氧化氮合酶(eNOS)的影响,初步探讨其相关作用。
1 材料与方法
1.1 实验动物健康雄性Sprague Dawley大鼠21只,体重150~170 g,购自上海西普尔-必凯实验动物有限公司(SPF级),动物合格证号:SCXK(沪)2018-0006。大鼠分笼饲养,室内温度(22±2)℃,湿度(50±5)%,标准实验大鼠饲料喂养,自由进食,纯净水自由饮用,自然光照,适应性喂养3 d后,进行跑台适应性训练(跑台速度15 m/min,坡度0°),每天训练15 min,共5 d。本研究动物操作方法遵循国家实验动物管理条例和细则,动物处置方法均符合伦理学标准(伦理批准号:2018JLHZXKT-001)。
1.2 实验动物分组和模型建立参照文献[4],适应性训练后,将大鼠采用随机数字表法分为3组:安静对照组(不运动)、运动力竭组和运动预适应组,每组7只。一次性力竭运动模型参照文献[5]标准建立,大鼠在跑台上进行持续性运动(跑台速度30 m/min,坡度0°),直至力竭。判断力竭状态的标准为: 大鼠伏卧于跑道,双眼无光,四肢瘫软,声、光等外界刺激均不能使其继续运动,翻转后无法翻正[6]。运动预适应组大鼠在跑台上进行重复4次的间歇性运动(跑台速度28~30 m/min),每次运动15 min、休息15 min,30 min后行一次性力竭运动。
1.3 HE染色观察心肌形态改变力竭运动后,留取大鼠新鲜左心室心尖部,4%多聚甲醛溶液固定,修剪脱水后石蜡包埋,标本按4~5 μm连续切片脱蜡至水后进行苏木素-伊红(HE)染色,镜下观察大鼠心肌组织改变。
1.4 TUNEL染色法检测心肌细胞凋亡指数大鼠新鲜左室心肌组织固定后制作石蜡切片,常规方法脱蜡水化,按原位末端转移酶标记法(TUNEL)凋亡检测试剂盒(美国Roche公司)说明进行心肌细胞凋亡原位检测。荧光显微镜下正常心肌细胞细胞核呈蓝色,凋亡心肌细胞细胞核呈绿色(TUNEL阳性)。随机计数5个非重叠高倍镜视野(×400)下凋亡心肌细胞数和心肌细胞总数,两者的比值即为心肌细胞凋亡指数。
1.5 氧化应激指标和一氧化氮测定实验结束后取静脉血,1500×g离心5 min,留取上清,4 ℃保存。严格按试剂盒(南京建成生物工程研究所有限公司)步骤操作,硫代巴比妥酸比色法在532 nm处测定丙二醛(MDA)含量,黄嘌呤氧化酶法在450 nm处测定超氧化物歧化酶(SOD)含量,比色法在550 nm处测定一氧化氮(NO)含量。
1.6 Western blot法测定大鼠心肌内皮型一氧化氮合酶(eNOS)水平力竭运动后,留取大鼠左心室心肌组织,液氮冷冻后-80℃保存。取大鼠心肌组织在组织裂解液中匀浆并离心,提取心肌组织总蛋白,考马斯亮蓝法蛋白定量。取蛋白40 μg,聚丙烯酰胺凝胶电泳分离蛋白,转移到硝酸纤维素膜后分别用eNOS一抗(1∶1000,美国CST公司),内参GAPDH抗体(1∶2500,美国CST公司)封闭,4 ℃过夜。再用辣根过氧化酶标记的二抗(1∶5000稀释)室温封闭,孵育2 h。使用Gel Doc2000凝胶图像专用软件(Bio-Rad公司)对目标条带进行分析,测积分吸光度值,以目的条带与GAPDH条带灰度值的比值表示结果。

2 结 果
2.1 心肌组织HE染色结果光镜下,安静对照组大鼠心肌纤维、胶原纤维等红染,染色均匀,结构清楚,心肌纤维形态结构正常,无水肿,心肌细胞排列规则,细胞核蓝染。运动力竭组大鼠心肌细胞染色欠均,排列较紊乱,部分肌纤维断裂、排列紊乱和局限性间质水肿。运动预适应组大鼠心肌染色比较均匀,少量心肌纤维排列紊乱、肿胀。见图1。
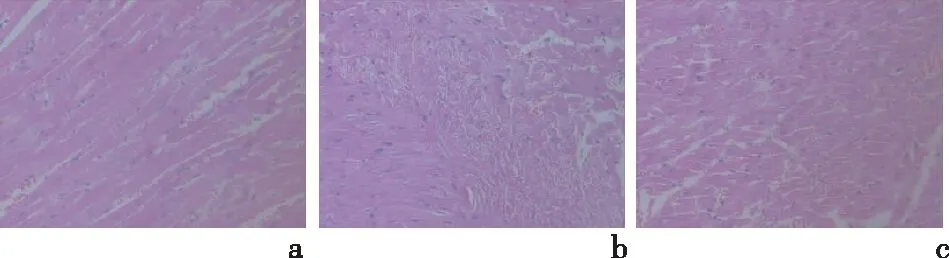
a:安静对照组;b:运动力竭组;c:运动预适应组
2.2 心肌细胞TUNEL染色及心肌细胞凋亡指数比较安静对照组大鼠未见心肌细胞凋亡,运动力竭组和运动预适应组均可见凋亡细胞,见图2。运动力竭组凋亡指数为(12.48±2.88)%,运动预适应组凋亡指数为(3.51±0.78)%,组间比较差异有统计学意义(P<0.05)。

a:安静对照组,未见凋亡心肌细胞;b:运动力竭组,可见凋亡细胞;c:运动预适应组,仅见少许凋亡心肌细胞
2.3 各组大鼠SOD活性、MDA含量和NO含量运动力竭组大鼠血清MDA含量较安静对照组明显升高,SOD活性和NO含量降低(P<0.05)。运动预适应后,MDA含量下降,SOD活性和NO含量均高于运动力竭组(P<0.05),见表1。
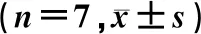
表1 各组大鼠SOD活性、MDA含量和NO含量比较
2.4 运动预适应对大鼠心肌组织中eNOS蛋白表达的影响Western blot法测定结果显示,运动力竭组eNOS蛋白表达(0.56±0.17)较安静对照组(1.00±0.12)下降,而运动预适应组(1.91±0.22)显著高于运动力竭组,差异均有统计学意义(P<0.05)。结果提示运动预适应增加了大鼠心肌组织中eNOS的蛋白表达水平。见图3。
GAPDH(内参):甘油醛-3-磷酸脱氢酶
3 讨 论
反复短暂的高强度运动,即运动预适应,可通过诱导内源性保护作用,增强机体对随后高强度运动的耐受性,减少机体损伤。研究表明,运动预适应可明显降低大强度力竭运动时心肌肌钙蛋白I和N端脑钠肽激素原的浓度,保护心肌[7]。运动预适应对心肌保护作用分早期保护和晚期保护两个时相,早期保护更为明显[8]。本研究观察光镜下心肌细胞的病理改变,结果发现,运动力竭组大鼠心肌细胞排列紊乱,伴部分肌纤维断裂和局限性间质水肿,而运动预适应后再进行力竭运动,心肌细胞损伤较轻,提示运动预适应减轻了力竭运动所致大鼠心肌的组织病理改变。
SOD是调节过氧化水平、清除过氧化物的主要酶,通过催化超氧阴离子的歧化反应,抑制超氧自由基的连锁反应,有效减缓机体内脂质过氧化程度,降低机体氧化应激损伤,是机体重要的氧自由基清除剂。MDA是氧自由基攻击细胞膜中不饱和脂肪酸,产生脂质过氧化作用的产物之一,可反映体内氧自由基活性[9-10]。本研究结果显示,大鼠力竭运动后血清SOD活性较安静对照组明显降低,MDA含量显著增加,运动预适应组与运动力竭组比较,SOD活性升高,MDA含量下降,提示力竭运动增加了机体氧化应激水平,而运动预适应提高抗氧化酶活性,使机体对活性氧产生适应能力,减少因机体组织缺血缺氧所致的氧自由基生成。
本研究进一步观察了运动力竭组和运动预适应组大鼠心肌凋亡指数,结果发现运动预适应组显著低于运动力竭组,提示一次性力竭运动可导致心肌细胞凋亡,而运动预适应能减少心肌凋亡。力竭运动导致心肌细胞凋亡可能与氧自由基过度生成和细胞能量代谢障碍有关。力竭运动时心肌细胞缺血缺氧,氧自由基大量生成,葡萄糖和脂质过氧化,细胞膜损伤,蛋白质氧化和核内DNA链断裂,诱导心肌细胞凋亡[11]。此外,力竭运动时心肌缺血缺氧,抑制线粒体氧化磷酸化,ATP生成减少,细胞能量代谢障碍,钙离子转运功能被抑制,胞浆和线粒体钙超载,通过激活磷脂酶破坏细胞膜和激活蛋白酶使蛋白分解,导致心肌细胞凋亡[12]。
NO是一种舒张血管的小分子化学物质,广泛存在于多种组织细胞中,通过升高环磷酸鸟苷含量诱导平滑肌舒张,在人体心脑血管、中枢神经系统和炎症免疫反应中参与生理和病理过程。生理浓度水平NO参与调节血管通透性和血管张力、稳定血压等生理过程。缺氧时,内皮细胞释放NO,激活鸟苷酸环化酶增加细胞内环磷酸鸟苷水平,通过降低血管平滑肌中钙离子水平,扩张血管平滑肌[13]。NO还能通过减少凋亡信号的释放来减少细胞凋亡[3]。一氧化氮合酶(NOS)是一氧化氮合成的关键酶,eNOS也称为NOS3,为钙离子依赖性酶,以L-精氨酸为底物,在血管内利用氧催化产生NO,参与生理调控,在维持血管稳态、调节心肌细胞功能中起重要作用[14]。既往研究表明,短期平板运动能显著增加大鼠脑血管和主动脉中eNOS的表达[15],长期运动训练能增加慢性心衰大鼠左室eNOS的活性[16]。本研究表明,与安静对照组相比,运动力竭组NO和心肌组织eNOS表达水平均下降,而运动预适应能上调心肌组织eNOS的表达水平,增加NO浓度,抑制心肌细胞凋亡。
综上所述,运动预适应能减轻一次性力竭运动大鼠心肌损伤所致心肌细胞凋亡和自由基释放,eNOS可能参与这一保护作用。
