近零磁场下东方黏虫转录组分析
2021-06-29闫蒙蒙张蕾程云霞江幸福
闫蒙蒙 张蕾 程云霞 江幸福


摘要 :为进一步探究黏虫的磁感应机制,明确磁场强度变化对黏虫相关基因表达的影响及相应的分子机制,本研究利用亥姆霍兹线圈装置产生近零磁场,使用Illumina技术,分别对近零磁场(小于500 nT)和地磁场(约54 000 nT)下饲养的黏虫雌蛾和雄蛾进行转录组测序分析。结果表明:相对于地磁场,近零磁场下雌、雄蛾分别鉴定出1 670和1 401个差异表达基因,其中雌蛾鉴定出614个上调基因,1 056个下调基因;雄蛾鉴定出545个上调基因,856个下调基因;雌、雄蛾共同差异表达基因274个。GO功能分析和pathway结果显示近零磁场胁迫与离子结合、催化和代谢等关键过程密切相关。对选取的10个差异基因进行荧光定量PCR验证,证明了转录组测序分析结果准确可靠。本试验为深入探究迁飞性昆虫的地磁定向机制提供了理论基础。
关键词 :近零磁场; 地磁场; 黏虫; 转录组
中图分类号:
S 433.4
文献标识码: A
DOI: 10.16688/j.zwbh.2020013
Transcriptome analysis of the oriental armyworm Mythimna separata in
a near-zero magnetic field
YAN Mengmeng, ZHANG Lei, CHENG Yunxia, JIANG Xingfu*
(State Key Laboratory for Biology of Plant Diseases and Insect Pests, Institute of Plant Protection, Chinese Academy of Agricultural Sciences, Beijing 100193, China)
Abstract
In order to further explore the mechanism of magnetoreception of Mythimna separata and clarify the effects of magnetic field changes on the expression of related genes, transcriptome analysis of M.separata in a near-zero magnetic field was carried out. In this study, Helmhortz coils were used to generate a near-zero magnetic field, and the Illumina technology was used to sequence the transcriptome of M.separata moths (female and male) raised in near-zero magnetic field (less than 500 nT) and normal geomagnetic field (about 54 000 nT). The results showed that compared with geomagnetic field, 1 670 and 1 401 differentially expressed genes were identified in female and male adults under near-zero magnetic field, respectively, among which 614 up-regulated genes and 1 056 down-regulated genes were identified in female adults, and 545 up-regulated genes and 856 down-regulated genes were identified in male adults. There were 274 common differentially expressed genes in male and female adults. The gene ontology (GO) functional annotation and pathway enrichment analysis results showed that near-zero magnetic field was related to key biological processes, such as ion binding, catalysis activity and metabolism process. The results of qRT-PCR showed that the transcriptome was accurate and reliable. Our study provided a theoretical fundament for further study of the mechanism of magnetoreception in migratory insects.
Key words
near-zero magnetic field; geomagnetic field; Mythimna separata; transcriptome
與温湿度、紫外线、CO2浓度一样,磁场同样是影响昆虫生存的非生物因素之一[1],然而却极易被人们忽略。地磁场作为地球上最基本的物理因素,时刻影响着地球上生物的发育与进化[2]。地磁场强度从赤道的约30 μT向两极逐渐递增到约65 μT,且其强度随着时间和空间的变化而不断变化。许多动物如鱼类、鸟类、昆虫等动物可依赖地球磁场进行洄游及飞行定向[35]。磁场的极性、强度和倾角都可以帮助昆虫确定目的地的地理位置进而帮助昆虫保持恒定航向[6]。磁场变化不仅会影响昆虫的定向行为,还会对昆虫生长发育产生影响,如磁场强度降低会延长棉铃虫Helicoverpa armigera和褐飞虱Nilaparvata lugens生长发育历期,降低褐飞虱产卵量,影响其翅型分化等[78]。尽管近年来开展了许多磁感应研究,然而关于生物磁效应机制目前尚不明确[9]。
黏虫Mythimna separata是我国重要的农业害虫之一,每年在我国南北往返季节性迁飞[1011]。其迁飞过程中,不仅湿度和温度在逐渐变化,地磁场强度和方向也在不断变化。前人研究表明,黏虫雌、雄蛾在人工模拟的强磁场、近零磁场下均没有显著的群体共同定向行为,且野外不同地区迁飞性黏虫的定向方向不同,表明黏虫可能根据磁场进行迁飞定向[1214]。因此,明确磁场变化对黏虫的影响及黏虫的地磁定向机制对黏虫发生的预测预报具有重要意义。
近零磁场又称为亚磁场,即屏蔽地磁场后产生的磁场强度接近零的磁场。近零磁场可用于揭示磁场强度降低对生物产生的影响及地磁场对生物的重要性[1516]。本研究通过直流电型亥姆霍兹线圈屏蔽地磁场,利用转录组测序技术探索黏虫对近零磁场的分子响应机制,进一步挖掘磁感受相关基因,以期为深入研究迁飞性昆虫的地磁定向机制提供理论依据。
1 材料与方法
1.1 供试虫源及饲养条件
以本实验室连续繁殖多代的黏虫为供试虫源,室内饲养条件为温度(26±1)℃,相对湿度(70±10)%,光周期L∥D=14 h∥10 h,幼虫饲养密度为10头/罐(罐直径9 cm,高13 cm),以人工饲料饲喂,幼虫老熟后置于含水量为15%的土壤中化蛹,成虫羽化后饲喂5%的蜂蜜水,取羽化后48 h的雌、雄蛾供试,并设置3次重复。
1.2 磁场发生装置
磁场发生装置由亥姆霍兹线圈和相连的两个电源箱组成(中国科学院电工所制),亥姆霍兹线圈为正方体形,线框直径为1 m,通过调节电源箱电流可在线圈中心区域(20 cm×20 cm×20 cm)内产生低于500 nT的磁场(近零磁场)。两个磁场发生装置放置在同一房间内(间隔3 m),一个用来产生近零磁场,另一个用来做假暴露以避免装置带来的误差。每次试验前及过程中均使用磁强计(CH-330F,北京翠海科技有限公司)检测磁场强度。
1.3 黏虫成虫RNA提取
供试黏虫从卵至成虫分别放置在近零磁场和正常地磁场中饲养。分别收集正常地磁场下和近零磁场下羽化48 h的雌、雄蛾虫体。不同磁场下每个性别各3个重复,共12个样品。每个样品由3头黏虫混合组成,液氮处理后储存在-80℃超低温冰箱中。以地磁场下黏虫雌、雄蛾为对照,近零磁场下雌、雄蛾为处理组进行转录组测序,地磁场下雌、雄蛾样品分别编号为GF1、GF2、GF3和GM1、GM2、GM3,近零磁场雌、雄蛾样品分别编号为OF1、OF2、OF3和OM1、OM2、OM3。采用TRIzol法提取不同处理组样品总RNA。1%的琼脂糖凝胶电泳检测RNA是否降解或污染,超微量紫外分光光度计(凯奥,K5500)检测RNA的纯度,使用安捷伦2100 RNA Nano 6000 Assay Kit(Agilent Technologies,CA, USA)检测RNA样品的完整性和浓度。
1.4 转录组测序及信息注释
检测合格的RNA样品在北京安诺优达公司进行cDNA文库构建以及Illumina平台测序。测序完成后,通过去除低质量序列、去接头等过程完成数据处理,得到高质量序列进行组装。选取| log2Ratio |≥1和q<0.05的基因作為差异显著表达基因。
1.5 GO功能分析
根据Gene Ontology数据库(http:∥www.geneontology.org/),使用GO功能来分析差异基因(DEG)的主要功能。计算每个GO条目的差异基因数目,应用超几何检验,找出与整个基因组背景相比,在差异表达基因中显著富集的GO条目。其计算公式为P=∑m-1i=0(Mi)(n-Mn-i)(Nn),其中N为所有基因中具GO功能注释的基因数目;n为N中差异表达基因的数目;M为所有基因中注释到某特定GO条目的基因数目;m为注释到某特定GO条目的差异表达基因数目。计算得到的P值经过校正后,以P<0.05为阈值,满足P<0.05的GO条目为差异表达基因中显著富集的GO条目。
1.6 pathway 富集分析
根据京都基因和基因组百科全书(KEGG)(http:∥www.genome.jp/kegg/),使用pathway分析确定差异表达基因的主要通路。以P<0.05为标准,对KEGG中每个pathway应用超几何检验进行富集分析,找出差异表达基因中显著富集的pathway。
1.7 qPCR定量分析
为验证转录组测序的准确性,从测序结果中随机选择10个差异表达基因采用荧光定量PCR进行验证。使用Beacon Designer设计基因特异性引物(表1),并由生工生物工程(上海)有限公司合成,以β-actin和18S rRNA为内参基因。将提取的RNA反转录合成cDNA第一条链;以合成的cDNA为模板,在Bio Rad 仪器上进行实时荧光定量PCR:35个循环,95℃变性15 s,60℃退火30 s,72℃延伸30 s。绘制熔解曲线,采用2-ΔΔCt法计算相对表达量。
1.8 数据统计
每个试验用重复3次的样品进行qPCR分析。文中数据均为平均值±标准误(SE)。均值用单因素方差分析作比较。当P<0.05时为差异显著。
2 结果与分析
2.1 转录组组装结果与质量评估
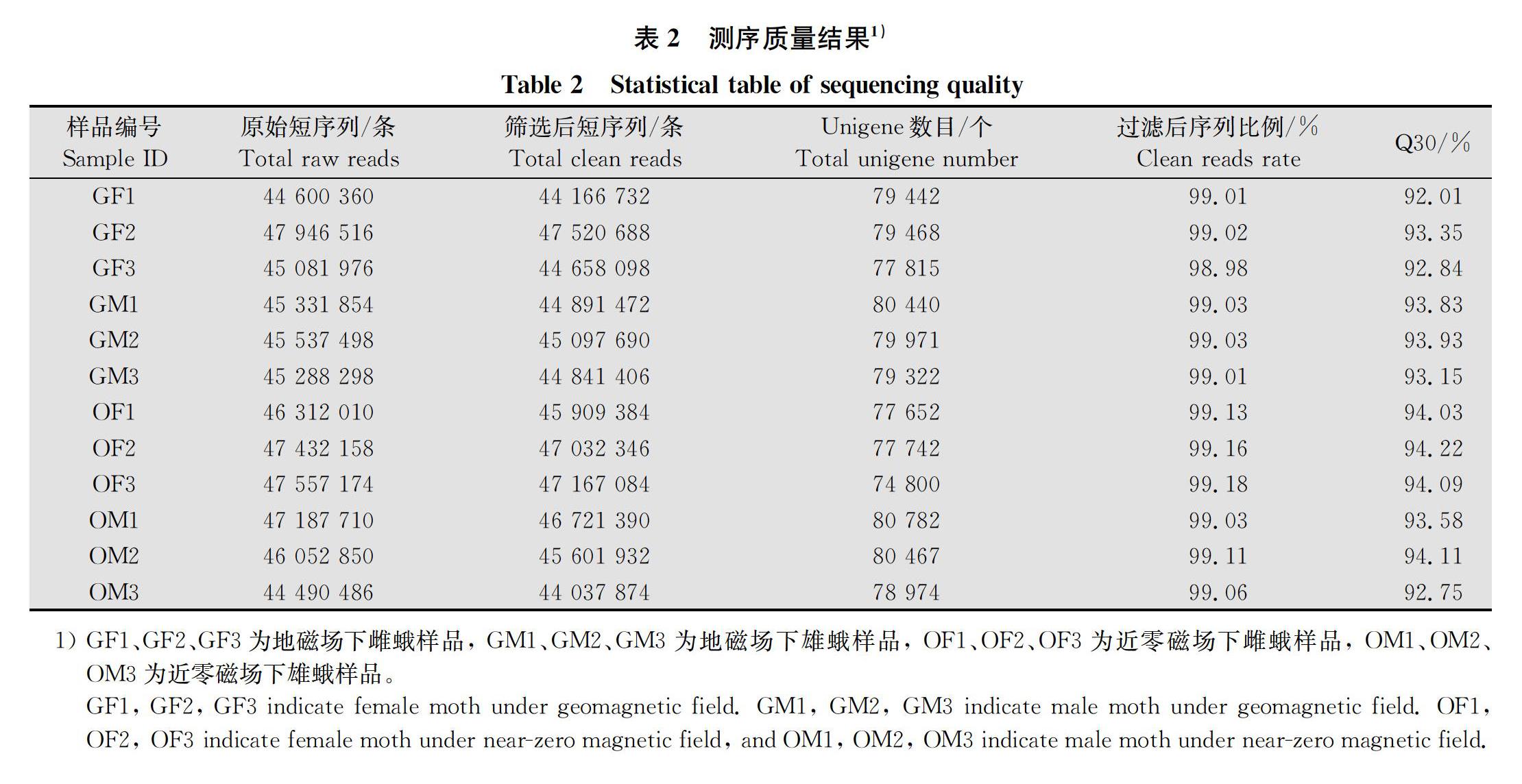
经检测,样品总RNA均满足后续试验分析要求。不同磁场下雌、雄蛾共12个样本转录组测序数据统计结果见表2。过滤后的reads数占总数的98%
以上。各样本的Q30(序列中质量大于30即错误率小于0.1%的碱基数的比例)均在92%以上,各样本GC含量均在40%左右,测序结果准确度较高,可用于后续分析。
1) GF1、GF2、GF3为地磁场下雌蛾样品, GM1、GM2、GM3为地磁场下雄蛾样品, OF1、OF2、OF3为近零磁场下雌蛾样品, OM1、OM2、OM3为近零磁场下雄蛾样品。
GF1, GF2, GF3 indicate female moth under geomagnetic field. GM1, GM2, GM3 indicate male moth under geomagnetic field. OF1, OF2, OF3 indicate female moth under near-zero magnetic field, and OM1, OM2, OM3 indicate male moth under near-zero magnetic field.
2.2 差异表达基因分析
相对于地磁场,近零磁场下雌、雄蛾分别鉴定出1 670个和1 401个差异表达基因,其中雌、雄蛾分别鉴定出614、545个上调基因和1 056、856个下调基因(图1~2)。其中雌、雄蛾共同差异表达基因274个。大部分差异表达基因的差异倍数分布在1倍~10倍之间,少部分差异倍数达到10倍以上。
2.3 GO功能分析
GO功能分析结果显示(图3),生物过程中,不同磁场下黏虫雌雄蛾差异基因主要集中在催化、合成和代谢过程;在分子功能中雌、雄蛾分别有53个和24个显著富集条目,大多为聚合酶、内切酶、水解酶、合成酶、核酸酶、还原酶和肽酶活性等;细胞组分中差异基因主要集中在细胞内和细胞质组分。
2.4 KEGG通路分析
在pathway分析中,除人类疾病外,雌蛾中细胞黏附分子通路富集到的差异基因最多,其次为AMPK信号通路、脂肪酸合成通路、细胞外基质受体交互作用通路、PI3K-Akt信号通路、嘌呤代谢、脂肪酸代谢、碳代谢、胆固醇代谢、神经活性配体—受体相互作用途径。雄蛾中雷帕霉素信号通路富集到的差异基因最多,其次为脂肪酸代谢、甘氨酸、丝氨酸和苏氨酸代谢、AMPK信号通路、细胞凋亡、自噬、脂肪酸合成,神经活性配体—受体相互作用途径。
2.5 qRT-PCR验证
从转录组中随机挑选了10个差异表达基因进行荧光定量PCR验证。结果表明差异基因定量表达结果与转录组测序结果一致(图4),其中7个基因表现为一致下调,3个基因表现为一致上调。说明转录组测序具有较高的准确性和可靠性。
3 讨论
自趋磁细菌发现以来,越来越多的国内外学者关注磁场的磁生物学效应。地磁定向是远距离迁飞昆虫的重要定向机制之一,也是目前生物磁效应研究热点[17]。目前,广泛认可的磁感应机制有两种,即依赖光的自由基对假说和磁颗粒假说,两种假说之间并不矛盾,两者可能同时存在于生物体内[1819]。
在依赖光的自由基对假说中,蓝光受体隐花色素CRYs被认为是最可能的磁感应受体。CRYs是紫外光和蓝色光感受器,存在于植物和动物中,含有黄素腺嘌呤二核苷酸(FAD)发色团,在光活化后形成自由基对[2021]。磁场还被认为是一种授时因子[2126],CRY作为核心生物钟基因,被认为参与了磁场影响果蝇昼夜节律的过程[27],同时CRY还参与介导磁场对果蝇趋地性、趋光性,交配行为等的影响过程[2829]。Mo等对近零磁场下培养的人神经瘤母细胞进行转录组测序,筛选到CRY2在近零磁场下差异表达[30],而在灰飞虱Laodelphax striatellus雌成虫的转录组测序结果中,CRYs在地磁场和近零磁场下并不存在显著差异表达[31]。在黏虫雌雄蛾转录组测序结果中也未筛选到CRYs基因在地磁场和近零磁场下差异表达,这可能与CRYs的调控时间和作用位置有关。万贵钧研究表明白背飞虱Sogatella furcifera体内CRY1和CRY2对近零磁场的响应存在时间特异性,可能是CRYs的生物钟功能和磁感受功能交互作用引起的[32]。
磁颗粒假说认为磁铁矿物晶体存在于生物体内,外界磁场对生物体内铁磁颗粒产生磁矩进而改变生物膜上的离子通道开关影响神经系统[19]。迁飞性昆虫褐飞虱、鳞翅目昆虫黑脉金斑蝶 Danaus plexippus体内均已发现铁磁性物质[3334]。而黏虫体内尚未发现存在铁磁性物质。Fitak等通过转录组测序开展了虹鳟鱼在基因水平对脉冲磁场的响应研究,发现与铁吸收和转运相关的ferritin基因参与虹鳟鱼的磁感受过程[35]。对近零磁场下培养的灰飞虱雌虫的转录组测序发现,与铁吸收相关的MVL基因在灰飞虱雌成虫中差异表达[31]。本研究发现黏虫雄蛾体内与Fe转运蛋白和铁硫结合相关基因差异表达,雌、雄蛾中分别筛选到17个和8个与铁离子转运结合相关的差异表达基因,推测磁颗粒感受机制可能在黏虫的磁响应过程中发挥作用。
在GO功能分析中,不同磁场下黏虫雌、雄蛾差异表达基因大多富集在离子结合、代谢和酶活过程,表明近零磁场对黏虫的生长发育也存在一定影响。这与前期研究发现近零磁场对黏虫的生长发育存在负面影响一致(未发表数据)。本试验中,近零磁场下黏虫雌、雄蛾下调基因数量都多于上调基因,与人神经瘤母细胞的测序结果[30]相似,而近零磁场下的灰飞虱雌虫转录测序得到数量相近的下调基因和上调基因[31],这可能是由于不同物种对近零磁场的响应存在特异性差异。近零磁场下雌、雄蛾转录组中,雌蛾比雄蛾多出269个差异基因,雌、雄蛾共同差异表达基因共274个,在GO功能分析的生物过程中,雌、雄蛾差异表达基因显著富集到的生物途径也有所不同,不同性别黏虫可能对近零磁场的敏感性不同。
昆虫的地磁定向機制是一个复杂的过程,不仅与地磁场强度有关,还可能与磁场的极性和磁倾角相关,而本试验仅考虑了磁场强度,并未涉及磁倾角的变化。昆虫的地磁定向机制应结合生物物理学、生态学、分子生物学、解剖学等多学科做进一步研究。
参考文献
[1] MARKOV M S. Electromagnetic fields—A new ecological factor [M]∥MARKO M, MARTIN 13. Electromagnetic fields and biomembranes. Springer US, 1988.
[2] OCCHIPINTI A, DE SANTS A, MAFFEI M E. Magnetoreception: an unavoidable step for plant evolution? [J]. Trends in Plant Science, 2014, 19(1): 14.
[3] QUINN T P. Evidence for celestial and magnetic compass orientation in lake migrating sockeye salmon fry [J]. Journal of Comparative Physiology, 1980, 137(3): 243248.
[4] QUINN T P, BRANNON E L. The use of celestial and magnetic cues by orienting sockeye salmon smolts [J]. Journal of Comparative Physiology, 1982, 147(4): 547552.
[5] WILTSCHKO W, WILTSCHKO R. Magnetic orientation in birds [J]. The Journal of Experimental Biology, 1996, 199(1): 2938.
[6] LOHMANN K J, LOHMANN C M F, PUTMAN N F. Magnetic maps in animals: natures GPS [J]. The Journal of Experimental Biology, 2007, 210(21): 36973705.
[7] WAN Guijun, JIANG Shoulin, ZHAO Zongchao, et al. Bio-effects of near-zero magnetic fields on the growth, development and reproduction of small brown plant hopper, Laodelphax striatellus and brown plant hopper, Nilaparvata lugens [J]. Journal of Insect Physiology, 2014, 68: 715.
[8] 董兆克, 戈峰. 磁場对棉铃虫生长发育及繁殖的影响[J]. 生态学杂志, 2013, 32(5): 12651268.
[9] NORDMANN G C, HOCHSTOEGER T, KEAYS D A. Unsolved mysteries: Magnetoreception-a sense without a receptor [J/OL]. PLoS Biology, 2017, 15(10): e2003234. DOI:10.1371/journal.pbio.2003234.
[10]李光博. 我国黏虫研究概况及主要进展[J]. 植物保护, 1993, 19(4): 24.
[11]江幸福, 张蕾, 程云霞, 等. 我国黏虫发生危害新特点及趋势分析[J]. 应用昆虫学报, 2014, 51(6): 14441449.
[12]王伟弘, 张蕾, 程云霞, 等. 黏虫飞行定向行为与不同磁场环境的关系[J]. 应用昆虫学报, 2018, 55(5): 2835.
[13]高月波, 胡高, 翟保平. 磁场变化对黏虫飞行定向行为的影响 [J]. 应用昆虫学报, 2014, 51(4): 899905.
[14]谢殿杰. 粘虫的定向行为及相关基因Cry2、MagR的功能验证[D]. 北京: 中国农业科学院, 2018.
[15]BINHI V N, SARIMOY R M. Zero magnetic field effect observed in human cognitive processes [J]. Electromagnetic Biology and Medicine, 2009, 28(3): 310315.
[16]ZHANG Bin, LU Huimin, WANG Xi, et al. Exposure to hypomagnetic field space for multiple generations causes amnesia in Drosophila melanogaster [J]. Neuroscience Letters, 2004, 371(2/3): 190195.
[17]贺静澜, 万贵钧, 张明, 等. 生物地磁响应研究进展[J]. 生物化学与生物物理进展, 2018, 45(7): 689704.
[18]RITZ T, ADEM S, SCHULTEN K. A model for photoreceptor-based magnetoreception in birds [J]. Biophysical Journal, 2000, 78(2): 707718.
[19]FLEISSNER G, STAHL B, THALAU P, et al. A novel concept of Fe-mineral-based magnetoreception: histological and physicochemical data from the upper beak of homing pigeons [J]. Naturwissenschaften, 2007, 94(8): 631642.
[20]CASHMORE A R, JARILLO J A, WU Yingjie, et al. Cryptochromes: blue light receptors for plants and animals [J]. Science, 1999, 284(5415): 760765.
[21]GIOVANI B, BYRDIN M, AHMAD M, et al. Light-induced electron transfer in a cryptochrome blue-light photoreceptor [J]. Nature Structural Biology, 2003, 10(6): 489490.
[22]WEVER R. Influence of weak electromagnetic fields on the circadian periodicity of humans [J]. The Science of Nature, 1968, 55(1): 2932.
[23]BLISS V L, HHEPPNER F H. Circadian activity rhythm influenced by near zero magnetic field [J]. Nature, 1976, 261(5559): 411412.
[24]MURAVEIKO V M, STEPANYUK I A, ZENZEROV V S. The response of the crab Paralithodes camtschaticus (Tilesius, 1815) to geomagnetic storms [J]. Doklady Biological Sciences, 2013, 448(1): 1012.
[25]MARTIN H, KORALLl H, FRSTER B. Magnetic field effects on activity and ageing in honeybees [J]. Journal of Comparative Physiology A: Sensory Neural and Behavioral Physiology, 1989, 164(4): 423431.
[26]MO Weichuan, FU Jinpeng, DING Huimin, et al. Hypomagnetic field alters circadian rhythm and increases algesia in adult male mice [J]. Progress in Biochemistry and Biophysics, 2015, 42(7): 639646.
[27]YOSHII T, AHMAD M, HELFRICH, F C, et al. Cryptochrome mediates light-dependent magnetosensitivity of Drosophilas circadian clock [J/OL]. PLoS Biology, 2009, 7(4): e1000086. DOI:10.1371/journal.pbio.1000086.
[28]BAE J E, BANG S, MIN S, et al. Positive geotactic behaviors induced by geomagnetic field in Drosophila [J]. Molecular Brain, 2016, 9(1): 5567.
[29]FEDELE G, GREEN E W, ROSATA E, et al. An electromagnetic field disrupts negative geotaxis in Drosophila via a CRY-dependent pathway [J/OL]. Nature Communications, 2014, 5: 4391.DOI:10.1038/ncomms5391.
[30]MO Weichuan, LIU Ying, BARTLETT P F, et al. Transcriptome profile of human neuroblastoma cells in the hypomagnetic field [J]. Science China Life Sciences, 2014, 57(4): 448461.
[31]劉凡奇. 近零磁场下灰飞虱的生长发育表型与转录组学分析研究[D]. 南京: 南京农业大学, 2017.
[32]万贵钧. 病毒和磁场对稻飞虱发育、生殖及行为的影响研究[D]. 南京: 南京农业大学, 2015.
[33]解春兰, 李志毅, 隋贺, 等. 褐飞虱成虫体内磁性物质检测[J]. 昆虫学报, 2011, 54(10): 11891193.
[34]JONE D S, MACFADDEN B J. Induced magnetization in the monarch butterfly, Danaus plexippus (Insecta, Lepidoptera) [J]. Journal of Experimental Biology, 1982, 96: 19.
[35]FITAK R R, WHEELER B R, ERNST D A. et al. Candidate genes mediating magnetoreception in rainbow trout (Oncorhynchus mykiss) [J/OL]. Biology Letters, 2017, 13(4): 20170142.DOI:10.1098/rsbl.2017.0142.
(责任编辑:杨明丽)
