超声图像中胆囊真假性息肉计算机辅助鉴别
2021-06-18余其徽袁海霞张燕群季正标王文平
余其徽 ,袁海霞 ,张燕群 ,俞 清 ,季正标 ,张 麒,5 ,王文平
(1.上海先进通信与数据科学研究院(上海大学),上海 200444;2.上海大学通信与信息工程学院,上海 200444;3.复旦大学附属中山医院超声科,上海 200032;4.复旦大学附属中山医院厦门医院超声科,福建 厦门 361015;5.杭州依图医疗研究院,浙江 杭州 310000)
0 引言
近年来,胆囊息肉样病变的发病率逐年升高,较为常见的两种息肉类型是胆囊胆固醇性息肉和胆囊腺瘤。前者不会发生恶变,称为假性息肉;而后者是一种起源于腺上皮的真性息肉,易发生不典型增生并发展为胆囊癌,属于癌前病变的一种[1-2]。目前,超声检查是区分胆囊真假性息肉首选的影像学方法。对于胆囊真性息肉,及时的胆囊切除术非常必要。临床外科学指南建议对于直径大于1 cm 的胆囊息肉进行胆囊切除术,但这经常受到学者和临床医生的质疑。他们认为,直径大于1 cm 的胆囊息肉中有许多良性息肉。如对良性息肉进行胆囊切除手术,会对患者的健康造成巨大的伤害,且占用公共卫生资源。同时,直径小于1 cm 的息肉也可能是真性息肉,仅超声观察其生长显然不合理[3-4]。因此,临床亟需一种可广泛应用的新技术,在术前尽早鉴别胆囊真假性息肉,从而仅对真性息肉进行胆囊切除术,降低医疗资源的浪费,提高患者的生存质量。
近年来,随着人工智能的迅猛发展,许多学者在医学影像领域取得了一定的进展。Dalmis 等提出人工智能多参数乳腺磁共振成像方法,实现了乳腺良恶性的病变分类[5]。Colling 等将图像分析和机器学习应用于组织病理学,加快了组织病理学在临床实践中的发展[6]。Weisberg 等将放射组学特征与深度学习模型相结合,实现了良好的胰腺癌早期诊断性能[7]。因此,考虑到计算机可能利用高维信息捕捉到宏观医学影像上的变化,其分辨率远远超过人眼的分辨率[8-9]。将基于计算机辅助分析超声图像,可获取客观的影像学特征,以鉴别胆囊良恶性息肉,为医生的临床决策提供精确、可靠的诊断建议。
本研究回顾性分析了经手术病理证实的胆囊胆固醇性息肉和胆囊腺瘤患者术前超声二维图像,通过计算机提取分析多组影像学特征,以期尽早发现这两种疾病的影像差异,从而辅助鉴别胆囊胆固醇性息肉和胆囊腺瘤。
1 材料和方法
首先,采集胆囊胆固醇息肉和胆囊腺瘤的超声图像并进行图像分割,以确定病灶位置。接着,用计算机提取病灶的空域、形态两类量化特征,并通过统计学分析对特征进行选择。最后,使用这些特征用于支持向量机(support vector machine,SVM)算法分类判决。胆囊胆固醇息肉和胆囊腺瘤的图像分析流程如图 1 所示。
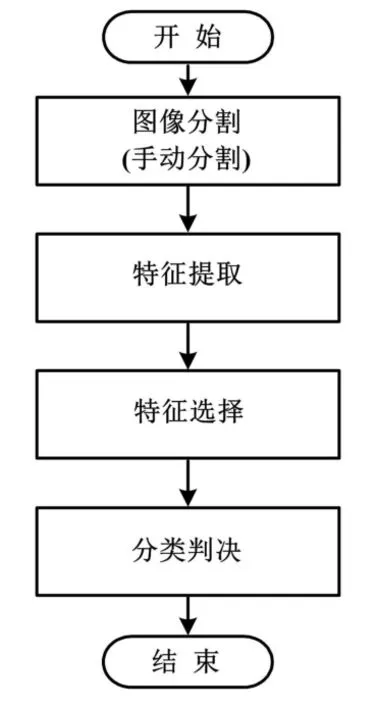
图1 胆囊胆固醇息肉和胆囊腺瘤的图像分析流程图Fig.1 Image analysis process of gallbladder cholesterol polyp and gallbladder adenoma
1.1 图像采集和图像分割
本文研究的病例超声图像来自于复旦大学附属中山医院超声科,共获得68 例患者69 个胆囊息肉术前超声图像资料。所有病例均行胆囊切除术并获得手术病理结果。其中,胆囊胆固醇息肉37 例38 个病灶,胆囊管状腺腺瘤31 例31 个病灶。病灶直径0.7~4.1 cm。超声检查仪器包括:Canon Aplio500(日本),Mindray Resona7s (中国),Hitachi Ascendus(日本)彩色多普勒超声诊断仪,探头频率3.5~5.0 MHz。患者超声检查前须空腹(禁食8 h 以上)。超声检查时,病灶局部放大并显示病变最大切面,测量病灶最大直径,并存储病灶原始超声图像。
在进行超声图像定量分析前,首先要确定病灶区域。胆囊腺瘤超声图像病灶处理如图2 所示。由于胆囊息肉、周边血管、腺体等组织器官结构复杂,图像自动分割技术并不能很好地对病灶进行准确分割。因此,本文由具有丰富临床经验的医生手动勾勒超声图像中的病灶轮廓,如图2(a)所示。接着,对超声图像进行二值化处理,得到掩膜图像,如图2(b)所示。其中,掩膜图像中白色像素点对应超声图像中的病灶区域,黑色像素点对应超声图像中的非病灶背景区域。
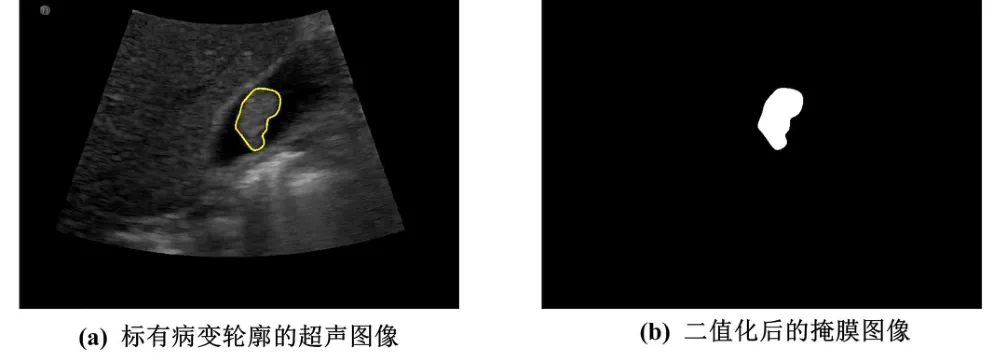
图2 胆囊腺瘤超声图像的病灶处理Fig.2 Lesion processing based on the ultrasound image of gallbladder adenoma
1.2 特征提取
本文将基于原始超声图像及其对应的掩膜图像提取病灶的影像学特征,包括空域特征和形态特征。首先,本文提取了病灶的空域特征。空域特征包括一阶统计量特征和灰度共生矩阵(gray level co-occurrence matrix,GLCM)特征。一阶统计量特征基于超声灰度图提取,包括:病灶内部像素的变异系数,其为离散程度的一个归一化量度,定义为标准差与平均值之比;相对中值比,其定义为病灶区域像素中值和参考区域 (病灶往外扩若干像素形成的矩形区域)像素中值的对应比值;相对均值比,其定义为病灶区域像素均值和参考区域 (病灶往外扩若干像素形成的矩形区域)像素均值的对应比值。
灰度共生矩阵是一种重要的纹理分析方法,其定义为图像上间隔距离为d和方向为θ的两个像素同时出现的联合概率分布G(i,j;d,θ)。共生矩阵的一个元素不仅可以反映像素的分布特性,也可以反映具有相同灰度或接近灰度的像素点之间的位置分布特性[10]。本文求取GLCM 特征时,为简化计算量,将原来的256 个灰度级重新量化到 8 个灰度级,即得到 8×8 的灰度共生矩阵G(i,j)(i=1,2,...,8;j=1,2,...,8)。同时,设定方向θ=0°,45°,90°,135°;距离d=1,2,...,15 像素。提取的GLCM 特征包括对比度和均一度。对比度反映原图像中病灶区域灰度值局部变化的情况。该值越大,说明病灶局部灰度变化越大。均一度反映原图像中纹理的相似度或同质性。该值越大,说明病灶局部间的灰度越接近、分布越均匀。
接着,本文提取了病灶的形态特征,如图3 所示。该类特征包括拟合椭圆的长轴长度和短轴长度,拟合椭圆是与病灶有相同标准二阶中心距的图形(椭圆所示)以及病灶的周长,其定义为病灶(不规则曲线所示)区域最外层像素点的个数。
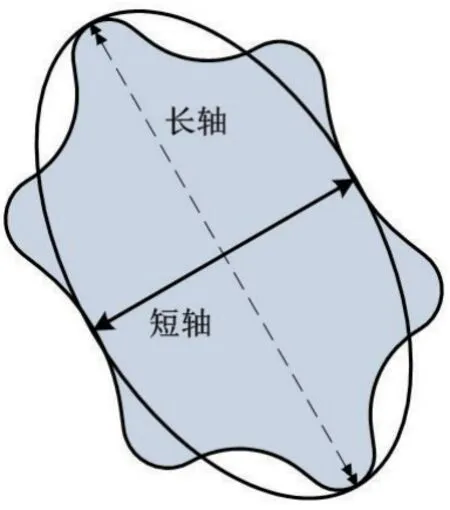
图3 病灶形态学特征的示意图Fig.3 Schematic diagram illustrating morphological features of lesion
1.3 特征选择
本文对提取的所有影像学特征进行了统计学检验。假设特征参数对应的数据为正态分布,采用非配对t检验;否则,采用KW 检验。其中,统计学检验输出概率p值小于0.05 表示有统计学差异,保留有统计学意义的特征,并依据这些特征进行后续的分类判决。
1.4 分类判决
由于医学数据获取的局限性及涉及的伦理问题,本文采集的胆囊息肉超声样本属于小样本集。考虑到SVM 对小样本集具有很高的适用性,本文选用SVM 算法对胆囊息肉进行分类判决。SVM 算法通过寻找一个决策边界来最大化两组之间的边界。这是一种非常流行的分类方法[11-12]。在本试验中,SVM 分类算法流程如图4 所示。图4 中,实线表示采用训练集训练,虚线表示使用测试集测试。
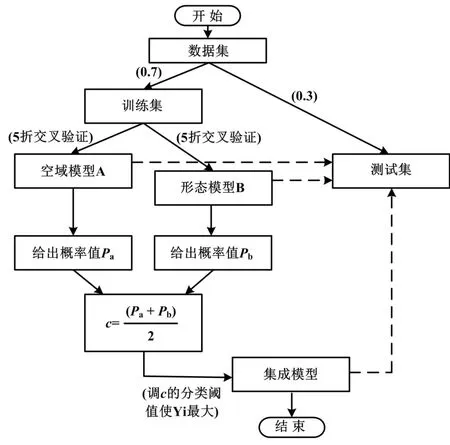
图4 SVM 分类算法流程图Fig.4 Flowchart of SVM classification algorithm
先按照7 ∶3 的比例将数据集分成训练集和测试集。在训练集上,本文分别采用5 次交叉验证方法,得到与空域特征相对应的最优模型A 和形态特征相对应的最优模型B。为集成A、B 两类模型,本文将模型A 训练集的输出概率值Pa和模型B 训练集的输出概率值Pb整合为特征c。对于每一个病例,c的定义如下:
然后,本文调整特征c的分类得分阈值以优化集成模型。其中,约登指数(youden index,Yi)作为参考指标,训练集Yi 最大值对应的最优分类得分阈值被用于测试集分类。最后,本文分析了模型A、模型B 和集成模型对应的测试集分类性能;同时,为了量化测试集的分类能力,通过10 次样本集随机划分,重复试验评估后取平均值作为测试集的评估结果。其中,本文采用的评估指标包括分类精度(accuracy,Acc)、分类灵敏度(sensitivity,Sen)、特异性(specificity,Spc)、受试者工作特征(receiver operating characteristic,ROS)和曲线下面积(area under the curve,AUC)。
2 结果分析
2.1 特征选择结果
所有入组病例均经手术病理证实,包括胆囊胆固醇性息肉37 例38 个病灶。胆囊腺瘤31 例31 个病灶。所有病例的病灶统计学分析结果如表1 所示。当特征参数对应的数据为正态分布时,给出对应特征的均值和标准差。否则,给出对应特征的中位数和四分位数。

表1 所有病例的病灶区域统计学分析Tab.1 Quantitative analysis results for lesion regions of all patients
在表2 中,从空域特征来看,对比度、均一度和相对中值比对胆囊胆固醇性息肉和胆囊腺瘤的鉴别有很大的参考价值(p<0.001)。相较于胆囊胆固醇性息肉,胆囊腺瘤的变异系数和对比度值更小,均一度更大,表明胆囊腺瘤的病灶区域的像素分布更均匀;同时,胆囊腺瘤的相对中值比和相对均值比更小,表明胆囊腺瘤的内部高亮区域相对占比更少。从形态特征来看,长轴长度、短轴长度和病灶的周长对胆囊胆固醇性息肉和胆囊腺瘤的鉴别有较大的参考作用(p<0.001),相较于胆囊胆固醇性息肉,胆囊腺瘤的长轴长度、短轴长度和周长更大,表明胆囊腺瘤的病灶区域外周轮廓更大,并且形态更不规则。
胆囊胆固醇息肉和胆囊腺瘤的超声图像如图5所示。
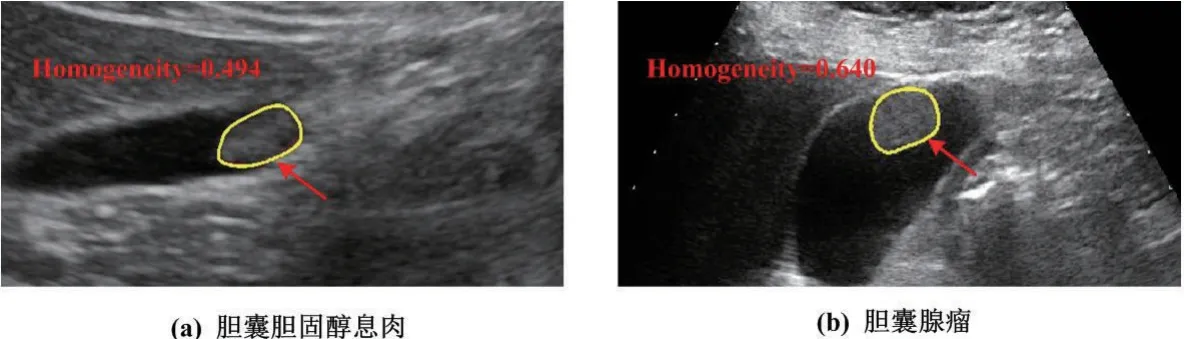
图5 胆囊胆固醇息肉和胆囊腺瘤的超声图像Fig.5 Ultrasound image of gallbladder cholesterol polyps and gallbladder tubular adenoma
通过超声图像影像学分析,胆囊腺瘤的均一度参数值(0.640)明显高于胆囊胆固醇息肉的均一度参数值(0.494)。分析结果表明,胆囊腺瘤病灶区域的像素分布较胆固醇性息肉更均匀。该特征有助于区分胆固醇息肉和胆囊腺瘤,对两种疾病的鉴别诊断有一定的潜在价值。
2.2 分类判决结果
使用SVM 分类算法,本文分别得到5 个空间特征对应的最优模型A 和3 个形态特征对应的最优模型B以及集成模型。测试集的分类性能如表2 所示。
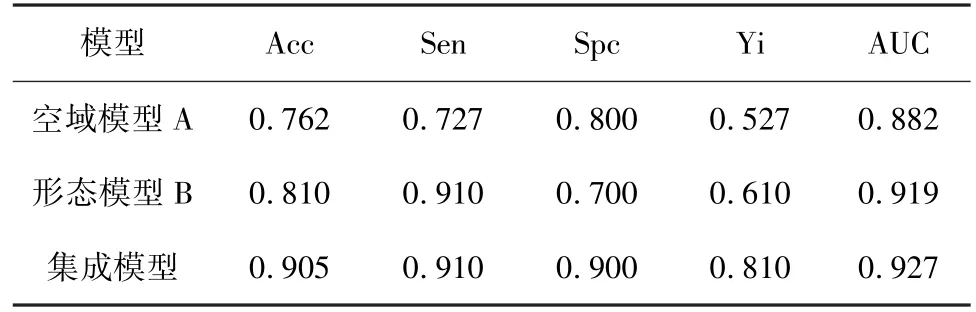
表2 测试集的分类结果Tab.2 Classification results of the test set
分类结果表明,与空域模型A 的分类性能相比,形态模型B 的Acc 更高,但Sen 和Spc 相对更不平衡。
不同模型的ROC 曲线如图6 所示。
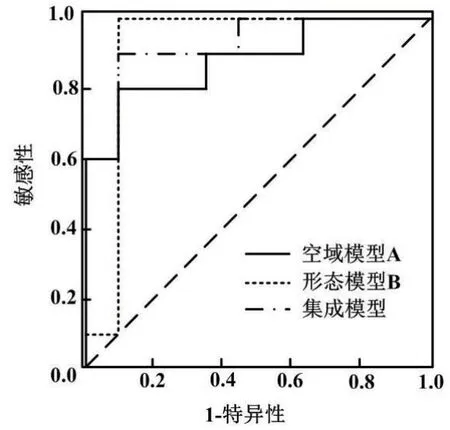
图6 不同模型的ROC 曲线Fig.6 ROC curves of different models
当集成模型A 和B 之后,测试集的Acc、Sen 和Spc 分别提高到0.905、0.910 和0.900。此时,平均分类得分阈值为0.351。同时,从图6 中可以看出,集成模型的AUC(0.927)最高,形态模型AUC(0.919)高于空间模型AUC(0.882)。
3 结论
本研究尝试将人工智能影像学技术应用于69例胆囊息肉的二维超声图像分析,以区分胆囊胆固醇息肉和胆囊腺瘤。空域特征研究显示,与胆囊胆固醇息肉相比,胆囊腺瘤的病灶区域像素分布更均匀(均一度;p<0.001),息肉内部高亮区域相对占比更少(相对中值比;p<0.001),胆囊腺瘤的这些影像学特征与其病理特征密切相关,表明均一度和相对中值比等特征确实具有潜在的分类能力,与文献报道相符[13]。同时,形态特征研究表明,相较于胆囊胆固醇性息肉,胆囊腺瘤的病灶区域形态周长更大(周长;p<0.001)。但胆囊腺瘤的平均直径大于胆囊胆固醇息肉,并不能表示较大的病灶中没有胆固醇息肉、较小的病灶中不存在胆囊腺瘤。这种仅依靠息肉的大小和形状来鉴别胆囊真假性息肉的方法过于简单化。因此,以考虑结合病灶空域和形态特征来鉴别胆囊腺瘤和胆固醇息肉为宜。本文SVM 集成模型分类准确率、敏感性、特异性分别达到90.5%、91.0%、90.0%,曲线下面积为0.927,表明借助计算机辅助分析胆囊息肉超声图像,有助于临床医生从其潜在的形态和空域特征中获益,从而对胆囊真假性息肉进行准确鉴别。
本研究也存在一定的局限性。首先,本文初步将人工智能技术应用于胆囊真性息肉与假性息肉鉴别,病例数还相对较少,需积累更多的病例以进一步验证方法的有效性及模型的泛化能力,从而为临床诊断提供更可靠的参数和诊断界值。其次,后续的研究将尝试提取更多的超声影像定量特征,并结合弹性超声、超声造影等多模态超声技术获取多模态超声特征,从而更全面、准确地表征胆囊息肉属性,实现更精准的真假性息肉鉴别。
