正交实验研究表面活性物含量对瓶片清洗影响及测试
2021-06-15潘宏瑞陈瑾影王永杰张础锐刘天祥张天翔
潘宏瑞,陈瑾影,王永杰,张础锐,刘天祥,张天翔
(沈阳工业大学石油化工学院,辽宁 辽阳 111003)
近年来,废弃塑料所引发的一系列问题受到社会各界的广泛关注。废弃塑料制品带来的环境污染问题日渐突出。塑料清洗剂是一种专门清洗塑料表面的溶剂,一般作用于塑料处理前的清洗系统中[1]。但是,洗脱后产生的大量废水具有较高的COD,无法直接排放,既造成水资源的浪费,又增加清洗成本[2-4]。目前,国内外的相关研究仍处于初始阶段,因此研制对环境友好的塑料清洗剂成为大规模推广运用的重中之重。对现有塑料清洗剂性能进行改进,保证清洗质量,提高清洗效率,无废水产生,可循环利用。尤其对于高纬度寒冷地区,保证清洗剂在 -15 ℃ 时不凝固,能够正常使用,落实大规模、可持续的绿色工业化生产,是本研究所要解决的主要问题。
本研究采用水溶性混合法,利用十二烷基苯磺酸钠、氢氧化钠、丙酸、丙酸(丙)酯及水复合物余量等主要原料与硫酸钠、甲醇钠、壬基酚聚氧乙烯醚(NP-10)、渗透剂T、脂肪醇聚氧乙烯醚硫酸钠、消泡剂等辅助原料进行复配研究,制备出一种环境友好型可回收循环利用塑料清洗剂。上述的丙酸、丙酸酯及水复合物余量采用的是生产丙酸乙酯、丙酸正丙酯后的副产物,是对工业废料的二次利用,不仅做到回收废料、大幅降低成本,还兼具抑菌、杀菌作用,减少了对环境的污染。通过正交实验测试研究清洗剂中表面活性物的含量对瓶片清洗行为的影响,研制出最优的清洗剂配方。本研究已经初步实现工业化,具有显著的社会效益和经济效益,为新型清洗剂工业化奠定基础,为其他清洗剂的复配提供理论指导。
1 实验部分
1.1 材料与仪器
酯化反应工艺水、甲醇钠(辽宁港隆化工有限公司);氢氧化钠(天津市瑞金特化学品有限公司);十二烷基苯磺酸、硫酸钠、脂肪醇聚氧乙烯醚硫酸钠、NP-10、渗透剂、消泡剂(郑州中扬化工产品有限公司);盐酸(上海试剂一厂);酚酞(沈阳试剂厂)。试剂均为分析纯,市售。
SHT型数显恒温磁力搅拌电热套(山东华鲁电热仪器有限公司);FV2004B型电子分析天平(上海佑科仪器有限公司);Nicolet5700红外光谱仪;GC9790Ⅱ气相色谱工作站;DGF702-1型电热鼓风干燥箱(大连实验设备厂);800A型多功能粉碎机(永康市穗机制制造厂);28-1型磁力加热搅拌器(常州国华电器有限公司)。
1.2 实验方法
1.2.1 清洗剂制备方法
在电子分析天平上称取 78 g 酯化反应工艺水,3 g 氢氧化钠加入容积为 250 mL 的烧杯内,用磁力搅拌器搅拌 1 min ,加入十二烷基苯磺酸 17 g,搅拌中和1~2 min,取样测pH值(8~9之间),若pH值不合格则需补加氢氧化钠。加 2 g 硫酸钠及 1 g 甲醇钠,搅拌1~2 min,搅拌均匀,至全部混合。加 6 g 脂肪醇聚氧乙烯醚硫酸钠,1 g NP-10,1 g 渗透剂T及少许消泡剂,搅拌1~2 min,搅拌均匀,至全部混合。测pH值(8~9之间)。
1.2.2 清洗剂瓶片清洗阶段的测试
1)瓶片的制备。本清洗实验选用生活中常见白色包装的乳制品饮料瓶以及透明包装的油壶瓶作为清洗对象,将收集来的塑料剪开,选取其中平整的部位剪成1×1 cm 的塑料小碎片。
2)瓶片的清洗。在 500 mL 烧杯中加入磁力转子,放入电子计价称上称量清零,向烧杯中加入 10 g 塑料瓶片,100 g 水,1 g 样品清洗剂及 1 g 氢氧化钠(所加入的含量以工业化清洗标准为参照),放入数显恒温磁力搅拌电热套加热到 90 ℃(以磁力搅拌代替揉搓机),时长设定为 5 min(工业化时长为 30 min,在本实验中由于清洗物较少故缩短清洗时间)。
3)瓶片的清洗效果测试。清洗结束后放入清水中漂洗(本实验以手工揉搓取代揉搓机),取出被清洗的瓶片,室温晾干,放在电热鼓风干燥箱 200 ℃,干燥 20 min,取出后放在白色比色卡中与标准瓶片作对比。评价瓶片的热稳定性,是否发黄。
4)清洗剂表面活性物含量的测试。测量第一次清洗过后的活性物含量以及pH。将清洗过后的清洗剩出液分层去掉固体杂质,如果清洗剂表面活性物含量低,可以补充表面活性剂。pH低,补充NaOH,再次循环清洗测试清洗效果,步骤与上述相同,如图1所示。

图1 清洗瓶片工艺流程图
1.2.3 经过N次清洗废水处理的实验方法
称取 50 mL 实验产生废水加入 100 mL 烧杯中,先加入2~5滴质量分数为 300 mg/kg 聚丙烯酰胺,后加入2~3滴质量分数为 300 mg/kg 硫酸铝溶液。静置 1 h 后,用漏斗过滤掉固体絮凝杂质,如遇油水分层应先用分液漏斗分层后再过滤,过滤后得到水的pH为中性时,可以重复利用。
2 结果与讨论
2.1 单因素实验
2.1.1 十二烷基苯磺酸对塑料清洗剂活性物的影响
十二烷基苯磺酸是清洗剂中的主要成分,以质量分数为变量开展因素实验。由最初实验研制清洗剂的质量分数为依据:酯化反应工艺水 78 g(78%)、氢氧化钠 3 g(3%)、十二烷基苯磺酸 17 g(17%)、硫酸钠 0.2 g(0.2%)、甲醇钠 1 g(1%)、脂肪醇聚氧乙烯醚硫酸钠 0.6 g(0.6%)、NP-10 0.1 g(0.1%)、渗透剂 0.1 g(0.1%)。故对十二烷基苯磺酸的质量分数以11%用量为起点,每次增加3%的量,共5组,其他组分不变。图2给出了十二烷基苯磺酸含量对塑料清洗剂活性物含量的影响。由图2可知,十二烷基苯磺酸的质量分数为17%时,塑料清洗剂活性物含量最高。
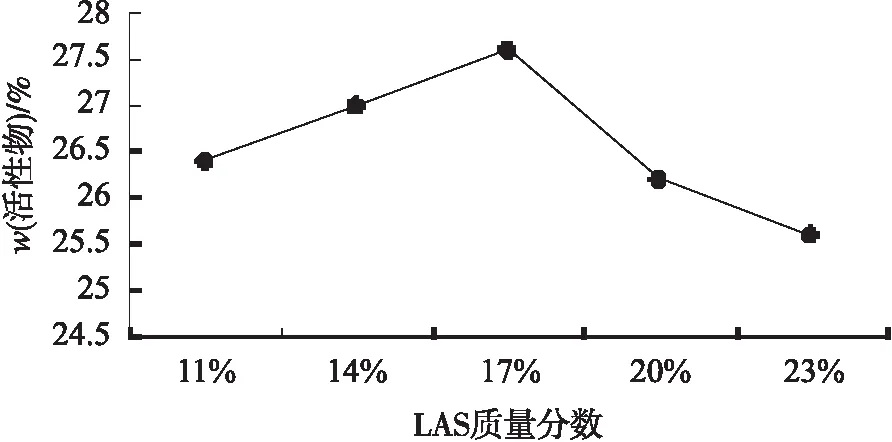
图2 十二烷基苯磺酸对塑料清洗剂活性物含量的影响
2.1.2 酯化反应工艺水对塑料清洗剂活性物含量的影响
酯化反应工艺水作为溶剂,对清洗剂的制备有着至关重要的作用。本实验设置5组以3%用量为增量,从72%递加到84%,观察单因素实验中酯化反应工艺水的最佳用量,如图3所示。由图3可知,酯化反应工艺水质量分数为78%时,塑料清洗剂活性物含量最高。

图3 酯化反应工艺水对塑料清洗剂活性物含量的影响
2.1.3 氢氧化钠对塑料清洗剂活性物含量的影响
氢氧化钠作为碱性清洁剂被广泛用于工业范围,本实验设置5组以1%为增量,从1%递加到3%,观察单因素实验中氢氧化钠的最佳用量,如图4所示。由图4可知,氢氧化钠质量分数为3%时,塑料清洗剂活性物含量最高。

图4 氢氧化钠对塑料清洗剂活性物含量的影响
2.2 正交实验
选用以十二烷基苯磺酸、酯化反应工艺水、氢氧化钠质量分数为影响塑料清洗剂活性物含量的主要因素,进行三因素三水平的正交实验。正交实验与水平数值选择见表1,实验结果与分析见表2。

表1 因素水平表
由表2得出,在该塑料清洗剂体系中,对实验结果的影响因素由强到弱依次为氢氧化钠、十二烷基苯磺酸、酯化反应工艺水。其中塑料清洗剂活性物含量最高的为第二组,即清洗剂中含有(质量分数)十二烷基苯磺酸17%,酯化反应工艺水78%,氢氧化钠3%。
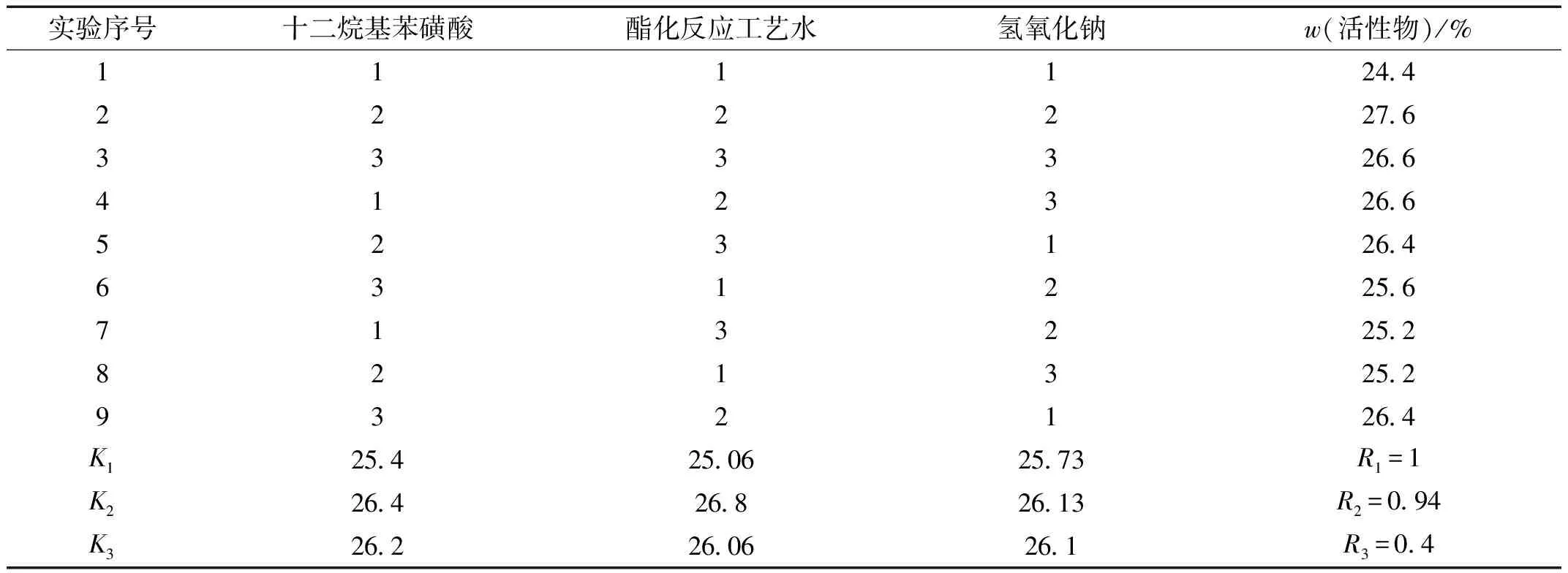
表2 正交实验结果与分析
2.3 重复性实验
对第二组正交试验进行重复性实验。重复性实验共分为三组,以酯化反应工艺水 78 g(78%)、氢氧化钠 3 g(3%)、十二烷基苯磺酸 17 g(17%)、硫酸钠 0.2 g(0.2%)、甲醇钠 1 g(1%)、脂肪醇聚氧乙烯醚硫酸钠 0.6 g(0.6%)、NP-100.1 g(0.1%)、渗透剂 0.1 g(0.1%)进行配置。

表3 重复性实验结果
2.4 清洗实验
清洗实验是生产的塑料清洗剂在实际生产中的应用,以瓶片清洗为依据设置三组清洗实验,工业清洗的流程有清水预洗、加热搅拌、二次加热搅拌、漂洗、二次漂洗、清水漂洗、甩干等步骤,塑料清洗结束活性物含量如表4所示。

表4 清洗实验结果
由表4可得:1)通过正交实验所得塑料清洗剂在清洗前及之后的表面活性较高,因此清洗效果较佳。2)温度升高水分蒸发使得活性物含量升高,使得清洗剂更容易被多次利用。3)通过观察清洗过后的瓶片,看到其表面污垢大部分被去除,瓶片由原来的黑色变为乳白色,处理后的污水变浑浊并产生少量泡沫。
2.5 清洗剂稳定性实验
为保证此种塑料清洗剂能够在较大温度区间保存,进行了稳定性测试,如表5所示。由表5可知,该塑料清洗剂稳定性良好,具有较强的市场前景。

表5 稳定性实验结果
2.6 废水处理实验
通过废水处理实验,探究该塑料清洗剂处理后的废水是否达到可排放标准和环保要求。通过加入聚丙烯酰胺以及硫酸铝作为絮凝剂使废水中的杂质沉淀,过滤观察到处理后的废水呈透明颜色,无异味,无悬浮颗粒,pH呈弱碱性。
3 结论
通过正交实验测试表面活性物含量对瓶片清洗行为的影响,配制得到了环保友好型塑料清洗剂。确定了该塑料清洗剂各组分的最佳配比为(质量分数):酯化反应工艺水(78%)、氢氧化钠(3%)、十二烷基苯磺酸(17%)、硫酸钠(0.2%)、甲醇钠(1%)、脂肪醇聚氧乙烯醚硫酸钠(0.6%)、壬基酚聚氧乙烯醚(0.1%)、渗透剂T(0.1%)。相较于传统塑料清洗剂,该塑料清洗剂具有较强的油污去除能力,且本清洗剂可重复利用,无味,不产生废水,不会造成环境危害。同时,该塑料清洗剂拥有较强的温度适应能力,在低温环境下不凝固,具有良好的流动性,抗硬水能力强,杀菌性能高,耐酸碱,利于工业化生产和大规模运用。
