载紫杉醇的透明质酸-熊果酸胶束冻干制剂的制备及质量评价
2021-06-10于英杰
朱 红,于英杰,董 优,宋 煜
(福建中医药大学药学院,福建 福州350122)
紫杉醇(paclitaxel,PTX)是从中药红豆杉中提取的抗肿瘤活性成分,在多种癌症的治疗上取得了一定的疗效[1-2]。传统紫杉醇注射剂以聚氧乙烯蓖麻油为溶剂,导致药物相关不良反应较多,患者耐受性差[3-4]。白蛋白结合型紫杉醇通过纳米技术,将紫杉醇与人血白蛋白相结合,一定程度上改善了传统紫杉醇制剂的超敏反应,但存在神经毒性、胃肠道反应、骨髓抑制等不良反应,制约着临床应用[5],因此紫杉醇制剂仍需进一步研究开发。本课题组前期以可主动靶向肿瘤细胞膜表面CD44受体的透明质酸[6]为亲水端,以在肿瘤高谷胱甘肽微环境中特异性降解的二硫键为连接臂,以协同抗癌成分熊果酸[7](ursolic acid,UA)为疏水链段,通过酰胺反应合成了还原敏感型透明质酸-熊果酸偶联物(hyaluronic acid-cystamine-ursolic acid,HSU),并以它为载体成功负载PTX制成载药纳米制剂,以期实现PTX-HSU胶束主动靶向于肿瘤部位、肿瘤细胞内定位触发释药、协同增效的目标。
由于此种液态的纳米制剂常存在粒子聚集、粒径变大的现象,不利于储存与运输[8],从而限制其临床应用。采用真空冷冻干燥技术制备冻干制剂是目前解决液态纳米制剂不能长期储存、提高制剂稳定性的最佳方法[9]。本研究拟制备PTX-HSU胶束冻干制剂,对冻干保护剂进行筛选,并考察冻干制剂的理化性质和稳定性。
1 仪器与试药
1.1 仪器 MS105DU十万分之一电子天平(梅特勒-托利多仪器有限公司);ALPHA1-2 LD plus冷冻干燥机(德国Christ公司);JY92-2D超声波细胞破碎仪(宁波新芝生物科技公司);Nicomp380ZLS激光粒度测定仪(美国PSS公司);LC2030高效液相色谱仪(日本岛津公司);H-7650透射电子显微镜(日本Hitachi公司)。
1.2 试药 PTX对照品(中国食品药品检定研究院,批号:100832-201603);PTX原料药(福建南方制药股份有限公司,批号:902-1812401);PTX-HSU胶束课题组自制;甲醇为色谱纯,其他试剂均为市售分析纯。
2 方法
2.1 PTX含量测定
2.1.1 色谱条件 色谱柱:Agilent 5 TC-C18(2)(250mm×4.6mm,5μm),流动相:甲醇-水(75∶25,v/v),柱温:30℃,流速:1mL/min,进样量:20μL,检测波长:227 nm[10]。
2.1.2 标准曲线绘制 精密称取PTX 2.0 mg,甲醇溶解并定容至10mL量瓶中,配制成200μg/mL的储备液。精密量取储备液适量,用甲醇分别稀释配制成系列浓度为0.5、1.0、2.0、5.0、10、20μg/mL的PTX对照品溶液,按“2.1.1”项中色谱条件测定,记录峰面积并绘制标准曲线。
2.2 PTX-HSU胶束冻干制剂制备 在透析法所制备的胶束溶液中加入一定量的冻干保护剂,溶解混合均匀,按2mL/皿分装,-20℃冰箱预冻24 h后,冷冻干燥即得。
2.3 冻干保护剂种类及浓度筛选 分别以冻干制剂的外观、复溶性、再分散性、粒径及复溶后PTX含量变化为考察指标,选择适合于工业化生产且安全性高的葡萄糖、乳糖、甘露醇作为冻干保护剂,并考察其不同用量(0.5%、1%、1.5%、3%、5%)对PTXHSU纳米胶束的保护效果。
2.4 PTX-HSU胶束冻干制剂的质量评价
2.4.1 外观及复溶性 评价PTX-HSU胶束冻干制剂的外观及复溶性。
2.4.2 粒径及zeta电位 PTX-HSU胶束冻干制剂复溶后,取500μL稀释至5mL,利用激光粒度测定仪(DLS)测定粒径和zeta电位。
2.4.3 形态学研究 采用滴染法制备透射电镜试样。吸取微量载药胶束溶液滴于铜网上(碳膜面),使用滤纸从边缘吸去多余溶液,滴加4%的磷钨酸溶液至铜网染色,1 min后使用滤纸从边缘吸去多余溶液,在透射电子显微镜下观察胶束的形貌。
2.5 PTX-HSU胶束冻干制剂稳定性影响因素试验
2.5.1 高温试验 PTX-HSU胶束冻干制剂置于密封洁净容器中,在60℃下放置10 d,在第5、10天取样,观察PTX-HSU胶束冻干制剂的外观,复溶后测定粒径、多分散系数、电位以及PTX含量变化(第0天溶液中PTX含量定为100%)。
2.5.2 高湿试验 PTX-HSU胶束冻干制剂置于密封洁净容器中,放置在25℃,相对湿度为(90±5)%的试验箱中放置10 d,于第5、10天取样,观察外观,复溶后测定粒径、多分散系数、电位以及PTX含量变化(第0天溶液中PTX含量定为100%)。
2.5.3 强光试验 PTX-HSU胶束冻干制剂于照度(4500±500)lx条件下放置10 d,在第5、10天取样,观察PTX-HSU胶束冻干制剂的外观,复溶后测定粒径、多分散系数、电位以及PTX含量变化(第0天溶液中PTX含量定为100%)。
2.6 统计学方法 采用SPSS 21.0软件进行统计学分析。计量数据用(±s)表示,采用One-Way ANOVA进行统计学分析。
3 结果
3.1 PTX含量测定 以PTX质量浓度(C)为横坐标,峰面积(A)为纵坐标,进行线性回归,得线性方程为A=47193 C+13167(r=0.9999)。结果表明,在0.5~20.0μg/mL范围内线性关系良好。
3.2 冻干保护剂种类及浓度筛选 PTX-HSU胶束加不同冻干保护剂的冻干制剂外观见图1。未加冻干保护剂的PTX-HSU胶束冻干制剂表面粗糙,有部分飞絮,质地松散,复溶后PTX含量明显降低;加入乳糖冻干保护剂之后有略微“结块”现象,部分坍塌皱缩,复溶后PTX含量略微降低;加入葡萄糖冻干保护剂之后冻干品色泽均匀,部分呈现结构松散的“皲裂”状,与其他冻干制剂相比复溶性较差;加入甘露醇冻干保护剂之后冻干品表面光洁、饱满,质地细腻,呈“薄饼”状,复溶性较好,PTX含量与未冻干前未出现明显下降。结果表明,加入冻干保护剂后的PTX-HSU胶束冻干制剂PTX含量下降状况得到改善,加入甘露醇后,胶束冻干制剂外观相对较好,且PTX含量下降较少,因此选定甘露醇为PTX-HSU胶束的冻干保护剂。为筛选冻干保护剂最佳浓度,进一步考察了不同浓度甘露醇对冻干粉针质量的影响,见表1。结果表明,甘露醇浓度为1%~5%(w/v)时,冻干制剂外观、复溶性及PTX含量未见明显差异。因此,最终选择以1%(w/v)甘露醇作为冻干保护剂。
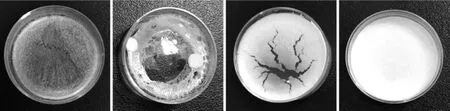
图1 冻干保护剂种类筛选
表1 冻干制剂复溶性及PTX百分含量(n=3,±s)

表1 冻干制剂复溶性及PTX百分含量(n=3,±s)
冻干保护剂无冻干保护剂乳糖葡萄糖复溶性甘露醇加入量(w/v)—5%5%5%3%1.5%1%0.5%易易难 易易易易易冻干前后PTX含量比/%94.48±0.9095.27±2.6396.31±2.3398.36±2.1299.39±5.3699.28±2.9099.63±2.2494.26±5.18
3.3 PTX-HSU胶束冻干制剂质量评价
3.3.1 外观及复溶性 PTX-HSU胶束冻干制剂表面饱满光洁,色泽均匀,质地细腻,复溶后稍加振摇即得淡蓝色乳光纳米胶束溶液。
3.3.2 粒径及zeta电位 PTX-HSU胶束冻干制剂复溶后的平均粒径为(152.8±8.5)nm,多分散系数为(0.105±0.010),zeta电位为(-20.98±3.44)mV(n=3)。纳米胶束尺寸较小,粒径分布均匀,见图2。

图2 PTX-HSU粒径分布
3.3.3 形态学研究 PTX-HSU胶束的透射电镜结果如图3所示,PTX-HSU胶束呈类球状,粒子在130 nm左右,分布均匀。PTX-HSU胶束通过透射电镜测定粒子尺寸相较激光粒度测定仪的粒径变小,推测可能是因为在透射电镜制样过程中挥干了水分,胶束的亲水性外壳发生皱缩,使得粒子变小。
3.4 PTX-HSU纳米胶束冻干制剂稳定性的影响因素试验 高温、高湿、强光实验结果见表2~4。结果表明,在高温、高湿、强光条件下,PTX-HSU胶束冻干制剂的外观均无明显变化。高温条件下载药纳米胶束PTX含量有所降低,粒径增大,复溶变得困难;高湿度使冻干制剂的复溶性变差;载药胶束冻干制剂对光不敏感,各项参数稳定;因此,该冻干制剂应避免在高温和高湿条件下储存使用,宜在低温干燥条件下保存。

图3 PTX-HSU透射电镜图(×100000)
4 讨论
液态的纳米胶束在长期储存中可能出现粒子聚集、粒径变大的现象,通过真空冷冻干燥技术制备胶束冻干制剂可以起到长期保存的作用。然而在冷冻干燥过程中存在药物随水分飞散造成成品含量偏低,以及冻干制剂呈现结构松散易吸潮的现象等,因此在冻干物固体含量小于5%时应加入冻干保护剂,保持其理化性质稳定。本研究对乳糖、葡糖糖、甘露醇3种冻干保护剂的冻干效果进行考察,发现加入冻干保护剂后的PTX-HSU胶束冻干制剂PTX含量下降状况得到改善,推测可能是由于加入冻干保护剂所形成的空间构架保护了载PTX胶束,从而减少了PTX从胶束中渗漏的现象。其中,甘露醇作为冻干保护剂时冻干效果最佳,且在浓度1%~5%冻干效果无差异,最后选择了1%甘露醇作为PTX-HSU胶束最佳冻干保护剂。
表2 冻干制剂高温影响因素实验结果(n=3,±s)

表2 冻干制剂高温影响因素实验结果(n=3,±s)
时间/d 复溶性0510物理性状白色饼状白色饼状白色饼状PTX含量比/%100.00±0.0098.77±1.0590.65±1.61粒径/nm 147.8±0.9185.2±1.8497.7±12.8多分散系数0.117±0.0040.122±0.0150.384±0.049 zeta/mV-15.48±3.29-14.45±3.02-33.10±1.89易难难
表3 冻干制剂高湿影响因素实验结果(n=3,±s)

表3 冻干制剂高湿影响因素实验结果(n=3,±s)
时间/d 复溶性0510物理性状白色饼状白色饼状白色饼状PTX含量比/%100.00±0.0096.94±9.8196.60±2.50粒径/nm 147.8±0.9167.2±0.4165.0±1.5多分散系数0.117±0.0040.122±0.0090.117±0.008 zeta/mV-15.48±3.29-13.30±6.74-19.80±1.18易易难
表4 冻干制剂强光影响因素实验结果(n=3,±s)

表4 冻干制剂强光影响因素实验结果(n=3,±s)
时间/d 复溶性0510物理性状白色饼状白色饼状白色饼状PTX含量比/%100.00±0.00101.03±2.5899.05±2.96粒径/nm 147.8±0.9161.5±1.9151.8±0.9多分散系数0.117±0.0040.110±0.0160.097±0.017 zeta/mV-15.48±3.29-9.74±5.46-20.55±0.78易易易
本研究制备的PTX-HSU胶束冻干制剂复溶后的粒径在152.8 nm左右,zeta电位稳定在-20 mV左右,zeta电位绝对值较大。其可能原因是HA结构中的-COOH在水中解离为带负电荷-COO-,使粒子间存在较大的斥力,有利于胶束制剂的物理稳定。高温条件下纳米胶束冻干制剂PTX含量有所降低,粒径增大,复溶变得困难,推测可能是纳米胶束结构遭到部分破坏的原因。因此胶束冻干制剂需储存在4℃干燥条件下。
本研究制备的PTX-HSU胶束制剂具有较好的理化性质,为继续开发PTX胶束奠定了良好基础,下一步我们将对胶束制剂的体内外药效学状况进行评价。
