准分子激光减容颈动脉粥样斑块可行性研究的体外实验:形态学及产物分析
2021-06-07谭晋韵史伟浩
杨 凯 谭晋韵 邓 颖 史伟浩 余 波,△
(1复旦大学附属浦东医院(上海市浦东医院)血管外科 上海 201399;2上海市血管病变调控与重塑重点实验室 上海 201399;3复旦大学附属华山医院血管外科 上海 200040)
颈动脉狭窄由颈动脉内膜形成粥样硬化斑块导致,是缺血性卒中的首要病因。临床上解决颈动脉硬化狭窄的主要方式有颈动脉内膜剥脱术(carotid endarterectomy,CEA)与颈动脉造影及支架植入术(carotid angiography and stenting,CAS)两种。CEA能够有效去除颈动脉粥样斑块,但由于是开放手术,创伤相对较大且伴有神经损伤风险;而微创的CAS并不适合合并主动脉弓部病变的患者,且具有较高的再狭窄发生率[1-3]。目前临床使用的准分子激光为氯化氙(XeCl)脉冲激光,波长为308 nm,主要应用于下肢动脉及冠脉发生的慢性完全闭塞病变、球囊无法通过及再开通失败的病变、支架内再狭窄等,国内外并无准分子激光应用于解除颈动脉硬化狭窄的临床报道,相关体外及动物实验开展极少且并未关注减容效率及远端颈动脉供应器官安全性问题[4-5]。本实验拟在体外开展准分子激光应用于颈动脉硬化狭窄的前期研究,探究准分子激光减容颈动脉斑块的可行性,着重分析减容效率的同时对产物进行分析。
材料和方法
体外颈动脉粥样斑块固定装置取一长约30 cm、内径与离体颈动脉粥样斑块相适应的透明硅胶管(上海亭芬生物科技有限公司)作为主管道,并在主管道上做一长约4 cm的“H”形切口。取两段长约1 cm的透明硅胶管,经“H”形切口置入于前后两端,用于实验过程中保持颈动脉粥样斑块不发生移动。另取一长约5 cm的透明硅胶管,用于封闭主管道的“H”形切口。
颈动脉CTA图像、颈动脉粥样斑块样品获取与处理对患有颈动脉硬化狭窄患者且符合外科干预指征的患者行颈动脉内膜剥除术,使用“en bloc”技术获得完整颈动脉粥样斑块6例,用生理盐水轻柔地洗去血液。将清洗后的颈动脉粥样斑块泡入生理盐水中,4℃冰盒转运,用于后续实验。获取实验所用颈动脉斑块对应的颈动脉CTA图像资料,通过Mimics Medical 21.0软件获取动脉管腔的面积、最大卡钳直径和最小卡钳直径数据。
实验与数据处理过程激光减容实验在体外进行。事先预热准分子激光设备(Spectranetics CVX-300,荷兰皇家飞利浦公司),设置参数为45 mJ/mm²,25 Hz。将颈动脉粥样斑块置入固定装置中,将0.018″导丝通过斑块,使用6F Turbo-Elite激光导管(型号420-006,导管直径2.0 mm,荷兰皇家飞利浦公司)推进3次,或使用8F Turbo-Elite激光导管(型号425-011,导管直径2.5 mm,荷兰皇家飞利浦公司)推进5次。激光导管推进速度小于1 mm/s,同时采用生理盐水滴注。在完成减容操作后往斑块固定装置中输注生理盐水并收集,后续经涂片实现对收集到的产物进行苏木精-伊红(HE)染色。在400×倍数下随机挑选5个视野拍摄HE染色结果图,并通过ImageJ(Version:1.52t)对图片内的碎屑进行计数,并收集碎屑的面积、最大卡钳直径和最小卡钳直径数据。在减容操作后,切取1 mm宽颈动脉粥样斑块组织,用2.5%戊二醛溶液固定用于后续的扫描电镜实验(场发射扫描电镜Quanta 250FEG,上海六欣科学仪器有限公司;电压20.00 kV),观察减容后颈动脉粥样斑块管腔面的微观结构。减容后剩余颈动脉粥样斑块组织用4%多聚甲醛固定,在完成Micro CT(SkyScan1176,布鲁克(北京)科技有限公司)拍摄后进行石蜡包埋,随后进行连续切片(切片厚度为5μm)。一张玻片用于贴附3张切片。在包含颈动脉粥样斑块最狭窄部位的1 cm范围内的切片中,随机选择跨越最狭窄部位上下共20张玻片,用于完成HE染色和Masson染色。Micro CT图像用于获取减容后斑块管腔面积、最大卡钳直径和最小卡钳直径数据。
颈动脉粥样斑块病理分型对于颈动脉粥样斑块的病理分型,一般采用美国心脏协会制定的标准。但本研究存在确定颈动脉粥样斑块病理类型与对斑块进行减容之间的矛盾,进行美国心脏协会病理分型后的颈动脉粥样斑块蜡块及切片无法满足减容实验的需求。所有颈动脉硬化狭窄患者在颈动脉内膜剥脱术术前均未开展颈动脉MRI检查。故本研究仅能通过减容后的颈动脉粥样斑块的HE染色结果对实验中使用的斑块样品进行简易分型。分型及对应判断依据如下:脂质斑块:总脂质核心与斑块的面积之比≥0.4;或脂质核心距离斑块管腔<200μm,则放宽总面积标准至30%;钙化斑块:总钙化与斑块的面积之比≥0.4;或钙化结节距离斑块管腔<200μm,则放宽总面积标准至30%;纤维斑块:上述两类斑块排除以后的归入纤维斑块这一类型。
统计学分析使用SPSS 26.0软件进行统计分析。采用Kolmogorov-Smirnov与Shapiro-Wilk正态性检验对数据是否符合正态分布进行检验。符合正态分布的计量资料以均数或±s表示,不符合正态分布的资料采用中位数及四分位间距表示。符合正态分布的资料采用两独立样本t检验进行比较,不符合正态分布的资料采用Mann-Whitney U检验进行比较。P<0.05为差异有统计学意义。
结 果
准分子激光减容颈动脉粥样斑块后管腔面积变化使用6F激光导管减容颈动脉粥样斑块后,斑 块 管 腔 面 积 显 著 增 加[(0.97±0.39) μm2vs.(5.62±2.05)μm2,P<0.001,图1H]。斑块切片(图1A、B)显示经6F激光导管减容后,部分斑块成分被清除,同时发现减容后的斑块管腔横截面为不规则形,呈现楔形深入斑块内部。在换用更大直径的8F导管并增加推进次数至5次后,斑块管腔面积同样显著增加[(7.29±6.81) μm2vs.(13.67±6.35)μm2,P=0.004,图1G]。8F导管减容后斑块管腔横截面较6F导管减容后的更加规则(图1C、D)。实验中我们取同一颈动脉粥样斑块,根据术前临床影像资料在最狭窄部位一切为二。针对其中一段使用8F激光导管进行减容,其后进行石蜡包埋并切片染色,结果如图1E、F显示,可见准分子激光去除了较多的斑块成分。此外,我们观察到减容区域的边缘颜色较周边组织深,但未发现热损伤后遗留的碳化现象。对管腔面积的最大卡钳直径与最小卡钳直径进行分析,结果与减容后管腔面积变化相似,经激光减容后,上述两项直径均显著增加(表1)。

表1 6F和8F激光导管各自在减容颈动脉粥样斑块后管腔的前后对比Tab 1 Comparison of lumen before and after debulking of carotid atherosclerotic plaque with 6F and 8F laser catheters
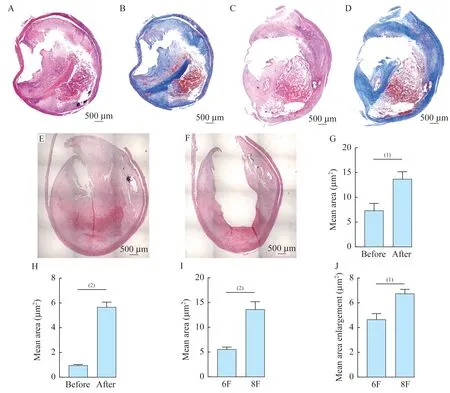
图1 6F与8F激光导管减容颈动脉粥样斑块的管腔比较Fig 1 Comparison of lumen after debulking of carotid atherosclerotic plaque by 6F and 8F laser catheters
准分子激光减容颈动脉斑块的碎屑分析对所有收集到的生理盐水进行涂片、HE染色,镜下均可检出碎屑(图2A、B)。经8F激光导管减容后,比6F激光导管产生更多的碎屑(6F:3044,8F:4583)。此外,我们收集并整理了碎屑的面积、最大卡钳直径及最小卡钳直径数据(表2)。两种管径的激光导管减容颈动脉粥样斑块所产生碎屑的面积都集中在0~10μm2,占比均超过95%(图2D、G)。对最大卡钳直径和最小卡钳直径进行分析,呈现出相似的情况(图2E、F、H、I)。
准分子激光减容颈动脉斑块后管腔面微观结构变化颈动脉粥样斑块经准分子激光减容后,对斑块管腔面进行扫描电镜拍摄,准分子激光减容区域中正常血管内膜消失,同时可见内膜下条索状纤维暴露(图2C)。
实验中使用的颈动脉粥样斑块病理类型6F激光导管减容的颈动脉粥样斑块病理类型包括脂质斑块2例、纤维斑块1例。8F激光导管减容的颈动脉粥样斑块病理类型为脂质斑块3例。两种尺寸的激光导管均未减容钙化斑块这一类型。
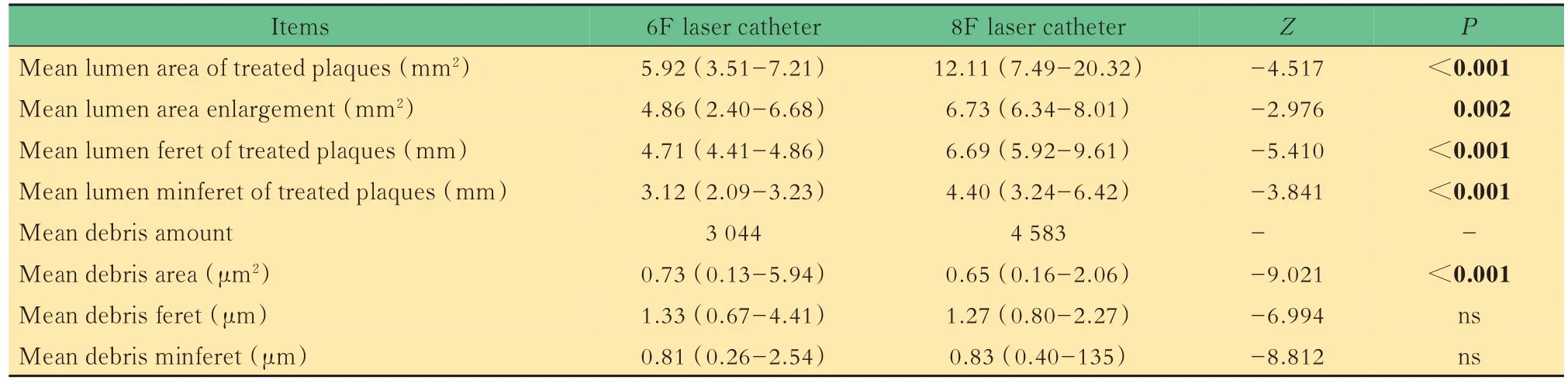
表2 6F和8F激光导管在减容颈动脉粥样斑块后管腔和碎屑的比较Tab 2 Comparison of lumen and debris between 6F and 8F laser cathetersafter debulking of carotid atherosclerotic plaque
Data is presented in median(interquartile interval)due to non-normal distribution.Feret:The maximum caliper diameter;Minferet:The minimum caliper diameter.ns:Not significant.

图2 准分子激光减容颈动脉粥样斑块的碎屑产物及斑块腔面微观形态Fig 2 The debirsproducts of carotid atherosclerotic plaque and the micromorphology of plaque lumen after excimer laser debulking
讨 论
临床上已将准分子激光应用于冠脉及下肢动脉疾病中以解除相应动脉狭窄。准分子激光具有应用于颈动脉硬化狭窄性疾病的潜力,但目前并未在临床上有所应用。在准分子激光应用于颈动脉粥样斑块减容前,需要在临床前研究中对其可行性、减容效率以及安全性进行细致评估。本研究拟在体外实验中探究准分子激光减容颈动脉粥样斑块的可行性及其效率。
准分子激光是一种脉冲式、紫外气态激光。准分子激光减容粥样硬化斑块的机制包括光化学效应、光热效应和光机械效应[6]。准分子激光通过打断分子间的碳键从而瓦解、汽化斑块中的有机成分;光热作用与光机械作用的叠加,使得减容过程中产生的气泡膨胀破裂,碎屑飞射,最终实现斑块减容。理论上准分子激光产生的碎屑尺寸小于25μm,也有报道在准分子激光消融组织遗留深坑中观察到1~10μm的碎屑[7]。通过对本实验中捕获的碎屑的直径进行定量发现:准分子激光在体外减容颈动脉粥样斑块所产生的碎屑中,接近100%的最大卡钳直径为0~20μm,其中约95%的碎屑集中在0~5μm。有研究提示直径为8~20μm的碎屑在造成颅脑微血管栓塞后可被转移出血管腔从而实现血管再通[8]。这些碎屑造成的临床结果不仅与直径相关,还与同时向远端脑血管中输注的数量相关,需要谨慎推导,因此还须开展在体的动物实验以明确其影响。我们还发现6F激光导管在减容颈动脉粥样斑块后产生的碎屑面积显著大于8F激光导管所产生的碎屑面积。考虑原因可能为:8F激光导管拥有更大的尺寸,能够容纳更多的光纤,即在单位面积内能够接收到更高的能量;实验过程中8F激光导管推进的次数多于6F激光导管。以上两点使得8F激光导管在减容颈动脉粥样斑块过程中能够对颈动脉粥样斑块成分进行更充分的消融。与Ar+、CO2、YAG等热激光采用热效应发挥作用不同,准分子激光被认为是“冷激光”。由于准分子激光是脉冲式发射,同时两次激光发射间隔远大于激光发射持续时间,加之生理盐水的输注技术,使得准分子激光减容区域能充分降温散热并减少损伤[9-11]。因此,准分子激光被认为无热损伤效应。既往通过准分子激光消蚀人离体主动脉及其斑块,发现汽化主动脉及斑块组织后遗留的汽化坑无热损伤迹象。我们观察到减容工作边缘组织着色加深,未观察到斑块组织碳化的迹象,与既往研究结果[12-14]一致。为明确准分子激光减容颈动脉粥样斑块后管腔的微观变化,我们利用扫描电镜对减容后斑块的管腔进行观察,发现减容区域中血管内膜结构消失,同时内膜下的纤维成分暴露。
准分子激光减容通过去除颈动脉粥样斑块的组成,实现了管腔面积的显著提升。这通过减容前后管腔面积、最大卡钳直径及最小卡钳直径的比较得以证实。既往研究中对主动脉或二尖瓣样品大多沿纵轴切开或切分为小块,随后使用激光导管垂直于腔面/内膜面进行消融;或者将离体冠脉切分成约3 mm的短段后进行消融[15-16]。而本实验中采用整体的颈动脉粥样斑块,并将激光导管置于腔内沿着纵轴方向进行减容,更符合临床实际操作。此外,本实验中评估减容效率所采用的定量方法有别于既往研究。既往研究中采用定量消蚀坑深度或减容前后样品质量变化作为评估效率的指标[16-17],我们采用减容前后管腔面积的变化为主要指标,同时还测量了管腔的最大及最小卡钳直径以辅助表征管腔的改变。残余狭窄是介入治疗术中一项重要的评价指标,我们对于管腔面积的定量更接近于临床实践。既往大多数的实验并未对消蚀坑深度定量,Grundfest等[12]的研究给出了消蚀坑深度与激光发射频率之间的线性数据。为实现不同定量数据之间的对比,我们对其数据进行了换算。25 Hz所对应的消蚀坑深度约为0.4 mm。理论上准分子激光的作用直径比导管直径大1/3,本实验中6F激光导管(直径2.0 mm)推进3次,故换算可得Grundfest等的研究中消蚀坑的面积约为3.2 mm2,略小于本实验中6F激光导管对应的平均管腔增加面积4.86 mm2。在实验中,我们发现6F激光导管虽然显著增加了斑块管腔面积,但是所增加的面积形态不规则。流体力学领域已经表明,管腔的局部狭窄可造成狭窄处血液流速增加、壁面剪切应力增加,随着血小板、血管平滑肌细胞、内皮细胞以及巨噬细胞等对刺激及生物信号做出反应,改变表型、状态与功能,可进一步加重狭窄,导致管腔闭塞或诱发远端靶器官的不良事件[18-20]。解除局部狭窄可改善该狭窄处的血流动力学状态[21]。6F激光导管减容颈动脉粥样斑块后可见楔形面积增加区域。这一楔形狭窄区域势必会增加局部血流流变不稳定性。为均匀地增加管腔面积,同时实现较为理想的、稳定的血流流变状态,我们换用了管径更大的8F导管,同时增加了导管推进的次数。与图1A相比,图1C中显示减容后的管腔更为规则。此外,换用了更大尺寸的激光导管在带来更规则管腔的同时更显著增加了管腔面积[(4.65±2.24)μm2vs.(6.71±1.58)μm2,P=0.0018,图1J]。显然,在斑块或血管尺寸允许的情况下,8F的激光导管能够获得更优的结果。6F与8F激光导管之间依次应用是否能够带来相加或者相乘的效应,或者在带来效率提升的同时是否伴随着不良事件(如穿孔、夹层)的发生尚未可知,需要后续开展进一步实验加以探讨。
基于本研究的实验结果以及国内外最新的研究进展,我们提出一个设想,即在特定的脑保护装置下(如TCAR技术将血流通过过滤后回输至静脉系统[22]),通过准分子激光等新型技术手段对颈动脉粥样斑块进行有效减容,配合可降解血管支架的植入,可实现在血管腔内完全模拟CEA手术的效果,达到去除颈动脉粥样斑块、重建颈动脉的目的,实现EndoCEA(全腔内CEA)技术。
本研究的局限性在于使用的颈动脉粥样斑块样品标本钙化程度均较轻,根据激光器械产商的建议选择了在下肢血管中的推荐参数。既往有研究提示,准分子激光需要在较高的能量下才能实现对于钙化结节的汽化[23]。此外,本研究的颈动脉粥样斑块标本的病理类型尚不全面、样本量相对较少。通过颈动脉内膜剥脱术获得不同病理类型的颈动脉粥样斑块非人为可控,加之减容完成后的“事后分型”,要实现覆盖所有病理类型,则需要扩大所使用的斑块数量,这一过程中难免造成个别类型斑块的“过量”,存在一定的“样本浪费”。考虑到样本的珍贵性及扩大样本量这一措施的效益不可控性,我们并未采取扩大样本量这一方式。未来的研究中需要实现在减容前对斑块进行分型并纳入钙化性斑块,同时需要寻找到一个适合消除颈动脉粥样斑块内钙化性结节而不影响准分子激光安全使用的能量。此外,本研究使用的颈动脉粥样斑块处于离体状态,已失去生物活性,无法观察减容后斑块表面是否形成血栓及斑块内细胞对应的反应,故今后开展在体动物实验非常必要。
综上,准分子激光能够显著去除颈动脉粥样斑块组织,获得斑块管腔面积的增长。本体外实验表明准分子激光具有临床应用于解除颈动脉硬化狭窄的可行性,且减容效率较高。通过Micro CT以及临床CTA影像实现了斑块管腔面积比较,这一减容效率的刻画更贴合临床实践。对碎屑产物的定量描述为下一阶段的安全性研究提供了数据支持。在此基础上结合国内外进展,我们创造性地提出了“Endo-CEA”这一新技术设想。未来寻找到合适的激光工作参数可以拓宽准分子激光能减容的颈动脉粥样斑块病理类型,更为重要的是开展临床实践之前需要进行相关在体动物实验,以明确碎屑可产生的影响以及斑块及血液成分对准分子激光减容的反应。
作者贡献声明杨凯 数据采集,统计分析,论文撰写与修订。谭晋韵 数据采集,统计分析,论文构思与修订。邓颖 数据采集,统计分析。史伟浩,余波 论文构思与修订。
利益冲突声明所有作者均声明不存在利益冲突。
