羟基磷灰石改性毛竹生物炭对铅污染土壤的钝化修复性能
2021-06-05闵彬彬冯国杰朱宗强
梁 宁, 闵彬彬, 冯国杰, 朱宗强
(1.桂林理工大学南宁分校, 南宁 530001; 2.桂林理工大学 a.广西环境污染控制理论与技术重点实验室; b.广西环境污染控制理论与技术重点实验室科教结合科技创新基地, 广西 桂林 541006; 3.北京高能时代环境技术股份有限公司, 北京 100095)
0 引 言
土壤污染是我国当前面临的主要环境问题之一, 而广西地区受矿产资源开发影响而造成的铅(Pb)等重金属污染尤为突出[1]。铅在土壤中分布广泛、生物毒性累积能力强。土壤Pb污染可通过手口活动直接暴露、呼吸道吸入及食物链传递等途径进入人体, 引发心血管系统、生殖系统、胃肠道系统、中枢神经系统、免疫系统等疾病, 严重影响人体的健康[2-6]。
当前, 国内外铅污染土壤修复方法主要有物理修复、化学修复、生物修复等[6-10]。而原位钝化修复成本较低, 对土壤的破坏力度小, 钝化修复剂的复合材料来源广泛、价格低廉。毛竹炭是具有天然分级多孔结构的生物炭, 环境友好, 是良好的土壤钝化修复剂载体。本研究以广西盛产的毛竹为模板原材料, 对其进行抽提、前驱液浸泡、焙烧等改性处理, 制备得到土壤钝化修复材料HAP@B, 以Pb(Ⅱ)外源污染型红壤为研究对象, 开展HAP@B对重金属污染土壤的钝化修复研究, 分析钝化修复效果的影响过程, 并探究其钝化机制。
1 材料与方法
1.1 实验材料
主要化学试剂: 氨水、氢氧化钙、磷酸、硝酸铅(西陇化工股份有限公司, 均为分析纯)、超纯水。主要原材料为广西毛竹。
1.2 土壤的采集与分析
实验用土取自广西当地红壤小山坡。土壤样品用棋盘法进行取样, 控制取样深度0 ~ 20 cm,取样点12个, 将各取样点的土样用四分法混合制成一个土壤样品。将采集回来的土样去除树枝、树根、碎石等杂物, 风干后过孔径2 mm尼龙筛, 装入封口袋供试验分析。
1.3 实验方法
1.3.1 HAP@B制备 以广西毛竹为原材料, 进行抽提、前驱液浸泡、焙烧等改性技术, 制备得到土壤修复材料HAP@B。具体制备方法: ①毛竹模板的预处理: 将毛竹杆材干燥后切成30 mm×10 mm×3 mm尺寸的块体, 在95~105 ℃条件下, 于稀氨水溶液(6%, 体积分数)中浸煮6~8 h后取出, 在80 ℃烘箱中干燥24 h; ②改性溶液的配制: 用0.02 mol/L的十二烷基硫酸钠溶液代替纯水, 配制获得0.1 mol/L的氢氧化钙溶液, 标记为SDS-Ca溶液; 用0.02 mol/L的十二烷基硫酸钠溶液代替纯水, 配制获得0.1 mol/L的磷酸溶液, 并用氨水调节pH值为10~11, 标记为SDS-P溶液; ③材料的浸渍程序: 将步骤①获得的毛竹块体在SDS-Ca溶液中45 ℃水浴下浸没48 h, 取出放入50 ℃烘箱中干燥2 h, 置于SDS-P溶液中45 ℃水浴条件下2 h, 依次在上述两种溶液中循环浸泡2 h, 共4次, 材料每次浸渍后用超纯水冲洗约20 s, 并置于50 ℃烘箱干燥2 h; ④材料的焙烧: 将步骤③获得的材料在马弗炉中于600 ℃焙烧4 h, 取出研磨过筛得到羟基磷灰石改性毛竹结构复合重金属吸附剂HAP@B。
1.3.2 钝化实验 将无污染的背景土壤, 按照《土壤环境质量标准》(GB 115618—2018)中风险管制值的1和2.5倍加入重金属铅外源污染物, 保持土壤30%的含水量, 人工静态培养模拟污染土壤20 d, 自然风干后过20目(0.840 mm)筛备用, 对土壤理化性质进行测定, 得到低浓度污染和高浓度污染(500、1 250 mg/kg)两种土壤供后续钝化实验、土壤重金属分析以及土壤表征分析。钝化实验的效果用重金属稳定率η表示:

式中:C0为钝化前目标物的CaCl2提取浓度(mg/L);C为钝化后目标物的CaCl2提取浓度(mg/L)。
2 结果与讨论
2.1 投加比例对土壤钝化的影响
分别称取20 g的污染土壤放入一系列100 mL烧杯中, 按照比值(钝化修复剂质量/土壤质量)为0、0.1%、0.5%、1%、2%、5%和10%加入过100目(0.150 mm)筛的HAP@B, 加入6 mL超纯水(保持含水率为30%左右), 搅拌均匀, 封上保鲜膜, 放入恒温恒湿培养箱中静态培养15 d后(温度25 ℃、湿度80%), 风干磨碎, 应用CaCl2和TCLP提取剂提取钝化修复后土壤的重金属, 分析钝化修复剂投加比例对钝化修复效果的影响。
不同投加比例对HAP@B钝化修复铅污染土壤的影响如图1所示。可以看出, 随着钝化修复剂投加比例的增加(0~10%), 重金属铅的稳定率迅速增加, 投加比例为5%时, 稳定率基本趋近100%, 500和1 250 mg/kg的铅污染土壤的钝化稳定率分别从28.65%和15.25%(投加比例0.1%, 下同)增加到99.95%和99.51%; 对应的TCLP浸出Pb浓度曲线呈下降趋势, 两种污染土壤的提取浓度分别从1.228和15.61 mg/L下降到0.048和1.725 mg/L。因为初期钝化修复剂投加比例的增加, 导致土壤中固定铅的活性点位快速增加, 土壤中铅被快速固化稳定, 但是随着投加比例的持续增加, 土壤中固定铅的活性点位过量, 钝化修复剂表面活性位点利用率下降, 导致曲线呈现出变缓趋势。综合考虑, 为了最大限度利用钝化修复剂, 选择5%的投加比例进行其他因素相关实验。

图1 投加比例对HAP@B钝化修复铅污染土壤的影响Fig.1 Effects of dosage ratios on lead in soil passivated by HAP@B
2.2 钝化修复时间对土壤钝化的影响
分别称取20 g污染土壤放入一系列100 mL烧杯中, 添加1 g过100目筛的HAP@B(投加比例为5%), 加入6 mL超纯水, 搅拌均匀, 封上保鲜膜, 放入恒温恒湿培养箱中分别培养1、2、3、5、10、15、20、30、40、50和60 d, 按时取出土样风干磨碎, 应用CaCl2和TCLP提取剂提取钝化后土壤的重金属, 分析时间对钝化修复效果的影响。
由图2可以看出, 500和1 250 mg/kg两种浓度的铅污染土壤稳定率曲线均随着钝化时间增长而上升, 直至趋近100%, 且钝化10 d基本都达到稳定平衡, 说明材料对铅污染土壤具有很好的钝化修复效果。钝化1 d时,两种浓度铅污染土壤的稳定率分别达到84.58%和72.74%, 这是由于在钝化前期钝化修复剂表面的可利用吸附点位较多, 土壤充分搅拌保持一定的含水率, 使得土壤中大量的铅被快速吸附、固定, 但是钝化修复剂表面吸附点位有限, 随着反应的继续, 钝化修复剂表面的活性点位逐渐饱和, 而土壤中铅含量降低, 浓度梯度降低, 钝化速率受影响, 且在低重金属浓度的土壤混合体系中, 铅寻找钝化修复剂内部剩余活性位点难度上升[11]。因此, 考虑到时间成本, 探究其他因素影响的实验, 钝化时间选择15 d。
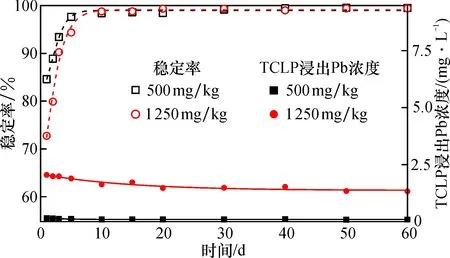
图2 钝化修复时间对HAP@B钝化修复铅污染土壤的影响Fig.2 Effect of passivation time on lead in soil passivated by HAP@B
2.3 钝化修复剂粒径对土壤钝化的影响
分别称取20g污染土壤放入一系列100 mL烧杯中, 加入不同粒径(块状、20~40目(0.420~0.840 mm)、40~60目(0.250~0.420 mm)、60~80目(0.178~0.250 mm)、80~100目(0.150~0.178 mm)、>100目(<0.150 mm))的HAP@B各1 g, 期间保持含水率30%, 保鲜膜封口后放入恒温恒湿培养箱中静态培养15 d, 风干磨碎, 应用CaCl2和TCLP提取剂提取钝化后土壤的重金属, 分析钝化修复剂粒径对钝化修复效果的影响。
从图3可以看出钝化修复剂粒径对钝化修复效果存在一定的影响, 具体表现为在钝化修复剂粒径为块状时两种浓度土壤稳定率分别为73.66%和67.29%, 明显低于其他粒径时的稳定率, TCLP浸出提取浓度分别为0.457和7.985 mg/L, 远高于其他粒径时的浓度。这是因为材料粒径太大, 呈小颗粒状甚至块状时, 不利于钝化修复剂与土壤充分接触, 钝化修复剂内部的孔隙结构和吸附位点利用率低, 不利于土壤中铅被吸附固定, 从而使得钝化修复效果不理想。但是当材料粒径在一定范围内(0.150~0.840 mm), 基本不影响钝化修复效果。钝化修复剂的粒径不再是影响钝化修复效果的主导因素。

图3 粒径对HAP@B钝化修复铅污染土壤的影响Fig.3 Effect of particle size on lead in soil passivated by HAP@B
2.4 土壤含水率对土壤钝化的影响
分别在一系列100 mL烧杯中放置20 g污染土壤, 添加1 g过100目筛的HAP@B(投加比例为5%), 然后分别按土壤含水率15%、20%、25%、30%、40%、50%和60%加入超纯水, 搅拌均匀, 封上保鲜膜, 放入恒温恒湿培养箱中培养15 d, 按时取出土样风干磨碎, 应用CaCl2和TCLP提取剂提取钝化后土壤的重金属, 分析土壤含水率对钝化修复效果的影响。
从图4可看出, 土壤含水率对HAP@B钝化铅污染土壤存在一定影响, 当含水率在15%~25%, 随着土壤含水率的增加, 两种浓度的铅污染土壤的稳定率也不断上升; 当土壤含水率增加到35%的时候, 其稳定率分别为99.37%和99.71%; 土壤含水率在15%时, 高浓度污染土壤组TCLP浸出Pb浓度高达5.849 mg/L, 当含水率提高到30%, TCLP浸出Pb浓度仅为1.748 mg/L, 下降了70.11%; 而当含水率继续增加,TCLP浸出Pb浓度几乎没有变化。因为随着含水率的增加, 溶出量增加, 稳定率也呈现上升趋势, 当达到一定值时, 溶出完全, 稳定率不再上升。

图4 土壤含水率对HAP@B钝化修复铅污染土壤的影响Fig.4 Effect of soil moisture content on HAP@B passivation repair of soil lead
2.5 土壤初始pH值对土壤钝化的影响
分别称取20 g污染土壤放入一系列100 mL烧杯中, 加入1 g过100目筛的HAP@B, 6 mL超纯水, 搅拌均匀, 保鲜膜密封后放入恒温恒湿培养箱中静态培养15 d后, 风干磨碎, 应用CaCl2和TCLP提取剂提取钝化修复后土壤的重金属, 分析土壤的pH值对钝化修复效果的影响。
由图5可知, 两种浓度土壤的稳定率曲线趋势基本类似, 稳定率先随着pH值增加而呈指数增加至接近100%, 然后趋于平衡。对于1 250 mg/kg浓度的铅污染土壤, 当pH<2.5时, HAP@B对Pb(Ⅱ)的稳定率为负值, 其中pH为1.42时, 稳定率仅为-136.12%; 而500 mg/kg浓度的铅污染土壤在pH<3.25时, 稳定率为负值, 其中pH值为2.79时稳定率仅为-120.94%。土壤的pH值小于一定数值时, 材料对铅的修复稳定率为负数, 说明材料此时的修复效果失活, 且出现溶出现象。两种浓度的TCLP浸出Pb浓度曲线存在一些区别, 500 mg/kg低浓度的铅污染土壤的TCLP浸出浓度水平处于较低值(0.107~0.774 mg/L); 1 250 mg/kg污染浓度的土壤的TCLP浸出浓度首先随着pH增大快速下降, 然后下降程度变缓, 直至0.045 mg/L。因此, pH值主导材料钝化铅污染土壤的修复效果[12], 提高土壤pH值对HAP@B钝化铅污染土壤是有利的, 当pH>4时, HAP@B对Pb(Ⅱ)的稳定率为99%以上。土壤pH值不仅影响HAP@B的带电性质, 还直接控制着材料负载的HAP的溶解程度、土壤中含铅沉淀物质的溶解以及重金属铅的离子形态[13]。

图5 土壤初始pH值对HAP@B钝化修复铅污染土壤的影响Fig.5 Effect of initial soil pH value on HAP@B passivation repair of soil lead
3 钝化修复机制分析
3.1 重金属形态分析
采用改进BCR连续浸提法[14]测定不同投加比例的HAP@B处理铅污染土壤的重金属形态分布。从图6可知, 铅污染土壤的赋存形态主要是: 弱酸提取态、可还原态、可氧化态、残渣态, 4种形态具体占比分别为51.65%、43.51%、3.04%和1.80%。供试铅污染土壤为广西红壤, 呈酸性(pH=4.69), 人工模拟污染后, pH值进一步下降至3.87, 在此酸性环境中, 土壤中的铅大部分处于迁移性大、可溶性强的形态, 从而使得铅的可还原态和弱酸可溶态占比较大。但随着HAP@B投加比例的增加, 弱酸提取态占比明显下降, 残渣态和可还原态占比显著增加。最为活泼的弱酸提取态从51.65%下降到21.21%, 较为稳定的可还原态从43.51%上升到66.58%, 最为稳定的残渣态则从1.80%增加到8.99%。这是因为材料中的P能与土壤中活泼形态的铅反应形成沉淀, 将其转化成稳定形态。付煜恒等[15]研究发现, 施加含磷材料可引起土壤中高活性的交换态、碳酸盐结合态、铁锰氧化态、有机结合态向稳定的残渣态转化, 残渣态Pb的形成源于形成的磷氯铅矿。所以推测本实验残渣态的占比增加则可能是与材料中的HAP形成极为稳定的Pb10(PO4)6(X)2(X为Cl、F、OH等)。由此可以判定, HAP@B钝化铅污染土壤的主要机理是降低弱酸提取态占比, 提高可还原态和残渣态的占比。重金属的赋存形态和重金属的生物有效性、迁移性息息相关, 材料影响重金属在土壤的赋存形态, 达到降低生物有效性的修复效果[14, 16-19]。

图6 不同含量HAP@B对土壤铅形态变化影响Fig.6 Effects of different contents of HAP@B on morphological change of lead in soil
3.2 钝化材料及土壤的表征分析
3.2.1 材料表征分析 (1)X射线衍射分析。对钝化修复铅污染土壤后的HAP@B进行XRD表征分析可知, 修复后的材料图谱衍射峰发生明显的变化(图7), 而羟基磷灰石的主峰强度却略为降低, 并出现了与Pb相关的衍射峰。经X′Pert High Score Plus处理, 钝化使用后的材料形成了Ca2.5Pb7.5(OH)2(PO4)6、Pb3(PO4)2、Pb10(PO4)6(OH)2和PbHPO4化合物, 推测可能是材料中的部分羟基磷灰石溶于土壤溶液发生了反应, 造成了羟基磷灰石的主峰强度的降低。通过对材料的XRD图谱分析, 可以推断HAP@B钝化修复剂对Pb(Ⅱ)的固定主要是通过沉淀和替代作用实现的[16-20]。

图7 钝化前后材料XRD对比Fig.7 XRD comparison of materials before and after passivation

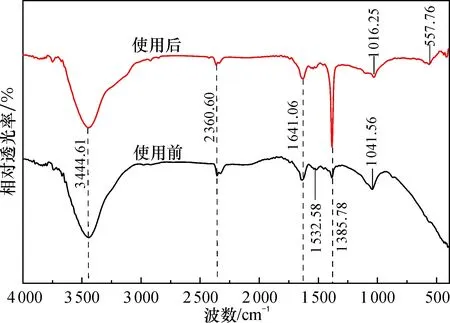
图8 钝化前后材料FT-IR对比Fig.8 FT-IR comparison of materials before and after passivation
(3)X射线光电子能谱分析(XPS)。对钝化前后的材料进行X射线光电子能谱分析, 结果如图9所示。钝化前后材料主要特征峰均由C1s、O1s、Ca2p、P2p组成, 钝化前其结合能分别在284.05、531.38、347.32和133.32 eV; 而钝化后结合能分别在284.28、531.8、346.9和132.78 eV。O的结合能向高结合能偏移, 从531.38 eV(O1s)偏移到531.8 eV(O1s), 偏移量为0.42 eV, 推测是Pb与—OH发生络合形成R—O—Pb造成的[21]。
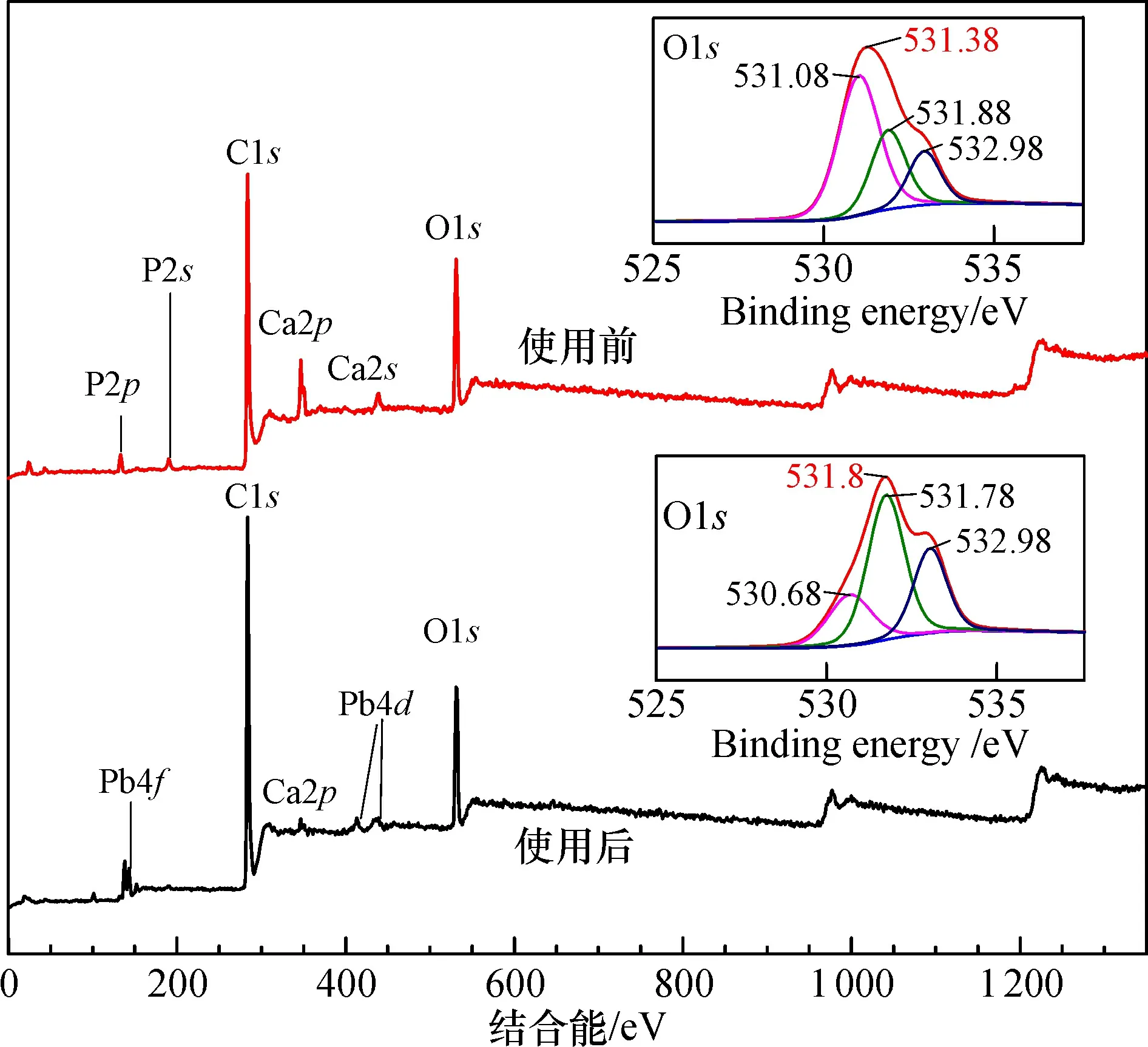
图9 钝化前后材料XPS对比Fig.9 XPS comparison of materials before and after passivation
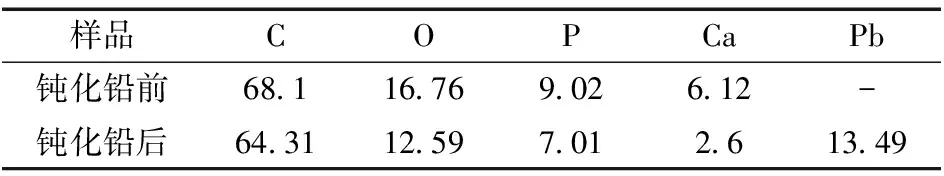
表1 材料钝化铅前后的各元素占比
3.2.2 土壤表征分析 (1)修复前后土壤SEM对比分析。图10为钝化修复前后铅污染土壤对比图, 钝化前(图10a)土壤团聚结构较为松散、表面较为粗糙、土壤颗粒易脱落;图10b中,土壤颗粒堆叠、不稳定;钝化后可以明显看到添加进入土壤的钝化修复剂HAP@B的存在,其多孔结构将土壤颗粒牢牢吸附,整体结构较为密实、表面相对光滑(图10c、d)。竹炭模板的存在利于将土壤中铅离子吸附固定在HAP@B材料上充分反应,将铅离子钝化修复成稳定型态物质存在。经过一定时间土壤内溶液浸泡冲刷,钝化材料载体竹炭的存在可提升土壤有机质含量,进而提升土壤肥力[22]。

图10 钝化修复前(a、b)后(c、d)铅污染土壤SEM图Fig.10 SEM of lead polluted soil before and after passivation

图11 铅污染土壤钝化前后XRD对比Fig.11 XRD comparison of lead polluted soil before and after passivation
4 结 论
(1)所制备的HAP@B材料对土壤中铅具有优秀的钝化能力。当选择5%的投加比例、15 d的钝化时间, 材料粒径20~100目(0.150~0.840 mm)、土壤含水率为30%及pH>4时, 外源添加铅污染土壤的钝化修复稳定率达90%以上。
(2)重金属形态分析结果得知, HAP@B的添加使得土壤中铅元素的赋存形态发生变化, 主要是降低了弱酸提取态占比, 提高了可还原态和残渣态的占比。可以通过降低活泼形态的比例, 提高稳定形态的比例来达到稳定修复效果。
(3)材料和土壤的表征分析得出HAP@B材料钝化铅污染土壤主要通过物理吸附、静电吸附,以及络合反应、离子交换和溶解沉淀作用。
