电解后溶液复原模型的构建及应用
2021-05-20陈碧琴
陈碧琴
(福建省莆田第二中学,福建莆田 351131)
引言
电化学是高中化学的重要内容,且原电池和电解池均是高考考查的重要知识点。其中,电解池溶液复原问题较为抽象,对学生分析问题的能力有一定的要求。一些学生分析问题时考虑不全面、不深入,出错率较高。为帮助学生更好地突破该类题型,提高学生解答该类问题的能力与效率,教师在课堂上应注重对该模型的构建及教学应用[1]。
一、例题分析
室温下,使用石墨电极电解饱和食盐水(已知食盐水的溶解度为36g),电解总的化学反应式为:经过一段时间后,以下措施中可将溶液恢复到原来的状态的操作是( )。
①向电解后的溶液中通入适量的HCl 气体;②向电解后的溶液中加适量浓盐酸;③向电解后的溶液中加适量该温度下的饱和氯化钠溶液;④向电解后的溶液中先加入适量的MgCl2,搅拌后再过滤。
A.①③ B.②③ C.①④ D.②④
电解池是高中化学电化学部分的重要组成部分,是高考考查的热门知识点。相关题型复杂多变,其中电解后溶液复原问题难度较大,需要学生深入理解电解池工作原理,准确把握各个阶段电解的物质及电解后给电解液造成的影响。本题对学生的综合能力要求较高,题干只是给出了总的化学反应式及充当电极的物质,学生只有熟练地掌握电解池原理,才能灵活运用所学知识分析出电解过程中参与电解的物质,把握电解产物,从而正确作答。课堂上,教师可先给学生预留一定的时间,要求学生采用常规思路作答,而后自然地引入模型构建内容,再要求学生使用构建的模型进行分析,对比两种解题思路的解题效率。这样,学生自然就形成了运用模型分析该类问题的意识。
二、模型建立
(一)模型背景
电解池中溶液复原模型的构建基于电解池,因此,学生在构建模型时需要熟悉电解池原理,牢固掌握相关基础知识。根据高中化学教材可知,电解池是一种将电能转化为化学能的装置,因此,电解需要外加电源。为使学生更好地理解模型,教师应引导学生掌握电子的运动规律,即从电源的负极流出到达电解池的阴极,引起电解质溶液中离子的定向移动,又从电解池的阳极流向电源的正极;同时,能够判断不同离子的放电顺序,准确写出不同阶段的电极反应式,即阳离子按照如下顺序放电:Ag+>Hg2+>Fe3+>Cu2+>H+(指酸电离的)>Pb2+>Sn2+>Fe2+>Zn2+> Al3+> Mg2+>Na+>Ca2+>K+。判断阳极放电情况时,学生需要分析电极材料及离子的放电顺序。阳极若为活性电极,电极本身溶解放电;若为惰性电极,则按照如下顺序放电:S2->I->Br->Cl->OH->NO3->SO4
2-(等含氧酸根离子)>F-。以使用石墨电极电解CuCl2溶液为例,阳极电极反应式为:2Cl--2e-=Cl2↑,阴极电极反应式为:Cu2++2e-=Cu。
(二)模型涉及的情境
根据电解池原理:电解质溶液复原模型包含三种情境:①电解电解质;②电解水;③电解电解质和水。其中,情境①只需添加电解质即可,如电解HCl 溶液时电池总反应式为:,若要使溶液恢复到原来的状态,向溶液中通入HCl 气体即可。情境②中要想使溶液恢复到原来的状态,向原溶液中加入水即可,如电解KNO3、Na2SO4、H2SO4等。情境③难度相对较大,所以学生需要进行综合考虑。以电解NaCl 溶液为例,总反应式为:2NaOH+H2↑+Cl2↑。如加入NaCl 和水,溶液中的NaOH无法消除。分析总的电池反应式可知,产生的H2和Cl2气体相当于HCl 气体,因此,可向溶液中通入HCl 气体。同时,HCl+NaOH=NaCl+H2O,因此,可使溶液恢复到电解前的状态。另外,电解CuSO4、AgNO3溶液可使用同样的思路分析。
(三)模型建立
结合上述分析构建如下模型(见表1),以指导学生更准确地分析相关习题。
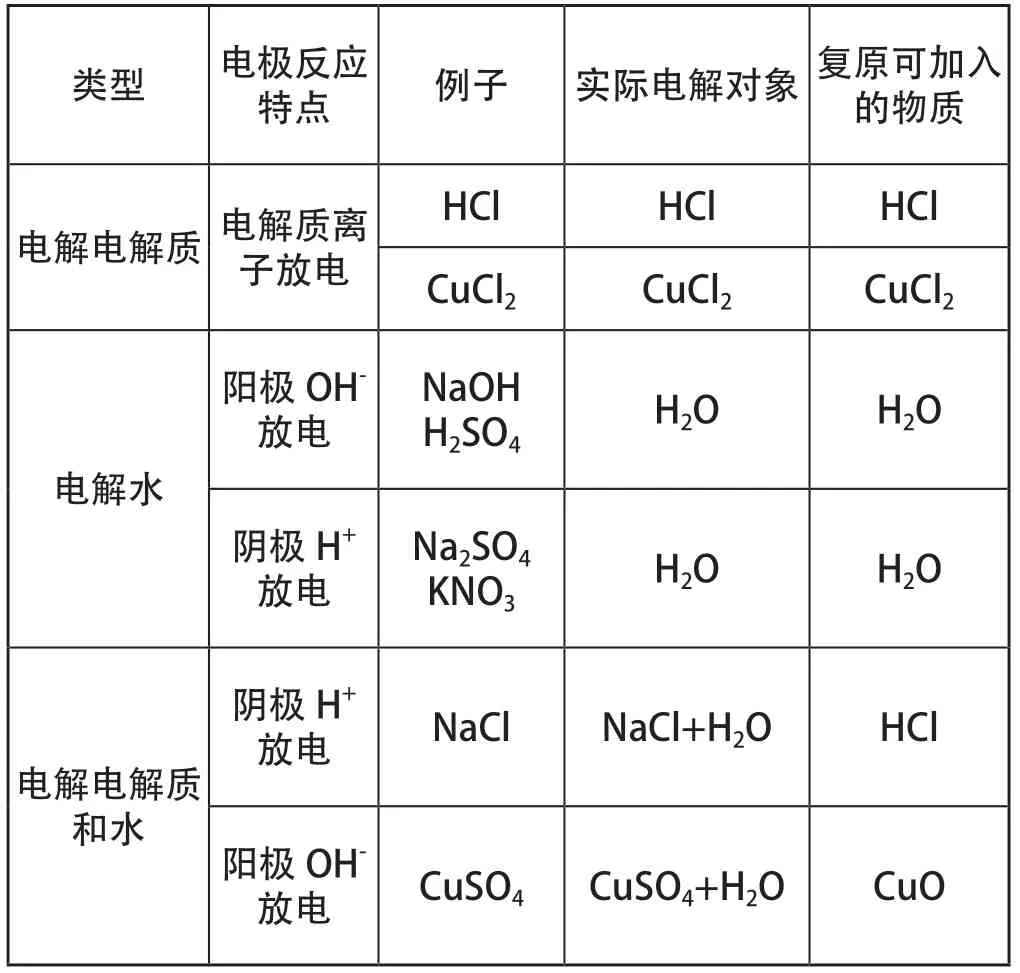
表1
三、例题的求解
根据上述模型中的三种情境,可知①的措施可行,②的措施不行。根据已知条件可知饱和的氯化钠溶液中溶质和水的质量之比为36∶100=9∶25,而被电解后溶液不再饱和,因此,措施③不可行。加入MgCl2,搅拌后再过滤。则发生反应:MgCl2+2NaOH=Mg(OH)2↓+2NaCl。从这一点来看,NaCl 的总量恢复了原来的状态,但水在电解过程中被消耗了,所以浓度还是恢复到了饱和状态,因此,措施④合理。综上可知,选择C 项。
通过对比常规思路及运用模型解题的解题效率,学生不难发现,虽然常规思路最终能够得出正确结果,但分析的时间较长,效率不高;而使用模型法解题,根据题干模型迅速找到对应的模型情境,能够及时做出准确的判断,从而提升解题效率。
四、模型的应用训练
化学课上,教师将惰性电极放入硫酸铜溶液中进行电解实验操作。经检测,当Cu2+浓度变为原来的一半时将电源断开。将以下物质加入溶液中,可使溶液恢复到电解前浓度的是( )。
A.CuSO4B.CuO C.Cu(OH)2D.CuSO4·5H2O
课堂上,教师应及时向学生展示相关问题,鼓励学生运用所学模型进行解答。教师运用构建的模型对学生进行解题训练,既能加深学生对模型的认识,使学生快速找到分析问题的思路,又能增强学生解题的自信心,从而获得了很好的教学效果[2]。
结 语
综上所述,教师在高中化学教学中不仅要重视基础知识教学,还应考虑如何提高学生的解题效率,尤其要结合自身经验做好高中化学常见模型的汇总,在课堂上以具体的习题为背景,为学生积极灌输建模知识,并与学生一起完成相关模型的构建。另外,为使学生更好地消化、吸收所学知识,教师应做好相关习题的设计,鼓励学生运用构建的模型进行解题,掌握解答相关化学题型的技巧。
